Кристаллическая решётка. Пособие по химии для поступающих в высшие учебные заведения
Твердые вещества, как правило, имеют кристаллическое строение. Оно характеризуется правильным расположением частиц в строго определенных точках пространства. При мысленном соединении этих точек пересекающимися прямыми линиями образуется пространственный каркас, который называюткристаллической решеткой . Точки, в которых размещены частицы, называются узлами кристаллической решетки . В узлах воображаемой решетки могут находиться ионы, атомы или молекулы. Они совершают колебательные движения. С повышением температуры амплитуда колебаний возрастает, что проявляется в тепловом расширении тел.
В зависимости от вида частиц и характера связи между ними различают 4 вида кристаллических решеток: ионные (NaCl, KCl), атомные, молекулярные и металлические.
Кристаллические решетки, состоящие из ионов, называются ионными . Их образуют вещества с ионной связью. Примером может служить кристалл хлорида натрия, в котором каждый ион натрия окружен 6 хлорид-ионами, а каждый хлорид-ион 6 ионами-натрия.
Кристаллическая решетка NaCl
Число ближайших соседних частиц, вплотную примыкающих к данной частице в кристалле или отдельной молекуле называется координационным число .
В решетке NaCl координационные числа обоих ионов равны 6. И так, в кристалле NaCl нельзя выделить отдельные молекулы соли. Их нет. Весь кристалл следует рассматривать как гигантскую макромолекулу, состоящую из равного числа ионов Na + и Cl - , Na n Cl n – где n большое число. Связи между ионами в таком кристалле весьма прочны. Поэтому вещества с ионной решеткой обладают сравнительно высокой твердостью. Они тугоплавки и малолетучи.
Плавление ионных кристаллов приводит к нарушению геометрически правильной ориентации ионов относительно друг друга и уменьшению прочности связи между ними. Поэтому расплавы их проводят электрический ток. Ионные соединения, как правило, легко растворяются в жидкостях, состоящих из полярных молекул, например, воде.
Кристаллические решетки, в узлах которых находятся отдельные атомы, называются атомными . Атомы в таких решетках соединены между собой прочными ковалентными связями. Примером может служить алмаз - одна из модификаций углерода. Алмаз состоит из атомов углерода, каждый из которых связан с 4 соседними атомами. Координационное число углерода в алмазе равно 4. Вещества с атомной кристаллической решеткой имеют высокую температуру плавления (у алмаза свыше 3500 о С), прочны и тверды, практически не растворимы в воде.
Кристаллические решетки, состоящие из молекул (полярных и неполярных), называются молекулярными . Молекулы в таких решетках соединены между собой сравнительно слабыми межмолекулярными силами. Поэтому вещества с молекулярной решеткой имеют малую твердость и низкую температуру плавления, нерастворимы или малорастворимы в воде, их растворы почти не проводят электрический ток. Примерами их являются лед, твердый СО 2 («сухой лед»), галогены, кристаллы водорода, кислорода, азота, благородных газов и др.
Валентность
Важной количественной характеристикой, показывающей число взаимодействующих между собой атомов в образовавшейся молекуле, является валентность – свойство атомов одного элемента присоединять определенное число атомов других элементов.
Количественно валентность определяется числом атомов водорода, которое данный элемент может присоединять или замещать. Так, например, в плавиковой кислоте (HF) фтор одновалентен, в аммиаке (NH 3) азот трехвалентен, в кремневодороде (SiH 4 – силан) кремний четырехвалентен и т.д.
Позже, с развитием представлений о строении атомов, валентность элементов стали связывать с числом неспаренных электронов (валентных), благодаря которым осуществляется связь между атомами. Таким образом, валентностьопределяется числом неспаренных электронов в атоме, принимающих участие в образовании химической связи (в основном или возбужденном состоянии). В общем случае валентность равна числу электронных пар, связывающих данный атом с атомами других элементов.
Кристаллические решетки
8 КЛАСС
* По учебнику: Габриелян О.С. Химия-8. М.: Дрофа, 2003.
Цели.
Обучающие.
Дать понятие о
кристаллическом и аморфном состоянии твердых
веществ; познакомиться с типами кристаллических
решеток, их взаимосвязью с видами химической
связи и влиянием на физические свойства веществ;
дать представление о законе постоянства состава
веществ.
Развивающие
. Развивать логическое
мышление, умения наблюдать и делать выводы.
Воспитательные
. Формировать
эстетический вкус и коллективизм, расширять
кругозор.
Оборудование и реактивы.
Модели
кристаллических решеток, диафильм «Зависимость
свойств веществ от состава и строения»,
диапозитивы «Химическая связь. Строение
вещества»; пластилин, жевательная резинка, смолы,
воск, поваренная соль NaCl, графит, сахар, вода.
Форма организации работы.
Групповая.
Методы и приемы.
Самостоятельная
работа, демонстрационный опыт, лабораторная
работа.
Эпиграф.
ХОД УРОКА
УЧИТЕЛЬ.
Кристаллы встречаются нам
повсюду. Мы ходим по кристаллам, строим из
кристаллов, создаем приборы и изделия из
кристаллов, широко применяем кристаллы в технике
и в науке, едим кристаллы, лечимся кристаллами,
находим кристаллы в живых организмах, выходим на
просторы космических дорог с помощью приборов из
кристаллов…
Что же такое кристаллы?
Вообразите на минутку, что ваши глаза стали
видеть атомы или молекулы; рост уменьшился, и вы
смогли войти внутрь кристалла. Цель нашего урока
– понять, что такое кристаллическое и аморфное
состояние твердых веществ, познакомиться с
типами кристаллических решеток, получить
представление о законе постоянства состава
веществ.
Какие агрегатные состояния веществ известны?
Твердое, жидкое и газообразное. Они
взаимосвязаны (схема 1).
Сказка о жадном хлоре
В некотором царстве, химическом государстве,
жил-был Хлор. И хотя принадлежал он к старинному
роду Галогенов, да и наследство получил немалое
(на внешнем энергетическом уровне у него было
семь электронов), был он очень жадным и
завистливым, а от злости даже стал желто-зеленым.
Днем и ночью мучило его желание сделаться
похожим на Аргон. Думал он думал и наконец
придумал: «У Аргона на внешнем уровне восемь
электронов, а у меня только семь. Значит, мне надо
заполучить еще один электрон, тогда я тоже буду
благородным». На следующий день собрался Хлор в
дорогу за заветным электроном, но далеко идти ему
не пришлось: возле самого дома встретил он атом,
похожий на него как две капли воды.
– Слушай, брат, дай мне свой электрон, –
заговорил Хлор.
– Нет уж, лучше ты дай мне электрон, – ответил
близнец.
– Ладно, давай тогда объединим наши электроны,
чтобы никому не было обидно, – сказал жадный
Хлор, надеясь, что потом он заберет электрон себе.
Но не тут-то было: оба атома в равной степени
пользовались общими электронами, несмотря на
отчаянные усилия жадного Хлора перетянуть их на
свою сторону.
УЧИТЕЛЬ.
Посмотрите на вещества на
ваших столах и распределите их на две группы.
Пластилин, жевательная резинка, смола, воск – это
аморфные вещества. У них часто нет постоянной
температуры плавления, наблюдается текучесть,
нет упорядоченного строения (кристаллической
решетки). Напротив, соль
NaCl, графит и сахар –
кристаллические вещества. Для них характерны
четкие температуры плавления, правильные
геометрические формы, симметрия.
Применение находят и аморфные, и кристаллические
вещества. Мы познакомимся с типами
кристаллических решеток и их влиянием на
физические свойства веществ. Помогут в
повторении видов химической связи
подготовленные вами творческие задания –
сказки.
Сказка про ковалентную полярную связь
В некотором царстве, в некотором государстве с названием «Периодическая система» жил-был маленький электрончик. У него не было друзей. Но однажды к нему в село под названием «Внешний уровень» пришел другой электрончик, точь-в-точь похожий на первого. Они сразу же подружились, ходили всегда вместе и даже не заметили, как оказались спаренными. Эти электроны прозвали ковалентными.
Сказка про ионную связь
В доме периодической системы Менделеева жили
два друга – металл Na и неметалл Cl. Каждый жил в
своей квартире: Na – в квартире под № 11, а Cl – под
№ 17.
И вот решили друзья поступить в кружок, а там им
сказали: чтобы поступить в этот кружок, надо
завершить энергетический уровень. Друзья
расстроились и поплелись домой. Дома они думали,
как завершить энергетический уровень. И вдруг Сl
сказал:
– Давай, ты мне подаришь со своего третьего
уровня один электрон.
– То есть как подарю? – спросил Na.
– А так, возьмешь и подаришь. У тебя будет два
уровня и все завершенные, а у меня будет три
уровня и тоже все завершенные. Тогда нас примут в
кружок.
– Ладно, забирай, – сказал Na и отдал свой
электрон.
Когда они пришли в кружок, то директор кружка
спросил: «Как вам это удалось?» Они все ему
рассказали. Директор сказал: «Молодцы, ребята» –
и принял их в свой кружок. Натрию директор дал
карточку со знаком «+1», а хлору – со знаком «–1».
И теперь он принимает в кружок всех желающих –
металлы и неметаллы. А то, что сделали Na и Сl, он
назвал ионной связью.
УЧИТЕЛЬ.
Вы хорошо разобрались в
типах химической связи? Эти знания пригодятся
при изучении кристаллических решеток. Мир
веществ велик и разнообразен. Они обладают
самыми разными свойствами. Различают физические
и химические свойства веществ. Какие свойства мы
отнесем к физическим?
Ответы учеников:
агрегатное состояние, цвет,
плотность, температуры плавления и кипения,
растворимость в воде, электропроводность.
УЧИТЕЛЬ.
Опишите физические
свойства веществ:
O 2 , H 2 O, NaCl, графит
С.
Ученики заполняют таблицу, которая в результате
приобретает следующий вид.
Таблица
| Физические свойства |
Вещества | |||
|---|---|---|---|---|
| О 2 | Н 2 О | NaCl | C | |
| Агрегатное состояние | Газ | Жидкость | Твердое | Твердое |
| Плотность, г/см 3 | 1,429 (г/л) | 1,000 | 2,165 | 2,265 |
| Цвет | Бесцветный | Бесцветный | Белый | Черный |
| t пл, °С | –218,8 | 0,0 | +801,0 | – |
| t кип, °С | –182,97 | +100 | +1465 | +3700 |
| Растворимость в воде | Малорастворим | – | Растворим | Нерастворим |
| Электропроводность | Неэлектропроводный | Слабая | Проводник | Проводник |
УЧИТЕЛЬ. По физическим свойствам веществ можно определить их строение.
Диапозитив.
УЧИТЕЛЬ. Кристалл – твердое тело, частицы которого (атомы, молекулы, ионы) расположены в определенном, периодически повторяющемся порядке (в узлах). При мысленном соединении узлов линиями образуется пространственный каркас – кристаллическая решетка. Различают четыре типа кристаллических решеток (схема 2 , см. с. 24).
Схема 2
КРИСТАЛЛИЧЕСКИЕ РЕШЕТКИ
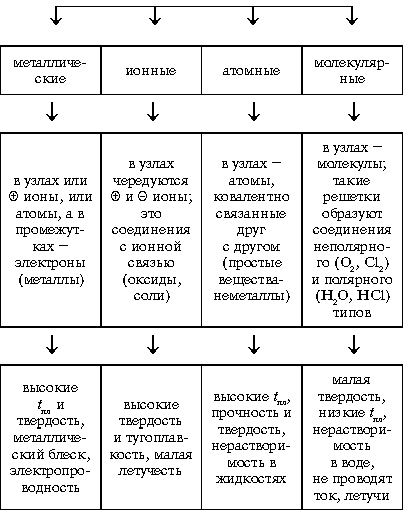
УЧИТЕЛЬ. Какие кристаллические решетки у О 2 , Н 2 О, NaCl, С?
Ответ учеников.
О 2 и Н 2 О –
молекулярные кристаллические решетки, NaCl –
ионная решетка,
С – атомная решетка.
Демонстрация моделей кристаллических
решеток:
NaCl, C (графит), Mg, CO 2 .
УЧИТЕЛЬ.
Обратите внимание на типы
кристаллических решеток простых веществ в
зависимости от их положения в периодической
системе (с. 79 учебника).
Какой тип решетки не встречается в простых
веществах?
Ответ учеников.
У простых веществ не бывает
ионных решеток.
 |
|
УЧИТЕЛЬ.
Для веществ с
молекулярной решеткой характерно явление
возгонки или сублимации.
Демонстрационный опыт.
Возгонка
бензойной кислоты или нафталина. (Возгонка – это
превращение (при нагревании) твердого вещества в
газ, минуя жидкую фазу, а затем снова
кристаллизация в виде инея.)
УЧИТЕЛЬ.
Вещества с молекулярным
строением подчиняются закону постоянства
состава вещества; вещества молекулярного
строения имеют постоянный состав независимо от
способа их получения. Закон был открыт
Ж.Л.Прустом. Он разрешил долгий спор К.Л.Бертолле
и Дж.Дальтона в пользу первого.
Например, углекислый газ или оксид углерода(IV)
CO 2
– сложное вещество молекулярного строения. Оно
состоит из двух элементов: углерода и кислорода,
причем в молекуле один атом углерода и два атома
кислорода. Относительная молекулярная масса M r (CO 2 )
= 44, молярная масса M(CO 2 ) = 44 г/моль.
Молярный объем V M (CO 2 ) = 22,4 моль (н.у.).
Число молекул в 1 моль вещества N A (CO 2 )
= 6 10 23 молекул.
Для веществ с ионным строением закон Пруста не
всегда выполняется.
Графический диктант
«Виды химических связей и типы кристаллических
решеток»
Знаками «+» и «–» отмечается, характерно ли
данное утверждение (1–20) для типа химической
связи указанного варианта.
Вариант 1.
Ионная связь.
Вариант 2.
Ковалентная неполярная
связь.
Вариант 3.
Ковалентная полярная
связь.
Утверждения.
1. Связь образуется между атомами металлов и
неметаллов.
2. Связь образуется между атомами металлов.
3. Связь образуется между атомами неметаллов.
4. В процессе взаимодействия атомов образуются
ионы.
5. Образовавшиеся молекулы поляризованы.
6. Связь устанавливается за счет спаривания
электронов без сдвига общих электронных пар.
7. Связь устанавливается путем спаривания
электронов и сдвига общей пары к одному из
атомов.
8. В процессе химической реакции происходит
полная передача валентных электронов от одного
атома реагирующих элементов к другому.
9. Степень окисления атомов в молекуле равна нулю.
10. Степени окисления атомов в молекуле равны
количеству отданных или принятых электронов.
11. Степени окисления атомов в молекуле равны
количеству смещенных общих электронных пар.
12. Соединения с данным видом связи образуют
кристаллическую решетку ионного типа.
13. Для соединений с этим видом химической связи
характерны кристаллические решетки
молекулярного типа.
14. Соединения с таким видом связи образуют
кристаллические решетки атомного типа.
15. Соединения могут быть газообразными при
обычных условиях.
16. Соединения твердые при обычных условиях.
17. Соединения с таким видом связи обычно
тугоплавкие.
18. Вещества с таким видом связи могут быть
жидкими при обычных условиях.
19. Вещества с такой химической связью имеют
запах.
20. Вещества с такой химической связью имеют
металлический блеск.
Ответы (самооценка).
Вариант 1
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| + | – | – | + | + | – | – | + | – | + |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| – | + | – | – | – | + | + | – | – | – |
Вариант 2
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| – | – | + | – | – | + | – | – | + | – |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| – | – | + | – | + | + | – | + | + | – |
Вариант 3
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| – | – | + | – | + | – | + | – | – | – |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| + | – | + | + | + | – | + | + | + | – |
Критерии оценки: 1–2 ошибки – «5», 3–4 ошибки – «4», 5–6 ошибок – «3».
Закрепление материала
Кремний имеет атомную кристаллическую
решетку. Каковы его физические свойства?
Какой тип кристаллической решетки у Na 2 SO 4 ?
Оксид СО 2 имеет низкую t
пл, а
кварц SiO 2 – очень высокую (кварц плавится
при 1725 °С). Какие кристаллические решетки они
должны иметь?
УЧИТЕЛЬ. Мы заглянули в нутро вещей, не правда ли? В заключение хочется упомянуть драгоценные камни: алмаз, сапфир, изумруд, александрит, аметист, жемчуг, опал и др. Драгоценным камням издавна приписывали целебные свойства. Считали, что кристалл аметиста предохраняет от пьянства и навевает счастливые сны. Изумруд спасает от бурь. Алмаз бережет от болезней. Топаз приносит счастье в ноябре, а гранат – в январе.
Драгоценные камни служили мерой
богатств князей и императоров. Иноземные послы,
побывавшие в XVII в. в России, писали, что ими
овладел «тихий ужас» при виде роскошных нарядов
царской семьи, сплошь унизанных драгоценными
камнями.
На голове царицы Ирины Годуновой была корона,
«как стена с зубцами», разделенная на 12 башенок,
искусно выделанных из рубинов, топазов, алмазов и
«скатных жемчугов», кругом корона была унизана
огромными аметистами и сапфирами.
 |
Известно, что шляпа князя Потемкина
Таврического так была усеяна бриллиантами и
из-за этого столь тяжела, что владелец не мог
носить ее на голове; адъютант нес шляпу в руках за
князем. На одном из платьев императрицы
Елизаветы было нашито столько драгоценных
камней, что она, не выдержав их тяжести, упала на
балу в обморок. Впрочем, еще раньше с супругой
царя Александра Михайловича случилось более
досадное происшествие: ей пришлось прервать
обряд венчания, чтобы снять с себя усыпанный
самоцветами наряд.
Самые большие в мире алмазы известны каждый под
своим названием: «Орлов», «Шах», «Конкур»,
«Регент» и др.
Кристаллы необходимы – в часах, эхолотах,
микрофонах; алмаз – «работник» (в подшипниках,
стеклорезах и др.).
«Камень сейчас в руках человека – не забава и
роскошь, а прекрасный материал, которому мы
сумели вернуть его место, материал, среди
которого прекраснее и веселее жить. Он не будет
“драгоценным камнем” – его время прошло: это
будет самоцвет, дающий красоту жизни. ...В нем
человек будет видеть воплощение непревзойденных
красок и нетленности самой природы, к которым
может прикоснуться только горящим огнем
вдохновения художник», – писал академик
А.Е.Ферсман.
Кристаллы можно вырастить даже в бытовых
условиях. Попробуйте выполнить творческое
домашнее задание по выращиванию кристаллов.
Домашнее задание
«Выращивание кристаллов»
Оборудование и реактивы. Чистые стаканы, картон, карандаш, нитки; вода, соль (NaCl, или СuSO 4 , или KNO 3 .)
Ход работы
Первый способ
.
Приготовьте
насыщенный раствор выбранной вами соли. Для
этого в горячую воду насыпьте порциями соль и
перемешивайте до растворения. Как только соль
перестанет растворяться, раствор насыщен.
Раствор профильтруйте через марлю. Этот раствор
налейте в стакан, положите карандаш с ниткой и
грузом (пуговичка, например). Через 2–3 дня груз
должен обрасти кристалликами.
Второй способ
.
Банку с насыщенным
раствором закройте картоном и подождите, пока
при медленном охлаждении на дно выпадут
кристаллы. Обсушите кристаллы на салфетке,
несколько самых привлекательных укрепите на
нитке, привяжите к карандашу и опустите в
насыщенный раствор, освобожденный от других
кристаллов. Кристаллы могут расти 2–3 недели.
Фазовые переходы бывают двух типов - первого и второго рода. К фазовым переходам первого рода относится изменение агрегатного состояния вещества: процессы плавления и кристаллизации, испарения и конденсации, сублимации или возгонки , при этом скачком изменяются плотность, внутренняя энергия, энтропия.
Следует заметить, что твердым считается кристаллическое состояние, т.е. состояние, в котором атомы располагаются в узлах кристаллической решетки. На рис. 2-5.1 изображена кристаллическая решетка каменной соли NaCl . Как видно из рисунка, кристалл, благодаря пространственной периодичности структуры, состоит как бы из повторяющихся частей.
В кристалле размером 1 мм повторяющееся расположение атомов встречается сотни тысяч раз. Поэтому к такому расположению атомов применяется термин “дальний порядок ”. Большинство твердых тел являются кристаллическими телами. В обычных условиях они состоят из сросшихся зерен размером порядка 0,001 мм. В таком зернышке отчетливо выражен дальний порядок.
Однако в природе встречаются твердые вещества со сложным молекулярным строением, например, стекла, смолы, пластики, которые не имеют периодической структуры. Это аморфные твердые тела, которые на самом деле являются жидкостями с аномально большой вязкостью. Такие тела приобретают свойство текучести не скачком, а путём постепенного уменьшения вязкости, которое вызывается повышением температуры. Аморфные твердые тела противопоставляются кристаллам, которые имеют форму правильного многогранника. Следует подчеркнуть, что кристалличность не обязательно проявляется в особенностях их внешней формы, это структура решетки (кусок металла не имеет правильной формы, но не является аморфным).
Каков же основной признак кристаллов? Этим признаком является наличие резко выраженной температуры плавления. Если подводить тепло к кристаллическому телу, то температура его будет повышаться до тех пор, пока не начнёт плавиться. После чего подъем температуры прекратится, и весь процесс плавления будет происходить при строго определённой постоянной температуре, называемой температурой плавления Т пл .
На рис. 2-5.2 изображены схемы строения кварца и кварцевого стекла. Одно и то же в химическом отношении вещество, но одно в кристаллическом, другое в аморфном виде. Характер окружения ближайшими соседями в обоих случаях одинаков, но в аморфном теле отсутствует дальний порядок; аморфное тело – это “испорченный кристалл”. Отсутствие дальнего порядка, характерного признака кристаллических тел, является непосредственной причиной отсутствия выраженной точки плавления. В точке плавления совершается переход, при котором дальний порядок исчезает и решетка распадается на легкоподвижные субмикроскопические области, имеющие то же расположение атомов, что и исходный кристалл, но статически беспорядочно ориентированные друг относительно друга, остаётся лишь ближний порядок в расположении атомов.
Схема строения кварца
а) кристаллический, б) аморфный
(рисунок соответствует упрощенной плоской модели)
В аморфных телах при повышении температуры характер расположения атомов не меняется, увеличивается их подвижность, атомы с увеличением температуры “выскальзывают” из своего окружения, меняя соседей. Наконец число таких перемен в секунду становится таким же большим, как для жидкости.
Выше мы говорили, что при всех агрегатных превращениях поглощается или выделяется энергия. Например, для превращения килограмма воды в пар необходимо затратить энергию 2,3×10 6 Дж. Эта энергия необходима для преодоления сил притяжения, действующих между молекулами воды.
Металлы начинают плавиться только тогда, когда начинает разрушаться их кристаллическая решетка, на что также необходимо затрачивать энергию. Эта энергия называется скрытой теплотой плавления. Теплота плавления, отнесённая к массе вещества, называется удельной скрытой теплотой плавления. Например, для цинка она составляет 1.11×10 5 Дж/кг, т.е. нужно количество теплоты 111 кДж/кг, чтобы при Т пл = 419.5°С перевести 1 кг цинка из твердого состояния в жидкое. На рис. 2-5.3 представлена кривая фазового перехода твердого тела в жидкость (1). Обратное превращение – кристаллизация (2) происходит при той же температуре и сопровождается поглощением того же количества энергии, что и при плавлении – скрытой теплоты кристаллизации. Скрытой теплота перехода называется потому, что подвод (поглощение) и отвод (выделение) этой теплоты не сопровождается таким эффектом, как повышение и понижение температуры. Несмотря на то, что мы продолжаем нагревать тело (кривая правления 1), во время плавления температура не повышается, так же во время кристаллизации (кривая кристаллизации 2) температура не понижается, хотя мы продолжаем охлаждать жидкость. Переход жидкость - твердое тело сопровождается выделением энергии. Энергия взаимодействия микроскопических кристаллов становится значительно выше энергии тепловых колебаний, жидкость кристаллизуется. Однако новая фаза при таком переходе образуется не сразу во всем объеме, сначала образуются зародыши ее, которые затем растут, распространяясь на весь объем.
К числу фазовых превращений первого рода относятся и некоторые переходы твердого тела из одной кристаллической модификации в другую. Эти превращения называются полиморфными. Кристаллы различной модификации состоят из одного и того же вещества и отличаются друг от друга лишь строением кристаллической решетки. Например, графит и алмаз состоят из одного и того же элемента – углерода. Разные структуры означают и разные физические свойства. Алмаз по физическим свойствам очень не похож на графит. Графит имеет черный цвет, он совершенно непрозрачен, алмаз же прозрачен и бесцветен; графит не горит даже при очень высоких температурах (он плавится при 385 °С), алмаз же в струе кислорода сгорает при 720 °С. Другой пример – белое и серое олово. Белое олово – блестящий, легкий и очень пластичный металл, серое олово – хрупкое и легко превращается в порошок.
Поваренная соль — это хлорид натрия, применяемый в качестве добавки к пище, консерванта продуктов питания. Используется также в химической промышленности, медицине. Служит важнейшим сырьем для получения едкого натра, соды и других веществ. Формула соли поваренной — NaCl.
Образование ионной связи между натрием и хлором
Химический состав хлорида натрия отражает условная формула NaCl, которая дает представление о равном количестве атомов натрия и хлора. Но вещество образовано не двухатомными молекулами, а состоит из кристаллов. При взаимодействии щелочного металла с сильным неметаллом каждый атом натрия отдает более электроотрицательному хлору. Возникают катионы натрия Na + и анионы кислотного остатка соляной кислоты Cl - . Разноименно заряженные частицы притягиваются, образуя вещество с ионной кристаллической решеткой. Маленькие катионы натрия расположены между крупными анионами хлора. Число положительных частиц в составе хлорида натрия равно количеству отрицательных, вещество в целом является нейтральным.
Химическая формула. Поваренная соль и галит
Соли — это сложные вещества ионного строения, названия которых начинаются с наименования кислотного остатка. Формула соли поваренной — NaCl. Геологи минерал такого состава называют «галит», а осадочную породу — «каменная соль». Устаревшей химический термин, который часто употребляется на производстве, — «хлористый натрий». Это вещество известно людям с глубокой древности, когда-то его считали «белым золотом». Современные ученики школ и студенты при чтении уравнений реакций с участием хлорида натрия называют химические знаки («натрий хлор»).
Проведем несложные расчеты по формуле вещества:
1) Mr (NaCl) = Ar (Na) + Ar (Cl) = 22,99 + 35,45 = 58,44.
Относительная составляет 58,44 (в а.е.м.).
2) Численно равна молекулярному весу молярная масса, но эта величина имеет единицы измерения г/моль: М (NaCl) = 58,44 г/моль.
3) Образец соли массой 100 г содержит 60,663 г атомов хлора и 39,337 г натрия.
Физические свойства поваренной соли
Хрупкие кристаллы галита — бесцветные или белые. В природе также встречаются месторождения каменной соли, окрашенной в серый, желтый либо голубой цвет. Иногда минеральное вещество обладает красным оттенком, что обусловлено видами и количеством примесей. Твердость галита по составляет всего 2-2,5, стекло оставляет на его поверхности черту.

Другие физические параметры хлорида натрия:
- запах — отсутствует;
- вкус — соленый;
- плотность — 2,165 г/ см3 (20 °C);
- температура плавления — 801 °C;
- точка кипения — 1413 °C;
- растворимость в воде — 359 г/л (25 °C);
Получение хлорида натрия в лаборатории
При взаимодействии металлического натрия с газообразным хлором в пробирке образуется вещество белого цвета — хлорид натрия NaCl (формула поваренной соли).

Химия дает представление о различных способах получения одного и того же соединения. Вот некоторые примеры:
NaOH (водн.) + HCl = NaCl + H 2 O.
Окислительно-восстановительная реакция между металлом и кислотой:
2Na + 2HCl = 2NaCl + Н 2 .
Действие кислоты на оксид металла: Na 2 O + 2HCl (водн.) = 2NaCl + H 2 O
Вытеснение слабой кислоты из раствора ее соли более сильной:
Na 2 CO 3 + 2HCl (водн.) = 2NaCl + H 2 O + CO 2 (газ).
Для применения в промышленных масштабах все эти методы слишком дорогие и сложные.
Производство поваренной соли
Еще на заре цивилизации люди знали, что после засолки мясо и рыба сохраняются дольше. Прозрачные, правильной формы кристаллы галита использовались в некоторых древних странах вместо денег и были на вес золота. Поиск и разработка месторождений галита позволили удовлетворить растущие потребности населения и промышленности. Важнейшие природные источники поваренной соли:
- залежи минерала галита в разных странах;
- вода морей, океанов и соленых озер;
- прослойки и корки каменной соли на берегах соленых водоемов;
- кристаллы галита на стенках вулканических кратеров;
- солончаки.

В промышленности используются четыре основных способа получения поваренной соли:
- выщелачивание галита из подземного слоя, испарение полученного рассола;
- добыча в ;
- выпаривание или рассола соленых озер (77% от массы сухого остатка приходится на хлорид натрия);
- использование побочного продукта опреснения соленых вод.
Химические свойства хлорида натрия

По своему составу NaCl — это средняя соль, образованная щелочью и растворимой кислотой. Хлорид натрия — сильный электролит. Притяжение между ионами настолько велико, что его могут разрушить только сильно полярные растворители. В воде вещества распадается, освобождаются катионы и анионы (Na + , Cl -). Их присутствием обусловлена электропроводность, которой обладает раствор поваренной соли. Формула в этом случае записывается так же, как для сухого вещества — NaCl. Одна из качественных реакций на катион натрия — окрашивание в желтый цвет пламени горелки. Для получения результата опыта нужно набрать на чистую проволочную петлю немного твердой соли и внести в среднюю часть пламени. Свойства поваренной соли также связаны с особенностью аниона, которая заключается в качественной реакции на хлорид-ион. При взаимодействии с нитратом серебра в растворе выпадает белый осадок хлорида серебра (фото). Хлороводород вытесняется из соли более сильными кислотами, чем соляная: 2NaCl + H 2 SO 4 = Na 2 SO 4 + 2HCl. При обычных условиях хлорид натрия не подвергается гидролизу.
Сферы применения каменной соли
Хлорид натрия снижает температуру плавления льда, поэтому зимой на дорогах и тротуарах используется смесь соли с песком. Она впитывает в себя большое количество примесей, при таянии загрязняет реки и ручьи. Дорожная соль также ускоряет процесс коррозии автомобильных кузовов, повреждает деревья, посаженные рядом с дорогами. В химической промышленности хлорид натрия используется как сырье для получения большой группы химических веществ:
- соляной кислоты;
- металлического натрия;
- газообразного хлора;
- каустической соды и других соединений.
Кроме того, поваренная соль применяется в производстве мыла, красителей. Как пищевой антисептик используется при консервировании, засолке грибов, рыбы и овощей. Для борьбы с нарушениями работы щитовидной железы у населения формула соли поваренной обогащается за счет добавления безопасных соединений йода, например, KIO 3 , KI, NaI. Такие добавки поддерживают выработку гормона щитовидной железы, предотвращают заболевание эндемическим зобом.
Значение хлорида натрия для организма человека

Формула соли поваренной, ее состав приобрел жизненно важное значение для здоровья человека. Ионы натрия участвуют в передаче нервных импульсов. Анионы хлора необходимы для выработки соляной кислоты в желудке. Но слишком большое содержание поваренной соли в пище может приводить к высокому кровяному давлению и повышению риска развития заболеваний сердца и сосудов. В медицине при большой кровопотере пациентам вводят физиологический солевой раствор. Для его получения в одном литре дистиллированной воды растворяют 9 г хлорида натрия. Человеческий организм нуждается в непрерывном поступлении этого вещества с пищей. Выводится соль через органы выделения и кожу. Среднее содержание хлорида натрия в теле человека составляет примерно 200 г. Европейцы потребляют в день около 2-6 г поваренной соли, в жарких странах эта цифра выше в связи с более высоким потоотделением.
В воде
35,9 г/100 мл (+25 °C)
39,1 г/100 мл (+100 °C)
Октаэдральная (Cl -)
Кристалл хлорида натрия
Хлори́д на́трия или хлористый натрий (NaCl) - натриевая соль соляной кислоты . Известен в быту под названием поваренной соли , основным компонентом которой и является. Хлорид натрия в значительном количестве содержится в морской воде , придавая ей солёный вкус [ ] . Встречается в природе в виде минерала галита (каменной соли). Чистый хлорид натрия представляет собой бесцветные кристаллы, но с различными примесями его цвет может принимать голубой, фиолетовый, розовый, жёлтый или серый оттенок.
Нахождение в природе и производство
В природе хлорид натрия встречается в виде минерала галита , который образует залежи каменной соли среди осадочных горных пород, прослойки и линзы на берегах солёных озёр и лиманов , соляные корки в солончаках и на стенках кратеров вулканов и в сольфатарах. Огромное количество хлорида натрия растворено в морской воде. Мировой океан содержит 4 × 10 15 тонн NaCl, то есть из каждой тонны морской воды можно получить в среднем 1,3 кг хлорида натрия. Следы NaCl постоянно содержатся в атмосфере в результате испарения брызг морской воды. В облаках на высоте полтора километра 30 % капель, больших 10 мкм по размеру, содержат NaCl. Также он найден в кристаллах снега.
Наиболее вероятно, что первое знакомство человека с солью произошло в лагунах тёплых морей или на соляных озёрах, где на мелководье солёная вода интенсивно испарялась под действием высокой температуры и ветра, а в осадке накапливалась соль. По образному выражению Пифагора , «соль была рождена благородными родителями: солнцем и морем» .
Галит
В природе хлорид натрия чаще всего встречается в виде минерала галита. Он имеет гранецентрированную кубическую решётку и содержит 39,34 % , 60,66 % . Другими химическими элементами, входящими в состав примесей, являются: , , , , , , , , , , , , , , , . Плотность 2,1-2, 2 г/см³, а твёрдость по шкале Мооса - 2. Бесцветный прозрачный минерал со стеклянным блеском. Распространённый минерал соленосных толщ. Образуется при осаждении в замкнутых водоёмах, а также как продукт сгона на стенках кратеров вулканов. Составляет пласты в осадочных породах лагунных и морских фаций, штокоподобные тела в соляных куполах и тому подобных.
Каменная соль
Каменной солью называют осадочную горную породу из группы эвапоритов, состоящую более чем на 90 % из галита. Галит также часто называют каменной солью. Эта осадочная горная порода может быть бесцветной или снежно-белой, но чаще она окрашена примесями глин, талька (серый цвет), оксидами и гидроксидами железа (жёлтый, оранжевый, розовый, красный), битумами (бурая). Каменная соль содержит хлориды и сульфаты натрия, калия, магния и кальция, бромиды, иодиды, бораты, гипс, примеси карбонатно-глинистого материала, доломита, анкериту, магнезита, битумов и так далее .
По условиям формирования месторождений каменную соль подразделяют на следующие виды :
- рассолы современных соляных бассейнов
- соляные подземные воды
- залежи минеральных солей современных соляных бассейнов
- ископаемые залежи (важнейшие для промышленности).
Морская соль
Морская соль является смесью солей (хлориды , карбонаты , сульфаты и т. д.), образующейся при полном испарении морской воды. Среднее содержание солей в морской воде составляет:

Очищенная кристаллическая морская соль
При испарении морской воды при температуре от +20 до +35 °C в осадке сначала кристаллизуются наименее растворимые соли - карбонаты кальция и магния и сульфат кальция. Затем выпадают более растворимые сульфаты натрия и магния, хлориды натрия, калия и магния, и после них - сульфаты калия и магния. Последовательность кристаллизации солей и состав осадка может несколько варьироваться в зависимости от температуры, скорости испарения и других условий. В промышленности морскую соль получают из морской воды, в основном методом обычного выпаривания. Она отличается от каменной соли значительно большим содержанием других химических солей, минералов и различных микроэлементов, в первую очередь йода, калия, магния и марганца. Соответственно, она отличается от хлорида натрия и по вкусу - горько-солёный привкус ей придают соли магния. Она используется в медицине: при лечении кожных заболеваний, таких как псориаз . Как лечебное вещество в аптечной и обычной торговой сети, распространённым продуктом является соль из Мёртвого моря . В очищенном виде этот вид соли также предлагается в продуктовой торговой сети - как натуральная и богатая йодом пищевая .
Залежи
Залежи каменной соли найдены во всех геологических системах. Важнейшие из них сосредоточены в кембрийских , девонских , пермских и третичных отложениях. Каменная соль составляет мощные пластовые залежи и ядра сводчатых структур (соляных куполов и штоков), образует прослойки, линзы, гнезда и вкрапления в других породах . Среди озёрных месторождений России крупнейшие - Эльтонское , Баскунчак в Прикаспии, Кучукское озеро , Кулундинское озеро , Эбейты и другие озёра в Западной Сибири.
Производство
В древности технология добычи соли заключалась в том, что соляную рапу (раствор) вытаскивали лошадиным приводом из шахт, которые назывались «колодцами» или «окнами», и были достаточно глубокими - 60-90 м. Извлечённый солевой раствор выливали в особый резервуар - творило , откуда она через отверстия стекала в нижний резервуар, и системой жёлобов подавалась в деревянные башни. Там её разливали в большие чаны, на которых соль вываривали.
На Руси поморы вываривали соль на побережье Белого моря и называли её морянка . В 1137 году новгородский князь Святослав определил налог на соляные варницы :
Беломорской солью, называемой «морянкой», торговали по всей Российской империи до начала XX века, пока её не вытеснила более дешёвая поволжская соль.
Современная добыча хлорида натрия механизирована и автоматизирована. Соль массово добывается выпариванием морской воды (тогда её называют морской солью) или рассола с других ресурсов, таких как соляные источники и соляные озера, а также разработкой соляных шахт и добычей каменной соли.
Для добычи хлорида натрия из морской воды необходимы условия жаркого климата с низкой влажностью воздуха, наличие значительных низменных территорий, лежащих ниже уровня моря, или затопляемых приливом, слабая водопроницаемость почвы испарительных бассейнов, малое количество осадков в течение сезона активного испарения, отсутствие влияния пресных речных вод и наличие развитой транспортной инфраструктуры.
Мировое производство соли в 2009 году оценивается в 260 миллионов тонн. Крупнейшими мировыми производителями являются Китай (60,0 млн тонн), США (46,0 млн тонн), Германия (16,5 млн тонн), Индия (15,8 млн тонн) и Канада (14 млн тонн) .

Применение
В пищевой промышленности и кулинарии
Соль поваренная
В пищевой промышленности и кулинарии используют хлорид натрия, чистота которого должна быть не менее 97 %. Его применяют как вкусовую добавку и для консервирования пищевых продуктов. Такой хлорид натрия имеет товарное название поваренная соль , порой также употребляются названия пищевая, столовая, а также уточнение названия в зависимости от её происхождения - каменная, морская, и по составу добавок - йодированная, фторированная и т. д. Такая соль является кристаллическим сыпучим продуктом с солёным вкусом без привкуса, без запаха (за исключением йодированной соли), в котором не допускаются посторонние примеси, не связанные с методом добывания соли. Кроме хлорида натрия, поваренная соль содержит небольшое количество солей кальция, магния, калия, которые придают ей гигроскопичности и жёсткости. Чем меньше этих примесей в соли, тем выше её качество.
Выделяют сорта: экстра, высший, первый и второй. Массовая доля хлористого натрия в сортах, %:
- экстра - не менее 99,5;
- высший - 98,2;
- первый - 97,5;
- второй - 97,0.
Массовая доля влаги в выварочной соли сорта «экстра» 0,1 %, в высшем сорте - 0,7 %. Допускают добавки йодида калия (йодистого калия), йодата калия, фторидов калия и натрия. Массовая доля йода должна составлять (40,0 ± 15,0) × 10 −4 %, фтора (25,0 ± 5,0) × 10 −3 %. Цвет экстра и высшего сортов - белый, однако для первого и второго допускается серый, желтоватый, розовый и голубоватый оттенки в зависимости от происхождения соли. Пищевую поваренную соль производят молотой и сеяной. По размеру зёрен молотую соль подразделяют на номера: 0, 1, 2, 3. Чем больше номер, тем больше зерна соли.
В кулинарии хлорид натрия потребляют как важнейшую приправу. Соль имеет характерный вкус, без которого пища кажется человеку пресной. Такая особенность соли обусловлена физиологией человека. Однако зачастую люди потребляют соли больше, чем нужно для физиологических процессов.
В коммунальном хозяйстве. Техническая соль
Зимой хлорид натрия, смешанный с другими солями, песком или глиной - так называемая техническая соль - применяется как антифриз против гололёда. Ею посыпают тротуары, хотя это отрицательно влияет на кожаную обувь и техническое состояние автотранспорта ввиду коррозийных процессов.
Регенерация Nа-катионитовых фильтров
Nа-катионитовые фильтры широко применяются в установках умягчения воды всех мощностей при водоподготовке. Катионитным материалом на современных водоподготовительных установках служат в основном глауконит , полимерные ионообменные смолы и сульфированные угли. Наиболее распространены сульфокатионитные ионообменные смолы.
Регенерацию Nа-катионитовых фильтров осуществляют 6-10%-м раствором поваренной соли, в результате катионит переводится в Na-форму, регенерируется. Реакции идут по уравнениям:
C a R 2 + 2 N a C l → 2 N a R + C a C l 2 {\displaystyle {\mathsf {CaR_{2}+2NaCl\rightarrow 2NaR+CaCl_{2}}}} M g R 2 + 2 N a C l → 2 N a R + M g C l 2 {\displaystyle {\mathsf {MgR_{2}+2NaCl\rightarrow 2NaR+MgCl_{2}}}}Химическая промышленность
Соль, наряду с каменным углем, известняками и серой, образует «большую четвёрку» продуктов минерального сырья, которые являются важнейшими для химической промышленности . Из неё получают соду, хлор, соляную кислоту, гидроксид натрия, сульфат натрия и металлический натрий. Кроме этого соль используется также для промышленного получения легкорастворимого в воде хлората натрия, который является средством для уничтожения сорняков . Суммарное уравнение реакции электролиза горячего раствора хлорида натрия :
N a C l + 3 H 2 O → N a C l O 3 + 3 H 2 {\displaystyle {\mathsf {NaCl+3H_{2}O\rightarrow NaClO_{3}+3H_{2}}}}Получение хлора и гидроксида натрия
- на катоде как побочный продукт выделяется водород вследствие восстановления ионов H + , образованных в результате электролитической диссоциации воды:
- поскольку (вследствие практически полной электролитической диссоциации NaCl), хлор в растворе находится в виде хлорид-ионов, они окисляются на аноде до свободного хлора в виде газа:
- суммарная реакция:
Как видно из уравнения суммарной реакции, ещё одним продуктом является гидроксид натрия. Расход электроэнергии на 1 т хлора составляет примерно 2700 кВт × час. Полученный хлор при повышенном давлении сжижается в жёлтую жидкость уже при обычной температуре .
Если между анодом и катодом нет диафрагмы, то растворённый в воде хлор начинает реагировать с гидроксидом натрия, образуя хлорид и гипохлорит натрия NaClO :
2 N a O H + C l 2 → N a C l + N a O C l + H 2 O {\displaystyle {\mathsf {2NaOH+Cl_{2}\rightarrow NaCl+NaOCl+H_{2}O}}} N a + + e − → N a (H g) {\displaystyle {\mathsf {Na^{+}+e^{-}\rightarrow Na_{(Hg)}}}}Амальгаму позже разлагают горячей водой с образованием гидроксида натрия и водорода, а ртуть перекачивают насосом обратно в электролизер:
2 N a (H g) + 2 H 2 O → 2 N a O H + H 2 {\displaystyle {\mathsf {2Na_{(Hg)}+2H_{2}O\rightarrow 2NaOH+H_{2}}}}Суммарная реакция процесса такая же, как и в случае диафрагменного метода.
Получение металлического натрия
Металлический натрий получают электролизом расплава хлорида натрия. Происходят следующие процессы:
- на катоде выделяется натрий:
- на аноде выделяется хлор (как побочный продукт):
- суммарная реакция:
Ванна электролизера состоит из стального кожуха с футеровкой , графитового анода и кольцевого железного катода. Между катодом и анодом располагается сетчатая диафрагма. Для снижения температуры плавления NaCl (+800 °C), электролитом является не чистый хлорид натрия, а его смесь с хлоридом кальция CaCl 2 (40:60) с температурой плавления +580 °C. Металлический натрий, который собирается в верхней части катодного пространства, содержит до 5 % примесь кальция, но последний со временем почти полностью отделяется, поскольку его растворимость в жидком натрии при температуре его плавления (+371 K = 98 °C) составляет всего 0,01 %. С расходованием NaCl его постоянно добавляют в ванну. Затраты электроэнергии составляют примерно 15 кВт × ч на 1 кг натрия .
Получение соляной кислоты и сульфата натрия
Среди многих промышленных методов получения соляной кислоты, то есть водного раствора хлороводорода (HCl), применяется реакция обмена между хлоридом натрия и серной кислотой:
N a C l + H 2 S O 4 → N a H S O 4 + H C l {\displaystyle {\mathsf {NaCl+H_{2}SO_{4}\rightarrow NaHSO_{4}+HCl\uparrow }}} N a C l + N a H S O 4 → N a 2 S O 4 + H C l {\displaystyle {\mathsf {NaCl+NaHSO_{4}\rightarrow Na_{2}SO_{4}+HCl\uparrow }}}Первая реакция происходит в значительной степени уже при обычных условиях, а при слабом нагреве идёт почти до конца. Вторая происходит лишь при высоких температурах. Процесс осуществляется в специальных механизированных печах большой мощности. Хлороводород , который выделяется, обеспыливают, охлаждают и поглощают водой с образованием соляной кислоты. Как побочный продукт образуется сульфат натрия Na 2 SO 4 .
Этот метод применяется также для получения хлороводорода в лабораторных условиях.
Физические и физико-химические свойства
Температура плавления +800,8 °С, кипения +1465 °С.
Умеренно растворяется в воде, растворимость мало зависит от температуры: коэффициент растворимости NaCl (в граммах на 100 г воды) равен 35,9 при +21 °C и 38,1 при +80 °C. Растворимость хлорида натрия существенно снижается в присутствии хлороводорода, гидроксида натрия, солей - хлоридов металлов. Растворяется в жидком аммиаке, вступает в реакции обмена. В чистом виде хлорид натрия не гигроскопичен. Однако соль часто бывает загрязнена примесями (преимущественно ионами Ca 2+ , Mg 2+ и SO2−
4
), и такая соль на воздухе сыреет . Кристаллогидрат NaCl · 2H 2 O можно выделить при температуре ниже +0,15 °C .
Смесь измельчённого льда с мелким порошком хлорида натрия является эффективным охладителем. Так, смесь состава 30 г NaCl на 100 г льда охлаждается до температуры −20 °C. Это происходит потому, что водный раствор соли замерзает при температуре ниже 0 °C. Лёд, имеющий температуру около 0 °C, плавится в таком растворе, поглощая тепло окружающей среды.
Диэлектрическая проницаемость NaCl - 6,3
Плотность и концентрация водных растворов NaCl
| Концентрация, % | Концентрация, г/л | Плотность, г/мл |
|---|---|---|
| 1 | 10,05 | 1,005 |
| 2 | 20,25 | 1,012 |
| 4 | 41,07 | 1,027 |
| 6 | 62,47 | 1,041 |
| 8 | 84,47 | 1,056 |
| 10 | 107,1 | 1,071 |
| 12 | 130,2 | 1,086 |
| 14 | 154,1 | 1,101 |
| 16 | 178,5 | 1,116 |
| 18 | 203,7 | 1,132 |
| 20 | 229,5 | 1,148 |
| 22 | 256 | 1,164 |
| 24 | 283,2 | 1,18 |
| 26 | 311,2 | 1,197 |
Лабораторное получение и химические свойства
При действии серной кислоты выделяет хлороводород.
2 N a C l + H 2 S O 4 → N a 2 S O 4 + 2 H C l {\displaystyle {\mathsf {2NaCl+H_{2}SO_{4}\rightarrow Na_{2}SO_{4}+2HCl}}}С раствором нитрата серебра образует белый осадок хлорида серебра (качественная реакция на хлорид-ион).
N a C l + A g N O 3 → N a N O 3 + A g C l {\displaystyle {\mathsf {NaCl+AgNO_{3}\rightarrow NaNO_{3}+AgCl}}}В кристаллической решётке между атомами преобладает ионная химическая связь , что является следствием действия электростатического взаимодействия противоположных по заряду ионов.
См. также
- Поваренная соль - специя и пищевая добавка
- Галит - минерал
Примечания
- Натрия хлорид на сайте англ. National Institute of Standards and Technology ) (англ.)
- Некрасов Б. В. Основы общей химии. Т. 2. Изд. 3-е, испр. и доп., М. : Химия , 1973. - 688 с.; 270 табл.; 426 рис.; Список литературы, ссылок. С. 218
- Пифагор. Золотой канон. Фигуры эзотерики. - М. : Изд-во Эксмо, 2003. - 448 с. (Антология мудрости).
- Малая горная энциклопедия . В 3 т. = Мала гірнича енциклопедія / (На укр. яз.). Под ред. В. С. Белецкого . - Донецк: Донбасс, 2004. - ISBN 966-7804-14-3 .
- УНИАН: Морская соль для красоты и здоровья кожи
- Российское законодательство Х-XX веков. Законодательство Древней Руси. Т. 1. М. , 1984. С. 224-225.
- В переводе с поморской «говори» слово чрен (црен) означает четырёхугольный ящик, кованный из листового железа, а салга - котёл, в котором варили соль. Пузом в беломорских солеварнях называли мешок соли в два четверика, то есть, объёмом около 52 литров.
- Соль (PDF) , Геологический обзор США на сайте Программы минеральных ресурсов (англ.)


 Юнна мориц рассказы о чудесном Большой лошадиный секрет
Юнна мориц рассказы о чудесном Большой лошадиный секрет Строение атома, изотопы, распространение в земной коре водорода, кислорода, серы и азота Области применения водорода
Строение атома, изотопы, распространение в земной коре водорода, кислорода, серы и азота Области применения водорода Топик по английскому языку "George Washington - Джордж Вашингтон"
Топик по английскому языку "George Washington - Джордж Вашингтон"