Φυσικοχημικές μέθοδοι για τον προσδιορισμό της φαινόλης. Χημική εμπειρία - παίρνουμε φλουορεσκεΐνη Παρασκευή από χλωροβενζόλιο
Ρεσορκινόλη
Ποιοτικές αντιδράσεις
1. Ένα διάλυμα ρεσορκινόλης από 1 σταγόνα διαλύματος χλωριούχου σιδήρου παίρνει διαφορετικές αποχρώσεις του μπλε, έως σκούρο μωβ, χρώμα.
2. Με προσεκτική θέρμανση 0,5 g ρεζορκινόλης με 0,1 g τρυγικού οξέος και ισχυρού θειικού οξέος, εμφανίζεται ένα σκούρο κόκκινο καρμίνιο χρώμα.
3. Όταν η ρεσορκινόλη θερμαίνεται με φθαλικό ανυδρίτη, σχηματίζεται φλουορεσκεΐνη:

4. Όταν θερμαίνουμε μερικά χιλιοστόλιτρα διαλύματος ρεσορκινόλης 2% σε διάλυμα καυστικού αλκαλίου σε υδατόλουτρο και προσθέτουμε μερικές σταγόνες χλωροφόρμιου (ή διαλύματος ένυδρης χλωράλης), το μείγμα μετατρέπεται σε έντονο κόκκινο χρώμα (σε αντίθεση με υδροκινόνη και κατεχόλη), μετατρέπεται σε κιτρινωπό μετά την οξίνιση αραιωμένο οξικό οξύ.
5. Καθιζάνει βρωμιούχο νερό - βλέπε Ποσοτικοποίηση.
ποσοτικοποίηση
Ο βρωμομετρικός προσδιορισμός βασίζεται στο γεγονός ότι το βρώμιο αλληλεπιδρά σε περίσσεια με τη ρεσορκινόλη για να σχηματίσει τριβρωμιο-σορκινόλη:

Η περίσσεια βρωμίου προσδιορίζεται ιωδομετρικά.
Διαλύουμε 1 g ρεσορκινόλης σε νερό σε ογκομετρική φιάλη των 100 ml και συμπληρώνουμε μέχρι τη χαραγή. 25 ml αυτού του διαλύματος χύνονται σε φιάλη 500 ml με αλεσμένο πώμα, 50 ml μείγματος βρωμιούχου βρωμιδίου (2,7833 g βρωμιούχου καλίου και 50 g βρωμιούχου καλίου σε 1 λίτρο διαλύματος), 50 ml νερού, 5 ml υδροχλωρικού οξέος (σ.σ. βάρος 1,15) και αφήστε για ένα λεπτό, μετά από το οποίο προστέθηκαν άλλα 20 ml νερού και 1 g ιωδιούχου καλίου. Το υγρό αφήνεται για 5 λεπτά και το απελευθερωμένο ιώδιο τιτλοδοτείται με 0,1 N. διάλυμα θειοθειικού νατρίου (δείκτης - διάλυμα αμύλου). 1 ml 0,1 n. διάλυμα βρωμικού καλίου αντιστοιχεί σε 0,001835 g ρεσορκινόλης.
Resorcinum Resorcinum
m-Διοξυβενζόλιο
Η ρεσορκινόλη είναι μια διυδρική φαινόλη και είναι μια άχρωμη ή ελαφρώς ροζ ή κίτρινη βελονοειδής κρύσταλλοι ή κρυσταλλική σκόνη. Μερικές φορές το χρώμα των κρυστάλλων είναι σχεδόν καφέ. Αυτό οφείλεται σε ακατάλληλη αποθήκευση της ρεσορκινόλης, η οποία οξειδώνεται πολύ εύκολα. Σε αντίθεση με άλλες φαινόλες, η ρεσορκινόλη είναι πολύ εύκολα διαλυτή στο νερό, το αλκοόλ και εύκολα στον αιθέρα. Διαλυτό σε λιπαρά έλαια και γλυκερίνη. Είναι δύσκολο να διαλυθεί σε χλωροφόρμιο. Όταν θερμαίνεται, εξατμίζεται τελείως.
Η ρεζορκινόλη είναι αναπόσπαστο μέρος πολλών ρητινών και τανινών, αλλά λαμβάνεται συνθετικά - από βενζόλιο με τη μέθοδο της σουλφόνωσης και της αλκαλικής τήξης. Το βενζόλιο υποβάλλεται σε επεξεργασία με πυκνό θειικό οξύ για να δώσει το βενζόλιο μεταδι-σουλφονικό οξύ I.
Στη συνέχεια, το μείγμα αντίδρασης υποβάλλεται σε επεξεργασία με ασβέστη: το σουλφο-οξύ υπό αυτές τις συνθήκες σχηματίζει ένα υδατοδιαλυτό άλας ασβεστίου (II), η περίσσεια του θειικού οξέος απομακρύνεται με τη μορφή θειικού ασβεστίου:

Η προκύπτουσα ρεσορκινόλη καθαρίζεται με απόσταξη.
Η ρεσορκινόλη, όπως και άλλες φαινόλες, οξειδώνεται εύκολα και είναι η ίδια αναγωγικός παράγοντας. Μπορεί να ανακτήσει ασήμι από διάλυμα αμμωνίας νιτρικού αργύρου.
Η ρεσορκινόλη δίνει όλες τις αντιδράσεις που είναι χαρακτηριστικές των φαινολών, συμπεριλαμβανομένων εκείνων με φορμαλίνη-θειικό οξύ (ένα κόκκινο ίζημα σχηματίζεται στον πυθμένα του δοκιμαστικού σωλήνα). Μια ειδική αντίδραση στη ρεσορκινόλη, που τη διακρίνει από όλες τις άλλες φαινόλες, είναι η αντίδραση της σύντηξής της με φθαλικό ανυδρίτη παρουσία πυκνού θειικού οξέος για να σχηματιστεί φλουορεσκεΐνη, ένα κιτρινοκόκκινο διάλυμα με πράσινο φθορισμό (αντίδραση φαρμακοποιίας).

Η αντισηπτική δράση της ρεσορκινόλης είναι πιο έντονη από αυτή της μονοϋδρικής φαινόλης. Αυτό οφείλεται στις ισχυρότερες αποκαταστατικές του ιδιότητες.
Η αναγωγική ικανότητα της ρεσορκινόλης εκδηλώνεται ιδιαίτερα σε ένα αλκαλικό μέσο.
Εφαρμόζεται εξωτερικά για δερματικές παθήσεις (έκζεμα, μυκητιάσεις κ.λπ.) σε μορφή υδατικών και αλκοολούχων διαλυμάτων 2-5% και αλοιφών 5-10-20%.
Φυλάσσεται σε καλά κλεισμένα πορτοκαλί γυάλινα βάζα (το φως διεγείρει την οξείδωση).
Παραλαβή.Λαμβάνεται από βενζόλιο.
Περιγραφή. Λευκό ή λευκό με ελαφρά κιτρινωπή απόχρωση κρυσταλλική σκόνη με ελαφρά χαρακτηριστική οσμή. Υπό την επίδραση του φωτός και του αέρα, σταδιακά γίνεται ροζ.
Διαλυτότητα. Πολύ εύκολα διαλυτό σε νερό και 95% αλκοόλη, ελεύθερα διαλυτό σε αιθέρα, πολύ ελαφρά διαλυτό σε χλωροφόρμιο, διαλυτό σε γλυκερίνη και λιπαρό έλαιο.
Αυθεντικότητα.
1) Όταν στο διάλυμα του φαρμάκου προστίθεται διάλυμα χλωριούχου σιδήρου, εμφανίζεται ένα μπλε-ιώδες χρώμα, που μετατρέπεται από την προσθήκη διαλύματος αμμωνίας σε καστανοκίτρινο.
2) Κατά τη σύντηξη πολλών κρυστάλλων του φαρμάκου με περίσσεια φθαλικού ανυδρίτη σε ένα κύπελλο πορσελάνης, λαμβάνεται ένα κιτρινοκόκκινο τήγμα. Όταν το τήγμα διαλύεται σε διάλυμα καυστικής σόδας, εμφανίζεται ένας έντονος πράσινος φθορισμός.
Θερμοκρασία τήξης 109-112°.
ποσοτικοποίηση.
βρωμομετρική μέθοδος ( επιλογή πίσω τιτλοδότησης).
Ένα ακριβές δείγμα του φαρμάκου τοποθετείται σε ογκομετρική φιάλη, διαλύεται σε νερό, προστίθεται περίσσεια 0,1 Μ KBrO 3 , KBr, H 2 SO 4, στη συνέχεια προστίθεται διάλυμα ιωδιούχου καλίου στο μείγμα, το μείγμα ανακινείται έντονα και αφήνουμε για 10 λεπτά σε σκοτεινό μέρος. Μετά από αυτό, προστίθεται χλωροφόρμιο και το απελευθερωμένο ιώδιο τιτλοδοτείται με διάλυμα θειοθειικού νατρίου 0,1 Μ μέχρι να γίνει άχρωμο.
KBrO 3 + 5KBr + 3H 2 SO 4 → 3Br 2 + 3K 2 SO 4 + 3H 2 O
Br 2 + 2KJ = J 2 + 2KBr
J 2 + 2Na 2 S 2 O 3 \u003d 2NaJ + Na 2 S 4 O 6
UCH = 1/6, τύπος αντίστροφης τιτλοδότησης
Αποθήκευση. Σε καλά κλεισμένα πορτοκαλί γυάλινα βάζα.
Εφαρμογή.Αντισηπτικό, για δερματικές παθήσεις, εκζέματα, εξωτερικά σε αλοιφές, πάστες ή διαλύματα, σπάνια χρησιμοποιείται εσωτερικά ως απολυμαντικό του γαστρεντερικού συστήματος.
Ρεσορκινόλη ασύμβατεςμε θυμόλη, μενθόλη, ασπιρίνη, καμφορά (σχηματίζει υγρά μείγματα).
Αποσυντίθεται εύκολα (σε αλκαλικό περιβάλλον) - οξειδώνεται, επαναφέρει τα παρασκευάσματα υδραργύρου στο μέταλλο.
Εκ. Εκπαιδευτικό και μεθοδολογικό εγχειρίδιο για ενδοφαρμακευτικό έλεγχο: οφθαλμικές σταγόνες - διάλυμα ρεσορκινόλης 1%.
Αρωματικά οξέα
Τα αρωματικά οξέα είναι οργανικές ενώσεις που έχουν μια λειτουργική ομάδα -COOH και έναν δακτύλιο βενζολίου ως ρίζα.
Ο απλούστερος εκπρόσωπος είναι το βενζοϊκό οξύ.
Οι ιδιότητες των αρωματικών οξέων καθορίζονται από:
1. Οι ιδιότητες του πυρήνα του βενζολίου, οι οποίες χαρακτηρίζονται από:
1.1. Αντιδράσεις υποκατάστασης υδρογόνου στον πυρήνα για ομάδες αλογόνου, NO 2 - , SO 3 2 - -.
2. Ιδιότητες - Ομάδες COOH.
2.1. Σχηματίστε άλατα με αλκάλια, βαρέα μέταλλα, αλκάλια, ανθρακικά άλατα αλκαλιμετάλλων.
2.2. Σχηματίστε ανυδρίτες, αλογονίδια οξέων, αμίδια.
2.3. Σχηματίζονται εστέρες παρουσία πυκνού θειικού οξέος.
3. Η αντίδραση του μέσου των αρωματικών οξέων προσδιορίζεται με δείκτες (όξινο).
Τα ελεύθερα αρωματικά οξέα χρησιμοποιούνται μόνο εξωτερικά, γιατί. διασπώνται σε ιόντα, διασπούν το ιόν Η+, το οποίο έχει ερεθιστική δράση, ακόμη και καυτηρίαση. Επιπλέον, μπαίνοντας στο αίμα, αλλάζει τη δομή των κυττάρων του αίματος, επομένως μόνο άλατα και εστέρες αρωματικών οξέων συνταγογραφούνται μέσα.
Στόχος της εργασίας
Στόχος της εργασίας είναι η διεξαγωγή αντιδράσεων οξείδωσης και συμπύκνωσης για τη φαινόλη και τα παράγωγά της.
Θεωρητικό μέρος
Οι φαινόλες είναι αρωματικές ενώσεις που έχουν ομάδες υδροξυλίου άμεσα συνδεδεμένες με τον αρωματικό πυρήνα. Ανάλογα με τον αριθμό των υδροξυλίων, διακρίνονται οι μονατομικές, διυδρικές και πολυϋδρικές φαινόλες. Το απλούστερο από αυτά, το οξυβενζόλιο, ονομάζεται φαινόλη. Τα οξυ-παράγωγα του τολουολίου (μεθυλφαινόλες) ονομάζονται ορθο-, μετα- και παρακρεσόλες, και τα οξυ-παράγωγα των ξυλενίων ονομάζονται ξυλενόλες. Οι φαινόλες της σειράς ναφθαλίνης ονομάζονται ναφθόλες. Οι απλούστερες διατομικές φαινόλες ονομάζονται: ο - διοξυβενζόλιο - πυροκατεχίνη, m - διοξυβενζόλιο - ρεσορκινόλη, ν-διοξυβενζόλιο - υδροκινόνη.
Πολλές φαινόλες οξειδώνονται εύκολα, συχνά καταλήγοντας σε ένα πολύπλοκο μείγμα προϊόντων. Ανάλογα με τον οξειδωτικό παράγοντα και τις συνθήκες αντίδρασης, μπορούν να ληφθούν διάφορα προϊόντα. Έτσι, κατά την οξείδωση σε φάση ατμού (t = 540 0) του ο-ξυλενίου, λαμβάνεται φθαλικός ανυδρίτης. Μια ποιοτική αντίδραση στις φαινόλες είναι μια δοκιμή με διάλυμα χλωριούχου σιδήρου και σχηματίζεται ένα έγχρωμο ιόν. Η φαινόλη δίνει ένα κόκκινο-ιώδες χρώμα, οι κρεσόλες - μπλε, άλλες φαινόλες - πράσινες.
Η αντίδραση συμπύκνωσης είναι μια ενδομοριακή ή διαμοριακή διαδικασία σχηματισμού ενός νέου δεσμού C-C, που συνήθως προχωρά με τη συμμετοχή αντιδραστηρίων συμπύκνωσης, ο ρόλος των οποίων μπορεί να είναι πολύ διαφορετικός: έχει μια σειρά από καταλυτικές επιδράσεις, δίνει ενδιάμεσα αντιδραστικά προϊόντα, απλώς δεσμεύει το διαχωρισμένο σωματίδιο, μετατοπίζοντας την ισορροπία στο σύστημα.
Η αντίδραση συμπύκνωσης με την αποβολή του νερού καταλύεται από μια ποικιλία αντιδραστηρίων: ισχυρά οξέα, ισχυρά αλκάλια (υδροξείδια, αλκοολικά, αμίδια, υδρίδια αλκαλιμετάλλων, αμμωνία, πρωτοταγείς και δευτεροταγείς αμίνες).
Εντολή εργασίας
Στην εργασία αυτή ελέγχουμε την πιθανότητα οξείδωσης των φαινολών και σχηματισμού φθαλεϊνών από την αντίδραση συμπύκνωσης.
3.1 Οξείδωση φαινόλης και ναφθόλης
Η οξείδωση πραγματοποιείται με διάλυμα υπερμαγγανικού καλίου παρουσία διαλύματος ανθρακικού νατρίου (σόδα).
3.1.1 Εξοπλισμός και αντιδραστήρια:
δοκιμαστικοι ΣΩΛΗΝΕΣ;
πιπέτες?
Φαινόλη - υδατικό διάλυμα;
Ναφθόλη - υδατικό διάλυμα.
Υπερμαγγανικό κάλιο (0,5% υδατικό διάλυμα);
Ανθρακικό νάτριο (5% υδατικό διάλυμα);
3.1.2 Διεξαγωγή του πειράματος:
α) βάλτε 1 ml υδατικού διαλύματος φαινόλης ή ναφθόλης σε δοκιμαστικό σωλήνα.
β) Προσθέστε 1 ml διαλύματος ανθρακικού νατρίου (σόδα).
γ) Προσθέστε στάγδην ένα διάλυμα υπερμαγγανικού καλίου ενώ ανακινείτε τον δοκιμαστικό σωλήνα. Παρατηρήστε την αλλαγή χρώματος του διαλύματος.
Η οξείδωση των φαινολών συνήθως προχωρά σε διαφορετικές κατευθύνσεις και οδηγεί στο σχηματισμό ενός πολύπλοκου μείγματος ουσιών. Η ευκολότερη οξειδωσιμότητα των φαινολών, σε σύγκριση με τους αρωματικούς υδρογονάνθρακες, οφείλεται στην επίδραση της ομάδας υδροξυλίου, η οποία αυξάνει απότομα την κινητικότητα των ατόμων υδρογόνου σε άλλα άτομα άνθρακα του δηλητηρίου του βενζολίου.
3.2 Σχηματισμός φθαλεϊνών.
3.2.1 Λήψη φαινολοφθαλεΐνης.
Η φαινολοφθαλεΐνη σχηματίζεται από την αντίδραση συμπύκνωσης της φαινόλης με τον φθαλικό ανυδρίτη παρουσία πυκνού θειικού οξέος.
Ο φθαλικός ανυδρίτης συμπυκνώνεται με φαινόλες για να δώσει παράγωγα τριφαινυλαιθανίου. Η συμπύκνωση συνοδεύεται από απομάκρυνση του νερού λόγω του οξυγόνου μιας από τις ομάδες καρβονυλίου του ανυδρίτη και των κινητών ατόμων υδρογόνου των πυρήνων βενζολίου δύο μορίων φαινόλης. Η εισαγωγή αφυδατωτικών παραγόντων όπως το πυκνό θειικό οξύ διευκολύνει πολύ αυτή τη συμπύκνωση.
Η φαινόλη σχηματίζει φαινολοφθαλεΐνη με την ακόλουθη αντίδραση:


 / \ /
/ \ /

 H H C
H H C
3.2.1.1 Εξοπλισμός και αντιδραστήρια:
δοκιμαστικοι ΣΩΛΗΝΕΣ;
πιπέτες?
Ηλεκτρική σόμπα;
Φθαλικός ανυδρίτης;
Θειικό οξύ αραιωμένο 1:5;
3.2.1.2 Διεξαγωγή του πειράματος:
β) προσθέστε περίπου διπλάσια ποσότητα φαινόλης στον ίδιο δοκιμαστικό σωλήνα.
γ) ανακινήστε το περιεχόμενο του σωλήνα αρκετές φορές και προσθέστε προσεκτικά 3-5 σταγόνες πυκνού θειικού οξέος σε αυτό, συνεχίζοντας να ανακινείτε.
δ) ζεστάνετε τον δοκιμαστικό σωλήνα σε ηλεκτρική κουζίνα μέχρι να εμφανιστεί ένα σκούρο κόκκινο χρώμα.
ε) Ψύξτε τον δοκιμαστικό σωλήνα και προσθέστε 5 ml νερού σε αυτόν.
στ) προσθέστε ένα αλκαλικό διάλυμα στάγδην στο διάλυμα που προκύπτει και παρατηρήστε την αλλαγή χρώματος.
ζ) μετά την αλλαγή του χρώματος, προσθέστε μερικές σταγόνες αραιού θειικού οξέος στο περιεχόμενο του δοκιμαστικού σωλήνα μέχρι να επιστρέψει το αρχικό χρώμα ή μέχρι να αποχρωματιστεί.
3.2.2 Παρασκευή φλουορεσκεΐνης.
Η φθορεσκίνη σχηματίζεται από την αντίδραση συμπύκνωσης της ρεσορκινόλης με φθαλικό ανυδρίτη παρουσία πυκνού θειικού οξέος.
Οι διατομικές φαινόλες με ομάδες υδροξυλίου στη μετα-θέση, μπαίνοντας σε συμπύκνωση, απελευθερώνουν δύο μόρια νερού, το ένα λόγω του οξυγόνου μιας από τις καρβονυλικές ομάδες του ανυδρίτη και τα κινητά άτομα υδρογόνου των πυρήνων βενζολίου δύο μορίων φαινόλης. το δεύτερο μόριο νερού απελευθερώνεται εις βάρος των υδροξυλομάδων δύο μορίων φαινόλης για να σχηματίσει έναν εξαμελή δακτύλιο.
Η ρεσορκινόλη σχηματίζει φλουορεσκεΐνη με την ακόλουθη αντίδραση:
Ω Ω Ω Ω ΧΟ Ω


 / \ / \ /
/ \ / \ /

 H H C
H H C
3.2.1.1 Εξοπλισμός και αντιδραστήρια:
δοκιμαστικοι ΣΩΛΗΝΕΣ;
πιπέτες?
Ηλεκτρική σόμπα;
Φθαλικός ανυδρίτης;
Ρεζορκινόλη;
Θειικό οξύ συμπυκνωμένο;
Διάλυμα καυστικού νατρίου (5-10%);
3.2.2.1 Διεξαγωγή του πειράματος:
α) ζυγίζονται 0,1-0,3 g φθαλικού ανυδρίτη και τοποθετούνται σε δοκιμαστικό σωλήνα.
β) Προσθέστε περίπου διπλάσια ποσότητα ρεσορκινόλης στο ίδιο σωληνάριο και ανακατέψτε ανακινώντας.
γ) Προσθέστε προσεκτικά 3-5 σταγόνες πυκνού θειικού οξέος στο περιεχόμενο του δοκιμαστικού σωλήνα.
δ) Θερμάνετε το μείγμα στον δοκιμαστικό σωλήνα μέχρι να εμφανιστεί ένα σκούρο κόκκινο χρώμα. Ζεσταίνετε σε ηλεκτρική κουζίνα.
ε) ψύξτε το περιεχόμενο του δοκιμαστικού σωλήνα και προσθέστε 5 ml νερού σε αυτό.
στ) Ρίξτε 2-3 σταγόνες από το προκύπτον διάλυμα σε καθαρό δοκιμαστικό σωλήνα, προσθέστε 1 ml αλκαλικού διαλύματος και αραιώστε με μεγάλη ποσότητα νερού. Προσέξτε για αλλαγή χρώματος.
3.2.3 Σχηματισμός ούρων
Το αυρίνη λαμβάνεται με τη συμπύκνωση του οξαλικού οξέος με φαινόλη παρουσία θειικού οξέος.
Όταν θερμαίνεται παρουσία θειικού οξέος, το οξαλικό οξύ συμπυκνώνεται με τρία μόρια φαινόλης, διασπώντας το νερό και το μονοξείδιο του άνθρακα για να σχηματίσει ουρίνη.
 |
|||
 |
|||
 H-O- - H H - -OH
H-O- - H H - -OH
 -Η. OHO=
-Η. OHO=
 | . C \u003d O + 3H 2 O + CO
| . C \u003d O + 3H 2 O + CO
 H-C
H-C
3.2.3.1. Εξοπλισμός και αντιδραστήρια:
δοκιμαστικοι ΣΩΛΗΝΕΣ;
πιπέτες?
Οξαλικό οξύ;
Θειικό οξύ συμπυκνωμένο;
3.2.3.2 Διεξαγωγή του πειράματος:
α) ζυγίζει 0,02-0,05 g οξαλικού οξέος και περίπου διπλάσια ποσότητα φαινόλης.
β) Τοποθετήστε και τα δύο αντιδραστήρια σε δοκιμαστικό σωλήνα και ανακατέψτε ανακινώντας.
γ) προσθέστε 1-2 σταγόνες πυκνού θειικού οξέος στον δοκιμαστικό σωλήνα.
δ) Ζεστάνετε προσεκτικά τον δοκιμαστικό σωλήνα με το μείγμα μέχρι να αρχίσει ο βρασμός και να εμφανιστεί ένα έντονο κίτρινο χρώμα.
ε) Ψύξτε τον δοκιμαστικό σωλήνα, προσθέστε 3-4 ml νερό σε αυτόν και ανακινήστε. Παρατηρήστε το αναδυόμενο χρώμα.
στ) προσθέστε μερικές σταγόνες αλκαλικού διαλύματος στο διάλυμα που προκύπτει και παρατηρήστε την αλλαγή χρώματος.
3.3 Αποσύνθεση της ουρίας (αμίδιο καρβομικού οξέος) όταν θερμαίνεται.
Όταν θερμαίνεται πάνω από το σημείο τήξης, η ουρία αποσυντίθεται με την απελευθέρωση αμμωνίας. Σε θερμοκρασία 150 0 - 160 0 C, δύο μόρια ουρίας διασπούν ένα μόριο αμμωνίας και δίνουν ένα διουρικό που είναι άμεσα διαλυτό σε ζεστό νερό:
H 2 N-OO-NH 2 + H-NH-OO-NH 2 H 2 N-CO-NH-CO-NH 2 + NH 3
Η διουρία χαρακτηρίζεται από το σχηματισμό μιας έντονο κόκκινου συμπλόκου ένωσης σε αλκαλικό διάλυμα με άλατα χαλκού, η οποία έχει την ακόλουθη σύνθεση σε διάλυμα υδροξειδίου του νατρίου:
(NH 2 CO NH CONH 2) 2 * 2NaOH * Cu (OH) 2
3.3.1 Εξοπλισμός και αντιδραστήρια:
δοκιμαστικοι ΣΩΛΗΝΕΣ;
Ηλεκτρική σόμπα;
Ουρία (καρβαμίδιο);
Διάλυμα καυστικού νατρίου (5-7%);
Διάλυμα θειικού χαλκού (1%).
3.3.2 Διεξαγωγή του πειράματος:
α) ζυγίστε 0,2-0,3 g ουρίας και τοποθετήστε σε στεγνό δοκιμαστικό σωλήνα.
β) θερμάνετε τον δοκιμαστικό σωλήνα σε ηλεκτρική κουζίνα.
γ) παρατηρήστε τις συνεχιζόμενες αλλαγές: τήξη, απελευθέρωση αμμωνίας, στερεοποίηση.
δ) ψύξτε τον δοκιμαστικό σωλήνα.
ε) Προσθέστε 1-2 ml ζεστού νερού σε ψυχόμενο δοκιμαστικό σωλήνα, ανακινήστε τον και αδειάστε τον σε άλλο δοκιμαστικό σωλήνα.
στ) Προσθέστε 3-4 σταγόνες διαλύματος υδροξειδίου του νατρίου στο θολό διάλυμα που προκύπτει μέχρι να γίνει διαφανές. Στη συνέχεια, προσθέστε μια σταγόνα διαλύματος θειικού χαλκού και παρατηρήστε την αλλαγή χρώματος (εμφανίζεται ένα όμορφο μωβ χρώμα).
Παρόμοιες πληροφορίες.
Μια οργανική ουσία από την ομάδα των φαινολών, μια απλή διατομική φαινόλη. Μεταξύ των χημικών, χρησιμοποιούνται επίσης τα ονόματα ρεσορκινόλη και 1,3-διυδροξυβενζόλιο. Ο τύπος της ρεσορκινόλης είναι παρόμοιος με τους τύπους της υδροκινόνης και της κατεχόλης, η διαφορά είναι στη δομή του μορίου. στο πώς συνδέονται οι ομάδες ΟΗ.
Ιδιότητες
Η ουσία είναι άχρωμοι κρύσταλλοι σε σχήμα βελόνας ή λευκή κρυσταλλική σκόνη με έντονη φαινολική οσμή. Μερικές φορές η σκόνη μπορεί να έχει ροζ ή κιτρινωπό χρώμα. Εάν έχει έντονο χρώμα, γίνει ροζ-πορτοκαλί ή καφέ, σημαίνει ότι το αντιδραστήριο αποθηκεύτηκε λανθασμένα και οξειδώθηκε. Η ρεσορκινόλη είναι εύφλεκτη. Διαλύεται καλά σε νερό, διαιθυλαιθέρα, αιθυλική αλκοόλη, ακετόνη. Μπορεί να διαλυθεί σε έλαια, γλυκερίνη. Σχεδόν αδιάλυτο σε χλωροφόρμιο, δισουλφίδιο του άνθρακα, βενζόλιο.
Το αντιδραστήριο εμφανίζει τις χημικές ιδιότητες των φαινολών. Ισχυρός αναγωγικός παράγοντας, που οξειδώνεται εύκολα. Αντιδρά με αλκάλια, σχηματίζοντας φαινολικά άλατα. με αμμωνία, αλογόνα, με ισχυρά οξέα (για παράδειγμα, με νιτρικό, θειικό, πικρικό, παγόμορφο οξικό).

Για τον ποιοτικό προσδιορισμό της ρεσορκινόλης, χρησιμοποιούνται οι ακόλουθες αντιδράσεις:
- με χλωριούχο σίδηρο - το διάλυμα γίνεται βαθύ μωβ, σχεδόν μαύρο.
- σύντηξη με φθαλικό ανυδρίτη παρουσία καταλύτη οδηγεί στο σχηματισμό μιας χαρακτηριστικής έγχρωμης, φθορίζουσας πράσινης ουσίας - φλουορεσκεΐνης. Η ίδια η φλουορεσκίνη έχει ένα κιτρινοκόκκινο χρώμα του διαλύματος (η αντίδραση διακρίνει τη ρεσορκινόλη από άλλες φαινόλες).
Η σκόνη ρεσορκινόλης και ιδιαίτερα οι ατμοί της ερεθίζουν το δέρμα, τα αναπνευστικά όργανα και τους βλεννογόνους των ματιών. Η εισπνοή ατμών και σκόνης του αντιδραστηρίου προκαλεί βήχα, ναυτία, αίσθημα παλμών, ζάλη, επομένως πρέπει να εργαστείτε με ρεσορκινόλη χρησιμοποιώντας αναπνευστήρες ή μάσκες, γυαλιά, σε φόρμες, σε αεριζόμενο χώρο. Εάν υπάρχει υποψία δηλητηρίασης, το σημείο έκθεσης στο αντιδραστήριο θα πρέπει να πλυθεί με άφθονο νερό, το θύμα θα πρέπει να βγαίνει στον καθαρό αέρα και να καλείται γιατρός.
Αποθηκεύστε τη ρεσορκινόλη σε σφραγισμένο δοχείο, σε σκοτεινά, ξηρά, δροσερά δωμάτια, αυστηρά χωριστά από εύφλεκτες ουσίες.
Εφαρμογή
Η ρεζορκινόλη είναι σε ζήτηση στη χημική βιομηχανία ως πρώτη ύλη  για την παραγωγή τεχνητών βαφών, φλουορεσκεΐνης, ρητινών ρεσορκινόλης-φορμαλδεΰδης, διαλυτών, σταθεροποιητών, πλαστικοποιητών και απορροφητών υπεριώδους ακτινοβολίας για πλαστικά.
για την παραγωγή τεχνητών βαφών, φλουορεσκεΐνης, ρητινών ρεσορκινόλης-φορμαλδεΰδης, διαλυτών, σταθεροποιητών, πλαστικοποιητών και απορροφητών υπεριώδους ακτινοβολίας για πλαστικά.
- Στην αναλυτική χημεία, χρησιμοποιείται σε χρωματομετρικές μελέτες. Με τη βοήθειά του προσδιορίζεται η περιεκτικότητα σε ψευδάργυρο, μόλυβδο, υδατάνθρακες, φουρφουράλη, λιγνίνη κ.λπ.
- Στη βιομηχανία καουτσούκ.
- Στη βιομηχανία γούνας, ως βαφή για γούνες.
- Χρησιμοποιείται ευρέως στην ιατρική και τη φαρμακευτική. Χρησιμοποιείται ως απολυμαντικό, καυτηριαστικό, επουλωτικό πληγών, ανθελμινθικό. Περιλαμβάνεται στη σύνθεση διαλυμάτων και αλοιφών για τη θεραπεία διαφόρων, συμπεριλαμβανομένων μυκητιακών και πυωδών, δερματικών παθήσεων. ακμή, σμηγματόρροια, δερματίτιδα, έκζεμα, κηλίδες ηλικίας.
- Για την απόκτηση εκρηκτικών.
 Μετατροπή δεκαδικού κλάσματος σε συνηθισμένο κλάσμα και αντίστροφα: κανόνας, παραδείγματα
Μετατροπή δεκαδικού κλάσματος σε συνηθισμένο κλάσμα και αντίστροφα: κανόνας, παραδείγματα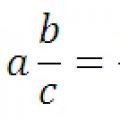 Μετατροπή δεκαδικών αριθμών σε κοινά κλάσματα
Μετατροπή δεκαδικών αριθμών σε κοινά κλάσματα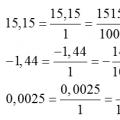 Μετατροπή συνηθισμένου κλάσματος σε δεκαδικό κλάσμα και αντίστροφα, κανόνες, παραδείγματα
Μετατροπή συνηθισμένου κλάσματος σε δεκαδικό κλάσμα και αντίστροφα, κανόνες, παραδείγματα