Формула марганца структурная химическая. Марганец: основные характеристики, производство и применение вещества
ОПРЕДЕЛЕНИЕ
Марганец - двадцать пятый элемент Периодической таблицы. Обозначение - Mn от латинского «manganum». Расположен в четвертом периоде, VIIB группе. Относится к металлам. Заряд ядра равен 25.
Марганец принадлежит к довольно распространенным элементам, составляя 0,1% (масс.) земной коры. Из соединений, содержащих марганец, наиболее часто встречается минерал пиролюзит, представляющий собой диоксид марганца MnO 2 . Большое значение имеют также минералы гаусманит Mn 3 O 4 и браунитMn 2 O 3 .
В виде простого вещества марганец представляет собой серебристо-белый (рис. 1) твердый хрупкий металл. Его плотность 7,44 г/см 3 , температура плавления 1245 o С.
Рис. 1. Марганец. Внешний вид.
Атомная и молекулярная масса марганца
Относительной молекулярная масса вещества (M r) - это число, показывающее, во сколько раз масса данной молекулы больше 1/12 массы атома углерода, а относительная атомная масса элемента (A r) — во сколько раз средняя масса атомов химического элемента больше 1/12 массы атома углерода.
Поскольку в свободном состоянии марганец существует в виде одноатомных молекул Mn, значения его атомной и молекулярной масс совпадают. Они равны 54,9380.
Аллотропия и аллотропные модификации марганца
Известны четыре кристаллические модификации марганца, каждая из которых термодинамически устойчива в определенном интервале температур. Ниже 707 o С устойчив α-марганец, имеющий сложную структуру - в его элементарную ячейку входят 58 атомов. Сложность структуры марганца при температурах ниже 707 o С обусловливают его хрупкость.
Изотопы марганца
Известно, что в природе марганец может находиться в виде единственного стабильного изотопа 55 Mn. Массовое число равно 55, ядро атома содержит двадцать пять протонов и тридцать нейтронов.
Существуют искусственные изотопы марганца с массовыми числами от 44-х до 69-ти, а также семь изомерных состояний ядер. Наиболее долгоживущим изотопом среди вышеперечисленных является 53 Mn с периодом полураспада равным 3,74 млн. лет.
Ионы марганца
На внешнем энергетическом уровне атома марганца имеется семь электронов, которые являются валентными:
1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 4s 2 .
В результате химического взаимодействия марганец отдает свои валентные электроны, т.е. является их донором, и превращается в положительно заряженный ион:
Mn 0 -2e → Mn 2+ ;
Mn 0 -3e → Mn 3+ ;
Mn 0 -4e → Mn 4+ ;
Mn 0 -6e → Mn 6+ ;
Mn 0 -7e → Mn 7+ .
Молекула и атом марганца
В свободном состоянии марганец существует в виде одноатомных молекул Mn. Приведем некоторые свойства, характеризующие атом и молекулу марганца:
Сплавы марганца
Марганец применяется главным образом в производстве легированных сталей. Марганцовистая сталь, содержащая до 15% Mn, обладает высокими твердостью и прочностью. Из неё изготовляют рабочие части дробильных машин, шаровых мельниц, железнодорожные рельсы. Кроме того, марганец входит в состав сплавов на основе магния; он повышает их стойкость против коррозии. Сплав меди с марганцем и никелем - манганин обладает низким температурным коэффициентом электрического сопротивления. В небольших количествах марганец входит во многие сплавы алюминия.
Примеры решения задач
ПРИМЕР 1
| Задание | Марганец получают восстановлением кремнием оксида марганца (III). Технический оксид массой 20 г (массовая доля примесей равна 5,2%) восстановили до металла. Рассчитайте массу полученного марганца. |
| Решение | Запишем уравнение реакции восстановления оксида марганца (III) кремнием до марганца:
2Mn 2 O 3 + 3Si = 3SiO 2 + 4Mn. Рассчитаем массу оксида марганца (III) без примесей: ω pure (Mn 2 O 3) = 100% — ω impurity ; ω pure (Mn 2 O 3) = 100% — 5,2 = 94,8% = 0,984. m pure (Mn 2 O 3) = m impurity (Mn 2 O 3) × ω pure (Mn 2 O 3) / 100%; m pure (Mn 2 O 3) = 20 × 0,984 = 19,68 г. Определим количество вещества оксида марганца (III) (молярная масса - 158 г/моль): n (Mn 2 O 3) = m (Mn 2 O 3) / M (Mn 2 O 3); n (Mn 2 O 3) = 19,68 / 158 = 0,12 моль. Согласно уравнению реакции n(Mn 2 O 3) :n(Si) = 2:3, значит, n(Si) = 3/2×n(Mn 2 O 3) = 3/2×0,12 = 0,2 моль. Тогда масса кремния будет равна (молярная масса - 28 г/моль): m (Si) = n (Si) × M (Si); m (Si) = 0,2 × 28 = 5,6 г. |
| Ответ | Масса кремния 5,6 г |
ПРИМЕР 2
| Задание | Вычислите массу перманганата калия, который необходим для окисления сульфита калия массой 7,9 г в нейтральной среде. |
| Решение | Запишем уравнение реакции окисления сульфита калия перманганатом калия в нейтральной среде:
2KMnO 4 + 3K 2 SO 3 + H 2 O = 2MnO 2 + 3K 2 SO 4 + 2KOH. Рассчитаем число моль сульфита калия (молярная масса - 158 г/моль): n (K 2 SO 3) = m (K 2 SO 3) / M (K 2 SO 3); n (K 2 SO 3) = 7,9 / 158 = 0,05 моль. Согласно уравнению реакции n(K 2 SO 3) :n(KMnO 4) = 3:2, значит, n(KMnO 4) = 2/3 × n(K 2 SO 3) = 2/3 × 0,05 = 0,03 моль. Масса перманганата калия необходимого для окисления сульфита калия в нейтральной среде равна (молярная масса - 158г/моль): m (KMnO 4) = n (KMnO 4) × M (KMnO 4); m (KMnO 4) = 0,03 × 158 = 4,74 г. |
| Ответ | Масса перманганата калия равна 4,74 г |
Выполнил : студент первого курса
инженерного факультета
15 б группы
Кошманов В.В.
Проверил: Харченко Н.Т.
Великие Луки 1998г.
Историческая справка. 3
Распространение в природе. 3
Физические и химические свойства. 3
Соединения двухвалентного марганца. 4
Соединения четырёхвалентного марганца. 4
Соединения шестивалентного марганца. 5
Соединения семивалентного марганца. 5
Получение. 6
Применение марганца и его соединений. 6
Литература. 7
Историческая справка.
Минералы Марганца известны издавна. Древнеримский натуралист Плиний упоминает о чёрном камне, который использовали для обесцвечивания жидкой стеклянной массы; речь шла о минерале пиролюзите MnO 2 . В Грузии пиролюзит с древнейших времён служил присадочным материалом при получении железа. Долгое время пиролюзит называли чёрной магнезией и считали разновидностью магнитного железняка. В 1774 году К.Шелле доказал, что это соединение неизвестного металла, а другой шведский учёный Ю.Гаи, сильно нагревая смесь пиролюзита с углём, получил Марганец загрязнённый углеродом. Название Марганец традиционно происходит от немецкого Marganerz- марганцевая руда.
Распространение в природе.
Среднее Содержание Марганца в земной коре 0.1%, в большинстве изверженных пород 0.06-0.2% по массе, где он находится в рассеянном состоянии в форме Mn2+ (аналог Fe 2+). На земной поверхности Mn 2+ легко окисляется, здесь известны также минералы Mn 3+ и Mn 4+ . В биосфере Марганец энергично мигрирует в восстановительных условиях и малоподвижен в окислительных условиях. Наиболее подвижен Марганец в кислых водах тундры и лесных ландшафтах, где он находится в форме Mn 2+ . Содержание Марганца здесь часто повышенно и культурные растения местами страдают от избытка Марганца; в почвах, озёрах, болотах образуются железно марганцовые конкуренции, озёрные и болотные руды. В сухих степях и пустынях в условиях щелочной окислительной среды Марганец малоподвижен. Организмы бедны Марганцем, культурные растения часто нуждаются в марганцовых микро удобрениях. Речные воды бедны Марганцем (10 -6 -10 -5 г/л.), однако суммарный вынос этого элемента огромен, причём основная его масса осаждается в прибрежной зоне.
Физические и химические свойства.
В чистом виде марганец получают либо электролизом раствора сульфата марганца ( II) , либо восстановлением из оксидов кремнием в электрических печках. Элементарный Марганец представляет собой серебристо-белый твердый, но хрупкий металл. Его хрупкость объясняется тем, что при нормальных температурах в элементарную ячейку Mn входит 58 атомов в сложной ажурной структуре, не относящейся к числу плотноупакованных. Плотность Марганца 7.44 г/см 3 , температура плавления 1244 о С, температура кипения 2150 о С. В реакциях проявляет валентность от 2 до 7, наиболее устойчивые степени окисления +2,+4,+7.
Соединения двухвалентного марганца.
Соли двухвалентного марганца можно получить при растворении в разбавленных кислотах: Mn+2HCl MnCl 2 +H2 При растворении в воде образуется гидроксид Mn(II): Mn+2HOH Mn(OH) 2 +H 2 Гидроксид марганца можно получить в виде белого осадка при действии на растворы солей двухвалентного марганца щелочью: MnSO 4 +2NaOH Mn(OH) 2 +NaSO 4Соединения Mn(II) на воздухе неустойчивы, и Mn(OH) 2 на воздухе быстро буреет, превращаясь в оксид-гидроксид четырёхвалентного марганца.
2 Mn(OH) 2 +O 2 MnO(OH) 2Гидроксид марганца проявляет только основные свойства и не реагирует со щелочами, а при взаимодействии с кислотами даёт соответствующие соли.
Mn(OH) 2 +2HCl MnCl 2 + 2H 2 OОксид марганца может быть получен при разложении карбоната марганца:
MnCO 3 MnO+CO 2Либо при восстановлении диоксида марганца водородом:
MnO 2 +H 2 MnO+H 2 OСоединения четырёхвалентного марганца.
Из соединений четырёхвалентного марганца наиболее известен диоксид марганца MnO 2 - пиролюзит. Поскольку валентность IV является промежуточной, соединения Mn (VI) образуются как при окислении двухвалентного марганца. Mn(NO 3) 2 MnO 2 +2NO 2Так и при восстановлении соединений марганца в щелочной среде:
3K 2 MnO 4 +2H 2 O 2KMnO 4 +MnO 2 +4KOH Последняя реакция является примером реакции самоокисления - самовосстановления, для которых характерно то, что часть атомов одного и того же элемента окисляется, восстанавливая одновременно оставшиеся атомы того же элемента:Mn 6+ +2e=Mn 4+ 1
Mn 6+ -e=Mn 7+ 2
В свою очередь Mn О 2 может окислять галогениды и галоген водороды, например HCl :
MnO 2 +4HCl MnCl 2 +Cl 2 +2H 2 OДиоксид марганца - твёрдое порошкообразное вещество. Он проявляет как основные, так и кислотные свойства.
Соединения шестивалентного марганца.
При сплавлении MnO 2 со щелочами в присутствии кислорода, воздуха или окислителей получают соли шестивалентного Марганца , называемые манганатами.
MnO 2 +2KOH+KNO 3 K 2 MnO 2 +KNO 2 +H 2 OСоединений марганца шестивалентного известно немного, и из них наибольшее значение соли марганцевой кислоты - манганаты.
Сама марганцевая кислота, как и соответствующей ей триоксид марганца MnO 3 , в свободном виде не существует вследствии неустойчивости к процессам окисления - восстановления. Замена протона в кислоте на катион металла приводит к устойчивости манганатов, но их способность к процессам окисления - восствновления сохраняется. Растворы манганатов окрашены в зелёный цвет. При их подкислении образуется марганцеватая кислота,разлагается до соединений марганца четырёхвалентного и семивалентного.
Сильные окислители переводят марганец шестивалентный в семивалентный.
2K 2 MnO 4 +Cl2 2 2KMnO 4 +2KClСоединения семивалентного марганца.
В семивалентном состоянии марганец проявляет только окислительные свойства. Среди применяемых в лабораторной практике и в промышленности окислителей широко применяется перманганат калия KMnO 2 , в быту называемый марганцовкой. Перманганат калия представляет собой кристаллы чёрно-фиолетового цвета. Водные растворы окрашены в фиолетовый цвет, характерный для иона MnO 4 - .
Перманганаты являются солями марганцевой кислоты, которая устойчива только в разбавленных растворах (до 20%). Эти растворы могут быть получены действием сильных окислителей на соединения марганца двухвалентного:
2Mn(NO 3 ) 2 +PbO 2 +6HNO 3 2HMnO 4 +5Pb(NO 3 ) 2 + 2H 2 OМарганец - элемент побочной подгруппы седьмой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 25. Обозначается символом Mn (лат. Manganum).
История открытия марганцаИзвестный естествоиспытатель и писатель древнего Рима Плиний Старший указывал на чудесную способность черного порошка осветлять стекло. Давно это вещество, дающее при размалывании черный порошок, называется пиролюзитом, или двуокисью марганца. О способности пиролюзита очищать стекло писал в 1540 г. и Ваноччио Бирингуччио. Пиролюзит является важнейшей рудой для получения марганца - металла, употребляемого главным образом в металлургии.
От слова "магнезия" получили свои названия марганец и магний. Происхождение наименования двух химических элементов от одного и того же слова объясняется тем, что пиролюзит долгое время противопоставлялся белой магнезии и назывался черной магнезией. После получения металла в чистом виде марганец был переименован. В основу названия было положено греческое слово "манганезе", что значило очищать (намек на его применение в древности в качестве "очистителя" стекла). Некоторые исследователи считают, что название элемента произошло от латинского слова "магнес" - магнит, так как пиролюзит, из которого добывают марганец, считался в древности разновидностью того вещества, которое теперь называется магнитным железняком.
Марганец был открыт в 1774 г. шведским химиком Карлом Вильгельмом Шееле. Правда, ни марганец, ни молибден, ни вольфрам Шееле не выделил в чистом виде; он только указал, что в исследованных им минералах содержатся эти новые элементы. Элемент №25 был обнаружен в минерале пиролюзите МnО 2 · Н 2 О, известном еще Плинию Старшему. Плиний считал его разновидностью магнитного железняка, хотя пиролюзит не притягивается магнитом. Этому противоречию Плиний дал объяснение.
В рукописях знаменитого алхимика Альберта Великого (XIII в.) этот минерал называется «магнезия». В XVI в. встречается уже название «манганезе», которое, возможно, дано стеклоделами и происходит от слова «манганидзейн» – чистить.
Когда Шееле в 1774 г. занимался исследованием пиролюзита, он посылал своему другу Юхану Готлибу Гану образцы этого минерала. Ган, впоследствии профессор, выдающийся химик своего времени, скатывал из пиролюзита шарики, добавляя к руде масло, и сильно нагревал пх в тигле, выложенном древесным углем. Получались металлические шарики, весившие втрое меньше, чем шарики из руды. Это и был марганец. Новый металл называли сначала «магнезия», но так как в то время уже была известна белая магнезия – окись магния, металл переименовали в «магнезиум»; это название и было принято Французской комиссией по номенклатуре в 1787 г. Но в 1808 г. Хэмфри Дэви открыл магнии и тоже назвал его «магнезиум»; тогда во избежание путаницы марганец стали называть «манганум. »
В России марганцем долгое время называли пиролюзит, пока в 1807 г. А.И. Шерер не предложил именовать марганцем металл, полученный из пиролюзита, а сам минерал в те годы называли черным марганцем.
Распространённость в природе марганцаМарганец - 14-й элемент по распространённости на Земле, а после железа - второй тяжёлый металл, содержащийся в земной коре (0,03 % от общего числа атомов земной коры). В биосфере Марганец энергично мигрирует в восстановительных условиях и малоподвижен в окислительной среде. Наиболее подвижен Марганец в кислых водах тундры и лесных ландшафтов, где он находится в форме Мn 2+ . Содержание Марганца здесь часто повышено и культурные растения местами страдают от избытка Марганца. Весовое количество марганца увеличивается от кислых (600 г/т) к основным породам (2,2 кг/т). Сопутствует железу во многих его рудах, однако встречаются и самостоятельные месторождения марганца. В чиатурском месторождении (район Кутаиси) сосредоточено до 40 % марганцевых руд. Марганец, рассеянный в горных породах вымывается водой и уносится в Мировой океан. При этом его содержание в морской воде незначительно (10 −7 -10 −6 %), а в глубоких местах океана его концентрация возрастает до 0,3 % вследствие окисления растворённым в воде кислородом с образованием нерастворимого в воде оксида марганца, который в гидратированной форме (MnO 2 ·x H 2 O) и опускается в нижние слои океана, формируя так называемые железо-марганцевые конкреции на дне, в которых количество марганца может достигать 45 % (также в них имеются примеси меди, никеля, кобальта). Такие конкреции могут стать в будущем источником марганца для промышленности.
Этот металл распространен примерно так же, как сера или фосфор. Богатые залежи марганцевых руд находятся в Индии, Бразилии, Западной и Южной Африке.
В России является остродефицитным сырьём, известны месторождения: «Усинское» в Кемеровской области, «Полуночное» в Свердловской, «Порожинское» в Красноярском крае, «Южно-Хинганское» в Еврейской автономной области, «Рогачёво-Тайнинская» площадь и «Северо-Тайнинское» поле на Новой Земле.
Получение марганцаПервый металлический марганец был получен при восстановлении пиролюзита древесным углем: МnО 2 + C → Mn + 2CO. Но это не был элементарный марганец. Подобно своим соседям по таблице Менделеева – хрому и железу, марганец реагирует с углеродом и всегда содержит примесь карбида. Значит, с помощью углерода чистый марганец не получить. Сейчас для получения металлического марганца применяют три способа: силикотермический (восстановление кремнием), алюминотермический (восстановление алюминием) и электролитический.
Наиболее широкое распространение нашел алюминотермический способ, разработанный в конце XIX в. В этом случае в качестве марганцевого сырья лучше применять не пиролюзит, а закись-окись марганца Mn 3 O 4 . Пиролюзит реагирует с алюминием с выделением такого большого количества тепла, что реакция легко может стать неуправляемой. Поэтому, прежде чем восстанавливать пиролюзит, его обжигают, а уже полученную закись-окись смешивают с алюминиевым порошком и поджигают в специальном контейнере. Начинается реакция 3Мn 3 O 4 + 8Аl → 9Мn + 4Аl 2 О 3 – достаточно быстрая и не требующая дополнительных затрат энергии. Полученный расплав охлаждают, скалывают хрупкий шлак, а слиток марганца дробят и отправляют на дальнейшую переработку.

Однако алюминотермический способ, как и силикотермический, не дает марганца высокой чистоты. Очистить алюминотермический марганец можно возгонкой, но этот способ малопроизводителен и дорог. Поэтому металлурги давно искали новые способы получения чистого металлического марганца и, естественно, прежде всего надеялись на электролитическое рафинирование. Но в отличие от меди, никеля и других металлов, марганец, откладывавшийся на электродах, не был чистым: его загрязняли примеси окислов. Более того, получался пористый, непрочный, неудобный для переработки металл.
Многие известные ученые пытались подобрать оптимальный режим электролиза марганцевых соединении, но безуспешно. Эту задачу разрешил и 1919 г. советский ученый Р.И. Агладзе (ныне действительный член Академии наук Грузинской ССР). По разработанной им технологии электролиза из хлористых и сернокислых солей получается достаточно плотный металл, содержащий до 99,98% элемента №25. Этот метод лег в основу промышленного получения металлического марганца.
Внешне этот металл похож на железо, только тверже его. На воздухе окисляется, но, как и у алюминия, пленка окисла быстро покрывает всю поверхность металла и препятствует дальнейшему окислению. С кислотами марганец реагирует быстро, с азотом образует нитриды, с углеродом – карбиды. В общем, типичный металл.
Физические свойства марганцаПлотность Марганца 7,2-7,4 г/см 3 ; t пл 1245 °С; t кип 2150 °С. Марганец имеет 4 полиморфные модификации: α-Мn (кубическая объемноцентрированная решетка с 58 атомами в элементарной ячейке), β-Мn (кубическая объемноцентрированная с 20 атомами в ячейке), γ-Мn (тетрагональная с 4 атомами в ячейке) и δ-Mn (кубическая объемноцентрированная). Температура превращений: α=β 705 °С; β=γ 1090 °С и γ=δ 1133 °С; α-модификация хрупка; γ (и отчасти β) пластична, что имеет важное значение при создании сплавов.
Атомный радиус Марганца 1,30 Å. ионные радиусы (в Å): Mn 2+ 0,91, Mn 4+ 0,52; Mn 7+ 0,46. Прочие физические свойства α-Mn: удельная теплоемкость (при 25°С) 0,478 кДж/(кг·К) [т. е. 0.114 ккал/(г·°С)]; температурный коэффициент линейного расширения (при 20°С) 22,3·10 -6 град -1 ; теплопроводность (при 25 °С) 66,57 Вт/(м·К) [т. е. 0,159 кал/(см·сек·°С)]; удельное объемное электрическое сопротивление 1,5-2,6 мком·м (т. е. 150-260 мком·см): температурный коэффициент электрического сопротивления (2-3)·10 -4 град -1 . Марганец парамагнитен.
Химические свойства марганца
Марганец достаточно активен, при нагревании энергично взаимодействует с неметаллами - кислородом (образуется смесь оксидов Марганца разной валентности), азотом, серой, углеродом, фосфором и другими. При комнатной температуре Марганец на воздухе не изменяется: очень медленно реагирует с водой. В кислотах (соляной, разбавленной серной) легко растворяется, образуя соли двухвалентного Марганца. При нагревании в вакууме Марганец легко испаряется даже из сплавов.
При окислении на воздухе пассивируется. Порошкообразный марганец сгорает в кислороде (Mn + O 2 → MnO 2). Марганец при нагревании разлагает воду, вытесняя водород (Mn + 2H 2 O →(t) Mn(OH) 2 + H 2 ), образующийся гидроксид марганца замедляет реакцию.
Марганец поглощает водород, с повышением температуры его растворимость в марганце увеличивается. При температуре выше 1200 °C взаимодействует с азотом, образуя различные по составу нитриды.
Углерод реагирует с расплавленным марганцем образуя карбиды Mn 3 C и другие. Образует также силициды, бориды, фосфиды.
C соляной и серной кислотами реагирует по уравнению:
Mn + 2H + → Mn 2+ + H 2
С концентрированной серной кислотой реакция идёт по уравнению:
Mn + 2H 2 SO 4 (конц.) → MnSO 4 + SO 2 + 2H 2 O
В щелочном растворе марганец устойчив.
Марганец образует следующие оксиды: MnO, Mn 2 O 3 , MnO 2 , MnO 3 (не выделен в свободном состоянии) и марганцевый ангидрид Mn 2 O 7 .
Mn 2 O 7 в обычных условиях жидкое маслянистое вещество тёмно-зелёного, очень неустойчивое; в смеси с концентрированной серной кислотой воспламеняет органические вещества. При 90 °C Mn 2 O 7 разлагается со взрывом. Наиболее устойчивы оксиды Mn 2 O 3 и MnO 2 , а также комбинированный оксид Mn 3 O 4 (2MnO·MnO 2 , или соль Mn 2 MnO 4).
При сплавлении оксида марганца (IV) (пиролюзит) со щелочами в присутствии кислорода образуются манганаты:
2MnO 2 + 4KOH + O 2 → 2K 2 MnO 4 + 2H 2 O
Раствор манганата имеет тёмно-зелёный цвет. При подкислении протекает реакция:
3K 2 MnO 4 + 3H 2 SO 4 → 3K 2 SO 4 + 2HMnO 4 + MnO(OH) 2 ↓ + H 2 O
Раствор окрашивается в малиновый цвет из-за появления аниона MnO 4 − и из него выпадает коричневый осадок гидроксида марганца (IV).
Марганцевая кислота очень сильная, но неустойчивая, её невозможно сконцентрировать более, чем до 20 %. Сама кислота и её соли (перманганаты) - сильные окислители. Например, перманганат калия в зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде - до соединений марганца (II), в нейтральной - до соединений марганца (IV), в сильно щелочной - до соединений марганца (VI).
При прокаливании перманганаты разлагаются с выделением кислорода (один из лабораторных способов получения чистого кислорода). Реакция идёт по уравнению (на примере перманганата калия):
2KMnO 4 →(t) K 2 MnO 4 + MnO 2 + O 2
Под действием сильных окислителей ион Mn 2+ переходит в ион MnO 4 − :
2MnSO 4 + 5PbO 2 + 6HNO 3 → 2HMnO 4 + 2PbSO 4 + 3Pb(NO 3) 2 + 2H 2 O
Эта реакция используется для качественного определения Mn 2+
При подщелачивании растворов солей Mn (II) из них выпадает осадок гидроксида марганца (II), быстро буреющий на воздухе в результате окислления.
Применение марганца в промышленностиМарганец содержится во всех видах стали и чугуна. Способность марганца давать сплавы с большинством известных металлов используется для получения не только различных сортов марганцевой стали, но и большого числа нежелезных сплавов (манганинов). Из них особенно замечательными являются сплавы марганца с медью (марганцевая бронза). Она, подобно стали, может закаляться и в то же время намагничиваться, хотя ни марганец, ни медь не обнаруживают заметных магнитных свойств.
Биологическая роль марганца и его содержание в живых организмахМарганец содержится в организмах всех растений и животных, хотя его содержание обычно очень мало, порядка тысячных долей процента, он оказывает значительное влияние на жизнедеятельность, то есть является микроэлементом. Марганец оказывает влияние на рост, образование крови и функции половых желёз. Особо богаты марганцем листья свёклы - до 0,03 %, а также большие его количества содержатся в организмах рыжих муравьёв - до 0,05 %. Некоторые бактерии содержат до нескольких процентов марганца.
Марганец активно влияет на обмен белков, углеводов и жиров. Важной также считается способность марганца усиливать действие инсулина и поддерживать определенный уровень холестерина в крови. В присутствии марганца организм полнее использует жиры. Сравнительно богаты этим микроэлементом крупы (в первую очередь овсяная и гречневая), фасоль, горох, говяжья печень и многие хлебобулочные изделия, которыми практически восполняется суточная потребность человека в марганце - 5,0-10,0 мг.
Не стоит забывать, что соединения марганца могут оказывать токсичное действие на организм человека. Предельно допустимая концентрация марганца в воздухе 0.3 мг/м 3 . При выраженном отравлении наблюдается поражение нервной системы с характерным синдромом марганцевого паркинсонизма.
Объёмы производства марганцевой руды в РоссииМарганецкий ГОК – 29%
Месторождение марганцевых руд было открыто в 1883 году. В
1985 г. на базе этого месторождения начал добычу руды Покровский рудник. По
мере развития рудника и возникновения новых карьеров и шахт сформировался
Марганецкий ГОК.
В составе производственной структуры комбината: два карьера для открытой добычи
марганцевой руды, пять шахт для подземной добычи, три обогатительных фабрики, а
также необходимые вспомогательные цеха и службы, в т.ч. ремонтно-механический,
транспортный и пр.
Орджоникидзевский ГОК – 71%
Основным видом выпускаемой продукции является марганцевый концентрат различных сортов с содержанием чистого марганца от 26% до 43% (в зависимости от сортности). Попутные продукты - керамзитовая глина и шламы.
Добычу марганцевой руды предприятие ведется на закрепленных за ним рудных полях. Запасов руд хватит на срок более 30 лет. Запасы марганцевой руды в Украине суммарно по Орджоникидзевскому и Марганцевому горно-обогатительным комбинатам составляет треть всех мировых запасов.
Марганец является химическим элементом, расположившимся в периодической системе Менделеева под атомным номером 25. Его соседями являются хром и железо, что обуславливает сходство физических и химических свойств этих трех металлов. Его ядро содержит 25 протонов и 30 нейтронов. Атомная масса элемента составляет 54,938.
Свойства марганца
Марганец является переходным металлом из d-семейства. Его электронная формула выглядит следующим образом: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 5 . Твердость марганца по шкале Мооса оценивается на 4. Металл является достаточно твердым, но, в то же время, хрупким. Его теплопроводность составляет 0,0782 Вт/см*К.. Элемент характеризуется серебристо-белым окрасом.
Существует четыре, известные человеку, модификации металла. Каждой из них присуща термодинамическая устойчивость при определенных температурных условиях. Так, а-марганец обладает достаточно сложной структурой и проявляет свою устойчивость при температуре, ниже 707 0 С, чем и обуславливается его хрупкость. Данная модификация металла в элементарной своей ячейке содержит 58 атомов.
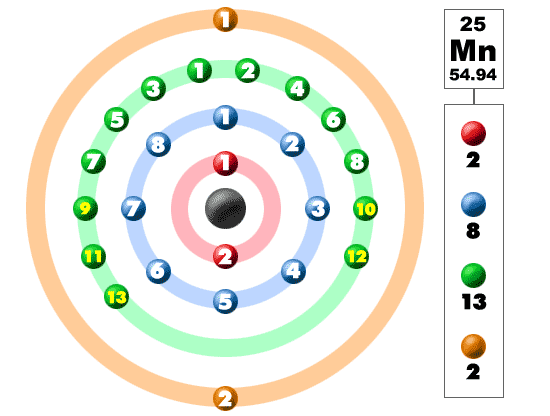
Марганец может иметь совершенно разную степень окисления - от 0 до +7, при этом +1 и +5 встречаются крайне редко. При взаимодействии металла с воздухом, он пассивируется. В кислороде происходит сгорание порошкообразного марганца:
Mn+O2=MnO2
Если воздействовать на металл повышенной температурой, т.е. нагреть, то произойдет его разложение на воду с вытеснением водорода:
Mn+2H0O=Mn(OH)2+H2
Стоит отметить, что гидроксид марганца, слой которого образуется в результате реакции, замедляет процесс реакции.
Водород поглощается металлом. Чем выше повышается температура, тем выше становится его растворимость в марганце. Если превысить температуру в 12000С, то марганец вступает в реакцию с азотом, в результате которой образуются нитриты, имеющие разный состав.
Металл также взаимодействует с углеродом. Результатом данной реакции является образование карбидов, а также силицидов, боридов, фосфидов.
Металл обладает устойчивостью к воздействию на него щелочными растворами.
Он способен образовывать следующие оксиды: MnO, Mn 2 O 3 , MnO 2 , MnO 3 , последний из которых в свободном состоянии не выделен, а также марганцевый ангидрид Mn 2 O 7 . При обычных условиях существования марганцевый ангидрид представляет собой жидкое маслянистое вещество темно-зеленого цвета, не имеющего особой устойчивости. Если температуру повысить до 90 0 С, то разложение ангидрида сопровождается взрывом. Среди оксидов, которые проявляют наибольшую устойчивость, выделяют Mn 2 O 3 и MnO 2 , а также комбинированный оксид Mn 3 O 4 (2MnO·MnO 2 , или соль Mn 2 MnO 4).
Оксиды марганца:
Во время сплавления пиролюзита и щелочей с присутствием кислорода, происходит реакция с образованием манганатов:
2MnO 2 +2KOH+O 2 =2K 2 MnO 4 +2H 2 O
Для раствора манганата характерен темно-зеленый окрас. Если его подкислить, то протекает реакция с подкрашиванием раствора в малиновый цвет. Это происходит по причине образования аниона MnO 4 − , из которого выпадает осадок оксида-гидроксида марганца, имеющего коричневый окрас.
Марганцевая кислота является сильной, однако не проявляет особой устойчивости, в связи с чем, допустимая максимальная ее концентрация составляет не более 20%. Сама же кислота, как и ее соли, выступает сильным окислителем.
Соли марганца не проявляют устойчивости. Для его гидроксидов характерный основный характер. Хлорид марганца разлагается при воздействии него высокими температурами. Именно данную схему применяют для получения хлора.

Применение марганца
Данный металл не является дефицитным - он относится к распространенным элементам: его содержание в земной коре составляет 0,03% от общего количества атомов. Ему принадлежит третье место в рейтинге среди тяжелых металлов, к которым относятся все элементы переходных рядов, пропустив вперед железо и титан. Тяжелыми металлами считаются те, атомный вес которых превышает 40.
Марганец в незначительных количествах можно обнаружить в некоторых горных породах. В основном, встречается локализация его кислородных соединений в виде минерала пиролюзита - MnO 2 .
Марганец имеет множество направлений своего применения. Он необходим для производства многих сплавов и химических веществ. Без марганца невозможно существование живых организмов, так он выступает в качестве активного микроэлемента, а также присутствует практически во всех живых и растительных организмах. Марганец позитивно влияет на процессы кроветворения в живых организмах. Также он содержится во многих пищевых продуктах.

Металл является незаменимым элементом в металлургии. Именно марганец применяется для удаления серы и кислорода из стали во время ее производства. Для данного процесса необходимы большие объемы металла. Но стоит сказать, что в расплав добавляется не чистый марганец, а его сплав с железом, именуемый ферромарганцем. Он получается в процессе восстановительной реакции пиролюзита углем. Также марганец выступает легирующим элементом для сталей. Благодаря добавке марганца к сталям, существенно увеличивается их износостойкость, а также они становятся менее подверженными механическим напряжениям. Присутствие марганца в составе цветных металлов существенно повышает их прочность и устойчивость к коррозии.
Диоксид металла нашел свое применение при окислении аммиака, а также он является участником органических реакций и реакций разложения неорганических солей. В данном случае диоксид марганца выступает катализатором.
Керамическая промышленность также не обходится без использования марганца, где MnO 2 применяется в качестве черного и темно-коричневого красителя для эмалей и глазурей. Оксид марганца является высокодисперсным. Ему присуща хорошая адсорбирующая способность, благодаря которой становится возможным удалять из воздуха вредные примеси.
Марганец вводится в бронзу и латунь. Некоторые соединения металла применяются в тонком органическом синтезе и в промышленном органическом синтезе. Арсениду марганца свойственен гигантский магнитокалорический эффект, который становится существенно сильнее, если воздействовать на него высоким давленим. Теллурид марганца выступает в качестве перспективного термоэлектрического материала.
В медицине также уместно использование марганца, а точнее его солей. Так, водный раствор перманганата калия используется в качестве антисептического средства, а также им можно промывать раны, полоскать горло, смазывать язвы и ожоги. При некоторых отравлениях алкалоидами и цианидами его раствор даже показан для приема во внутрь.

Важно: Не смотря на огромное количество положительных сторон использования марганца, в некоторых случаях его соединения могут пагубно влиять на организм человека и даже оказывать токсичное действие. Так, максимально допустимым значением концентрации марганца в воздухе является 0,3 мг/м 3 . В случае ярко выраженного отравления веществом поражается нервная система человека, для чего характерным является синдром марганцевого паркинсонизма.
Получение марганца
Металл можно получить несколькими способами. Среди наиболее популярных методов выделяют следующие:
- алюминотермический. Марганец получается из его оксида Mn 2 O 3 путем восстановительной реакции. Оксид, в свою очередь, образуется во время прокаливания пиролюзита:
4MnO 2 = 2Mn 2 O 3 +O 2
Mn 2 O 3 +2Al = 2Mn+Al 2 O 3
- восстановительный. Марганец получают путем восстановления металла коксом из марганцевых руд, в результате чего образуется ферромарганец (сплав марганца и железа). Данный метод является наиболее распространенным, так как основная масса от общей добычи металла используется во время производства разнообразных сплавов, основным компонентом которых является железо, в связи с этим из руд марганец извлекают не в чистом виде, а в сплаве с ним;
- электролиза. Металл в чистом виде получают с помощью данного способа из его солей.
Истинная, эмпирическая, или брутто-формула: Mn
Молекулярная масса: 54,938
Марганец - элемент побочной подгруппы седьмой группы четвёртого периода периодической системы химических элементов Д. И. Менделеева с атомным номером 25. Обозначается символом Mn (лат. Manganum, ма́нганум, в составе формул по-русски читается как марганец, например, KMnO 4 - калий марганец о четыре). Простое вещество марганец (CAS-номер: 7439-96-5) - металл серебристо-белого цвета. Наряду с железом и его сплавами относится к чёрным металлам. Известны пять аллотропных модификаций марганца - четыре с кубической и одна с тетрагональной кристаллической решёткой.
История открытия
Один из основных минералов марганца - пиролюзит - был известен в древности как чёрная магнезия и использовался при варке стекла для его осветления. Его считали разновидностью магнитного железняка, а тот факт, что он не притягивается магнитом, Плиний Старший объяснил женским полом чёрной магнезии, к которому магнит «равнодушен». В 1774 г. шведский химик К. Шееле показал, что в руде содержится неизвестный металл. Он послал образцы руды своему другу химику Ю. Гану, который, нагревая в печке пиролюзит с углем, получил металлический марганец. В начале XIX века для него было принято название «манганум» (от немецкого Manganerz - марганцевая руда).
Распространённость в природе
Марганец - 14-й элемент по распространённости на Земле, а после железа - второй тяжёлый металл, содержащийся в земной коре (0,03 % от общего числа атомов земной коры). Весовое количество марганца увеличивается от кислых (600 г/т) к основным породам (2,2 кг/т). Сопутствует железу во многих его рудах, однако встречаются и самостоятельные месторождения марганца. В чиатурском месторождении (район Кутаиси) сосредоточено до 40 % марганцевых руд. Марганец, рассеянный в горных породах, вымывается водой и уносится в Мировой океан. При этом его содержание в морской воде незначительно (10−7-10−6%), а в глубоких местах океана его концентрация возрастает до 0,3 % вследствие окисления растворённым в воде кислородом с образованием нерастворимого в воде оксида марганца, который в гидратированной форме (MnO2·xH2O) и опускается в нижние слои океана, формируя так называемые железо-марганцевые конкреции на дне, в которых количество марганца может достигать 45 % (также в них имеются примеси меди, никеля, кобальта). Такие конкреции могут стать в будущем источником марганца для промышленности.
В России является остродефицитным сырьём, известны месторождения: «Усинское» в Кемеровской области, «Полуночное» в Свердловской, «Порожинское» в Красноярском крае, «Южно-Хинганское» в Еврейской автономной области, «Рогачёво-Тайнинская» площадь и «Северо-Тайнинское» поле на Новой Земле.
Минералы марганца
- пиролюзит MnO 2 ·xH 2 O, самый распространённый минерал (содержит 63,2 % марганца);
- манганит (бурая марганцевая руда) MnO(OH) (62,5 % марганца);
- браунит 3Mn 2 O 3 ·MnSiO3 (69,5 % марганца);
- гаусманит (MnIIMn2III)O 4 ;
- родохрозит (марганцевый шпат, малиновый шпат) MnCO 3 (47,8 % марганца);
- псиломелан mMnO MnO 2 nH 2 O (45-60 % марганца);
- пурпурит Mn 3 +, (36,65 % марганца).
Получение
- Алюминотермическим методом, восстанавливая оксид Mn 2 O 3 , образующийся при прокаливании пиролюзита.
- Восстановлением железосодержащих оксидных руд марганца коксом. Этим способом в металлургии обычно получают ферромарганец (~80 % Mn).
- Чистый металлический марганец получают электролизом.
Физические свойства
Некоторые свойства приведены в таблице. Другие свойства марганца:
- Работа выхода электрона: 4,1 эВ
- Коэффициент линейного температурного расширения: 0,000022 см/см/°C (при 0 °C)
- Электропроводность: 0,00695·106 Ом -1 ·см -1
- Теплопроводность: 0,0782 Вт/см·K
- Энтальпия атомизации: 280,3 кДж/моль при 25 °C
- Энтальпия плавления: 14,64 кДж/моль
- Энтальпия испарения: 219,7 кДж/моль
- Твёрдость
- по шкале Бринелля: Мн/м²
- по шкале Мооса: 4
- Давление паров: 121 Па при 1244 °C
- Молярный объём: 7,35 см³/моль
Химические свойства
Характерные степени окисления марганца: 0, +2, +3, +4, +6, +7 (степени окисления +1, +5 малохарактерны). При окислении на воздухе пассивируется. Порошкообразный марганец сгорает в кислороде.
Марганец при нагревании разлагает воду , вытесняя водород. При этом слой образующегося гидроксида марганца замедляет реакцию. Марганец поглощает водород, с повышением температуры его растворимость в марганце увеличивается. При температуре выше 1200 °C взаимодействует с азотом, образуя различные по составу нитриды.
Углерод реагирует с расплавленным марганцем, образуя карбиды Mn 3 C и другие. Образует также силициды, бориды, фосфиды. В щелочном растворе марганец устойчив.
Марганец образует следующие оксиды: MnO, Mn 2 O 3 , MnO 2 , MnO 3 (не выделен в свободном состоянии) и марганцевый ангидрид Mn 2 O 7 .
Mn 2 O 7 в обычных условиях жидкое маслянистое вещество тёмно-зелёного цвета, очень неустойчивое; в смеси с концентрированной серной кислотой воспламеняет органические вещества. При 90 °C Mn2O7 разлагается со взрывом. Наиболее устойчивы оксиды Mn 2 O 3 и MnO 2 , а также комбинированный оксид Mn 3 O 4 (2MnO·MnO 2 , или соль Mn 2 MnO 4). При сплавлении оксида марганца (IV) (пиролюзит) со щелочами в присутствии кислорода образуются манганаты. Раствор манганата имеет тёмно-зелёный цвет. Раствор окрашивается в малиновый цвет из-за появления аниона MnO 4 − , и из него выпадает коричневый осадок оксида-гидроксида марганца (IV).
Марганцевая кислота очень сильная, но неустойчивая, её невозможно сконцентрировать более, чем до 20 %. Сама кислота и её соли (перманганаты) - сильные окислители. Например, перманганат калия в зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде - до соединений марганца (II), в нейтральной - до соединений марганца (IV), в сильно щелочной - до соединений марганца (VI).
При прокаливании перманганаты разлагаются с выделением кислорода (один из лабораторных способов получения чистого кислорода). Под действием сильных окислителей ион Mn 2+ переходит в ион MnO 4 - . Эта реакция используется для качественного определения Mn 2+ (см. в разделе «Определение методами химического анализа»).
При подщелачивании растворов солей Mn (II) из них выпадает осадок гидроксида марганца (II), быстро буреющий на воздухе в результате окисления. Подробное описание реакции см. в разделе «Определение методами химического анализа».
Соли MnCl 3 , Mn 2 (SO 4) 3 неустойчивы. Гидроксиды Mn(OH) 2 и Mn(OH) 3 имеют основный характер, MnO(OH) 2 - амфотерный. Хлорид марганца (IV) MnCl 4 очень неустойчив, разлагается при нагревании, чем пользуются для получения хлора. Нулевая степень окисления у марганца проявляется в соединениях с σ-донорными и π-акцепторными лигандами. Так, для марганца и известен карбонил состава Mn 2 (CO) 10 .
Известны и другие соединения марганца с σ-донорными и π-акцепторными лигандами (PF 3 , NO, N 2 , P(C 5 H 5) 3).
Применение в промышленности
Применение в металлургии
Марганец в виде ферромарганца применяется для «раскисления» стали при её плавке, то есть для удаления из неё кислорода. Кроме того, он связывает серу, что также улучшает свойства сталей. Введение до 12-13 % Mn в сталь (так называемая Сталь Гадфильда), иногда в сочетании с другими легирующими металлами, сильно упрочняет сталь, делает её твёрдой и сопротивляющейся износу и ударам (эта сталь резко упрочняется и становится твёрже при ударах). Такая сталь используется для изготовления шаровых мельниц, землеройных и камнедробильных машин, броневых элементов и т. д. В «зеркальный чугун» вводится до 20 % Mn. В 1920-х-40х годах применение Марганца позволяло выплавлять броневую сталь. В начале 1950-х годов в журнале Сталь возникла дискуссия по вопросу о возможности снижения содержания марганца в чугуне, и тем самым отказа от поддержки определенного содержания марганца в процессе мартеновской плавки, в которой вместе с В.И. Явойским и В. И. Баптизманским принял участие Е. И. Зарвин, который на основе производственных экспериментов показал нецелесообразность существовавшей технологии. Позже он показал возможность ведения мартеновского процесса на маломарганцовистом чугуне. С пуском ЗСМК началась разработка передела низкомарганцовистых чугунов в конвертерах. Сплав 83 % Cu, 13 % Mn и 4 % Ni (манганин) обладает высоким электросопротивлением, мало изменяющимся с изменением температуры. Поэтому его применяют для изготовления реостатов и пр. Марганец вводят в бронзы и латуни.
Применение в химии
Значительное количество диоксида марганца потребляется при производстве марганцево-цинковых гальванических элементов, MnO 2 используется в таких элементах в качестве окислителя-деполяризатора. Соединения марганца также широко используются как в тонком органическом синтезе (MnO 2 и KMnO 4 в качестве окислителей), так и промышленном органическом синтезе (компоненты катализаторов окисления углеводородов, например, в производстве терефталевой кислоты окислением p-ксилола, окисление парафинов в высшие жирные кислоты). Арсенид марганца обладает гигантским магнитокалорическим эффектом, усиливающимся под давлением. Теллурид марганца перспективный термоэлектрический материал (термо-э. д. с 500 мкВ/К).
Биологическая роль и содержание в живых организмах
Марганец содержится в организмах всех растений и животных, хотя его содержание обычно очень мало, порядка тысячных долей процента, он оказывает значительное влияние на жизнедеятельность, то есть является микроэлементом. Марганец оказывает влияние на рост, образование крови и функции половых желёз. Особо богаты марганцем листья свёклы - до 0,03 %, а также большие его количества содержатся в организмах рыжих муравьёв - до 0,05 %. Некоторые бактерии содержат до нескольких процентов марганца. Избыточное накопление марганца в организме сказывается, в первую очередь, на функционировании центральной нервной системы. Это проявляется в утомляемости, сонливости, ухудшении функций памяти. Марганец является политропным ядом, поражающим также лёгкие, сердечно-сосудистую и гепатобиллиарную системы, вызывает аллергический и мутагенный эффект
Токсичность
Токсическая доза для человека составляет 40 мг марганца в день. Летальная доза для человека не определена. При пероральном поступлении марганец относится к наименее ядовитым микроэлементам. Главными признаками отравления марганцем у животных являются угнетение роста, понижение аппетита, нарушение метаболизма железа и изменение функции мозга. Сообщений о случаях отравления марганцем у людей, вызванных приёмом пищи с высоким содержанием марганца, нет. В основном отравление людей наблюдается в случаях хронической ингаляции больших количеств марганца на производстве. Оно проявляется в виде тяжёлых нарушений психики, включая гиперраздражительность, гипермоторику и галлюцинации - «марганцевое безумие». В дальнейшем развиваются изменения в экстрапирамидной системе, подобные болезни Паркинсона. Чтобы развилась клиническая картина хронического отравления марганцем, обычно требуется несколько лет. Она характеризуется достаточно медленным нарастанием патологических изменений в организме, вызываемых повышенным содержанием марганца в окружающей среде (в частности, распространение эндемического зоба, не связанного с дефицитом йода).
Месторождение
Усинское месторождение марганца
 Материк евразия краткое описание для детей Местность евразии
Материк евразия краткое описание для детей Местность евразии Исследовательская работа " Проблемы молодежи" творческая работа учащихся по немецкому языку (9 класс) на тему Топик по немецкому проблемы молодежи
Исследовательская работа " Проблемы молодежи" творческая работа учащихся по немецкому языку (9 класс) на тему Топик по немецкому проблемы молодежи Восприятие учебной информации, психофизиологические особенности Психологические условия развития восприятия учебного материала учащимися
Восприятие учебной информации, психофизиологические особенности Психологические условия развития восприятия учебного материала учащимися