Što je situacija teža, to hrabrije idete naprijed. Lavr Kornilov: “Što je situacija teža, to hrabrije idemo naprijed.”
PRAKTIČNI RAD (1 sat) 8. RAZRED
Rad izvode učenici samostalno pod nadzorom nastavnika.
Predstavljam rezultat svog višegodišnjeg rada na pripremi i izvođenju praktične nastave u srednjoj školi na nastavi kemije u 8. – 9. razredu:
- “Dobijanje i svojstva kisika”,
- “Priprema otopina soli s određenim masenim udjelom otopljene tvari”,
- “Uopćavanje informacija o najvažnijim klasama anorganskih spojeva”,
- "Elektrolitička disocijacija"
- “Podskupina kisika” (vidi sljedeći broj novina “Kemija”).
Sve sam ih testirao u učionici. Mogu se koristiti pri proučavanju školskog tečaja kemije prema novom programu O.S. Gabrielyana i prema programu G.E.Rudzitisa, F.G.
Učenički pokus je vrsta samostalnog rada. Eksperiment ne samo da obogaćuje učenike novim pojmovima, vještinama i sposobnostima, već je i način provjere istinitosti znanja koje su stekli, pridonosi dubljem razumijevanju gradiva i asimilaciji znanja. Omogućuje vam potpuniju implementaciju načela varijabilnosti u percepciji okolnog svijeta, budući da je glavna bit ovog načela povezanost sa životom, s budućim praktičnim aktivnostima učenika.
Ciljevi. Znati dobiti kisik u laboratoriju i prikupiti ga pomoću dvije metode: istiskivanjem zraka i istiskivanjem vode; eksperimentalno potvrditi svojstva kisika; znati sigurnosna pravila.
Oprema. Metalni stalak s nožicom, alkoholna lampa, šibice, epruveta s izlaznom cijevi za plin, epruveta, kuglica vate, pipeta, menzura, iver, igla (ili žica) za seciranje, kristalizator s vodom, dvije konusne tikvice s čepovima.
Reagensi. KMnO 4 kristalni (5-6 g), vapnena voda Ca(OH) 2, drveni ugljen,
Fe (čelična žica ili spajalica).
Sigurnosne mjere.
Pažljivo rukujte kemijskom opremom!
Zapamtiti! Epruveta se zagrijava držeći je u nagnutom položaju cijelom dužinom uz dva-tri pomaka u plamenu alkoholne lampe. Prilikom zagrijavanja otvor epruvete usmjerite dalje od sebe i svojih susjeda.
Prethodno učenici dobivaju domaću zadaću koja se odnosi na proučavanje sadržaja nadolazećeg rada, a istovremeno koriste materijale iz udžbenika za 8. razred O.S.Gabrielyana (§ 14, 40) ili G.E.Rudzitis, F.G. U bilježnice za praktični rad zapišite naziv teme, svrhu, navedite pribor i reagense te izradite tablicu za izvješće.
TIJEKOM NASTAVE
Stavila sam jedno iskustvo gore
od tisuću mišljenja
rođen samo
mašta.
M.V. Lomonosov
Dobivanje kisika
metoda istiskivanja zraka
(10 min)
1. Stavite kalijev permanganat (KMnO4) u suhu epruvetu. Stavite labavu kuglicu vate na otvor epruvete.
2. Zatvorite epruvetu čepom s izlaznom cijevi za plin i provjerite ima li curenja (slika 1).
|
Riža. 1.
|
(Objašnjenja nastavnika kako provjeriti nepropusnost uređaja.) Učvrstiti uređaj u nozi stativa.
3. Spustite izlaznu cijev za plin u staklo, bez dodirivanja dna, na udaljenosti od 2-3 mm (slika 2).
4. Zagrijte tvar u epruveti. (Zapamtite sigurnosna pravila.)
5. Provjerite prisutnost plina s tinjajućom krhotinom (ugljen). Što promatraš? Zašto se kisik može prikupiti istiskivanjem zraka?
6. Prikupite dobiveni kisik u dvije tikvice za sljedeće pokuse. Zatvorite tikvice čepovima.
7. Ispunite izvješće pomoću tablice. 1, koju stavite na rašir svoje bilježnice.
Dobivanje kisika
metoda istiskivanja vode
(10 min)
1. Napunite epruvetu vodom. Zatvorite epruvetu palcem i okrenite je naopako. U tom položaju spustite ruku s epruvetom u kristalizator s vodom. Stavite epruvetu na kraj izlazne cijevi za plin bez vađenja iz vode (slika 3).
2. Kada kisik istisne vodu iz epruvete, zatvorite je palcem i izvadite iz vode. Zašto se kisik može prikupiti istiskivanjem vode?
Pažnja! Uklonite izlaznu cijev za plin iz kristalizatora dok nastavljate zagrijavati epruvetu KMnO4. Ako se to ne učini, voda će prijeći u vruću epruvetu. Zašto?
Izgaranje ugljena u kisiku
(5 minuta)
1. Pričvrstite ugljen na metalnu žicu (disecirajuću iglu) i stavite je u plamen alkoholne lampe.
2. Stavite vrući ugljen u tikvicu s kisikom. Što promatraš? Dajte objašnjenje (slika 4).
3. Nakon što izvadite neizgoreni ugljen iz tikvice, ulijte u nju 5-6 kapi vapnene vode
Ca(OH) 2. Što promatraš? Dajte objašnjenje.
4. Pripremite izvješće o radu u tablici. 1.
Gori čelična (željezna) žica
u kisiku
(5 minuta)
1. Pričvrstite komad šibice na jedan kraj čelične žice. Zapali šibicu. Stavite žicu sa zapaljenom šibicom u tikvicu s kisikom. Što promatraš? Dajte objašnjenje (slika 5).
2. Pripremite izvješće o radu u tablici. 1.
stol 1
| Operacije izvedene (što su radili) |
Crteži s oznakama polaznih i dobivenih tvari | Zapažanja. Uvjeti izvođenje reakcija. Jednadžbe reakcija |
Objašnjenja opažanja. zaključke |
|---|---|---|---|
| Sastavljanje uređaja za proizvodnju kisika. Provjera curenja uređaja | |||
| Dobivanje kisika od KMnO 4 pri zagrijavanju |
|||
| Dokaz o dobivanju kisika pomoću tinjajući iver |
|||
| Karakteristike fizikalnih svojstava O 2. Prikupljanje O 2 pomoću dvije metode: istiskivanjem zraka, istiskivanjem vode |
|||
| Karakteristično kemijska svojstva O2. Interakcija s jednostavnim tvarima: gorući ugljen, goruće željezo (čelična žica, spajalica) |
Pisani opći zaključak o obavljenom poslu (5 min).
ZAKLJUČAK. Jedan od načina dobivanja kisika u laboratoriju je razgradnja KMnO 4. Kisik je plin bez boje i mirisa, 1,103 puta teži od zraka ( gosp(O 2) = 32, gosp(zrak) = 29, što implicira 32/29 1,103), slabo topljiv u vodi. Reagira s jednostavnim tvarima, stvarajući okside.
Uredite svoje radno mjesto (3 min): rastavite uređaj, stavite posuđe i pribor na svoja mjesta.
Predajte svoje bilježnice na provjeru.
Domaća zadaća.
Zadatak. Odredite koji je od spojeva željeza - Fe 2 O 3 ili Fe 3 O 4 - bogatiji željezom?
| S obzirom: | Pronaći: |
| Fe 2 O 3, Fe 3 O 4 . |
(Fe) u Fe 2 O 3, (Fe) u Fe3O4 |
Riješenje
(X) = n A r(X)/ gosp, Gdje n– broj atoma elementa X u formuli tvari.
gosp(Fe 2 O 3) = 56 2 + 16 3 = 160,
(Fe) = 56 2/160 = 0,7,
(Fe) = 70%,
gosp(Fe 3 O 4) = 56 3 + 16 4 = 232,
" (Fe) = 56 3/232 = 0,724,
" (Fe) = 72,4%.
Odgovor. Fe 3 O 4 je bogatiji željezom od Fe 2 O 3.
Tijekom praktičnog rada nastavnik prati pravilno izvođenje tehnika i operacija kod učenika i bilježi ih na kartici vještina (Tablica 2).
tablica 2
Kartica vještina
| Praktične operacije | Imena učenika | |||||
|---|---|---|---|---|---|---|
| A | B | U | G | D | E | |
| Sastavljanje uređaja za proizvodnju kisika | ||||||
| Provjera curenja uređaja | ||||||
| Ojačanje epruvete u nozi stalka | ||||||
| Rukovanje alkoholnom lampom | ||||||
| Zagrijavanje epruvete s KMnO 4 | ||||||
| Provjera otpuštanja O2 | ||||||
| Sakupljanje O2 u posudu pomoću dvije metode: istiskivanjem zraka, istiskivanjem vode |
||||||
| Izgaranje ugljena | ||||||
| Spaljivanje Fe (čelična žica) | ||||||
| Kultura eksperimentiranja | ||||||
| Priprema rada u bilježnici | ||||||
Uzorak izvješća o obavljenom praktičnom radu (Tablica 1)
tinjajući iver
(ugljen) jako svijetli
u O 2
fizička svojstva O2. Prikupljanje O 2 pomoću dvije metode:
istiskivanjem zraka(a),
istiskivanjem vode (b)

malo teži od zraka, dakle
skuplja se u posudu postavljenu na dno. Kisik je slabo topljiv u vodi


Vapnena voda postaje mutna jer nastaje u vodi netopljivi talog CaCO 3:
CO 2 + Ca(OH) 2 CaCO 3 + H 2 O. Željezo gori svijetlim plamenom u kisiku:

s jednostavnim
tvari – metali i nemetali. Stvaranje bijelog taloga potvrđuje prisutnost CO 2 u tikvici
8. razred PROIZVODNJA I SVOJSTVA KISIKA
(praktični rad br. 3)
Ciljevi: učvrstiti znanja o načinima dobivanja i svojstvima kisika; razviti kod učenika nove vještine korištenja laboratorijske opreme, naučiti prikupljati kisik metodom istiskivanja zraka i metodom istiskivanja vode, prepoznati ga i dokazati njegova svojstva, zapažati; crtati nacrte instrumenata, sastavljati jednadžbe reakcije, donositi zaključke, pridržavati se sigurnosnih pravila.
Oprema i reagensi: KMPO 4, ugljen, vata, suho gorivo, vapnena voda, epruvete, čep s izlaznom cijevi za plin.
Potezlekcija
ja. Priprema za praktični rad.
Sigurnosne upute pri radu sa suhim gorivom.
Tehnički brifing o praktičnom radu.
IIObnavljanje znanja
Navedite reagense za dobivanje 0 2 . (Kalijev permanganat, odnpermanganat K.)
Opišite shemu za dobivanje OKO 2
Kako provjeriti dobiva li se čisti kisik? (Goriiver.)
Učenici rade koristeći priručnik s uputamaNika (str. 70, rad 3).
III. Izvođenje praktičnog rada (prema opcijama).
Opcijaja
1) Sastavite uređaj prema sl. 24, str. 54.
Dobiti kisik.
Sastavite ga metodom istiskivanja zraka. Potpunost punjenja posude kisikom
provjeriti tinjajućim iverjem.
OpcijaII
Sastavite uređaj prema sl. 25, str. 54.
Provjerite ima li curenja.
Dobiti kisik.
Sakupite ga metodom istiskivanja vode. Potpunost punjenja posude kisikom
provjeriti tinjajućim iverjem.
Spaliti ugljen u kisiku.
III. Konsolidacija znanja, vještina, sposobnosti.
Nakon obavljenog rada izvedite zaključak, sve rezultate zapišite u bilježnicu, a izvješće o radu upišite u tablicu:
| Što si učinio, | Ono što je promatrano, jednadžbe | ||
Domaća zadaća:§ 21; odgovoriti na pitanja 11, 12 (str. 60); pripremiti poruku o zaštiti atmosferskog zraka.

 Gdje ići studirati: pregled sveučilišta Kursk Sveučilišta Kursk na međunarodnim i nacionalnim ljestvicama
Gdje ići studirati: pregled sveučilišta Kursk Sveučilišta Kursk na međunarodnim i nacionalnim ljestvicama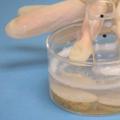 Kako i kada tekućine prelaze u plinove?
Kako i kada tekućine prelaze u plinove? Nuklearna izomerija "nuklearna izomerija" u knjigama
Nuklearna izomerija "nuklearna izomerija" u knjigama