Как выглядит кальций в чистом виде. Кальций и его характеристики
Соединения кальция - известняк, мрамор, гипс (а также известь - продукт известняка) уже в глубокой древности применялись в строительном деле. Вплоть до конца 18 века химики считали известь простым телом. В 1789 году А. Лавуазье предположил, что известь, магнезия, барит, глинозём и кремнезём - вещества сложные. В 1808 году Дэви, подвергая электролизу с ртутным катодом смесь влажной гашеной извести с окисью ртути, приготовил амальгаму кальция, а отогнав из неё ртуть, получил металл, названный «кальций» (от лат. Calх, род. падеж calcis - известь).
Размещение электронов по орбиталям.
+20Са… |3s 3p 3d | 4s
Кальций называется щелочноземельным металлом, его относят к S - элементам. На внешнем электронном уровне у кальция два электрона, поэтому он даёт соединения: CaO, Ca(OH)2, CaCl2, CaSO4, CaCO3 и т.д. Кальций относится к типичным металлам - он имеет большое сродство к кислороду, восстанавливает почти все металлы из их окислов, образует довольно сильное основание Ca(OH)2.
Кристаллические решётки металлов могут быть различных типов, однако для кальция характерна гранецентрированная кубическая решётка.
Размеры, форму и взаимное расположение кристаллов в металлах излучают металлографическими методами. Наиболее полную оценку структуры металла в этом отношении даёт микроскопический анализ его шлифа. Из испытуемого металла вырезают образец и его плоскость шлифуют, полируют и протравливают специальным раствором (травителем). В результате травления выделяется структура образца, которую рассматривают или фотографируют с помощью металлографического микроскопа.
Кальцый - лёгкий металл (d = 1,55), серебристо-белого цвета. Он более твёрд и плавится при более высокой температуре (851 °С) по сравнению с натрием, который расположен рядом с ним в периодической системе. Это объясняется тем, что на один ион кальция в металле приходится два электрона. Поэтому химическая связь между ионами и электронным газом у него более прочная, чем у натрия. При химических реакциях валентные электроны кальция переходят к атомам других элементов. При этом образуются двухзарядные ионы.
Кальций обладает большой химической активностью по отношению к металлам, особенно к кислороду. На воздухе он окисляется медленнее щелочных металлов, так как окисная плёнка на нём менее проницаема для кислорода. При нагревании кальций сгорает с выделением громадных количеств теплоты:
C водой кальций вступает в реакцию, вытесняя из неё водород и образуя основание:
Са + 2H2O = Ca(OH)2 + H2
Благодаря большой химической активности к кислороду кальций находит некоторое применение для получения редких металлов из их окислов. Окислы металлов нагревают совместно с кальциевой стружкой; в результате реакций получается окись кальция и металл. На этом же свойстве основано применение кальция и его некоторых сплавов для так называемого раскисления металлов. Кальций добавляют в расплавленный металл, и он удаляет следы растворённого кислорода; образующаяся окись кальция всплывает на поверхность металла. Кальций входит в состав некоторых сплавов.
Получают кальций электролизом расплавленного хлорида кальция или алюминотермическим методом. Окись кальция, или гашеная известь, представляет собой порошок белого цвета, плавится она при 2570 °С. Получают её прокаливанием известняка:
СаСО3 = СаО + СО2^
Окись кальция - основной окисел, поэтому она вступает в реакцию с кислотами и ангидридами кислот. С водой она даёт основание - гидроокись кальция:
СаО + H2О = Са(ОН)2
Присоединение воды к окиси кальция, называемое гашением извести, протекает с выделением большого количества теплоты. Часть воды при этом превращается в пар. Гидроокись кальция, или гашеная известь, - вещество белого цвета, немного растворимое в воде. Водный раствор гидроокиси кальция называется известковой водой. Такой раствор обладает довольно сильными щелочными свойствами, так как гидроокись кальция хорошо диссоциирует:
Са(ОН)2 = Са + 2ОН
По сравнению с гидратами окислов щелочных металлов гидроокись кальция - более слабое основание. Объясняется это тем, что ион кальция двухзарядный и более сильно притягивает гидроксильные группы.
Гашеная известь и её раствор, называемый известковой водой, вступают в реакции с кислотами и ангидридами кислот, в том числе и с двуокисью углерода. Известковая вода служит в лабораториях для открытия двуокиси углерода, так как образующийся нерастворимый углекислый кальций вызывает помутнение воды:
Са + 2ОН + СО2 = СаСО3v + Н2О
Однако при длительном пропускании двуокиси углерода раствор снова становится прозрачным. Это объясняется тем, что карбонат кальция превращается в растворимую соль - гидрокарбонат кальция:
СаСО3 + СО2 + Н2О = Са(НСО3)2
В промышленности кальций получают двумя способами:
Нагреванием брикетированной смеси СаО и порошка Аl при 1200 °С в вакууме 0,01 - 0,02 мм. рт. ст.; выделяющиеся по реакции:
6СаО + 2Аl = 3CaO · Al2O3 + 3Ca
Пары кальция кондонсируются на холодной поверхности.
Электролизом расплава СаСl2 и КСl с жидким медно-кальциевым катодом приготовляют сплав Сu - Ca (65% Ca), из которого кальций отгоняют при температуре 950 - 1000 °С в вакууме 0,1 - 0,001 мм.рт.ст.
Разработан также способ получения кальция термической диссоциацией карбида кальция СаС2.
Кальций принадлежит к числу самых распространённых в природе элементов. В земной коре его содержится приблизительно 3% (масс.). Соли кальция образуют в природе большие скопления в виде карбонатов (мел, мрамор), сульфатов (гипс), фосфатов (фосфоритов). Под действием воды и двуокиси углерода карбонаты переходят в раствор в виде гидрокарбонатов и переносятся подземными и речными водами на большие расстояния. При вымывании солей кальция могут образовываться пещеры. За счёт испарения воды или повышения температуры на новом месте могут образовываться отложения карбоната кальция. Так, например, образуются сталактиты и сталагмиты в пещерах.
Растворимые соли кальция и магния обуславливают общую жёсткость воды. Если они присутствуют в воде в небольших количествах, то вода называется мягкой. При большом содержании этих солей (100 - 200 мг. солей кальция - в 1 л. в пересчёте на ионы) вода считается жёсткой. В такой воде мыло плохо пенится, так как соли кальция и магния образуют с ним нерастворимые соединения. В жёсткой воде плохо развариваются пищевые продукты, и при кипячении она даёт на стенках паровых котлов накипь. Накипь плохо проводит теплоту, вызывает увеличение расхода топлива и ускоряет изнашивание стенок котла. Образование накипи - сложный процесс. При нагревании кислые соли угольной кислоты кальция и магния разлагаются и переходят в нерастворимые карбонаты:
Са + 2НСО3 = Н2О + СО2 + СаСО3v
Растворимость сульфата кальция СаSO4 при нагревании также снижается, поэтому он входит в состав накипи.
Жёсткость вызванная присутствием в воде гидрокарбонатов кальция и магния, называется карбонатной или временной, так как она устраняется при кипячении. Помимо карбонатной жёсткости, различают ещё некарбонатную жёсткость, которая зависит от содержания в воде сульфатов и хлоридов кальция и магния. Эти соли не удаляются при кипячении, и поэтому некарбонатную жёсткость называют также постоянной жёсткостью. Карбонатная и некарбонатная жёсткость в сумме даёт общую жёсткость.
Для полного устранения жёсткости воду иногда перегоняют. Для устранения карбонатной жёсткости воду кипятят. Общую жёсткость устраняют или добавлением химических веществ, или при помощи так называемых катионитов. При использовании химического метода растворимые соли кальция и магния переводят в нерастворимые карбонаты, например добавляют известковое молоко и соду:
Са + 2НСО3 + Са + 2ОН = 2Н2О + 2СаСО3v
Са + SO4 + 2Na + CO3 = 2Na + SO4 + CaCO3v
Устранение жёсткости при помощи катионитов - процесс более совершенный. Катиониты - сложные вещества (природные соединения кремния и алюминия, высокомалекулярные органические соединения), состав которых можно выразить формулой Na2R, где R - сложный кислотный остаток. При фильтровании воды через слой катионита происходит обмен ионов (катионов) Na на ионы Са и Mg:
Са + Na2R = 2Na + CaR
Следовательно, ионы Са из раствора переходят в катионит, а ионы Na переходят из катионита в раствор. Для восстановления использованного катионита его промывают раствором поваренной соли. При этом происходит обратный процесс: ионы Са в катионите заменяются на ионы Na:
2Na + 2Cl + CaR = Na2R + Ca + 2Cl
Регенерированный катионит можно снова применять для очистки воды.
В виде чистого металла Са применяют как восстановитель U, Th, Cr, V, Zr, Cs, Rb и некоторых редкоземельных металлов и их соединений. Его используют также для раскисления сталей, бронз и других сплавов, для удаления серы из нефтепродуктов, для обезвоживания органических жидкостей, для очистки аргона от примесей азота и в качества поглотителя газов в электровакуумных приборах. Большое применение в технике получили антификционные материалы системы Pb - Na - Ca, а также сплавы Pb - Ca, служащие для изготовления оболочки электрических кабелей. Сплав Ca - Si - Ca (силикокальций) применяется как раскислитель и дегазатор в производстве качественных сталей.
Кальций - один из биогенных элементов, необходимых для нормального протекания жизненных процессов. Он присутствует во всех тканях и жидкостях животных и растений. Лишь редкие организмы могут развиваться в среде, лишённой Са. У некоторых организмов содержание Са достигает 38% : у человека - 1,4 - 2 %. Клетки растительных и животных организмов нуждаются в строго определённых соотношениях ионов Са, Na и К во внеклеточных средах. Растения получают Са из почвы. По их отношению к Са растения делят на кальцефилов и кальцефобов. Животные получают Са с пищей и водой. Са необходим для образования ряда клеточных структур, поддержания нормальной проницаемости наружных клеточных мембран, для оплодотворения яйцеклеток рыб и других животных, активизации ряда ферментов. Ионы Са передают возбуждение на мышечное волокно, вызывая его сокращение, увеличивают силу сердечных сокращений, повышают фагоцитарную функцию лейкоцитов, активируют систему защитных белков крови, участвуют в её свёртывании. В клетках почти весь Са находится в виде соединений с белками, нуклеиновыми кислотами, фосфолипидами, в комплексах с неорганическими фосфатами и органическими кислотами. В плазме крови человека и высших животных только 20 - 40 % Са может быть связано с белками. У животных, обладающих скелетом, до 97 - 99 % всего Са используется в качестве строительного материала: у беспозвоночных в основном в виде СаСО3 (раковина моллюсков, кораллы), у позвоночных - в виде фосфатов. Многие беспозвоночные запасают Са перед линькой для построения нового скелета или для обеспечения жизненных функций в неблагоприятных условиях. Содержание Са в крови человека и высших животных регулируется гормонами паращитовидных и щитовидной желёз. Важнейшую роль в этих процессах играет витамин D. Всасывание Са происходит в переднем отделе тонкого кишечника. Усвоение Са ухудшается при снижении кислотности в кишечнике и зависит от соотношения Са, фосфора и жира в пище. Оптимальные соотношения Са/Р в коровьем молоке около 1,3 (в картофеле 0,15, в бобах 0,13, в мясе 0,016). При избытке в пище Р и щавелевой кислоты всасывание Са ухудшается. Желчные кислоты ускоряют его всасывание. Оптимальные соотношения Са/жир в пище человека 0,04 - 0,08 г. Са на 1г. жира. Выделение Са происходит главным образом через кишечник. Млекопитающие в период лактации теряют много Са с молоком. При нарушениях фосфорно-кальциевого обмена у молодых животных и детей развивается рахит, у взрослых животных - изменение состава и строения скелета (остеомаляция).
В медицине препаратов Са устраняет нарушения, связанные с недостатком ионов Са в организме (при тетании, спазмофилии, рахите). Препараты Са снижают повышенную чувствительность к аллергенам и используются для лечения аллергических заболеваний (сывороточная болезнь, сонная лихорадка и др.). Препараты Са уменьшают повышенную проницаемость сосудов и оказывают противовоспалительное действие. Их применяют при геморрагическом васкулите, лучевой болезни, воспалительных процессах (пневмания, плеврит и др.) и некоторых кожных заболеваниях. Назначают каккровоостанавливающее средство, для улучшения деятельности сердечной мышцы и усиления действия препаратов наперстянки, как противоядия при отравлении солями магния. Вместе с другими средствами препараты Са применяют для стимулирования родовой деятельности. Хлористый Са вводят через рот и внутривенно. Оссокальцинол (15 % -ная стерильная суспензия особым образом приготовленного костного порошка в персиковом масле) предложен для тканевой терапии.
К препаратам Са относятся также гипс (СаSО4), применяемый в хирургии для гипсовых повязок, и мел (СаСО3), назначаемый внутрь при повышенной кислотности желудочного сока и для приготовления зубного порошка.
КАЛЬЦИЙ (латинский Calcium), Са, химический элемент II группы короткой формы (2-й группы длинной формы) периодической системы; относится к щёлочноземельным металлам; атомный номер 20; атомная масса 40,078. В природе существует 6 стабильных изотопов: 40 Са (96,941%), 42 Са (0,647%), 43 Са (0,135%), 44 Са (2,086%), 46 Са (0,004%), 48 Са (0,187%); искусственно получены радиоизотопы с массовыми числами 34-54.
Историческая справка. Многие природные соединения кальция были известны в глубокой древности и широко применялись в строительстве (например, гипс, известь, мрамор). Металлический кальций впервые выделен Г. Дэви в 1808 при электролизе смеси оксидов СаО и HgO и последующем разложении образовавшейся амальгамы кальция. Название происходит от латинского calx (родительный падеж calcis) - известь, мягкий камень.
Распространённость в природе . Содержание кальция в земной коре составляет 3,38% по массе. Из-за высокой химической активности в свободном состоянии не встречается. Наиболее распространены минералы анортит Ca, ангидрит CaSO 4 , апатит Ca 5 (РО 4) 3 (F,Cl,ОН), гипс CaSO 4 ·2Н 2 О, кальцит и арагонит СаСО 3 , перовскит CaTiO 3 , флюорит CaF 2 , шеелит CaWO 4 . Минералы кальция входят в состав осадочных (например, известняк), магматических и метаморфических горных пород. Соединения кальция содержатся в живых организмах: являются основными компонентами костных тканей позвоночных (гидроксиапатит, фторапатит), скелетов кораллов, раковин моллюсков (карбонат и фосфаты кальция) и др. Присутствие ионов Са 2+ определяет жёсткость воды.
Свойства . Конфигурация внешней электронной оболочки атома кальция 4s 2 ; в соединениях проявляет степень окисления +2, редко +1 ; электроотрицательность по Полингу 1,00, атомный радиус 180 пм, радиус иона Са 2+ 114 пм (координационное число 6). кальций - серебристо-белый мягкий металл; до 443 °С устойчива модификация с кубической гранецентрированной кристаллической решёткой, выше 443 °С - с кубической объёмно-центрированной решёткой; t пл 842°С, t кип 1484 °С, плотность 1550 кг/м 3 ; теплопроводность 125,6 Вт/(м·К).
Кальций - металл высокой химической активности (хранят в герметически закрытых сосудах или под слоем минерального масла). При нормальных условиях легко взаимодействует с кислородом (образуется кальция оксид СаО), при нагревании - с водородом (гидрид СаН 2), галогенами (кальция галогениды), бором (борид СаВ 6), углеродом (кальция карбид СаС 2), кремнием (силициды Ca 2 Si, CaSi, CaSi 2 , Ca 3 Si 4), азотом (нитрид Ca 3 N 2), фосфором (фосфиды Са 3 Р 2 , СаР, СаР 5), халькогенами (халькогениды состава СаХ, где Х - S, Se, Те). Кальций взаимодействует с другими металлами (Li, Cu, Ag, Au, Mg, Zn, Al, Pb, Sn и др.) с образованием интерметаллидов. Металлический кальций взаимодействует с водой с образованием кальция гидроксида Са(ОН) 2 и Н 2 . Энергично взаимодействует с большинством кислот, образуя соответствующие соли (например, кальция нитрат, кальция сульфат, кальция фосфаты). Растворяется в жидком аммиаке с образованием тёмно-синего раствора с металлической проводимостью. При испарении аммиака из такого раствора выделяется аммиакат . Постепенно кальций взаимодействует с аммиаком с образованием амида Ca(NH 2) 2 . Образует различные комплексные соединения, наибольшее значение имеют комплексы с кислородсодержащими полидентатными лигандами, например комплексонаты Са.
Биологическая роль . Кальций относится к биогенным элементам. Суточная потребность человека в кальции - около 1 г. В живых организмах ионы кальция участвуют в процессах сокращения мышц, передачи нервных импульсов.
Получение . Металлический кальций получают электролитическим и металлотермическим способами. Электролитический способ основан на электролизе расплавленного хлорида кальция с катодом касания или жидким медно-кальциевым катодом. Из образующегося медно-кальциевого сплава отгоняют кальций при температуре 1000-1080 °С и давлении 13-20 кПа. Металлотермический способ основан на восстановлении кальция из его оксида алюминием или кремнием при 1100-1200 °С. При этом образуется алюминат или силикат кальция, а также газообразный кальций, который затем конденсируют. Мировое производство соединений кальция и материалов, содержащих кальций, около 1 миллиарда т/год (1998).
Применение . Кальций применяют в качестве восстановителя при получении многих металлов (Rb, Cs, Zr, Hf, V и др.). Силициды кальция, а также сплавы кальция с натрием, цинком и другими металлами используют в качестве раскислителей и десульфураторов некоторых сплавов и нефти, для очистки аргона от кислорода и азота, в электровакуумных приборах в качестве поглотителя газов. Хлорид СаСl 2 используют в качестве осушителя в химическом синтезе, гипс применяют в медицине. Кальция силикаты являются основными компонентами цемента.
Лит.: Родякин В. В. Кальций, его соединения и сплавы. М., 1967; Спицын В. И., Мартыненко Л. И. Неорганическая химия. М., 1994. Ч. 2; Неорганическая химия / Под редакцией Ю. Д. Третьякова. М., 2004. Т. 2.
Л. Н. Комиссарова, М. А. Рюмин.
Кальций (латинское Calcium, обозначается символом Ca) - элемент с атомным номером 20 и атомной массой 40,078. Является элементом главной подгруппы второй группы, четвёртого периода периодической системы химических элементов Дмитрия Ивановича Менделеева. При нормальных условиях простое вещество кальций - легкий (1,54 г/см3) ковкий, мягкий химически активный щелочноземельный металл серебристо-белого цвета.
В природе кальций представлен в виде смеси шести изотопов: 40Ca (96,97 %), 42Ca (0,64 %), 43Ca (0,145 %), 44Ca (2,06 %), 46Ca (0,0033 %) и 48Ca (0,185 %). Основным изотопом двадцатого элемента - наиболее распространенным - является 40Са, его изотопная распространенность порядка 97 %. Из шести природных изотопов кальция пять стабильны, шестой изотоп 48Ca, самый тяжелый из шести и довольно редкий (его изотопная распространенность всего 0,185 %), как было недавно установлено, испытывает двойной β-распад с периодом полураспада 5,3∙1019 лет. Полученные искусственным путем изотопы с массовыми числами 39, 41, 45, 47 и 49 - радиоактивны. Чаще всего они используются в качестве изотопного индикатора при изучении процессов минерального обмена в живом организме. 45Ca, получаемый облучением металлического кальция или его соединений нейтронами в урановом реакторе, играет большую роль при изучении обменных процессов, происходящих в почвах, и при исследовании процессов усвоения кальция растениями. Благодаря этому же изотопу удалось обнаружить источники загрязнения различных сортов стали и сверхчистого железа соединениями кальция в процессе выплавки.
Соединения кальция - мрамор, гипс, известняк и известь (продукт обжига известняка) были известны с древнейших времен и широко применялись в строительстве и медицине. Древние Египтяне использовали соединения кальция при строительстве своих пирамид, а жители великого Рима изобрели бетон - используя смесь из дробленого камня, извести и песка. До самого конца XVIII века химики были убеждены, что известь - простое тело. Лишь в 1789 году Лавуазье предположил, что известь, глинозем и некоторые другие соединения - сложные вещества. В 1808 году металлический кальций был получен Г.Дэви путем электролиза.
Применение металлического кальция связано с его высокой химической активностью. Он используется для восстановления из соединений некоторых металлов, например, тория, урана, хрома, циркония, цезия, рубидия; для удаления из стали и из некоторых других сплавов кислорода, серы; для обезвоживания органических жидкостей; для поглощения остатков газов в вакуумных приборах. Кроме того, металлический кальций служит легирующим компонентом некоторых сплавов. Гораздо шире применяются соединения кальция - их используют в строительстве, пиротехнике, производстве стекла, медицине и многих других областях.
Кальций - один из важнейших биогенных элементов, он необходим большинству живых организмов для нормального протекания жизненных процессов. В организме взрослого человека содержится до полутора килограмм кальция. Он присутствует во всех тканях и жидкостях живых организмов. Двадцатый элемент необходим для формирования костной ткани, поддержания сердечного ритма, свертываемости крови, поддержания нормальной проницаемости наружных клеточных мембран, образования ряда ферментов. Список функций, которые выполняет кальций в организмах растений и животных весьма велик. Достаточно сказать, что лишь редкие организмы способны развиваться в среде, лишенной кальция, а другие организмы на 38 % состоят из этого элемента (человеческий организм содержит всего примерно 2 % кальция).
Биологические свойства
Кальций - один из биогенных элементов, его соединения находятся практически во всех живых организмах (немногие организмы способны развиваться в среде, лишенной кальция), обеспечивая нормальное протекание жизненных процессов. Двадцатый элемент присутствует во всех тканях и жидкостях животных и растений, его большая часть (в организмах позвоночных - в том числе и человека) содержится в скелете и зубах в виде фосфатов (например, гидроксиапатит Ca5(PO4)3OH или 3Ca3(PO4)2 Са(OH)2). Использование двадцатого элемента в качестве строительного материала костей и зубов связано с тем, что ионы кальция не используются в клетке. Концентрацию кальция контролируют особые гормоны, их совместное действие сохраняет и поддерживает структуру костей. Скелеты большинства групп беспозвоночных (моллюски, кораллы, губки и прочие) построены из различных форм карбоната кальция CaCO3 (извести). Многие беспозвоночные запасают кальций перед линькой для построения нового скелета или для обеспечения жизненных функций в неблагоприятных условиях. Животные получают кальций с пищей и водой, а растения - из почвы и по отношению к данному элементу делятся на кальцефилов и кальцефобов.
Ионы этого важного микроэлемента участвуют в процессах свертывания крови, а также в обеспечении постоянного осмотического давления крови. Кроме того, кальций необходим для образования ряда клеточных структур, поддержания нормальной проницаемости наружных клеточных мембран, для оплодотворения яйцеклеток рыб и других животных, активации ряда ферментов (возможно, данное обстоятельство связано с тем, что кальций замещает ионы магния). Ионы кальция передают возбуждение на мышечное волокно, вызывая его сокращение, увеличивают силу сердечных сокращений, повышают фагоцитарную функцию лейкоцитов, активируют систему защитных белков крови, регулируют экзоцитоз, в том числе секрецию гормонов и нейромедиаторов. Кальций влияет на проходимость сосудов - без этого элемента жиры, липиды и холестерин осели бы на стенках сосудов. Кальций способствует выделению из организма солей тяжелых металлов и радионуклидов, выполняет антиоксидантные функции. Кальций влияет на систему воспроизводства, оказывает антистрессовый эффект и обладает антиаллергическим действием.
Содержание кальция в организме взрослого человека (массой 70 кг) составляет 1,7 кг (в основном в составе межклеточного вещества костной ткани). Потребность в данном элементе зависит от возраста: для взрослых необходимая дневная норма составляет от 800 до 1 000 миллиграммов, для детей от 600 до 900 миллиграммов. Для детей особенно важно потребление необходимой дозы для интенсивного роста и развития костей. Основным источником поступления кальция в организм служат молоко и молочные продукты, остальной кальций поступает с мясом, рыбой, некоторыми растительными продуктами (особенно с бобовыми). Всасывание катионов кальция происходит в толстом и тонком кишечнике, усвоению способствуют кислая среда, витамины C и D, лактоза (молочная кислота), а также ненасыщенные жирные кислоты. В свою очередь аспирин, щавелевая кислота, производные эстрогенов значительно снижают усвояемость двадцатого элемента. Так, соединяясь с щавелевой кислотой, кальций дает нерастворимые в воде соединения, которые являются компонентами камней в почках. Велика роль магния в кальциевом обмене - при его недостатке кальций «вымывается» из костей и осаждается в почках (почечные камни) и мышцах. Вообще в организме существует сложная система хранения и высвобождения двадцатого элемента, по этой причине содержание кальция в крови точно регулируется, и при правильном питании недостатка либо переизбытка не возникает. Длительная кальциевая диета способна вызвать судороги, боли в суставах, запоры, усталость, сонливость, задержки роста. Продолжительное отсутствие кальция в рационе питания приводит к развитию остеопороза. Никотин, кофеин и алкоголь являются одними из причин недостатка кальция в организме, так как способствуют его интенсивному выведению с мочой. Однако и избыток двадцатого элемента (либо витамина D) приводит к отрицательным последствиям - развивается гиперкальцемия, последствием которой является интенсивная кальцификация костей и тканей (в основном затрагивает мочевыделительную систему). Длительный профицит кальция нарушает функционирование мышечных и нервных тканей, увеличивает свертываемость крови и уменьшает усвояемость цинка клетками костной ткани. Возможно появление остеоартрита, катаракты, проблем с артериальным давлением. Из сказанного можно заключить, что клетки растительных и животных организмов нуждаются в строго определенных соотношениях ионов кальция.
В фармакологии и медицине соединения кальция используются для изготовления витаминов, таблеток, пилюль, инъекций, антибиотиков, а также для изготовления ампул, медицинской посуды.
Оказывается, довольно распространенной причиной мужского бесплодия является нехватка кальция в организме! Дело в том, что головка сперматозоида имеет стреловидное образование, которое полностью состоит из кальция, при достаточном количестве данного элемента сперматозоид способен преодолеть оболочку и оплодотворить яйцеклетку, при недостаточном наступает бесплодие.
Американские ученые выяснили, что недостаток ионов кальция в крови приводит к ослаблению памяти и снижению интеллекта. Так, например, из известного в США журнала Science News стало известно об опытах, которые подтвердили, что у кошек вырабатывается условный рефлекс лишь в том случае, если клетки их мозга содержат больше кальция, чем кровь.
Высоко ценимое в сельском хозяйстве соединение цианамид кальция, используется не только в качестве азотного удобрения и источника получения мочевины - ценнейшего удобрения и сырья для производства синтетических смол, но и в качестве вещества, с помощью которого удалось механизировать уборку хлопковых полей. Дело в том, что после обработки этим соединением хлопчатник моментально сбрасывает листву, что позволяет людям предоставить сбор хлопка машинам.
Говоря о пище богатой кальцием, всегда упоминают молочные продукты, однако само молоко содержит от 120 мг (коровье) до 170 мг (овечье) кальция на 100 г; творог и того беднее - всего 80 мг на 100 грамм. Из молочных продуктов лишь сыр содержит от 730 мг (гауда) до 970 мг (эмменталь) кальция на 100 г продукта. Однако рекордсменом по содержанию двадцатого элемента является мак - в 100 граммах маковых зерен содержится почти 1 500 мг кальция!
Хлорид кальция CaCl2, использующийся, например, в холодильных установках, является отходом многих химико-технологических процессов, в частности, крупномасштабного производства соды. Однако, несмотря на широкое использование хлорида кальция в различных областях, его потребление значительно уступает его производству. По этой причине, например, около заводов, производящих соду, образуются целые озера из рассола хлорида кальция. Подобные пруды-накопители не редкость.
Для того чтобы понять, как много потребляется соединений кальция, стоит привести всего пару примеров. При производстве стали известь используют для удаления фосфора, кремния, марганца и серы, в кислородно-конверторном процессе на тонну стали расходуется 75 килограмм извести! Другой пример из совершенно иной области - пищевой промышленности. При производстве сахара для осаждения сахарата кальция проводят реакцию сырого сахарного сиропа с известью. Так вот, тростниковый сахар обычно требует порядка 3-5 кг извести на тонну, а свекловичный сахар - в сто раз больше, то есть около полутонны извести на тонну сахара!
«Жёсткость» воды - это ряд свойств, которые придают воде растворенные в ней соли кальция и магния. Жесткость подразделяют на временную и постоянную. Временная или карбонатная жесткость обуславливается наличием в воде растворимых гидрокарбонатов Са(НCO3)2 и Mg(HCO3)2. Избавиться от карбонатной жесткости очень легко - при кипячении воды гидрокарбонаты превращаются в нерастворимые в воде карбонаты кальция и магния, выпадая в осадок. Постоянная жесткость создается сульфатами и хлоридами тех же металлов, однако избавиться от нее гораздо сложнее. Жесткая вода страшна не столько тем, что препятствует образованию мыльной пены и поэтому хуже отстирывает белье, гораздо страшнее то, что она образует слой накипи в паровых котлах и котельных установках, тем самым, снижая их КПД и приводя к аварийным ситуациям. Что интересно - определять жесткость воды умели еще в Древнем Риме. В качестве реактива использовалось красное вино - его красящие вещества образуют осадок с ионами кальция и магния.
Весьма интересен процесс подготовки кальция к хранению. Металлический кальций сохраняется в течение длительного времени в виде кусков массой от 0,5 до 60 кг. Эти «чушки» упаковывают в бумажные мешки, затем помещают в железные оцинкованные емкости с пропаянными и прокрашенными швами. Плотно закрытые емкости укладывают в деревянные ящики. Куски весом менее полукилограмма долго хранить нельзя - окисляясь, они быстро превращаются в окись, гидроокись и карбонат кальция.
История
Металлический кальций был получен сравнительно недавно - в 1808 году, однако с соединениями данного металла человечество знакомо очень давно. С древнейших времен люди использовали известняк, мел, мрамор, алебастр, гипс и прочие кальцийсодержащие соединения в строительстве и медицине. Известняк CaCO3, скорее всего, был первым строительным материалом, который использовал человек. Его применяли при возведении египетских пирамид и Великой китайской стены. Многие храмы и церкви на Руси, а также большинство зданий древней Москвы были построены с использованием известняка - белого камня. Еще в давние времена человек, обжигая известняк, получал негашеную известь (CaO), о чем свидетельствуют труды Плиния Старшего (I век н.э.) и Диоскорида - врача при римской армии, которой в сочинении «О лекарственных средствах» ввел для окиси кальция название «негашеная известь», которое сохранилось и в наше время. И всё это притом, что чистый оксид кальция был впервые описан немецким ученым-химиком И. Потом лишь в 1746 году, а в 1755 году химик Дж. Блэк, изучая процесс обжига, выявил, что потеря массы известняка при обжиге происходит за счет выделения углекислого газа:
CaCO3 ↔ CO2 + CaO
Египетские строительные растворы, которые использовались в пирамидах Гизы, были основаны на частично обезвоженном гипсе CaSO4 2H2O или говоря иначе - алебастре 2CaSO4∙H2O. Он же является основой всей штукатурки в гробнице Тутанхамона. Жженый гипс (алебастр) египтяне использовали в качестве вяжущего вещества при строительстве ирригационных сооружений. Обжигая природный гипс при высоких температурах, египетские строители добивались его частичного обезвоживания, причем от молекулы отщеплялась не только вода, но и серный ангидрид. В дальнейшем при разведении водой получалась очень прочная масса, которая не боялась воды и колебаний температуры.
Римлян по праву можно назвать изобретателями бетона, ведь в своих постройках они использовали одну из разновидностей данного строительного материала - смесь дробленого камня, песка и извести. Существует описание Плиния Старшего постройки цистерн из такого бетона: «Для постройки цистерн берут пять частей чистого гравийного песка, две части самой лучшей гашеной извести и обломки силекса (твердая лава) весом не больше фунта каждый, после смешивания уплотняют нижнюю и боковые поверхности ударами железной трамбовки». Во влажном климате Италии бетон был наиболее устойчивым материалом.
Получается, что человечеству были давно известны соединения кальция, которые они широко употребляли. Однако вплоть до конца XVIII века химики считали известь простым телом, лишь в преддверии нового века началось изучение природы извести и прочих соединений кальция. Так Шталь предположил, что известь сложное тело, состоящее из землистого и водного начал, а Блэк установил различие между едкой известью и углекислой известью, содержавшей «фиксированный воздух». Антуан Лоран Лавуазье относил известковую землю (CaO) к числу элементов, то есть к простым веществам, хотя в 1789 году предположил, что известь, магнезия, барит, глинозём и кремнезём - вещества сложные, но доказать это будет возможно лишь разложив «упрямую землю» (оксид кальция). И первым, кому это удалось, был Хэмфри Дэви. После успешного разложения электролизом окислов калия и натрия химик решил получить тем же путем щелочноземельные металлы. Однако первые попытки были неудачны - англичанин пытался разложить известь путем электролиза на воздухе и под слоем нефти, затем прокаливал известь с металлическим калием в трубке и производил многие другие опыты, но безуспешно. Наконец, в приборе с ртутным катодом он получил электролизом извести амальгаму, а из нее металлический кальций. Довольно скоро этот метод получения металла был усовершенствован И. Берцелиусом и М. Понтиным.
Название новый элемент получил от латинского слова «calx» (в родительном падеже calcis) - известь, мягкий камень. Кальксом (calx) называли мел, известковый камень, вообще камень-голыш, но чаще же всего строительный раствор на основе извести. Это понятие употребляли и древние авторы (Витрувий, Плиний Старший, Диоскорид), описывая обжиг известняка, гашения извести и приготовления строительных растворов. Позже в кругу алхимиков «calx» обозначало продукт обжига вообще - в частности металлов. Так, например, оксиды металлов назывались металлическими известями, а сам процесс обжига - кальцинацией (calcinatio). В древнерусской рецептурной литературе встречается слово кал (грязь, глина), так в сборнике Троице-Сергиевской лавры (XV век) говорится: «обрящи кал, от него же творят златарие горнила». Лишь позднее слово кал, которое, несомненно, связано со словом «calx», стало синонимом слова навоз. В русской литературе начала XIX века кальций называли иногда основанием известковой земли, известковием (Щеглов, 1830), известковистостью (Иовский), калцием, кальцием (Гесс).
Нахождение в природе
Кальций один из самых распространенных элементов на нашей планете - пятый по количественному содержанию в природе (из неметаллов больше только кислорода - 49,5 % и кремния - 25,3 %) и третий среди металлов (более распространены лишь алюминий - 7,5 % и железо - 5,08 %). Кларк (среднее содержание в земной коре) кальция по разным оценкам составляет от 2,96 % по массе до 3,38 %, определенно можно сказать, что цифра эта порядка 3 %. В наружной оболочке атома кальция два валентных электрона, связь которых с ядром довольно непрочна. По этой причине кальций обладает высокой химической активностью и в природе в свободном виде не встречается. Однако он активно мигрирует и накапливается в различных геохимических системах, образуя приблизительно 400 минералов: силикаты, алюмосиликаты, карбонаты, фосфаты, сульфаты, боросиликаты, молибдаты, хлориды и прочие, занимая по этому показателю четвертое место. При расплавлении базальтовых магм кальций накапливается в расплаве и входит в состав главных породообразующих минералов, при фракционировании которых его содержание в ходе дифференциации магмы от основных к кислым породам падает. По большей части кальций залегает в нижней части земной коры, накапливаясь в основных породах (6,72 %); в земной мантии кальция мало (0,7 %) и, вероятно, еще меньше в земном ядре (в схожих с ядром железных метеоритах двадцатого элемента всего 0,02 %).
Правда, кларк кальция в каменных метеоритах составляет 1,4 % (встречается редкий сульфид кальция), в средних породах - 4,65 %, кислые породы содержат 1,58 % кальция по массе. Основная часть кальция содержится в составе силикатов и алюмосиликатов различных горных пород (граниты, гнейсы и т. п.), особенно в полевом шпате - анортите Ca, а также диопсиде CaMg, волластоните Са3. В виде осадочных пород соединения кальция представлены мелом и известняками, состоящими в основном из минерала кальцита (CaCO3).
Карбонат кальция СаCO3 - одно из самых распространенных на Земле соединений - минералы на основе карбоната кальция покрывают примерно 40 миллионов квадратных километров земной поверхности. Во многих частях поверхности Земли имеются значительные осадочные залежи карбоната кальция, которые образовались из остатков древних морских организмов - мел, мрамор, известняки, ракушечники - все это СаCO3 с незначительными примесями, а кальцит - чистый СаCO3. Самый важный из этих минералов - известняк, точнее - известняки - ведь каждое месторождение отличается по плотности, составу и количеству примесей. Например, ракушечник - известняк органического происхождения, а имеющий меньше примесей карбонат кальция образует прозрачные кристаллы известкового или исландского шпата. Мел - еще одна часто встречаемая разновидность углекислого кальция, а вот мрамор - кристаллическая форма кальцита - встречается в природе гораздо реже. Принято считать, что мрамор образовался из известняка в древние геологические эпохи. При движении земной коры отдельные залежи известняка оказались погребенными под слоями других пород. Под действием высокого давления и температуры происходил процесс перекристаллизации, и известняк превращался в более плотную кристаллическую породу - мрамор. Причудливые сталактиты и сталагмиты - минерал арагонит, являющийся еще одной разновидностью карбоната кальция. Орторомбический арагонит образуется в теплых морях - громадными пластами карбоната кальция в виде арагонита образованы Багамы, острова Флорида-Кис и бассейн Красного моря. Также довольно широко распространены такие минералы кальция, как флюорит CaF2, доломит MgCO3 CaCO3, ангидрит CaSO4, фосфорит Са5(РО4)3(ОН,СО3) (с различными примесями) и апатиты Ca5(PO4)3(F,Cl,OH) - формы фосфорнокислого кальция, алебастр CaSO4 0,5H2O и гипс CaSO4 2H2O (формы сернокислого кальция) и другие. В кальцийсодержащих минералах присутствуют замещающие его изоморфно элементы-примеси (например, натрий, стронций, редкоземельные, радиоактивные и другие элементы).
Большое количество двадцатого элемента находится в природных водах вследствие существования глобального «карбонатного равновесия» между плохо растворимым СаСО3, хорошо растворимым Са(НСО3)2 и находящимся в воде и воздухе СО2:
CaCO3 + H2O + CO2 = Ca(HCO3)2 = Са2+ + 2HCO3-
Эта реакция обратима и является основой перераспределения двадцатого элемента - при высоком содержании углекислого газа в водах кальций находится в растворе, а при низком содержании CO2 в осадок выпадает минерал кальцит CaCO3, образуя мощные залежи известняка, мела, мрамора.
Немалое количество кальция входит в состав живых организмов, например, гидроксиапатит Ca5(PO4)3OH, или, в другой записи, 3Ca3(PO4)2 Са(OH)2 - основа костной ткани позвоночных, в том числе и человека. Карбонат кальция СаСО3 - основная составляющая панцирей и раковин многих беспозвоночных, яичной скорлупы, кораллов и даже жемчуга.
Применение
Металлический кальций используется довольно редко. В основном этот металл (как и его гидрид) применяется при металлотермическом получении трудновосстанавливаемых металлов - урана, титана, тория, циркония, цезия, рубидия и ряда редкоземельных металлов из их соединений (оксидов или галогенидов). Кальций используют как восстановитель при получении никеля, меди и нержавеющей стали. Также двадцатый элемент используют для раскисления сталей, бронз и других сплавов, для удаления серы из нефтепродуктов, для обезвоживания органических растворителей, для очистки аргона от примеси азота и в качестве поглотителя газов в электровакуумных приборах. Металлический кальций находит применение при получении антифрикционных сплавов системы Pb-Na-Ca (используются в подшипниках), а также сплава Pb-Ca, служащего для изготовления оболочки электрических кабелей. Сплав силикокальций (Ca-Si-Ca) применяется в качестве раскислителя и дегазатора в производстве качественных сталей. Кальций применяется и как легирующий элемент для алюминиевых сплавов и в качестве модифицирующей добавки для магниевых сплавов. Так, например, введение кальция повышает прочность алюминиевых подшипников. Чистый кальций применяется и для легирования свинца, идущего на изготовление аккумуляторных пластин, необслуживаемых стартерных свинцово-кислотных аккумуляторов с малым саморазрядом. Также металлический кальций идет на производство качественных кальциевых баббитов БКА. С помощью кальция регулируют содержание углерода в чугуне и удаляют висмут из свинца, очищают сталь от кислорода, серы и фосфора. Кальций, а также его сплавы с алюминием и магнием используются в резервных тепловых электрических батареях в качестве анода (например, кальций-хроматный элемент).
Однако значительно шире используются соединения двадцатого элемента. И в первую очередь речь идет о природных соединениях кальция. Одно из самых распространенных на Земле соединений кальция - карбонат СаCO3. Чистый карбонат кальция - минерал кальцит, а известняк, мел, мрамор, ракушечник - СаCO3 с незначительными примесями. Смешанный карбонат кальция и магния носит название доломит. Известняк и доломит используются, главным образом, в качестве строительных материалов, дорожных покрытий либо реагентов, понижающих кислотность почвы. Карбонат кальция СаCO3 необходим для получения оксида кальция (негашеной извести) CaO и гидроксида кальция (гашеной извести) Ca(OH)2. В свою очередь CaO и Ca(OH)2 являются основными веществами во многих областях химической, металлургической и машиностроительной промышленности - оксид кальция, как в свободном виде, так и в составе керамических смесей, применяется в производстве огнеупорных материалов; колоссальные объёмы гидроксида кальция необходимы целлюлозно-бумажной промышленности. Кроме того, Ca(OH)2 применяется при производстве хлорной извести (хорошее отбеливающее и дезинфицирующее средство), бертоллетовой соли, соды, некоторых ядохимикатов для борьбы с вредителями растений. Огромное количество извести расходуется при производстве сталей - для удаления серы, фосфора, кремния и марганца. Другая роль извести в металлургии - это производство магния. Известь используется также в качестве смазочного материала при вытягивании стальной проволоки и нейтрализации отходов травильных жидкостей, содержащих серную кислоту. Кроме того, именно известь - самый распространенный химический реагент в обработке питьевой и промышленной воды (совместно с квасцами или солями железа она коагулирует суспензии и удаляет осадок, а также смягчает воду за счет удаления временной - гидрокарбонатной - жесткости). В быту и медицине осажденный карбонат кальция применяется как средство, нейтрализующее кислоту, мягкий абразив в зубных пастах, источник дополнительного кальция в диетах, составная часть жевательной резинки и наполнитель в косметике. СаСО3 также используется как наполнитель в резинах, латексах, красках и эмалях, а также в пластиках (около 10 % по массе) для улучшения их термостойкости, жесткости, твердости и обрабатываемости.
Особую важность имеет фторид кальция CaF2, ведь в виде минерала (флюорит) он является единственным промышленно важным источником фтора! Фторид кальция (флюорит) применяется в виде монокристаллов в оптике (астрономические объективы, линзы, призмы) и как лазерный материал. Дело в том, что стекла лишь из фторида кальция проницаемы для всей области спектра. Вольфрамат кальция (шеелит) в виде монокристаллов применяется в лазерной технике, а также как сцинтиллятор. Не менее важен хлорид кальция CaCl2 - компонент рассолов для холодильных установок и для заполнения шин тракторов и иного транспорта. С помощью хлорида кальция очищают дороги и тротуары от снега и льда, это соединение применяется для защиты угля и руды от замерзания при транспортировке и хранении, его раствором пропитывают древесину для придания ей огнестойкости. CaCl2 используют в бетонных смесях для ускорения начала схватывания, повышения начальной и конечной прочности бетона.
Искусственно получаемый карбид кальция CaC2 (при прокаливании в электропечах оксида кальция с коксом) применяется для получения ацетилена и для восстановления металлов, а также при получении цианамида кальция, который, в свою очередь, под действием водяного пара освобождает аммиак. Кроме этого, цианамид кальция идет на производство мочевины - ценнейшего удобрения и сырья для производства синтетических смол. Нагреванием кальция в атмосфере водорода получают CaH2 (гидрид кальция), используемый в металлургии (металлотермии) и при получении водорода в полевых условиях (из 1 килограмма гидрида кальция можно получить более кубометра водорода), что используется для заполнения аэростатов, например. В лабораторной практике гидрид кальция используется как энергичный восстановитель. Инсектицид арсенат кальция, который получают нейтрализацией мышьяковой кислоты известью, широко используется для борьбы с хлопковым долгоносиком, яблонной плодожоркой, табачным червем, колорадским жуком. Важными фунгицидами являются известково-сульфатные аэрозоли и бордосские смеси, которые получают из сульфата меди и гидроксида кальция.
Производство
Первым, кто получил металлический кальций, был английский химик Хэмфри Дэви. В 1808 году он произвел электролиз смеси влажной гашеной извести Са(ОН)2 с оксидом ртути HgO на платиновой пластине, служившей анодом (в качестве катода выступала платиновая проволока, погруженная в ртуть), в результате чего Дэви получил амальгаму кальция, отогнав из нее ртуть, химик получил новый металл, который он назвал кальцием.
В современной промышленности свободный металлический кальций получают электролизом расплава хлорида кальция СаСl2, доля которого составляет 75-85 % и хлорида калия КСl (возможно использование смеси СаСl2 и CaF2) либо алюмотермическим восстановлением оксида кальция СаО при температуре 1 170-1 200 °C. Необходимый для электролиза чистый безводный хлорид кальция получают хлорированием окиси кальция при нагреве в присутствии угля или обезвоживанием СаСl2∙6Н2О, полученного действием соляной кислоты на известняк. Электролитический процесс происходит в электролизной ванне, в которую помещают сухую, очищенную от примесей соль хлорида кальция и хлористый калий, необходимый для понижения температуры плавления смеси. Над ванной помещают графитовые блоки - анод, чугунная или стальная ванна, заполненная медно-кальциевым сплавом, выступает в роли катода. В процессе электролиза кальций переходит в медно-кальциевый сплав, существенно обогащая его, часть обогащенного сплава постоянно извлекается, взамен добавляют сплав, обедненный кальцием (30-35 % Са), в тоже время хлор образует хлорвоздушную смесь (анодные газы), которая в последствии поступает на хлорирование известкового молока. Обогащенный медно-кальциевый сплав можно использовать непосредственно как сплав или направлять на очистку (дистилляцию), где отгонкой в вакууме (при температуре 1 000-1 080 °С и остаточном давлении 13-20 кПа) из него получают металлический кальций ядерной чистоты. Для получения высокочистого кальция его перегоняют дважды. Процесс электролиза проводится при температуре 680-720 °С. Дело в том, что это наиболее оптимальная температура для электролитического процесса - при более низкой температуре обогащенный кальцием сплав всплывает на поверхность электролита, а при более высокой происходит растворение кальция в электролите с образованием СаСl. При электролизе с жидкими катодами из сплавов кальция и свинца или кальция и цинка непосредственно получают используемые в технике сплавы кальция со свинцом (для подшипников) и с цинком (для получения пенобетона - при взаимодействии сплава с влагой выделяется водород и создается пористая структура). Иногда процесс ведут с железным охлаждаемым катодом, который только соприкасается с поверхностью расплавленного электролита. По мере выделения кальция катод постепенно поднимают, вытягивают из расплава стержень (50-60 см) из кальция, защищенный от кислорода воздуха слоем затвердевшего электролита. «Методом касания» получают кальций сильно загрязненный хлористым кальцием, железом, алюминием, натрием, очищение проводится переплавкой в атмосфере аргона.
Другой метод получения кальция - металлотермический - был теоретически обоснован еще в 1865 году известным русским химиком Н. Н. Бекетовым. Алюмотермический метод основан на реакции:
6CaO + 2Al → 3CaO Al2O3 + 3Ca
Из смеси окиси кальция с порошкообразным алюминием прессуют брикеты, их помещают в реторту из хромоникелевой стали и отгоняют образовавшийся кальций при 1 170-1 200 °С и остаточном давлении 0,7-2,6 Па. Кальций получается при этом в виде пара, который затем конденсируют на холодной поверхности. Алюмотермический способ получения кальция применяется в Китае, во Франции и ряде других стран. В промышленных масштабах металлотермический способ получения кальция первыми применили США в годы второй мировой войны. Таким же образом кальций может быть получен восстановлением СаО ферросилицием или силикоалюминием. Кальций выпускают в виде слитков или листов с чистотой 98-99 %.
Плюсы и минусы существуют в обоих методах. Электролитический метод многооперационен, энергоемок (на 1 кг кальция расходуется энергии 40-50 кВт.ч.), к тому же экологически не безопасен, требует большого количества реагентов и материалов. Однако выход кальция при данном методе составляет 70-80 %, в то время как при алюмотермическом методе выход составляет всего 50-60 %. К тому же при металлотермическом способе получения кальция минус в том, что необходимо осуществлять повторную дистилляцию, а плюс - в низком расходе электроэнергии, и в отсутствии газовых и жидких вредных выбросов.
Не так давно был разработан новый метод получения металлического кальция - он основан на термической диссоциации карбида кальция: раскаленный в вакууме до 1 750 °C карбид разлагается с образованием паров кальция и твердого графита.
До середины XX века металлический кальций производился в очень малых количествах, так как почти не находил применения. Например, в Соединенных Штатах Америки в годы второй мировой войны потреблялось не более 25 тонн кальция, а в Германии всего 5-10 тонн. Лишь во второй половине XX века, когда выяснилось, что кальций активный восстановитель многих редких и тугоплавких металлов, начался стремительный рост потребления (порядка 100 тонн в год) и, как следствие, производства данного металла. С развитием атомной промышленности, где кальций используется в качестве компонента металлотермического восстановления урана из тетрафторида урана (исключение США, где вместо кальция применяется магний), спрос (около 2 000 тонн в год) на элемент номер двадцать, как и его производство, возросло многократно. На данный момент основными производителями металлического кальция можно считать Китай, Россию, Канаду и Францию. Из этих стран кальций направляется в США, Мексику, Австралию, Швейцарию, Японию, Германию, Великобританию. Цены на металлический кальций неуклонно росли до тех пор, пока Китай не стал производить металл в таких объемах, что на мировом рынке появился излишек двадцатого элемента, что привело к резкому снижению цены.
Физические свойства
Что же представляет собой металлический кальций? Какими же свойствами обладает этот элемент, полученный в 1808 году английским химиком Хэмфри Дэви, металл, масса которого в организме взрослого человека может составлять до 2 килограмм?
Простое вещество кальций - серебристо-белый легкий металл. Плотность кальция всего 1,54 г/см3 (при температуре 20 °C), что значительно меньше плотности железа (7,87 г/см3), свинца (11,34 г/см3), золота (19,3 г/см3) или платины (21,5 г/см3). Кальций легче даже, чем такие «невесомые» металлы как алюминий (2,70 г/см3) или магний (1,74 г/см3). Немногие металлы могут «похвастать» плотностью меньшей, чем у двадцатого элемента - натрий (0,97 г/см3), калий (0,86 г/см3), литий (0,53 г/см3). По плотности кальций очень похож на рубидий (1,53 г/см3). Температура плавления кальция 851 °C, температура кипения 1 480 °C. Схожие температуры плавления (хотя и немного ниже) и кипения у других щелочноземельных металлов - стронция (770 °C и 1 380 °C) и бария (710 °C и 1 640 °C).
Металлический кальций существует в двух аллотропических модификациях: при нормальной температуре до 443 °С устойчив α-кальций с кубической гранецентрированной решеткой типа меди, с параметрами: а = 0,558 нм, z = 4, пространственная группа Fm3m, атомный радиус 1,97 A, ионный радиус Ca2+ 1,04 A; в интервале температур 443-842 °С устойчив β-кальций с кубической объемноцентрированной решеткой типа α-железа, с параметрами а = 0,448 нм, z = 2, пространственная группа Im3m. Стандартная энтальпия перехода из α-модификации в β-модификацию составляет 0,93 кДж/моль. Температурный коэффициент линейного расширения для кальция в интервале температур 0-300 °C составляет 22 10-6. Теплопроводность двадцатого элемента при 20 °C равна 125,6 Вт/(м К) или 0,3 кал/(см сек °C). Удельная теплоемкость кальция в интервале от 0 до 100° C равна 623,9 дж/(кг К) или 0,149 кал/(г °C). Удельное электросопротивление кальция при температуре 20° C составляет 4,6 10-8 ом м или 4,6 10-6 ом см; температурный коэффициент электросопротивления элемента номер двадцать 4,57 10-3 (при 20 °C). Модуль упругости кальция 26 Гн/м2 или 2600 кгс/мм2; предел прочности при растяжении 60 Мн/м2 (6 кгс/мм2); предел упругости для кальция равен 4 Мн/м2 или 0,4 кгс/мм2, предел текучести 38 Мн/м2 (3,8 кгс/мм2); относительное удлинение двадцатого элемента 50 %; твердость кальция по Бринеллю 200-300 Мн/м2 или 20-30 кгс/мм2. При постепенном повышении давления кальций начинает проявлять свойства полупроводника, но не становится им в полном смысле этого слова (при этом металлом он уже тоже не является). При дальнейшем повышении давления кальций возвращается в металлическое состояние и начинает проявлять сверхпроводящие свойства (температура сверхпроводимости в шесть раз выше, чем у ртути, и намного превосходит по проводимости все остальные элементы). Уникальное поведение кальция похоже во многом на стронций (то есть параллели в периодической системе сохраняются).
Механические свойства элементарного кальция не отличаются от свойств других представителей семейства металлов, являющихся великолепными конструкционными материалами: металлический кальций высокой чистоты пластичен, хорошо прессуется и прокатывается, вытягивается в проволоку, куётся и поддается обработке резанием - его можно обтачивать на токарном станке. Однако, несмотря на все эти великолепные качества конструкционного материала, кальций таковым не является - причиной всему его высокая химическая активность. Правда не стоит забывать о том, что кальций - незаменимый конструкционный материал костной ткани, а его минералы - строительный материал уже на протяжении многих тысячелетий.
Химические свойства
Конфигурация внешней электронной оболочки атома кальция 4s2, что обуславливает валентность 2 двадцатого элемента в соединениях. Два электрона внешнего слоя сравнительно легко отщепляются от атомов, которые превращаются при этом в положительные двухзарядные ионы. По этой причине в отношении химической активности кальций лишь немного уступает щелочным металлам (калий, натрий, литий). Подобно последним, кальций уже при обычной комнатной температуре легко взаимодействует с кислородом, углекислым газом и влажным воздухом, покрываясь при этом тускло-серой пленкой из смеси оксида СаО и гидроксида Са(ОН)2. Поэтому хранят кальций в герметично закрытом сосуде под слоем минерального масла, жидкого парафина либо же керосина. При нагревании в кислороде и на воздухе кальций воспламеняется, сгорая ярко-красным пламенем, при этом образуется основной оксид СаО, который представляет собой белое, весьма огнестойкое вещество, температура плавления которого примерно 2 600 °C. Оксид кальция также известен в технике как негашеная или жженая известь. Получены также пероксиды кальция - CaO2 и CaO4. С водой кальций реагирует с выделением водорода (в ряду стандартных потенциалов кальций расположен слева от водорода и способен вытеснять его из воды) и образованием гидроксида кальция Са(ОН)2, причем в холодной воде скорость реакции постепенно уменьшается (вследствие образования на поверхности металла слоя малорастворимого гидроксида кальция):
Ca + 2Н2О → Ca(ОН)2 + Н2 + Q
Более энергично кальций взаимодействует с горячей водой, бурно вытесняя водород и образуя Са(ОН)2. Гидроксид кальция Са(ОН)2 - сильное основание, мало растворимое в воде. Насыщенный раствор гидроксида кальция называется известковой водой и имеет щелочную реакцию. На воздухе известковая вода быстро становится мутной вследствие поглощения ею диоксида углерода и образования нерастворимого карбоната кальция. Несмотря на столь бурные процессы, происходящие при взаимодействии двадцатого элемента с водой, всё же, в отличие от щелочных металлов, реакция взаимодействия кальция с водой протекает менее энергично - без взрывов и воспламенений. Вообще химическая активность кальция ниже, чем у других щелочноземельных металлов.
Кальций активно соединяется с галогенами, образуя при этом соединения типа СаХ2 - с фтором он реагирует на холоду, а с хлором и бромом при температуре выше 400 °C, давая соответственно CaF2, CaCl2 и CaBr2. Эти галогениды в расплавленном состоянии образуют с кальцием моногалогениды типа СаХ - CaF, CaCl, в которых кальций формально одновалентен. Данные соединения стабильны только выше температур плавления дигалогенидов (они диспропорционируют при охлаждении с образованием Са и СаХ2). Кроме того, кальций активно взаимодействует, особенно при нагревании, с различными неметаллами: с серой при нагревании получается сульфид кальция CaS, последний присоединяет серу, образуя полисульфиды (CaS2, CaS4 и другие); взаимодействуя с сухим водородом при температуре 300-400 °C, кальций образует гидрид CaH2 - ионное соединение, в котором водород является анионом. Гидрид кальция CaH2 - белое солеобразное вещество, бурно реагирующее с водой с выделением водорода:
CaH2 + 2H2O → Ca(OH)2 + 2H2
При нагревании (порядка 500° C) в атмосфере азота кальций загорается и образует нитрид Ca3N2, известный в двух кристаллических формах - высокотемпературной α и низкотемпературной β. Также был получен нитрид Ca3N4 при нагревании в вакууме амида кальция Ca(NH2)2. При нагревании без доступа воздуха с графитом (углеродом), кремнием или фосфором кальций дает соответственно карбид кальция CaC2, силициды Ca2Si, Ca3Si4, CaSi, CaSi2 и фосфиды Ca3P2, СаР и СаР3. Большинство из соединений кальция с неметаллами легко разлагается водой:
СаН2 + 2Н2О → Са(ОН)2 + 2Н2
Ca3N2 + 6Н2О → 3Са(ОН)2 + 2NH3
С бором кальций образует борид кальция СаВ6, с халькогенами - халькогениды CaS, CaSe, СаТе. Известны также полихалькогениды CaS4, CaS5, Са2Те3. Кальций образует интерметаллические соединения с различными металлами - алюминием, золотом, серебром, медью, свинцом и прочими. Будучи энергичным восстановителем кальций вытесняет при нагревании почти все металлы из их окислов, сульфидов и галогенидов. Кальций хорошо растворяется в жидком аммиаке NH3 с образованием синего раствора, при испарении которого выделяется аммиакат [Са(NН3)6] - твердое соединение золотистого цвета с металлической проводимостью. Соли кальция обычно получают взаимодействием кислотных оксидов с оксидом кальция, действием кислот на Са(ОН)2 или СаСО3, обменными реакциями в водных растворах электролитов. Многие соли кальция хорошо растворимы в воде (хлорид CaCl2, бромид CaBr2, иодид CaI2 и нитрат Ca(NO3)2), они почти всегда образуют кристаллогидраты. Нерастворимы в воде фторид CaF2, карбонат CaCO3, сульфат CaSO4, ортофосфат Ca3(PO4)2, оксалат СаС2О4 и некоторые другие.
Кальций - элемент главной подгруппы второй группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 20. Обозначается символом Ca (лат. Calcium ). Простое вещество кальций - мягкий, химически активный щёлочноземельный металл серебристо-белого цвета.
Кальций в окружающей средеВ природе его очень много: из солей кальция образованы горные массивы и глинистые породы, он есть в морской и речной воде, входит в состав растительных и животных организмов. На долю кальция приходится 3,38 % массы земной коры (5-е место по распространенности после кислорода, кремния, алюминия и железа).
Изотопы кальцияКальций встречается в природе в виде смеси шести изотопов: 40 Ca, 42 Ca, 43 Ca, 44 Ca, 46 Ca и 48 Ca, среди которых наиболее распространённый - 40 Ca - составляет 96,97 %.
Из шести природных изотопов кальция пять стабильны. Шестой изотоп 48 Ca, самый тяжелый из шести и весьма редкий (его изотопная распространённость равна всего 0,187 %), как было недавно обнаружено, испытывает двойной бета-распад с периодом полураспада 5,3×10 19 лет.
Содержание кальция в горных породах и минералахБольшая часть кальция содержится в составе силикатов и алюмосиликатов различных горных пород (граниты, гнейсы и т. п.), особенно в полевом шпате - анортите Ca.
В виде осадочных пород соединения кальция представлены мелом и известняками, состоящими в основном из минерала кальцита (CaCO 3). Кристаллическая форма кальцита - мрамор - встречается в природе гораздо реже.
Довольно широко распространены такие минералы кальция, как кальцит CaCO 3 , ангидрит CaSO 4 , алебастр CaSO 4 ·0.5H 2 O и гипс CaSO 4 ·2H 2 O, флюорит CaF 2 , апатиты Ca 5 (PO 4) 3 (F,Cl,OH), доломит MgCO 3 ·CaCO 3 . Присутствием солей кальция и магния в природной воде определяется её жёсткость.
Кальций, энергично мигрирующий в земной коре и накапливающийся в различных геохимических системах, образует 385 минералов (четвёртое место по числу минералов).
Миграция кальция в земной кореВ естественной миграции кальция существенную роль играет «карбонатное равновесие», связанное с обратимой реакцией взаимодействия карбоната кальция с водой и углекислым газом с образованием растворимого гидрокарбоната:
СаСО 3 + H 2 O + CO 2 ↔ Са (НСО 3) 2 ↔ Ca 2+ + 2HCO 3 -
(равновесие смещается влево или вправо в зависимости от концентрации углекислого газа).
Огромную роль играет биогенная миграция.
Содержание кальция в биосфереСоединения кальция находятся практически во всех животных и растительных тканях (см. тж. ниже). Значительное количество кальция входит в состав живых организмов. Так, гидроксиапатит Ca 5 (PO 4) 3 OH, или, в другой записи, 3Ca 3 (PO 4) 2 ·Са(OH) 2 - основа костной ткани позвоночных, в том числе и человека; из карбоната кальция CaCO 3 состоят раковины и панцири многих беспозвоночных, яичная скорлупа и др. В живых тканях человека и животных 1,4-2 % Са (по массовой доле); в теле человека массой 70 кг содержание кальция - около 1,7 кг (в основном в составе межклеточного вещества костной ткани).
Получение кальцияКальций впервые получен Дэви в 1808 г. с помощью электролиза. Но, как и другие щелочные и щелочноземельные металлы, элемент №20 нельзя получить электролизом из водных растворов. Кальций получают при электролизе его расплавленных солей.

Это сложный и энергоемкий процесс. В электролизере расплавляют хлорид кальция с добавками других солей (они нужны для того, чтобы снизить температуру плавления СаСl 2).
Стальной катод только касается поверхности электролита; выделяющийся кальций прилипает и застывает на нем. По мере выделения кальция катод постепенно поднимают и в конечном счете получают кальциевую «штангу» длиной 50...60 см. Тогда ее вынимают, отбивают от стального катода и начинают процесс сначала. «Методом касания» получают кальций сильно загрязненный хлористым кальцием, железом, алюминием, натрием. Очищают его переплавкой в атмосфере аргона.
Если стальной катод заменить катодом из металла, способного сплавляться с кальцием, то при электролизе будет получаться соответствующий сплав. В зависимости от назначения его можно использовать как сплав, либо отгонкой в вакууме получить чистый кальций. Так получают сплавы кальция с цинком, свинцом и медью.
Другой метод получения кальция – металлотермический – был теоретически обоснован еще в 1865 г. известным русским химиком Н.Н. Бекетовым. Кальций восстанавливают алюминием при давлении всего в 0,01 мм ртутного столба. Температура процесса 1100...1200°C. Кальций получается при этом в виде пара, который затем конденсируют.
В последние годы разработан еще один способ получения элемента. Он основан на термической диссоциации карбида кальция: раскаленный в вакууме до 1750°C карбид разлагается с образованием паров кальция и твердого графита.
Физические свойства кальцияМеталл кальций существует в двух аллотропных модификациях. До 443 °C устойчив α-Ca с кубической гранецентрированной решеткой (параметр а = 0,558 нм), выше устойчив β-Ca с кубической объемно-центрированной решеткой типа α-Fe (параметр a = 0,448 нм). Стандартная энтальпия ΔH 0 перехода α → β составляет 0,93 кДж/моль.
При постепенном повышении давления начинает проявлять свойства полупроводника, не становится полупроводником в полном смысле этого слова (металлом уже тоже не является). При дальнейшем повышении давления возвращается в металлическое состояние и начинает проявлять сверхпроводящие свойства (температура сверхпроводимости в шесть раз выше, чем у ртути, и намного превосходит по проводимости все остальные элементы). Уникальное поведение кальция похоже во многом на стронций.
Несмотря на повсеместную распространенность элемента, даже химики и то не все видели элементарный кальций. А ведь этот металл и внешне и по поведению совсем непохож на щелочные металлы, общение с которыми чревато опасностью пожаров и ожогов. Его можно спокойно хранить на воздухе, он не воспламеняется от воды. Механические свойства элементарного кальция не делают его «белой вороной» в семье металлов: по прочности и твердости кальций превосходит многие из них; его можно обтачивать на токарном станке, вытягивать в проволоку, ковать, прессовать.
И все-таки в качестве конструкционного материала элементарный кальций почти не применяется. Для этого он слишком активен. Кальций легко реагирует с кислородом, серой, галогенами. Даже с азотом и водородом при определенных условиях он вступает в реакции. Среда окислов углерода, инертная для большинства металлов, для кальция – агрессивная. Он сгорает в атмосфере CO и CO 2 .
Естественно, что, обладая такими химическими свойствами, кальций не может находиться в природе в свободном состоянии. Зато соединения кальция – и природные и искусственные – приобрели первостепенное значение.
Химические свойства кальцияКальций - типичный щелочноземельный металл. Химическая активность кальция высока, но ниже, чем всех других щелочноземельных металлов. Он легко взаимодействует с кислородом, углекислым газом и влагой воздуха, из-за чего поверхность металлического кальция обычно тускло серая, поэтому в лаборатории кальций обычно хранят, как и другие щелочноземельные металлы, в плотно закрытой банке под слоем керосина или жидкого парафина.
В ряду стандартных потенциалов кальций расположен слева от водорода. Стандартный электродный потенциал пары Ca 2+ /Ca 0 −2,84 В, так что кальций активно реагирует с водой, но без воспламенения:
Ca + 2Н 2 О = Ca(ОН) 2 + Н 2 + Q.
С активными неметаллами (кислородом, хлором, бромом) кальций реагирует при обычных условиях:
2Са + О 2 = 2СаО, Са + Br 2 = CaBr 2 .
При нагревании на воздухе или в кислороде кальций воспламеняется. С менее активными неметаллами (водородом, бором, углеродом, кремнием, азотом, фосфором и другими) кальций вступает во взаимодействие при нагревании, например:
Са + Н 2 = СаН 2 , Ca + 6B = CaB 6 ,
3Ca + N 2 = Ca 3 N 2 , Са + 2С = СаС 2 ,
3Са + 2Р = Са 3 Р 2 (фосфид кальция), известны также фосфиды кальция составов СаР и СаР 5 ;
2Ca + Si = Ca 2 Si (силицид кальция), известны также силициды кальция составов CaSi, Ca 3 Si 4 и CaSi 2 .
Протекание указанных выше реакций, как правило, сопровождается выделением большого количества теплоты (то есть эти реакции - экзотермические). Во всех соединениях с неметаллами степень окисления кальция +2. Большинство из соединений кальция с неметаллами легко разлагается водой, например:
СаН 2 + 2Н 2 О = Са(ОН) 2 + 2Н 2 ,
Ca 3 N 2 + 3Н 2 О = 3Са(ОН) 2 + 2NH 3 .
Ион Ca 2+ бесцветен. При внесении в пламя растворимых солей кальция пламя окрашивается в кирпично-красный цвет.
Такие соли кальция, как хлорид CaCl 2 , бромид CaBr 2 , иодид CaI 2 и нитрат Ca(NO 3) 2 , хорошо растворимы в воде. Нерастворимы в воде фторид CaF 2 , карбонат CaCO 3 , сульфат CaSO 4 , ортофосфат Ca 3 (PO 4) 2 , оксалат СаС 2 О 4 и некоторые другие.
Важное значение имеет то обстоятельство, что, в отличие от карбоната кальция СаСО 3 , кислый карбонат кальция (гидрокарбонат) Са(НСО 3) 2 в воде растворим. В природе это приводит к следующим процессам. Когда холодная дождевая или речная вода, насыщенная углекислым газом, проникает под землю и попадает на известняки, то наблюдается их растворение:
СаСО 3 + СО 2 + Н 2 О = Са(НСО 3) 2 .
В тех же местах, где вода, насыщенная гидрокарбонатом кальция, выходит на поверхность земли и нагревается солнечными лучами, протекает обратная реакция:
Са(НСО 3) 2 = СаСО 3 + СО 2 + Н 2 О.
Так в природе происходит перенос больших масс веществ. В результате под землей могут образоваться огромные провалы, а в пещерах образуются красивые каменные «сосульки» - сталактиты и сталагмиты.
Наличие в воде растворенного гидрокарбоната кальция во многом определяет временную жёсткость воды. Временной её называют потому, что при кипячении воды гидрокарбонат разлагается, и в осадок выпадает СаСО 3 . Это явление приводит, например, к тому, что в чайнике со временем образуется накипь.
Применение кальцияДо последнего времени металлический кальций почти не находил применения. США, например, до второй мировой войны потребляли в год всего 10...25 т кальция, Германия – 5...10 т. Но для развития новых областей техники нужны многие редкие и тугоплавкие металлы. Выяснилось, что кальции – очень удобный и активный восстановитель многих из них, и элемент стали применять при получении тория, ванадия, циркония, бериллия, ниобия, урана, тантала и других тугоплавких металлов. Чистый металлический кальций широко применяется в металлотермии при получении редких металлов.
Чистый кальций применяется для легирования свинца, идущего на изготовление аккумуляторных пластин, необслуживаемых стартерных свинцово-кислотных аккумуляторов с малым саморазрядом. Также металлический кальций идет на производство качественных кальциевых баббитов БКА.
Применение металлического кальцияГлавное применение металлического кальция - это использование его как восстановителя при получении металлов, особенно никеля, меди и нержавеющей стали. Кальций и его гидрид используются также для получения трудновосстанавливаемых металлов, таких, как хром, торий и уран. Сплавы кальция со свинцом находят применение в аккумуляторных батареях и подшипниковых сплавах. Кальциевые гранулы используются также для удаления следов воздуха из электровакуумных приборов.
Природный мел в виде порошка входит в составы для полировки металлов. Но чистить зубы порошком из природного мела нельзя, так как он содержит остатки раковин и панцирей мельчайших животных, которые обладают повышенной твердостью и разрушают зубную эмаль.
Использование кальция в ядерном синтезе
Изотоп 48 Ca - наиболее эффективный и употребительный материал для производства сверхтяжёлых элементов и открытия новых элементов таблицы Менделеева. Например, в случае использования ионов 48 Ca для получения сверхтяжёлых элементов на ускорителях ядра этих элементов образуются в сотни и тысячи раз эффективней, чем при использовании других «снарядов» (ионов). Радиоактивный кальций широко используют в биологии и медицине в качестве изотопного индикатора при изучении процессов минерального обмена в живом организме. С его помощью установлено, что в организме происходит непрерывный обмен ионами кальция между плазмой, мягкими тканями и даже костной тканью. Большую роль сыграл 45 Са также при изучении обменных процессов, происходящих в почвах, и при исследовании процессов усвоения кальция растениями. С помощью этого же изотопа удалось обнаружить источники загрязнения стали и сверхчистого железа соединениями кальция в процессе выплавки.
Способность кальция связывать кислород и азот позволила применить его для очистки инертных газов и как геттер (Геттер – вещество, служащее для поглощения газов и создания глубокого вакуума в электронных приборах.) в вакуумной радиоаппаратуре.
Применение соединений кальцияНекоторые соединения кальция, получаемые искусственным путем, стали даже более известными и привычными, чем известняки или гипс. Так, гашеную Са(OH) 2 и негашеную СаО известь применяли еще строители древности.
Цемент – это тоже соединение кальция, полученное искусственным путем. Сначала обжигают смесь глины или песка с известняком и получают клинкер, который затем размалывают в тонкий серый порошок. О цементе (вернее, о цементах) можно рассказывать очень много, это тема самостоятельной статьи.
То же самое относится и к стеклу, в состав которого тоже обычно входит элемент.
Гидрид кальция
Нагреванием кальция в атмосфере водорода получают CaH 2 (гидрид кальция), используемый в металлургии (металлотермии) и при получении водорода в полевых условиях.
Оптические и лазерные материалы
Фторид кальция (флюорит) применяется в виде монокристаллов в оптике (астрономические объективы, линзы, призмы) и как лазерный материал. Вольфрамат кальция (шеелит) в виде монокристаллов применяется в лазерной технике, а также как сцинтиллятор.
Карбид кальция
Карбид кальция – вещество, открытое случайно при испытании новой конструкции печи. Еще недавно карбид кальция CaCl 2 использовали главным образом для автогенной сварки и резки металлов. При взаимодействии карбида с водой образуется ацетилен, а горение ацетилена в струе кислорода позволяет получать температуру почти 3000°C. В последнее время ацетилен, а вместе с ним и карбид все меньше расходуются для сварки и все больше – в химической промышленности.
Кальций как химический источник тока
Кальций, а также его сплавы с алюминием и магнием используются в резервных тепловых электрических батареях в качестве анода(например кальций-хроматный элемент). Хромат кальция используется в таких батареях в качестве катода. Особенность таких батарей - чрезвычайно долгий срок хранения (десятилетия) в пригодном состоянии, возможность эксплуатации в любых условиях (космос, высокие давления), большая удельная энергия по весу и объёму. Недостаток в недолгом сроке действия. Такие батареи используются там, где необходимо на короткий срок создать колоссальную электрическую мощность (баллистические ракеты, некоторые космические аппараты и.др.).
Огнеупорные материалы из кальция
Оксид кальция, как в свободном виде, так и в составе керамических смесей, применяется в производстве огнеупорных материалов.
Лекарственные средства
Соединения кальция широко применяются в качестве антигистаминного средства.
- Хлорид кальция
- Глюконат кальция
- Глицерофосфат кальция
Кроме того, соединения кальция вводят в состав препаратов для профилактики остеопороза, в витаминные комплексы для беременных и пожилых.
Кальций в организме человекаКальций - распространенный макроэлемент в организме растений, животных и человека. В организме человека и других позвоночных большая его часть содержится в скелете и зубах в виде фосфатов. Из различных форм карбоната кальция (извести) состоят скелеты большинства групп беспозвоночных (губки, коралловые полипы, моллюски и др.). Потребность в кальции зависит от возраста. Для взрослых необходимая дневная норма составляет от 800 до 1000 миллиграммов (мг), а для детей от 600 до 900 мг, что для детей очень важно из-за интенсивного роста скелета. Большая часть кальция, поступающего в организм человека с пищей, содержится в молочных продуктах, оставшийся кальций приходится на мясо, рыбу, и некоторые растительные продукты (особенно много содержат бобовые).
Усваиванию кальция препятствуют аспирин, щавелевая кислота, производные эстрогенов. Соединяясь с щавелевой кислотой, кальций дает нерастворимые в воде соединения, которые являются компонентами камней в почках.
Избыточные дозы кальция и витамина Д могут вызвать гиперкальцемию, после которой следует интенсивная кальцификация костей и тканей (в основном затрагивает мочевыделительную систему). Максимальная дневная безопасная доза составляет для взрослого от 1500 до 1800 миллиграмм.
Кальций в жёсткой воде
Комплекс свойств, определяемых одним словом «жесткость», воде придают растворенные в ней соли кальция и магния. Жесткая вода непригодна во многих случаях жизни. Она образует слой накипи в паровых котлах и котельных установках, затрудняет окраску и стирку тканей, но годится для варки мыла и приготовления эмульсий в парфюмерном производстве. Поэтому раньше, когда способы умягчения воды были несовершенны, текстильные и парфюмерные предприятия обычно размещались поблизости от источников «мягкой» воды.
Различают жесткость временную и постоянную. Временную (или карбонатную) жесткость придают воде растворимые гидрокарбонаты Са(НCO 3) 2 и Mg(HCO 3) 2 . Устранить ее можно простым кипячением, при котором гидрокарбонаты превращаются в нерастворимые в воде карбонаты кальция и магния.
Постоянная жесткость создается сульфатами и хлоридами тех же металлов. И ее можно устранить, но сделать это намного сложнее.
Сумма обоих жесткостей составляет общую жесткость воды. Оценивают ее в разных странах по-разному. Принято выражать жесткость воды числом миллиграмм-эквивалентов кальция и магния в одном литре воды. Если в литре воды меньше 4 мг-экв, то вода считается мягкой; по мере увеличения их концентрации – все более жесткой и, если содержание превышает 12 единиц, – очень жесткой.
Жесткость воды обычно определяют с помощью раствора мыла. Такой раствор (определенной концентрации) прибавляют по каплям к отмеренному количеству воды. Пока в воде есть ионы Са 2+ или Mg 2+ , они будут мешать образованию пены. По затратам мыльного раствора до появления пены вычисляют содержание ионов Са 2+ и Mg 2+ .
Интересно, что аналогичным путем определяли жесткость воды еще в Древнем Риме. Только реактивом служило красное вино – его красящие вещества тоже образуют осадок с ионами кальция и магния.
Хранение кальция
Металлический кальций длительно хранить можно в кусках весом от 0,5 до 60 кг. Такие куски хранят в бумажных мешках, вложенных в железные оцинкованные барабаны с пропаянными и покрашенными швами. Плотно закрытые барабаны укладывают в деревянные ящики. Куски весом меньше 0,5 кг подолгу хранить нельзя – они быстро превращаются в окись, гидроокись и карбонат кальция.
Кальций — химический элемент II группы с атомным номером 20 в периодической системе, обозначается символом Ca (лат. Calcium). Кальций - мягкий щелочно-земельный металл серебристо-серого цвета.
20 элемент таблицы МенделееваНазвание элемента происходит от лат. calx (в родительном падеже calcis) — «известь», «мягкий камень». Оно было предложено английским химиком Хэмфри Дэви, в 1808 г. выделившим металлический кальций.
Соединения кальция — известняк, мрамор, гипс (а также известь — продукт обжига известняка) применялись в строительном деле уже несколько тысячелетий назад.
Кальций один из наиболее распространенных на Земле элементов. Соединения кальция находятся практически во всех животных и растительных тканях. На его долю приходится 3,38 % массы земной коры (5-е место по распространенности после кислорода, кремния, алюминия и железа).
Нахождение кальция в природе
Из-за высокой химической активности кальций в свободном виде в природе не встречается.
На долю кальция приходится 3,38 % массы земной коры (5-е место по распространенности после кислорода, кремния, алюминия и железа). Содержание элемента в морской воде — 400 мг/л.
Изотопы
Кальций встречается в природе в виде смеси шести изотопов: 40Ca, 42Ca, 43Ca, 44Ca, 46Ca и 48Ca, среди которых наиболее распространённый — 40Ca — составляет 96,97 %. Ядра кальция содержат магическое число протонов: Z = 20. Изотопы
40
20
Ca20 и
48
20
Ca28 являются двумя из пяти существующих в природе ядер с дважды магическим числом.
Из шести природных изотопов кальция пять стабильны. Шестой изотоп 48Ca, самый тяжелый из шести и весьма редкий (его изотопная распространённость равна всего 0,187 %), испытывает двойной бета-распад с периодом полураспада 1,6·1017 лет.
В горных породах и минералах
Большая часть кальция содержится в составе силикатов и алюмосиликатов различных горных пород (граниты, гнейсы и т. п.), особенно в полевом шпате — анортите Ca.
В виде осадочных пород соединения кальция представлены мелом и известняками, состоящими в основном из минерала кальцита (CaCO3). Кристаллическая форма кальцита — мрамор — встречается в природе гораздо реже.
Довольно широко распространены такие минералы кальция, как кальцит CaCO3, ангидрит CaSO4, алебастр CaSO4·0.5H2O и гипс CaSO4·2H2O, флюорит CaF2, апатиты Ca5(PO4)3(F,Cl,OH), доломит MgCO3·CaCO3. Присутствием солей кальция и магния в природной воде определяется её жёсткость.
Кальций, энергично мигрирующий в земной коре и накапливающийся в различных геохимических системах, образует 385 минералов (четвёртое место по числу минералов).
Биологическая роль кальция
Кальций — распространенный макроэлемент в организме растений, животных и человека. В организме человека и других позвоночных большая его часть находится в скелете и зубах. В костях кальций содержится в виде гидроксиапатита. Из различных форм карбоната кальция (извести) состоят «скелеты» большинства групп беспозвоночных (губки, коралловые полипы, моллюски и др.). Ионы кальция участвуют в процессах свертывания крови, а также служат одним из универсальных вторичных посредников внутри клеток и регулируют самые разные внутриклеточные процессы — мышечное сокращение, экзоцитоз, в том числе секрецию гормонов и нейромедиаторов. Концентрация кальция в цитоплазме клеток человека составляет около 10−4 ммоль/л, в межклеточных жидкостях около 2,5 ммоль/л.
Потребность в кальции зависит от возраста. Для взрослых в возрасте 19-50 лет и детей 4-8 лет включительно дневная потребность (RDA) составляет 1000 мг (содержится примерно в 790 мл молока с жирностью 1 %), а для детей в возрасте от 9 до 18 лет включительно — 1300 мг в сутки (содержится примерно в 1030 мл молока жирностью 1 %). В подростковом возрасте потребление достаточного количества кальция очень важно из-за интенсивного роста скелета. Однако по данным исследований в США всего 11 % девочек и 31 % мальчиков в возрасте 12-19 лет достигают своих потребностей. В сбалансированной диете большая часть кальция (около 80 %) поступает в организм ребёнка с молочными продуктами. Оставшийся кальций приходится на зерновые (в том числе цельнозерновой хлеб и гречку), бобовые, апельсины, зелень, орехи. В «молочных» продуктах на основе молочного жира (сливочном масле, сливках, сметане, мороженом на основе сливок) кальция практически не содержится. Чем больше в молочном продукте молочного жира, тем меньше в нём кальция. Всасывание кальция в кишечнике происходит двумя способами: чрезклеточно (трансцеллюлярно) и межклеточно (парацелюллярно). Первый механизм опосредован действием активной формы витамина D (кальцитриола) и её кишечными рецепторами. Он играет большую роль при малом и умеренном потреблении кальция. При большем содержании кальция в диете основную роль начинает играть межклеточная абсорбция, которая связана с большим градиентом концентрации кальция. За счёт чрезклеточного механизма кальций всасывается в большей степени в двенадцатиперстной кишке (из-за наибольшей концентрации там рецепторов в кальцитриолу). За счёт межклеточного пассивного переноса абсорбция кальция наиболее активна во всех трёх отделах тонкого кишечника. Всасыванию кальция парацеллюлярно способствует лактоза (молочный сахар).
Усвоению кальция препятствуют некоторые животные жиры (включая жир коровьего молока и говяжий жир, но не сало) и пальмовое масло. Содержащиеся в таких жирах пальмитиновая и стеариновая жирные кислоты отщепляются при переваривании в кишечнике и в свободном виде прочно связывают кальций, образуя пальмитат кальция и стеарат кальция (нерастворимые мыла). В виде этого мыла со стулом теряется как кальций, так и жир. Этот механизм ответственен за снижение всасывания кальция, снижение минерализации костей и снижение косвенных показателей их прочности у младенцев при использовании детских смесей на основе пальмового масла (пальмового олеина). У таких детей образование кальциевых мыл в кишечнике ассоциируется с уплотнением стула, уменьшением его частоты, а также более частым срыгиванием и коликами.
Концентрация кальция в крови из-за её важности для большого числа жизненно важных процессов точно регулируется, и при правильном питании и достаточном потреблении обезжиренных молочных продуктов и витамина D дефицита не возникает. Длительный дефицит кальция и/или витамина D в диете приводит к увеличению риска остеопороза, а в младенчестве вызывает рахит.
Избыточные дозы кальция и витамина D могут вызвать гиперкальцемию. Максимальная безопасная доза для взрослых в возрасте от 19 до 50 лет включительно составляет 2500 мг в сутки (около 340 г сыра Эдам).
 Корпускулярные и волновые свойства частиц
Корпускулярные и волновые свойства частиц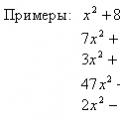 Уравнения онлайн X 5 0 решение
Уравнения онлайн X 5 0 решение Предельные монокарбоновые кислоты
Предельные монокарбоновые кислоты