2 วิธีในการแยกส่วนผสมที่ต่างกัน การแยกสารผสม
บล็อกทางทฤษฎี
คำจำกัดความของแนวคิด "ส่วนผสม" มีให้ไว้ในศตวรรษที่ 17 นักวิทยาศาสตร์ชาวอังกฤษ โรเบิร์ต บอยล์: “ของผสมคือระบบบูรณาการที่ประกอบด้วยส่วนประกอบที่ต่างกัน”
ลักษณะเปรียบเทียบของสารผสมและสารบริสุทธิ์
สัญญาณของการเปรียบเทียบ | สารบริสุทธิ์ | ส่วนผสม |
คงที่ | ไม่แน่นอน |
|
สาร | สิ่งเดียวกัน | หลากหลาย |
คุณสมบัติทางกายภาพ | ถาวร | ไม่แน่นอน |
การเปลี่ยนแปลงพลังงานระหว่างการก่อตัว | กำลังเกิดขึ้น | ไม่เกิดขึ้น |
แยก | โดยผ่านปฏิกิริยาเคมี | โดยวิธีการทางกายภาพ |
ส่วนผสมมีลักษณะแตกต่างกันออกไป
การจำแนกประเภทของสารผสมแสดงไว้ในตาราง:
เราจะยกตัวอย่างสารแขวนลอย (ทรายแม่น้ำ + น้ำ) อิมัลชัน (น้ำมันพืช + น้ำ) และสารละลาย (อากาศในขวด เกลือแกง + น้ำ การเปลี่ยนแปลงเล็กน้อย: อลูมิเนียม + ทองแดง หรือ นิกเกิล + ทองแดง)
วิธีการแยกสารผสม
ในธรรมชาติ สารมีอยู่ในรูปของสารผสม สำหรับการวิจัยในห้องปฏิบัติการ การผลิตทางอุตสาหกรรม และสำหรับความต้องการด้านเภสัชวิทยาและการแพทย์ จำเป็นต้องใช้สารบริสุทธิ์
มีวิธีแยกสารผสมหลายวิธีเพื่อทำให้สารบริสุทธิ์
การระเหยคือการแยกของแข็งที่ละลายในของเหลวโดยแปลงเป็นไอน้ำ

การกลั่น-การกลั่น การแยกสารที่บรรจุอยู่ในของเหลวผสมตามจุดเดือด ตามด้วยการระบายความร้อนของไอน้ำ
ในธรรมชาติ น้ำไม่ได้เกิดขึ้นในรูปแบบบริสุทธิ์ (ไม่มีเกลือ) มหาสมุทร ทะเล แม่น้ำ บ่อน้ำ และน้ำพุเป็นสารละลายเกลือในน้ำประเภทหนึ่ง อย่างไรก็ตาม ผู้คนมักต้องการน้ำสะอาดที่ไม่มีเกลือ (ใช้ในเครื่องยนต์ของรถยนต์ ในการผลิตสารเคมีเพื่อให้ได้สารละลายและสารต่างๆ ในการถ่ายภาพ) น้ำดังกล่าวเรียกว่าน้ำกลั่น และวิธีการได้มาเรียกว่าการกลั่น

การกรอง - กรองของเหลว (ก๊าซ) ผ่านตัวกรองเพื่อทำความสะอาดจากสิ่งสกปรกที่เป็นของแข็ง

วิธีการเหล่านี้ขึ้นอยู่กับความแตกต่างในคุณสมบัติทางกายภาพของส่วนประกอบของสารผสม
พิจารณาวิธีการแยก ต่างกันและของผสมที่เป็นเนื้อเดียวกัน.
ตัวอย่างของส่วนผสม | วิธีการแยก |
ระบบกันสะเทือน - ส่วนผสมของทรายแม่น้ำและน้ำ | การสนับสนุน แยก ปกป้องขึ้นอยู่กับความหนาแน่นของสารที่แตกต่างกัน ทรายที่หนักกว่าจะตกลงไปที่ด้านล่าง คุณยังสามารถแยกอิมัลชันออกได้ โดยแยกน้ำมันหรือน้ำมันพืชออกจากน้ำ ในห้องปฏิบัติการ สามารถทำได้โดยใช้กรวยแยก ปิโตรเลียมหรือน้ำมันพืชจะอยู่ชั้นบนสุดและสีอ่อนกว่า ผลจากการตกตะกอน น้ำค้างตกลงมาจากหมอก เขม่าจางหายไปจากควัน และครีมก็ตกตะกอนในนม แยกส่วนผสมของน้ำและน้ำมันพืชโดยการตกตะกอน |
ส่วนผสมของทรายและเกลือแกงในน้ำ | การกรอง พื้นฐานสำหรับการแยกสารผสมที่ต่างกันโดยใช้คืออะไร การกรองความสามารถในการละลายต่างๆ ของสารในน้ำและขนาดอนุภาคต่างๆ มีเพียงอนุภาคของสารที่เทียบเคียงได้เท่านั้นที่จะผ่านเข้าไปในรูพรุนของตัวกรอง ในขณะที่อนุภาคขนาดใหญ่กว่าจะยังคงอยู่บนตัวกรอง วิธีนี้จะทำให้คุณสามารถแยกส่วนผสมที่ต่างกันของเกลือแกงและทรายแม่น้ำออกได้ สารที่มีรูพรุนต่างๆ สามารถใช้เป็นตัวกรองได้: สำลี ถ่านหิน ดินเหนียว แก้วอัด และอื่นๆ วิธีการกรองเป็นพื้นฐานสำหรับการทำงานของเครื่องใช้ในครัวเรือน เช่น เครื่องดูดฝุ่น มันถูกใช้โดยศัลยแพทย์ - ผ้าพันแผลผ้ากอซ; ช่างเจาะและคนงานลิฟต์ - หน้ากากช่วยหายใจ Ostap Bender ฮีโร่ของผลงานของ Ilf และ Petrov ใช้ที่กรองชากรองใบชา จัดการเก้าอี้ตัวหนึ่งจาก Ellochka the Ogress (“Twelve Chairs”) การแยกส่วนผสมแป้งและน้ำโดยการกรอง |
ส่วนผสมของเหล็กและผงกำมะถัน | การกระทำด้วยแม่เหล็กหรือน้ำ ผงเหล็กถูกดึงดูดด้วยแม่เหล็ก แต่ผงกำมะถันไม่ได้ถูกดึงดูด ผงกำมะถันที่ไม่เปียกลอยอยู่บนผิวน้ำ และผงเหล็กหนักที่เปียกได้ตกลงไปที่ด้านล่าง แยกส่วนผสมของกำมะถันและเหล็กโดยใช้แม่เหล็กและน้ำ |
สารละลายเกลือในน้ำเป็นส่วนผสมที่เป็นเนื้อเดียวกัน | การระเหยหรือการตกผลึก น้ำจะระเหยออกไป เหลือผลึกเกลือไว้ในถ้วยพอร์ซเลน เมื่อน้ำระเหยจากทะเลสาบ Elton และ Baskunchak จะได้เกลือแกง วิธีการแยกนี้ขึ้นอยู่กับความแตกต่างของจุดเดือดของตัวทำละลายและตัวถูกละลาย หากสารเช่นน้ำตาลสลายตัวเมื่อถูกความร้อนน้ำจะไม่ระเหยไปจนหมด - สารละลายจะระเหยออกไปจากนั้นผลึกน้ำตาลจะตกตะกอนจากสารละลายอิ่มตัว บางครั้งจำเป็นต้องขจัดสิ่งเจือปนออกจากตัวทำละลายที่มีจุดเดือดต่ำกว่า เช่น เกลือ ออกจากน้ำ ในกรณีนี้ ไอระเหยของสารจะต้องถูกรวบรวมและควบแน่นเมื่อเย็นลง วิธีการแยกส่วนผสมที่เป็นเนื้อเดียวกันนี้เรียกว่า การกลั่นหรือการกลั่น- ในอุปกรณ์พิเศษ - เครื่องกลั่นจะได้รับน้ำกลั่นซึ่งใช้สำหรับความต้องการของเภสัชวิทยาห้องปฏิบัติการและระบบทำความเย็นในรถยนต์ ที่บ้านคุณสามารถสร้างเครื่องกลั่นได้: หากคุณแยกส่วนผสมของแอลกอฮอล์กับน้ำ แอลกอฮอล์ที่มีจุดเดือด = 78 °C จะถูกกลั่นออกก่อน (เก็บในหลอดทดลองที่รับ) และน้ำจะยังคงอยู่ในหลอดทดลอง การกลั่นใช้ในการผลิตน้ำมันเบนซิน น้ำมันก๊าด และน้ำมันแก๊สจากน้ำมัน การแยกสารผสมที่เป็นเนื้อเดียวกัน |
วิธีการพิเศษในการแยกส่วนประกอบโดยพิจารณาจากการดูดซึมที่แตกต่างกันของสารบางชนิดคือ โครมาโตกราฟี.
นักพฤกษศาสตร์ชาวรัสเซียใช้โครมาโทกราฟีในการแยกคลอโรฟิลล์จากส่วนสีเขียวของพืชเป็นครั้งแรก ในอุตสาหกรรมและห้องปฏิบัติการ แป้ง ถ่านหิน หินปูน และอลูมิเนียมออกไซด์ถูกนำมาใช้แทนกระดาษกรองสำหรับโครมาโตกราฟี จำเป็นต้องใช้สารที่มีระดับการทำให้บริสุทธิ์เท่ากันเสมอหรือไม่
เพื่อวัตถุประสงค์ที่แตกต่างกัน จำเป็นต้องใช้สารที่มีระดับการทำให้บริสุทธิ์ต่างกัน น้ำปรุงอาหารควรปล่อยให้ยืนเพียงพอเพื่อขจัดสิ่งเจือปนและคลอรีนที่ใช้ฆ่าเชื้อ ต้องต้มน้ำสำหรับดื่มก่อน และในห้องปฏิบัติการเคมีเพื่อเตรียมสารละลายและทำการทดลองในทางการแพทย์จำเป็นต้องใช้น้ำกลั่นและทำให้บริสุทธิ์จากสารที่ละลายในนั้นให้มากที่สุด สารบริสุทธิ์โดยเฉพาะซึ่งมีปริมาณสารเจือปนไม่เกินหนึ่งในล้านเปอร์เซ็นต์นั้นถูกใช้ในอุตสาหกรรมอิเล็กทรอนิกส์ เซมิคอนดักเตอร์ เทคโนโลยีนิวเคลียร์ และอุตสาหกรรมที่มีความแม่นยำอื่นๆ
วิธีแสดงองค์ประกอบของสารผสม
· เศษส่วนมวลของส่วนประกอบในส่วนผสม- อัตราส่วนของมวลของส่วนประกอบต่อมวลของส่วนผสมทั้งหมด โดยปกติแล้วเศษส่วนมวลจะแสดงเป็น % แต่ก็ไม่จำเป็นเสมอไป
ω ["โอเมก้า"] = mcomponent / mmmixture
· เศษส่วนโมลของส่วนประกอบในส่วนผสม- อัตราส่วนของจำนวนโมล (ปริมาณของสาร) ของส่วนประกอบต่อจำนวนโมลทั้งหมดของสารทั้งหมดในส่วนผสม ตัวอย่างเช่น หากส่วนผสมมีสาร A, B และ C ดังนั้น:
χ ["chi"] องค์ประกอบ A = ส่วนประกอบ A / (n(A) + n(B) + n(C))
· อัตราส่วนฟันกรามของส่วนประกอบบางครั้งปัญหาของส่วนผสมอาจบ่งบอกถึงอัตราส่วนโมลของส่วนประกอบต่างๆ ตัวอย่างเช่น:
ไม่มีองค์ประกอบ A: ไม่มีองค์ประกอบ B = 2: 3
· ปริมาตรของส่วนประกอบในส่วนผสม (สำหรับก๊าซเท่านั้น)- อัตราส่วนของปริมาตรของสาร A ต่อปริมาตรรวมของส่วนผสมก๊าซทั้งหมด
φ ["phi"] = Vcomponent / Vmixture
บล็อกการปฏิบัติ
ลองดูตัวอย่างปัญหาสามประการที่สารผสมของโลหะทำปฏิกิริยากัน เกลือกรด:
ตัวอย่างที่ 1เมื่อส่วนผสมของทองแดงและเหล็กน้ำหนัก 20 กรัมสัมผัสกับกรดไฮโดรคลอริกส่วนเกิน จะปล่อยก๊าซ 5.6 ลิตร (n.e.) ออกมา กำหนดเศษส่วนมวลของโลหะในส่วนผสม
ในตัวอย่างแรก ทองแดงไม่ทำปฏิกิริยากับกรดไฮโดรคลอริก กล่าวคือ ไฮโดรเจนจะถูกปล่อยออกมาเมื่อกรดทำปฏิกิริยากับเหล็ก ดังนั้นเมื่อรู้ปริมาตรของไฮโดรเจน เราก็สามารถหาปริมาณและมวลของเหล็กได้ทันที และตามด้วยเศษส่วนมวลของสารในส่วนผสม
วิธีแก้ตัวอย่างที่ 1
n = V / Vm = 5.6 / 22.4 = 0.25 โมล
2. ตามสมการปฏิกิริยา:
3. ปริมาณธาตุเหล็กก็เท่ากับ 0.25 โมล คุณสามารถค้นหามวลของมันได้:
mFe = 0.25 56 = 14 กรัม
คำตอบ: เหล็ก 70%, ทองแดง 30%
ตัวอย่างที่ 2เมื่อส่วนผสมของอะลูมิเนียมและเหล็กที่มีน้ำหนัก 11 กรัมสัมผัสกับกรดไฮโดรคลอริกส่วนเกิน จะเกิดก๊าซ 8.96 ลิตร (n.e.) ที่ถูกปล่อยออกมา กำหนดเศษส่วนมวลของโลหะในส่วนผสม
ในตัวอย่างที่สอง ปฏิกิริยาคือ ทั้งคู่โลหะ ในกรณีนี้ ไฮโดรเจนถูกปล่อยออกมาจากกรดแล้วในปฏิกิริยาทั้งสอง ดังนั้นจึงไม่สามารถใช้การคำนวณโดยตรงได้ที่นี่ ในกรณีเช่นนี้ จะสะดวกในการแก้โดยใช้ระบบสมการง่ายๆ โดยให้ x เป็นจำนวนโมลของโลหะชนิดใดชนิดหนึ่ง และ y เป็นปริมาณของสารในวินาที
วิธีแก้ตัวอย่างที่ 2
1. ค้นหาปริมาณไฮโดรเจน:
n = V / Vm = 8.96 / 22.4 = 0.4 โมล
2. ให้ปริมาณอะลูมิเนียมเท่ากับ x โมล และปริมาณเหล็กเท่ากับ x โมล จากนั้นเราสามารถแสดงปริมาณไฮโดรเจนที่ปล่อยออกมาในรูปของ x และ y ได้:
2HCl = FeCl2 + |
4. เรารู้ปริมาณไฮโดรเจนทั้งหมด: 0.4 โมล วิธี,
1.5x + y = 0.4 (นี่คือสมการแรกในระบบ)
5. สำหรับส่วนผสมของโลหะคุณต้องแสดงออก มวลชนผ่านปริมาณของสาร
ม. = ม
ดังนั้นมวลของอะลูมิเนียม
มอล = 27x,
มวลของเหล็ก
ม.เฟ = 56у,
และมวลของส่วนผสมทั้งหมด
27x + 56y = 11 (นี่คือสมการที่สองในระบบ)
6. เรามีระบบสองสมการ:
7. สะดวกกว่ามากในการแก้ระบบดังกล่าวโดยใช้วิธีการลบโดยคูณสมการแรกด้วย 18:
27x + 18y = 7.2
และลบสมการแรกออกจากสมการที่สอง:
8. (56 − 18)y = 11 − 7.2
y = 3.8 / 38 = 0.1 โมล (เฟ)
x = 0.2 โมล (อัล)
mFe = n M = 0.1 56 = 5.6 กรัม
มิลลิอัล = 0.2 27 = 5.4 กรัม
ωFe = mFe / mm ส่วนผสม = 5.6 / 11 = 0.50.91%)
ตามลำดับ
ωอัล = 100% - 50.91% = 49.09%
คำตอบ: เหล็ก 50.91%, อลูมิเนียม 49.09%
ตัวอย่างที่ 3ส่วนผสมของสังกะสีอลูมิเนียมและทองแดง 16 กรัมได้รับการบำบัดด้วยสารละลายกรดไฮโดรคลอริกส่วนเกิน ในกรณีนี้ปล่อยก๊าซ (n.o.) จำนวน 5.6 ลิตร และสาร 5 กรัมไม่ละลาย กำหนดเศษส่วนมวลของโลหะในส่วนผสม
ในตัวอย่างที่สาม โลหะสองชนิดทำปฏิกิริยา แต่โลหะตัวที่สาม (ทองแดง) ไม่ทำปฏิกิริยา ดังนั้นส่วนที่เหลือของ 5 กรัมคือมวลของทองแดง ปริมาณของโลหะสองชนิดที่เหลือ ได้แก่ สังกะสีและอะลูมิเนียม (โปรดทราบว่ามวลรวมของโลหะทั้งสองคือ 16 − 5 = 11 กรัม) สามารถพบได้โดยใช้ระบบสมการ ดังตัวอย่างที่ 2
ตอบตัวอย่างที่ 3: สังกะสี 56.25%, อลูมิเนียม 12.5%, ทองแดง 31.25%
ตัวอย่างที่ 4ส่วนผสมของเหล็ก อลูมิเนียม และทองแดงได้รับการบำบัดด้วยกรดซัลฟิวริกเข้มข้นเย็นที่มากเกินไป ในกรณีนี้ส่วนผสมบางส่วนละลายและปล่อยก๊าซ 5.6 ลิตร (n.o.) ของผสมที่เหลือถูกบำบัดด้วยสารละลายโซเดียมไฮดรอกไซด์ที่มากเกินไป ปล่อยก๊าซออกมา 3.36 ลิตร และยังมีสารตกค้างที่ไม่ละลายน้ำ 3 กรัม กำหนดมวลและองค์ประกอบของส่วนผสมเริ่มต้นของโลหะ
ในตัวอย่างนี้ เราต้องจำไว้ว่า เข้มข้นเย็นกรดซัลฟิวริกไม่ทำปฏิกิริยากับเหล็กและอลูมิเนียม (ทู่) แต่ทำปฏิกิริยากับทองแดง สิ่งนี้จะปล่อยซัลเฟอร์ (IV) ออกไซด์ออกมา
มีฤทธิ์เป็นด่างตอบสนอง อลูมิเนียมเท่านั้น- โลหะแอมโฟเทอริก (นอกเหนือจากอลูมิเนียม สังกะสี และดีบุกยังละลายในอัลคาไล และเบริลเลียมก็สามารถละลายในอัลคาไลเข้มข้นที่ร้อนได้เช่นกัน)
เฉลยตัวอย่างที่ 4
1. มีเพียงทองแดงเท่านั้นที่ทำปฏิกิริยากับกรดซัลฟิวริกเข้มข้น จำนวนโมลของก๊าซ:
nSO2 = V / Vm = 5.6 / 22.4 = 0.25 โมล
2H2SO4 (เข้มข้น) = CuSO4 + |
2. (อย่าลืมว่าปฏิกิริยาดังกล่าวจะต้องทำให้เท่ากันโดยใช้เครื่องชั่งอิเล็กทรอนิกส์)
3. เนื่องจากอัตราส่วนโมลาร์ของทองแดงและซัลเฟอร์ไดออกไซด์คือ 1:1 ดังนั้นทองแดงจึงเป็น 0.25 โมลด้วย คุณสามารถค้นหามวลทองแดงได้:
mCu = n M = 0.25 64 = 16 กรัม
4. อลูมิเนียมทำปฏิกิริยากับสารละลายอัลคาไลซึ่งส่งผลให้เกิดไฮดรอกโซคอมเพล็กซ์ของอลูมิเนียมและไฮโดรเจน:
2Al + 2NaOH + 6H2O = 2Na + 3H2
Al0 − 3e = Al3+ | ||
5. จำนวนโมลของไฮโดรเจน:
nH2 = 3.36 / 22.4 = 0.15 โมล
อัตราส่วนโมลของอลูมิเนียมและไฮโดรเจนคือ 2:3 ดังนั้น
nAl = 0.15 / 1.5 = 0.1 โมล
น้ำหนักอลูมิเนียม:
mAl = n M = 0.1 27= 2.7 กรัม
6. ส่วนที่เหลือเป็นเหล็กหนัก 3 กรัม คุณสามารถหามวลของส่วนผสมได้:
มิลลิเมตรส่วนผสม = 16 + 2.7 + 3 = 21.7 กรัม
7. เศษส่วนมวลของโลหะ:
ωCu = mCu / mm ส่วนผสม = 16 / 21.7 = 0.7.73%)
ωอัล = 2.7 / 21.7 = 0.1.44%)
ωเฟ = 13.83%
คำตอบ: ทองแดง 73.73% อลูมิเนียม 12.44% เหล็ก 13.83%
ตัวอย่างที่ 5ของผสมของสังกะสีและอะลูมิเนียม 21.1 กรัมถูกละลายในสารละลายกรดไนตริก 565 มิลลิลิตรที่มี 20 น้ำหนัก % НNO3 และมีความหนาแน่น 1.115 กรัม/มิลลิลิตร ปริมาตรของก๊าซที่ปล่อยออกมาซึ่งเป็นสารเดี่ยวและเป็นผลิตภัณฑ์เดียวที่ช่วยลดกรดไนตริกได้คือ 2.912 ลิตร (หมายเลข) กำหนดองค์ประกอบของสารละลายที่ได้เป็นเปอร์เซ็นต์มวล (สธธ.)
ข้อความของปัญหานี้แสดงให้เห็นอย่างชัดเจนถึงผลคูณของการลดไนโตรเจน - "สารธรรมดา" เนื่องจากกรดไนตริกกับโลหะไม่ได้ผลิตไฮโดรเจน จึงเป็นไนโตรเจน โลหะทั้งสองละลายในกรด
ปัญหาไม่ได้ถามถึงองค์ประกอบของส่วนผสมเริ่มต้นของโลหะ แต่เป็นองค์ประกอบของสารละลายที่เกิดขึ้นหลังปฏิกิริยา ทำให้งานยากขึ้น
เฉลยตัวอย่างที่ 5
1. กำหนดปริมาณของสารก๊าซ:
nN2 = V / Vm = 2.912 / 22.4 = 0.13 โมล
2. หามวลของสารละลายกรดไนตริก มวลและปริมาณของ HNO3 ที่ละลาย:
msolution = ρ V = 1.115 565 = 630.3 กรัม
mHNO3 = ω mสารละลาย = 0.2 630.3 = 126.06 กรัม
nHNO3 = m / M = 126.06 / 63 = 2 โมล
โปรดทราบว่าเนื่องจากโลหะละลายหมดแล้ว จึงหมายความว่า - มีกรดเพียงพอแน่นอน(โลหะเหล่านี้ไม่ทำปฏิกิริยากับน้ำ) ดังนั้นจึงจำเป็นต้องตรวจสอบ มีกรดมากเกินไปหรือไม่?และจะเหลือปริมาณเท่าใดหลังจากปฏิกิริยาในสารละลายที่ได้
3. เราเขียนสมการปฏิกิริยา ( อย่าลืมเกี่ยวกับเครื่องชั่งอิเล็กทรอนิกส์ของคุณ) และเพื่อความสะดวกในการคำนวณ เราจะเอา 5x เป็นปริมาณสังกะสี และ 10y เป็นปริมาณอะลูมิเนียม จากนั้นตามค่าสัมประสิทธิ์ในสมการ ไนโตรเจนในปฏิกิริยาแรกจะเป็น x โมล และในวินาที - 3y โมล:
12HNO3 = 5Zn(NO3)2 + |
Zn0 − 2e = Zn2+ | ||
36HNO3 = 10อัล(NO3)3 + |
Al0 − 3e = Al3+ | ||
5. จากนั้น เมื่อพิจารณาว่ามวลของส่วนผสมของโลหะคือ 21.1 กรัม มวลโมลของพวกมันคือ 65 กรัม/โมลสำหรับสังกะสี และ 27 กรัม/โมลสำหรับอะลูมิเนียม เราจะได้ระบบสมการต่อไปนี้:
6. สะดวกในการแก้ระบบนี้โดยการคูณสมการแรกด้วย 90 แล้วลบสมการแรกออกจากสมการที่สอง
7. x = 0.04 ซึ่งหมายถึง nZn = 0.04 5 = 0.2 โมล
y = 0.03 ซึ่งหมายถึง nAl = 0.03 10 = 0.3 โมล
8. ตรวจสอบมวลของส่วนผสม:
0.2 65 + 0.3 27 = 21.1 ก.
9. ตอนนี้เรามาดูองค์ประกอบของการแก้ปัญหากันดีกว่า จะสะดวกในการเขียนปฏิกิริยาอีกครั้งและเขียนปริมาณของสารที่เกิดปฏิกิริยาและเกิดทั้งหมดเหนือปฏิกิริยา (ยกเว้นน้ำ):
10. คำถามต่อไป สารละลายมีกรดไนตริกเหลืออยู่หรือไม่ และเหลืออยู่เท่าใด
ตามสมการปฏิกิริยา ปริมาณของกรดที่ทำปฏิกิริยา:
nHNO3 = 0.48 + 1.08 = 1.56 โมล
กล่าวคือ มีกรดมากเกินไป และคุณสามารถคำนวณส่วนที่เหลือในสารละลายได้:
nHNO3res = 2 − 1.56 = 0.44 โมล
11. เอาล่ะเข้า ทางออกสุดท้ายประกอบด้วย:
ซิงค์ไนเตรตในปริมาณ 0.2 โมล:
mZn(NO3)2 = n M = 0.2 189 = 37.8 กรัม
อลูมิเนียมไนเตรตจำนวน 0.3 โมล:
มิลลิอัล(NO3)3 = n M = 0.3 · 213 = 63.9 กรัม
กรดไนตริกส่วนเกินในปริมาณ 0.44 โมล:
mHNO3rest. = n M = 0.44 63 = 27.72 กรัม
12. มวลของสารละลายสุดท้ายคือเท่าใด?
ให้เราจำไว้ว่ามวลของสารละลายสุดท้ายประกอบด้วยส่วนประกอบที่เราผสม (สารละลายและสารต่างๆ) ลบด้วยผลิตภัณฑ์ที่ทำปฏิกิริยาที่ทิ้งสารละลายไว้ (ตะกอนและก๊าซ):
13.
จากนั้นสำหรับงานของเรา:
14. มนิว สารละลาย = มวลของสารละลายกรด + มวลของโลหะผสม - มวลของไนโตรเจน
mN2 = n M = 28 (0.03 + 0.09) = 3.36 กรัม
ใหม่ สารละลาย = 630.3 + 21.1 − 3.36 = 648.04 กรัม
ωZn(NO3)2 = mv-va / mr-ra = 37.8 / 648.04 = 0.0583
ωAl(NO3)3 = mv-va / mr-ra = 63.9 / 648.04 = 0.0986
ωHNO3ส่วนที่เหลือ = mv-va / mr-ra = 27.72 / 648.04 = 0.0428
คำตอบ: ซิงค์ไนเตรต 5.83%, อลูมิเนียมไนเตรต 9.86%, กรดไนตริก 4.28%
ตัวอย่างที่ 6เมื่อส่วนผสมของทองแดง เหล็ก และอลูมิเนียม 17.4 กรัมได้รับการบำบัดด้วยกรดไนตริกเข้มข้นที่มากเกินไป จะปล่อยก๊าซ 4.48 ลิตร (n.e.) ออกมา และเมื่อส่วนผสมนี้สัมผัสกับกรดไฮโดรคลอริกส่วนเกินที่มีมวลเท่ากัน จะได้ 8.96 ลิตรของ ก๊าซ (n.e.) ถูกปล่อยออกมา กำหนดองค์ประกอบของส่วนผสมเริ่มต้น (สธธ.)
เมื่อแก้ไขปัญหานี้ เราต้องจำไว้ว่า ประการแรก กรดไนตริกเข้มข้นกับโลหะที่ไม่ใช้งาน (ทองแดง) จะผลิต NO2 แต่เหล็กและอลูมิเนียมไม่ทำปฏิกิริยากับมัน กรดไฮโดรคลอริกไม่ทำปฏิกิริยากับทองแดง
ตอบตัวอย่างที่ 6: ทองแดง 36.8%, เหล็ก 32.2%, อลูมิเนียม 31%
ปัญหาสำหรับการแก้ปัญหาอย่างอิสระ
1. ปัญหาง่ายๆ กับส่วนผสมสองอย่าง
1-1. ส่วนผสมของทองแดงและอลูมิเนียมที่มีน้ำหนัก 20 กรัมได้รับการบำบัดด้วยสารละลายกรดไนตริก 96% และปล่อยก๊าซ (n.o.) จำนวน 8.96 ลิตร หาสัดส่วนมวลของอะลูมิเนียมในส่วนผสม
1-2. ส่วนผสมของทองแดงและสังกะสีที่มีน้ำหนัก 10 กรัมได้รับการบำบัดด้วยสารละลายอัลคาไลเข้มข้น ในกรณีนี้มีการปล่อยก๊าซ 2.24 ลิตร (ny) คำนวณเศษส่วนมวลของสังกะสีในส่วนผสมตั้งต้น.
1-3. ส่วนผสมของแมกนีเซียมและแมกนีเซียมออกไซด์ที่มีน้ำหนัก 6.4 กรัมได้รับการบำบัดด้วยกรดซัลฟิวริกเจือจางในปริมาณที่เพียงพอ ในกรณีนี้ปล่อยก๊าซ (n.o.) จำนวน 2.24 ลิตร หาสัดส่วนมวลของแมกนีเซียมในส่วนผสม.
1-4. ส่วนผสมของสังกะสีและซิงค์ออกไซด์ที่มีน้ำหนัก 3.08 กรัมถูกละลายในกรดซัลฟิวริกเจือจาง เราได้รับซิงค์ซัลเฟตที่มีน้ำหนัก 6.44 กรัม คำนวณเศษส่วนมวลของสังกะสีในส่วนผสมดั้งเดิม
1-5. เมื่อส่วนผสมของเหล็กและผงสังกะสีที่มีน้ำหนัก 9.3 กรัมสัมผัสกับสารละลายคอปเปอร์ (II) คลอไรด์ส่วนเกิน จะเกิดทองแดงขึ้น 9.6 กรัม กำหนดองค์ประกอบของส่วนผสมเริ่มต้น
1-6. จะต้องใช้สารละลายกรดไฮโดรคลอริก 20% มวลเท่าใดในการละลายส่วนผสมของสังกะสีและซิงค์ออกไซด์ 20 กรัมอย่างสมบูรณ์หากปล่อยไฮโดรเจนออกมาพร้อมกันด้วยปริมาตร 4.48 ลิตร (หมายเลข)
1-7. เมื่อส่วนผสมของเหล็กและทองแดง 3.04 กรัมละลายในกรดไนตริกเจือจาง ไนโตรเจนออกไซด์ (II) จะถูกปล่อยออกมาด้วยปริมาตร 0.896 ลิตร (หมายเลข) กำหนดองค์ประกอบของส่วนผสมเริ่มต้น
1-8. เมื่อส่วนผสมของตะไบเหล็กและอะลูมิเนียม 1.11 กรัมละลายในสารละลายกรดไฮโดรคลอริก 16% (ρ = 1.09 กรัม/มิลลิลิตร) ไฮโดรเจน 0.672 ลิตร (n.e.) จะถูกปล่อยออกมา ค้นหาเศษส่วนมวลของโลหะในส่วนผสมและหาปริมาตรของกรดไฮโดรคลอริกที่ใช้ไป
2. งานมีความซับซ้อนมากขึ้น
2-1. ส่วนผสมของแคลเซียมและอลูมิเนียมน้ำหนัก 18.8 กรัมถูกเผาโดยไม่มีอากาศและมีผงกราไฟท์มากเกินไป ผลิตภัณฑ์ที่ทำปฏิกิริยาได้รับการบำบัดด้วยกรดไฮโดรคลอริกเจือจาง และก๊าซ 11.2 ลิตร (n.o.) ถูกปล่อยออกมา กำหนดเศษส่วนมวลของโลหะในส่วนผสม
2-2. ในการละลายโลหะผสมแมกนีเซียม-อลูมิเนียม 1.26 กรัม ให้ใช้สารละลายกรดซัลฟิวริก 19.6% 35 มล. (ρ = 1.1 กรัม/มิลลิลิตร) กรดส่วนเกินทำปฏิกิริยากับสารละลายโพแทสเซียมไบคาร์บอเนต 28.6 มิลลิลิตร ที่ความเข้มข้น 1.4 โมล/ลิตร กำหนดเศษส่วนมวลของโลหะในโลหะผสมและปริมาตรของก๊าซ (หมายเลข) ที่ปล่อยออกมาระหว่างการละลายของโลหะผสม
กับ วิธีการแยกสารผสม (ทั้งต่างกันและเป็นเนื้อเดียวกัน) ขึ้นอยู่กับข้อเท็จจริงที่ว่าสารที่รวมอยู่ในส่วนผสมยังคงรักษาคุณสมบัติส่วนบุคคลไว้ สารผสมที่ต่างกันอาจแตกต่างกันในองค์ประกอบและสถานะเฟส เช่น ก๊าซ + ของเหลว ของแข็ง+ของเหลว ของเหลวที่ผสมไม่ได้สองชนิด ฯลฯ วิธีการหลักในการแยกสารผสมแสดงไว้ในแผนภาพด้านล่าง พิจารณาแต่ละวิธีแยกกัน
การแยกสารผสมที่ต่างกัน
สำหรับ การแยกสารผสมที่ต่างกันแทนระบบของแข็ง-ของเหลวหรือของแข็ง-ก๊าซ มีสามวิธีหลัก:
- การกรอง,
- การตกตะกอน (การกลั่น,
- การแยกแม่เหล็ก
การกรอง
วิธีการขึ้นอยู่กับความสามารถในการละลายของสารต่างๆ และขนาดอนุภาคที่แตกต่างกันของส่วนประกอบของส่วนผสม การกรองช่วยให้คุณสามารถแยกของแข็งออกจากของเหลวหรือก๊าซได้
ในการกรองของเหลว คุณสามารถใช้กระดาษกรองซึ่งโดยปกติจะพับเป็นสี่ส่วนแล้วสอดเข้าไปในกรวยแก้ว วางกรวยไว้ในแก้วซึ่งสะสมอยู่ กรอง- ของเหลวที่ไหลผ่านตัวกรอง
ขนาดของรูพรุนในกระดาษกรองช่วยให้โมเลกุลของน้ำและโมเลกุลของตัวถูกละลายรั่วซึมได้โดยไม่มีสิ่งกีดขวาง อนุภาคที่มีขนาดใหญ่กว่า 0.01 มม. จะยังคงอยู่ในตัวกรองและไม่เป็นเช่นนั้นผ่านไปจนเกิดเป็นชั้นตะกอน
จดจำ!การใช้การกรองเป็นไปไม่ได้ที่จะแยกสารละลายที่แท้จริงของสารออก กล่าวคือ สารละลายที่มีการละลายเกิดขึ้นที่ระดับโมเลกุลหรือไอออน
นอกจากกระดาษกรองแล้ว ห้องปฏิบัติการเคมียังใช้ตัวกรองพิเศษด้วย
ขนาดรูพรุนที่แตกต่างกัน
การกรองส่วนผสมของก๊าซไม่แตกต่างจากการกรองของเหลวโดยพื้นฐาน ข้อแตกต่างเพียงอย่างเดียวคือเมื่อกรองก๊าซจากอนุภาคแขวนลอย (SPM) ตัวกรองที่มีการออกแบบพิเศษ (กระดาษ คาร์บอน) และปั๊มจะถูกนำมาใช้เพื่อบังคับส่วนผสมของก๊าซผ่านตัวกรอง เช่น กรองอากาศในรถยนต์หรือเครื่องดูดควัน เหนือเตา
สามารถแยกได้โดยการกรอง:
- ธัญพืชและน้ำ
- ชอล์กและน้ำ
- ทรายและน้ำ ฯลฯ
- ฝุ่นและอากาศ (เครื่องดูดฝุ่นดีไซน์ต่างๆ)
การตั้งถิ่นฐาน
วิธีการนี้ขึ้นอยู่กับอัตราการตกตะกอนที่แตกต่างกันของอนุภาคของแข็งที่มีน้ำหนัก (ความหนาแน่น) ต่างกันในสภาพแวดล้อมของเหลวหรืออากาศ วิธีการนี้ใช้เพื่อแยกสารที่เป็นของแข็งที่ไม่ละลายน้ำตั้งแต่ 2 ชนิดขึ้นไปออกจากน้ำ (หรือตัวทำละลายอื่นๆ) ส่วนผสมของสารที่ไม่ละลายน้ำจะถูกใส่ลงในน้ำและผสมให้เข้ากัน หลังจากนั้นครู่หนึ่ง สสารที่มีความหนาแน่นมากกว่าหนึ่งจะตกลงไปที่ด้านล่างของภาชนะ และสสารที่มีความหนาแน่นน้อยกว่าหนึ่งจะลอยขึ้นสู่พื้นผิว หากมีสารหลายชนิดที่มีแรงโน้มถ่วงต่างกันในส่วนผสม สารที่หนักกว่าก็จะตกลงไปที่ชั้นล่างและสารที่เบากว่า เลเยอร์ดังกล่าวสามารถแยกออกได้ ก่อนหน้านี้ นี่เป็นวิธีที่แยกเม็ดทองคำออกจากหินที่มีทองคำบด ทรายที่มีทองคำวางอยู่บนร่องลึกซึ่งมีน้ำไหลผ่าน กระแสน้ำพัดพาก้อนหินที่รกร้างออกไป และมีเม็ดทองคำหนักตกลงอยู่ที่ก้นคูน้ำ ในกรณีของส่วนผสมของแก๊ส อนุภาคของแข็งจะเกาะอยู่บนพื้นผิวแข็งด้วย เช่น ฝุ่นเกาะบนเฟอร์นิเจอร์หรือใบพืช
วิธีนี้สามารถใช้ในการแยกของเหลวที่ผสมไม่ได้เข้าด้วยกัน เมื่อต้องการทำเช่นนี้ ให้ใช้กรวยแยก
ตัวอย่างเช่น หากต้องการแยกน้ำมันเบนซินและน้ำ ส่วนผสมจะถูกวางในกรวยแยกและรอจนกระทั่งขอบเขตเฟสที่ชัดเจนปรากฏขึ้น จากนั้นค่อยเปิดก๊อกน้ำแล้วน้ำไหลเข้าแก้ว
ส่วนผสมสามารถแยกออกได้ด้วยการตกตะกอน:
- ทรายแม่น้ำและดินเหนียว
- ตกตะกอนผลึกหนักจากสารละลาย
- น้ำมันและน้ำ
- น้ำมันพืชและน้ำ ฯลฯ
การแยกแม่เหล็ก
วิธีการนี้ขึ้นอยู่กับคุณสมบัติทางแม่เหล็กที่แตกต่างกันของส่วนประกอบที่เป็นของแข็งของส่วนผสม วิธีการนี้ใช้เมื่อส่วนผสมมีสารเฟอร์โรแมกเนติก ซึ่งก็คือสารที่มีคุณสมบัติเป็นแม่เหล็ก เช่น เหล็ก
สสารทั้งหมดที่เกี่ยวข้องกับสนามแม่เหล็กสามารถแบ่งออกเป็นสามกลุ่มใหญ่:
- ฟีโรแมกเนติก: แม่เหล็กดึงดูด - Fe, Co, Ni, Gd, Dy
- พาราแมกเนติก: ดึงดูดเล็กน้อย - Al, Cr, Ti, V, W, Mo
- วัสดุแม่เหล็ก: ลอกด้วยแม่เหล็ก - Cu, Ag, Au, Bi, Sn, ทองเหลือง
การแยกแม่เหล็กสามารถแยกออกได้ข:
- กำมะถันและผงเหล็ก
- เขม่าและเหล็ก ฯลฯ
การแยกสารผสมที่เป็นเนื้อเดียวกัน
สำหรับ การแยกสารผสมที่เป็นเนื้อเดียวกันของของเหลว (สารละลายที่แท้จริง)ใช้วิธีการต่อไปนี้:
- การระเหย (การตกผลึก)
- การกลั่น (การกลั่น)
- โครมาโตกราฟี
การระเหย การตกผลึก
วิธีการนี้ขึ้นอยู่กับอุณหภูมิจุดเดือดที่แตกต่างกันของตัวทำละลายและตัวถูกละลาย ใช้เพื่อแยกของแข็งที่ละลายน้ำได้จากสารละลาย โดยปกติการระเหยจะดำเนินการดังนี้: เทสารละลายลงในถ้วยพอร์ซเลนและให้ความร้อนโดยกวนสารละลายอย่างต่อเนื่อง น้ำจะค่อยๆระเหยและมีของแข็งเหลืออยู่ที่ด้านล่างของถ้วย
คำนิยาม
การตกผลึก- การเปลี่ยนเฟสของสารจากสถานะก๊าซ (ไอ) ของเหลวหรือของแข็งเป็นสถานะผลึก
ในกรณีนี้ สารระเหย (น้ำหรือตัวทำละลาย) อาจถูกรวบรวมโดยการควบแน่นบนพื้นผิวที่เย็นกว่า ตัวอย่างเช่น หากคุณวางสไลด์แก้วเย็นลงบนจานระเหย หยดน้ำก็จะก่อตัวขึ้นบนพื้นผิว วิธีการกลั่นก็ใช้หลักการเดียวกัน
การกลั่น การกลั่น
หากสารเช่นน้ำตาลสลายตัวเมื่อถูกความร้อนน้ำจะไม่ระเหยไปจนหมด - สารละลายจะระเหยออกไปจากนั้นผลึกน้ำตาลจะตกตะกอนจากสารละลายอิ่มตัว บางครั้งจำเป็นต้องขจัดสิ่งเจือปนออกจากตัวทำละลาย เช่น เกลือ ออกจากน้ำ ในกรณีนี้ ตัวทำละลายจะต้องถูกระเหย จากนั้นไอของตัวทำละลายจะต้องถูกรวบรวมและควบแน่นเมื่อเย็นลง วิธีการแยกส่วนผสมที่เป็นเนื้อเดียวกันนี้เรียกว่า การกลั่นหรือการกลั่น
ในธรรมชาติ น้ำไม่ได้เกิดขึ้นในรูปแบบบริสุทธิ์ (ไม่มีเกลือ) มหาสมุทร ทะเล แม่น้ำ บ่อน้ำ และน้ำพุเป็นสารละลายเกลือในน้ำประเภทหนึ่ง อย่างไรก็ตาม ผู้คนมักต้องการน้ำสะอาดที่ไม่มีเกลือ (ใช้ในเครื่องยนต์ของรถยนต์ ในการผลิตสารเคมีเพื่อให้ได้สารละลายและสารต่างๆ ในการถ่ายภาพ) น้ำนี้เรียกว่า กลั่นเป็นสิ่งที่ใช้ในห้องปฏิบัติการเพื่อทำการทดลองทางเคมีอย่างแม่นยำ
การกลั่นสามารถแบ่งออกเป็น:
- น้ำและแอลกอฮอล์
- น้ำมัน (เป็นเศษส่วนต่างๆ)
- อะซิโตนและน้ำ ฯลฯ
หัวข้อ: “วิธีการแยกสารผสม” (เกรด 8)โครมาโตกราฟี
วิธีการแยกและวิเคราะห์สารผสม ขึ้นอยู่กับอัตราการกระจายตัวของสารทดสอบที่แตกต่างกันระหว่างสองเฟส - แบบอยู่กับที่และแบบเคลื่อนที่ (ชะล้าง- ตามกฎแล้ว เฟสคงที่คือตัวดูดซับ (ผงละเอียด เช่น อลูมิเนียมออกไซด์หรือซิงค์ออกไซด์หรือกระดาษกรอง) ที่มีพื้นผิวที่พัฒนาแล้ว และเฟสเคลื่อนที่คือการไหลของก๊าซหรือของเหลว การไหลของเฟสเคลื่อนที่จะถูกกรองผ่านชั้นตัวดูดซับหรือเคลื่อนไปตามชั้นตัวดูดซับ ตัวอย่างเช่น ไปตามพื้นผิวของกระดาษกรอง
คุณสามารถรับโครมาโตแกรมได้อย่างอิสระและดูสาระสำคัญของวิธีการในทางปฏิบัติ คุณต้องผสมหมึกหลาย ๆ ชนิดแล้วหยดส่วนผสมที่ได้ลงบนกระดาษกรอง จากนั้นตรงกลางจุดสีเราจะเริ่มเทน้ำสะอาดทีละหยด ควรใช้แต่ละหยดหลังจากการดูดซึมก่อนหน้านี้แล้วเท่านั้น น้ำมีบทบาทเป็นตัวชะที่จะถ่ายโอนสารทดสอบผ่านกระดาษที่มีรูพรุนของตัวดูดซับ สารที่รวมอยู่ในส่วนผสมจะถูกกักไว้โดยกระดาษในรูปแบบต่างๆ: บางชนิดจะถูกเก็บรักษาไว้อย่างดี ในขณะที่สารอื่นๆ จะถูกดูดซึมได้ช้ากว่าและยังคงแพร่กระจายไปตามน้ำต่อไปอีกระยะหนึ่ง ในไม่ช้า โครมาโตกราฟีที่มีสีสันจริงๆ จะเริ่มกระจายไปทั่วแผ่นกระดาษ โดยมีจุดสีเดียวอยู่ตรงกลาง ล้อมรอบด้วยวงแหวนศูนย์กลางหลากสี
โครมาโตกราฟีแบบชั้นบางได้แพร่หลายโดยเฉพาะในการวิเคราะห์สารอินทรีย์ ข้อดีของโครมาโทกราฟีแบบชั้นบางก็คือ คุณสามารถใช้วิธีการตรวจจับที่ง่ายที่สุดและละเอียดอ่อนมาก นั่นคือการควบคุมด้วยภาพ จุดที่มองไม่เห็นด้วยตาสามารถเปิดเผยได้โดยใช้รีเอเจนต์หลายชนิด เช่นเดียวกับการใช้แสงอัลตราไวโอเลตหรือการถ่ายภาพด้วยรังสีอัตโนมัติ
โครมาโตกราฟีแบบกระดาษใช้ในการวิเคราะห์สารอินทรีย์และอนินทรีย์ มีการพัฒนาวิธีการมากมายสำหรับการแยกส่วนผสมที่ซับซ้อนของไอออน เช่น การผสมของธาตุหายาก ผลิตภัณฑ์ฟิชชันของยูเรเนียม ธาตุในกลุ่มแพลตตินัม
วิธีการแยกสารผสมที่ใช้ในอุตสาหกรรม
วิธีการแยกสารผสมที่ใช้ในอุตสาหกรรมมีความแตกต่างกันเล็กน้อยจากวิธีการในห้องปฏิบัติการที่อธิบายไว้ข้างต้น
การแก้ไข (การกลั่น) มักใช้เพื่อแยกน้ำมัน กระบวนการนี้อธิบายไว้ในรายละเอียดเพิ่มเติมในหัวข้อ "การกลั่นน้ำมัน".
วิธีการทำให้บริสุทธิ์และแยกสารที่ใช้กันทั่วไปในอุตสาหกรรม ได้แก่ การตกตะกอน การกรอง การดูดซับ และการสกัด วิธีการกรองและการตกตะกอนจะดำเนินการคล้ายกับวิธีการในห้องปฏิบัติการ โดยมีความแตกต่างในการใช้ถังตกตะกอนและตัวกรองปริมาณมาก ส่วนใหญ่มักจะใช้วิธีการเหล่านี้ในการบำบัดน้ำเสีย ดังนั้นเรามาดูวิธีการต่างๆ กันดีกว่า การสกัดและ การดูดซึม
คำว่า "การสกัด" สามารถนำไปใช้กับสมดุลของเฟสต่างๆ ได้ (ของเหลว-ของเหลว, ก๊าซ-ของเหลว, ของเหลว-ของแข็ง ฯลฯ) แต่บ่อยครั้งมักใช้กับระบบของเหลว-ของเหลว ดังนั้น คำจำกัดความต่อไปนี้จึงมักพบได้บ่อยที่สุด : :
คำนิยาม
การสกัด i เป็นวิธีการแยก การทำให้บริสุทธิ์ และการแยกสารตามกระบวนการกระจายสารระหว่างตัวทำละลาย 2 ตัวที่ละลายไม่ได้
ตัวทำละลายที่ละลายไม่ได้ตัวหนึ่งมักเป็นน้ำ ส่วนตัวที่สองคือตัวทำละลายอินทรีย์ แต่ไม่จำเป็น วิธีการสกัดมีความหลากหลาย เหมาะสำหรับการแยกองค์ประกอบเกือบทั้งหมดที่มีความเข้มข้นต่างกัน การสกัดทำให้คุณสามารถแยกสารผสมที่มีองค์ประกอบหลายองค์ประกอบที่ซับซ้อนได้ ซึ่งมักจะมีประสิทธิภาพและรวดเร็วกว่าวิธีอื่นๆ การดำเนินการแยกหรือแยกการสกัดไม่จำเป็นต้องใช้อุปกรณ์ที่ซับซ้อนหรือมีราคาแพง กระบวนการนี้สามารถเป็นไปโดยอัตโนมัติและควบคุมจากระยะไกลได้หากจำเป็น
คำนิยาม
การดูดซับ- วิธีการแยกและทำให้สารบริสุทธิ์โดยอาศัยการดูดซึมโดยตัวของแข็ง (การดูดซับ) หรือตัวดูดซับของเหลว (การดูดซึม) ของสารต่าง ๆ (ซอร์เบต) จากก๊าซหรือของเหลวผสม
ส่วนใหญ่ในอุตสาหกรรมมักใช้วิธีการดูดซับเพื่อกรองการปล่อยก๊าซและอากาศให้บริสุทธิ์จากฝุ่นหรืออนุภาคควัน รวมถึงก๊าซพิษ ในกรณีของการดูดซึมสารที่เป็นก๊าซ อาจเกิดปฏิกิริยาทางเคมีระหว่างตัวดูดซับและสารที่ละลายได้ เช่นเมื่อดูดซับก๊าซแอมโมเนียเอ็นเอช 3สารละลายของกรดไนตริก HNO 3 จะผลิตแอมโมเนียมไนเตรต NH 4 NO 3(แอมโมเนียมไนเตรต) ซึ่งสามารถใช้เป็นปุ๋ยไนโตรเจนที่มีประสิทธิภาพสูง
บล็อกทางทฤษฎี
คำจำกัดความของแนวคิด "ส่วนผสม" มีให้ไว้ในศตวรรษที่ 17 นักวิทยาศาสตร์ชาวอังกฤษ โรเบิร์ต บอยล์: “ของผสมคือระบบบูรณาการที่ประกอบด้วยส่วนประกอบที่ต่างกัน”
ลักษณะเปรียบเทียบของสารผสมและสารบริสุทธิ์
|
สัญญาณของการเปรียบเทียบ |
สารบริสุทธิ์ |
ส่วนผสม |
|
สารประกอบ |
คงที่ |
ไม่แน่นอน |
|
สาร |
สิ่งเดียวกัน |
หลากหลาย |
|
คุณสมบัติทางกายภาพ |
ถาวร |
ไม่แน่นอน |
|
การเปลี่ยนแปลงพลังงานระหว่างการก่อตัว |
กำลังเกิดขึ้น |
ไม่เกิดขึ้น |
|
แยก |
โดยผ่านปฏิกิริยาเคมี |
โดยวิธีการทางกายภาพ |
ส่วนผสมมีลักษณะแตกต่างกันออกไป
การจำแนกประเภทของสารผสมแสดงไว้ในตาราง:
เราจะยกตัวอย่างสารแขวนลอย (ทรายแม่น้ำ + น้ำ) อิมัลชัน (น้ำมันพืช + น้ำ) และสารละลาย (อากาศในขวด เกลือแกง + น้ำ การเปลี่ยนแปลงเล็กน้อย: อลูมิเนียม + ทองแดง หรือ นิกเกิล + ทองแดง)
วิธีการแยกสารผสม
ในธรรมชาติ สารมีอยู่ในรูปของสารผสม สำหรับการวิจัยในห้องปฏิบัติการ การผลิตทางอุตสาหกรรม และสำหรับความต้องการด้านเภสัชวิทยาและการแพทย์ จำเป็นต้องใช้สารบริสุทธิ์
มีวิธีแยกสารผสมหลายวิธีเพื่อทำให้สารบริสุทธิ์

การระเหยคือการแยกของแข็งที่ละลายในของเหลวโดยแปลงเป็นไอน้ำ

การกลั่นคือการกลั่นการแยกสารที่มีอยู่ในของผสมของเหลวตามจุดเดือดตามด้วยการทำให้ไอเย็นลง
ในธรรมชาติ น้ำไม่ได้เกิดขึ้นในรูปแบบบริสุทธิ์ (ไม่มีเกลือ) มหาสมุทร ทะเล แม่น้ำ บ่อน้ำ และน้ำพุเป็นสารละลายเกลือในน้ำประเภทหนึ่ง อย่างไรก็ตาม ผู้คนมักต้องการน้ำสะอาดที่ไม่มีเกลือ (ใช้ในเครื่องยนต์ของรถยนต์ ในการผลิตสารเคมีเพื่อให้ได้สารละลายและสารต่างๆ ในการถ่ายภาพ) น้ำดังกล่าวเรียกว่าน้ำกลั่น และวิธีการได้มาเรียกว่าการกลั่น

การกรอง - กรองของเหลว (ก๊าซ) ผ่านตัวกรองเพื่อทำความสะอาดจากสิ่งสกปรกที่เป็นของแข็ง

วิธีการเหล่านี้ขึ้นอยู่กับความแตกต่างในคุณสมบัติทางกายภาพของส่วนประกอบของสารผสม
พิจารณาวิธีการแยก ต่างกัน
และของผสมที่เป็นเนื้อเดียวกัน.
|
ตัวอย่างของส่วนผสม |
วิธีการแยก |
|
ระบบกันสะเทือน - ส่วนผสมของทรายแม่น้ำและน้ำ |
การสนับสนุน แยก ปกป้องขึ้นอยู่กับความหนาแน่นของสารที่แตกต่างกัน ทรายที่หนักกว่าจะตกลงไปที่ด้านล่าง คุณยังสามารถแยกอิมัลชันออกได้ โดยแยกน้ำมันหรือน้ำมันพืชออกจากน้ำ ในห้องปฏิบัติการ สามารถทำได้โดยใช้กรวยแยก ปิโตรเลียมหรือน้ำมันพืชจะอยู่ชั้นบนสุดและสีอ่อนกว่า ผลจากการตกตะกอน น้ำค้างตกลงมาจากหมอก เขม่าจางหายไปจากควัน และครีมก็ตกตะกอนในนม แยกส่วนผสมของน้ำและน้ำมันพืชโดยการตกตะกอน
|
|
ส่วนผสมของทรายและเกลือแกงในน้ำ |
การกรอง พื้นฐานสำหรับการแยกสารผสมที่ต่างกันโดยใช้คืออะไร การกรองความสามารถในการละลายต่างๆ ของสารในน้ำและขนาดอนุภาคต่างๆ มีเพียงอนุภาคของสารที่เทียบเคียงได้เท่านั้นที่จะผ่านเข้าไปในรูพรุนของตัวกรอง ในขณะที่อนุภาคขนาดใหญ่กว่าจะยังคงอยู่บนตัวกรอง วิธีนี้จะทำให้คุณสามารถแยกส่วนผสมที่ต่างกันของเกลือแกงและทรายแม่น้ำออกได้ สารที่มีรูพรุนต่างๆ สามารถใช้เป็นตัวกรองได้: สำลี ถ่านหิน ดินเหนียว แก้วอัด และอื่นๆ วิธีการกรองเป็นพื้นฐานสำหรับการทำงานของเครื่องใช้ในครัวเรือน เช่น เครื่องดูดฝุ่น มันถูกใช้โดยศัลยแพทย์ - ผ้าพันแผลผ้ากอซ; ช่างเจาะและคนงานลิฟต์ - หน้ากากช่วยหายใจ Ostap Bender ฮีโร่ของผลงานของ Ilf และ Petrov ใช้ที่กรองชากรองใบชา จัดการเก้าอี้ตัวหนึ่งจาก Ellochka the Ogress (“Twelve Chairs”) การแยกส่วนผสมแป้งและน้ำโดยการกรอง
|
|
ส่วนผสมของเหล็กและผงกำมะถัน |
การกระทำด้วยแม่เหล็กหรือน้ำ ผงเหล็กถูกดึงดูดด้วยแม่เหล็ก แต่ผงกำมะถันไม่ได้ถูกดึงดูด ผงกำมะถันที่ไม่เปียกลอยอยู่บนผิวน้ำ และผงเหล็กหนักที่เปียกได้ตกลงไปที่ด้านล่าง แยกส่วนผสมของกำมะถันและเหล็กโดยใช้แม่เหล็กและน้ำ
|
|
สารละลายเกลือในน้ำเป็นส่วนผสมที่เป็นเนื้อเดียวกัน |
การระเหยหรือการตกผลึก น้ำจะระเหยออกไป เหลือผลึกเกลือไว้ในถ้วยพอร์ซเลน เมื่อน้ำระเหยจากทะเลสาบ Elton และ Baskunchak จะได้เกลือแกง วิธีการแยกนี้ขึ้นอยู่กับความแตกต่างของจุดเดือดของตัวทำละลายและตัวถูกละลาย หากสาร เช่น น้ำตาล สลายตัวเมื่อถูกความร้อน น้ำจะไม่ระเหยไปจนหมด สารละลายจะระเหยออกไป จากนั้นจึงตกตะกอนเป็นผลึกน้ำตาลจาก สารละลายอิ่มตัว บางครั้งจำเป็นต้องขจัดสิ่งเจือปนออกจากตัวทำละลายโดยใช้จุดเดือดที่อุณหภูมิต่ำกว่า เช่น น้ำออกจากเกลือ ในกรณีนี้ ไอระเหยของสารจะต้องถูกรวบรวมและควบแน่นเมื่อเย็นลง วิธีการแยกส่วนผสมที่เป็นเนื้อเดียวกันนี้เรียกว่า การกลั่นหรือการกลั่น- ในอุปกรณ์พิเศษ - เครื่องกลั่นจะได้รับน้ำกลั่นซึ่งใช้สำหรับความต้องการของเภสัชวิทยาห้องปฏิบัติการและระบบทำความเย็นในรถยนต์ ที่บ้านคุณสามารถสร้างเครื่องกลั่นได้: หากคุณแยกส่วนผสมของแอลกอฮอล์กับน้ำ แอลกอฮอล์ที่มีจุดเดือด = 78 °C จะถูกกลั่นออกก่อน (เก็บในหลอดทดลองที่รับ) และน้ำจะยังคงอยู่ในหลอดทดลอง การกลั่นใช้ในการผลิตน้ำมันเบนซิน น้ำมันก๊าด และน้ำมันแก๊สจากน้ำมัน การแยกสารผสมที่เป็นเนื้อเดียวกัน
|
วิธีการพิเศษในการแยกส่วนประกอบโดยพิจารณาจากการดูดซึมที่แตกต่างกันของสารบางชนิดคือ โครมาโตกราฟี.
M.S. Tsvet นักพฤกษศาสตร์ชาวรัสเซียเป็นคนแรกที่แยกคลอโรฟิลล์ออกจากส่วนสีเขียวของพืชโดยใช้โครมาโตกราฟี ในอุตสาหกรรมและห้องปฏิบัติการ แป้ง ถ่านหิน หินปูน และอลูมิเนียมออกไซด์ถูกนำมาใช้แทนกระดาษกรองสำหรับโครมาโตกราฟี จำเป็นต้องใช้สารที่มีระดับการทำให้บริสุทธิ์เท่ากันเสมอหรือไม่
เพื่อวัตถุประสงค์ที่แตกต่างกัน จำเป็นต้องใช้สารที่มีระดับการทำให้บริสุทธิ์ต่างกัน น้ำปรุงอาหารควรปล่อยให้ยืนเพียงพอเพื่อขจัดสิ่งเจือปนและคลอรีนที่ใช้ฆ่าเชื้อ ต้องต้มน้ำสำหรับดื่มก่อน และในห้องปฏิบัติการเคมีเพื่อเตรียมสารละลายและทำการทดลองในทางการแพทย์จำเป็นต้องใช้น้ำกลั่นและทำให้บริสุทธิ์จากสารที่ละลายในนั้นให้มากที่สุด สารบริสุทธิ์โดยเฉพาะซึ่งมีปริมาณสารเจือปนไม่เกินหนึ่งในล้านเปอร์เซ็นต์นั้นถูกใช้ในอุตสาหกรรมอิเล็กทรอนิกส์ เซมิคอนดักเตอร์ เทคโนโลยีนิวเคลียร์ และอุตสาหกรรมที่มีความแม่นยำอื่นๆ
วิธีแสดงองค์ประกอบของสารผสม
เศษส่วนมวลของส่วนประกอบในส่วนผสม- อัตราส่วนของมวลของส่วนประกอบต่อมวลของส่วนผสมทั้งหมด โดยปกติแล้วเศษส่วนมวลจะแสดงเป็น % แต่ก็ไม่จำเป็นเสมอไป
เศษส่วนโมลของส่วนประกอบในส่วนผสม- อัตราส่วนของจำนวนโมล (ปริมาณของสาร) ของส่วนประกอบต่อจำนวนโมลทั้งหมดของสารทั้งหมดในส่วนผสม ตัวอย่างเช่น หากส่วนผสมมีสาร A, B และ C ดังนั้น:
อัตราส่วนฟันกรามของส่วนประกอบบางครั้งปัญหาของส่วนผสมอาจบ่งบอกถึงอัตราส่วนโมลของส่วนประกอบต่างๆ ตัวอย่างเช่น:
ปริมาตรของส่วนประกอบในส่วนผสม (สำหรับก๊าซเท่านั้น)- อัตราส่วนของปริมาตรของสาร A ต่อปริมาตรรวมของส่วนผสมก๊าซทั้งหมด
บล็อกการปฏิบัติ
ลองดูตัวอย่างปัญหาสามประการที่สารผสมของโลหะทำปฏิกิริยากัน เกลือกรด:
ตัวอย่างที่ 1เมื่อส่วนผสมของทองแดงและเหล็กน้ำหนัก 20 กรัมสัมผัสกับกรดไฮโดรคลอริกส่วนเกิน จะปล่อยก๊าซ (หมายเลข) 5.6 ลิตร กำหนดเศษส่วนมวลของโลหะในส่วนผสม
ในตัวอย่างแรก ทองแดงไม่ทำปฏิกิริยากับกรดไฮโดรคลอริก กล่าวคือ ไฮโดรเจนจะถูกปล่อยออกมาเมื่อกรดทำปฏิกิริยากับเหล็ก ดังนั้นเมื่อรู้ปริมาตรของไฮโดรเจน เราก็สามารถหาปริมาณและมวลของเหล็กได้ทันที และตามด้วยเศษส่วนมวลของสารในส่วนผสม
วิธีแก้ตัวอย่างที่ 1
การหาปริมาณไฮโดรเจน:
n = V / V m = 5.6 / 22.4 = 0.25 โมล
ตามสมการปฏิกิริยา:
ปริมาณธาตุเหล็กก็เท่ากับ 0.25 โมล คุณสามารถค้นหามวลของมันได้:
ม. เฟ = 0.25 56 = 14 กรัม
ตอนนี้คุณสามารถคำนวณเศษส่วนมวลของโลหะในส่วนผสมได้แล้ว:
ω Fe = m Fe /m ของส่วนผสมทั้งหมด = 14/20 = 0.7 = 70%
ตัวอย่างที่ 2เมื่อส่วนผสมของอลูมิเนียมและเหล็กน้ำหนัก 11 กรัมสัมผัสกับกรดไฮโดรคลอริกส่วนเกิน จะปล่อยก๊าซ 8.96 ลิตร (n.s.) กำหนดเศษส่วนมวลของโลหะในส่วนผสม
ในตัวอย่างที่สอง ปฏิกิริยาคือ ทั้งคู่โลหะ ในกรณีนี้ ไฮโดรเจนถูกปล่อยออกมาจากกรดแล้วในปฏิกิริยาทั้งสอง ดังนั้นจึงไม่สามารถใช้การคำนวณโดยตรงได้ที่นี่ ในกรณีเช่นนี้ จะสะดวกในการแก้โดยใช้ระบบสมการง่ายๆ โดยให้ x เป็นจำนวนโมลของโลหะชนิดใดชนิดหนึ่ง และ y เป็นปริมาณของสารในวินาที
วิธีแก้ตัวอย่างที่ 2
การหาปริมาณไฮโดรเจน:
n = V / V ม. = 8.96 / 22.4 = 0.4 โมล
ให้ปริมาณอะลูมิเนียมเป็น x โมล และปริมาณเหล็กเป็น x โมล จากนั้นเราสามารถแสดงปริมาณไฮโดรเจนที่ปล่อยออกมาในรูปของ x และ y ได้:
สะดวกกว่ามากในการแก้ระบบดังกล่าวโดยใช้วิธีการลบโดยคูณสมการแรกด้วย 18:
27x + 18y = 7.2
และลบสมการแรกออกจากสมการที่สอง:
(56 − 18)y = 11 − 7.2
y = 3.8 / 38 = 0.1 โมล (เฟ)
x = 0.2 โมล (อัล)
ต่อไปเราจะพบมวลของโลหะและเศษส่วนของมวลในส่วนผสม:
ม. อัล = 0.2 27 = 5.4 ก
ω Fe = m ส่วนผสม Fe / m = 5.6 / 11 = 0.50909 (50.91%)
ตามลำดับ
ω อัล = 100% - 50.91% = 49.09%
คำตอบ: เหล็ก 50.91%, อลูมิเนียม 49.09%
ตัวอย่างที่ 3ส่วนผสมของสังกะสีอลูมิเนียมและทองแดง 16 กรัมได้รับการบำบัดด้วยสารละลายกรดไฮโดรคลอริกส่วนเกิน ในกรณีนี้ มีการปล่อยก๊าซ 5.6 ลิตร (n.s.) และสาร 5 กรัมไม่ละลาย กำหนดเศษส่วนมวลของโลหะในส่วนผสม
ในตัวอย่างที่สาม โลหะสองชนิดทำปฏิกิริยา แต่โลหะตัวที่สาม (ทองแดง) ไม่ทำปฏิกิริยา ดังนั้นส่วนที่เหลือของ 5 กรัมคือมวลของทองแดง ปริมาณของโลหะสองชนิดที่เหลือ ได้แก่ สังกะสีและอะลูมิเนียม (โปรดทราบว่ามวลรวมของโลหะทั้งสองคือ 16 − 5 = 11 กรัม) สามารถพบได้โดยใช้ระบบสมการ ดังตัวอย่างที่ 2
ตอบตัวอย่างที่ 3: สังกะสี 56.25%, อลูมิเนียม 12.5%, ทองแดง 31.25%
ตัวอย่างที่ 4ส่วนผสมของเหล็ก อลูมิเนียม และทองแดงได้รับการบำบัดด้วยกรดซัลฟิวริกเข้มข้นเย็นที่มากเกินไป ในกรณีนี้ ส่วนหนึ่งของส่วนผสมละลาย และปล่อยก๊าซ 5.6 ลิตร (n.s.) ของผสมที่เหลือถูกบำบัดด้วยสารละลายโซเดียมไฮดรอกไซด์ที่มากเกินไป ปล่อยก๊าซออกมา 3.36 ลิตร และยังมีสารตกค้างที่ไม่ละลายน้ำ 3 กรัม กำหนดมวลและองค์ประกอบของส่วนผสมเริ่มต้นของโลหะ
ในตัวอย่างนี้ เราต้องจำไว้ว่า เข้มข้นเย็นกรดซัลฟิวริกไม่ทำปฏิกิริยากับเหล็กและอลูมิเนียม (ทู่) แต่ทำปฏิกิริยากับทองแดง สิ่งนี้จะปล่อยซัลเฟอร์ (IV) ออกไซด์ออกมา
มีฤทธิ์เป็นด่างตอบสนอง อลูมิเนียมเท่านั้น- โลหะแอมโฟเทอริก (นอกเหนือจากอลูมิเนียม สังกะสี และดีบุกยังละลายในอัลคาไล และเบริลเลียมก็สามารถละลายในอัลคาไลเข้มข้นที่ร้อนได้เช่นกัน)
เฉลยตัวอย่างที่ 4
มีเพียงทองแดงเท่านั้นที่ทำปฏิกิริยากับกรดซัลฟิวริกเข้มข้น จำนวนโมลของก๊าซคือ:
SO2 = V / Vm = 5.6 / 22.4 = 0.25 โมล
0,25
0,25
ซียู+
2H 2 SO 4 (เข้มข้น) = CuSO 4 +
SO 2 + 2H 2 O
(อย่าลืมว่าปฏิกิริยาดังกล่าวจะต้องทำให้เท่ากันโดยใช้เครื่องชั่งอิเล็กทรอนิกส์)
เนื่องจากอัตราส่วนโมลาร์ของทองแดงและซัลเฟอร์ไดออกไซด์คือ 1:1 ดังนั้นทองแดงจึงเป็น 0.25 โมลเช่นกัน คุณสามารถค้นหามวลทองแดงได้:
ม. Cu = n M = 0.25 64 = 16 ก.
อลูมิเนียมทำปฏิกิริยากับสารละลายอัลคาไล ส่งผลให้เกิดไฮดรอกโซเชิงซ้อนของอลูมิเนียมและไฮโดรเจน:
2Al + 2NaOH + 6H 2 O = 2Na + 3H 2
อัล 0 − 3e = อัล 3+
2
2H + + 2e = ชม 2
3
จำนวนโมลของไฮโดรเจน:
n H2 = 3.36 / 22.4 = 0.15 โมล
อัตราส่วนโมลของอลูมิเนียมและไฮโดรเจนคือ 2:3 ดังนั้น
n อัล = 0.15 / 1.5 = 0.1 โมล
น้ำหนักอลูมิเนียม:
ม. อัล = n M = 0.1 27 = 2.7 ก
ส่วนที่เหลือเป็นเหล็กหนัก 3 กรัม คุณสามารถหามวลของส่วนผสมได้:
ม. ส่วนผสม = 16 + 2.7 + 3 = 21.7 กรัม
เศษส่วนมวลของโลหะ:
ω อัล = 2.7 / 21.7 = 0.1244 (12.44%)
ω เฟ = 13.83%
คำตอบ: ทองแดง 73.73% อลูมิเนียม 12.44% เหล็ก 13.83%
ตัวอย่างที่ 5ของผสมของสังกะสีและอะลูมิเนียม 21.1 กรัมถูกละลายในสารละลายกรดไนตริก 565 มิลลิลิตรที่มี 20 น้ำหนัก %เอชเอ็นโอ 3 และมีความหนาแน่น 1.115 กรัม/มิลลิลิตร ปริมาตรของก๊าซที่ปล่อยออกมาซึ่งเป็นสารเดี่ยวและเป็นผลิตภัณฑ์เดียวที่ช่วยลดกรดไนตริกได้คือ 2.912 ลิตร (n.s.) กำหนดองค์ประกอบของสารละลายที่ได้เป็นเปอร์เซ็นต์มวล (สธธ.)
ข้อความของปัญหานี้แสดงให้เห็นอย่างชัดเจนถึงผลคูณของการลดไนโตรเจน - "สารธรรมดา" เนื่องจากกรดไนตริกกับโลหะไม่ได้ผลิตไฮโดรเจน จึงเป็นไนโตรเจน โลหะทั้งสองละลายในกรด
ปัญหาไม่ได้ถามถึงองค์ประกอบของส่วนผสมเริ่มต้นของโลหะ แต่เป็นองค์ประกอบของสารละลายที่เกิดขึ้นหลังปฏิกิริยา ทำให้งานยากขึ้น
เฉลยตัวอย่างที่ 5
กำหนดปริมาณของสารก๊าซ:
n N2 = V / Vm = 2.912 / 22.4 = 0.13 โมล
กำหนดมวลของสารละลายกรดไนตริก มวลและปริมาณของ HNO3 ที่ละลาย:
ม. HNO3 = ω ม. สารละลาย = 0.2 630.3 = 126.06 กรัม
n HNO3 = m / M = 126.06 / 63 = 2 โมล
โปรดทราบว่าเนื่องจากโลหะละลายหมดแล้ว จึงหมายความว่า - มีกรดเพียงพอแน่นอน(โลหะเหล่านี้ไม่ทำปฏิกิริยากับน้ำ) ดังนั้นจึงจำเป็นต้องตรวจสอบ มีกรดมากเกินไปหรือไม่?และจะเหลือปริมาณเท่าใดหลังจากปฏิกิริยาในสารละลายที่ได้
เราเขียนสมการปฏิกิริยา ( อย่าลืมเกี่ยวกับเครื่องชั่งอิเล็กทรอนิกส์ของคุณ) และเพื่อความสะดวกในการคำนวณ เราจะเอา 5x เป็นปริมาณสังกะสี และ 10y เป็นปริมาณอะลูมิเนียม จากนั้นตามค่าสัมประสิทธิ์ในสมการ ไนโตรเจนในปฏิกิริยาแรกจะเป็น x โมล และในวินาที - 3y โมล:
|
5x |
x | ||
|
5Zn |
+ 12HNO 3 = 5Zn(หมายเลข 3) 2 + |
ยังไม่มีข้อความ 2 |
+6H2O |
|
สังกะสี 0 − 2e = สังกะสี 2+ |
|
5 |
|
2N +5 + 10e = ยังไม่มีข้อความ 2 |
1 |
|
10ป |
3ปี | ||
|
10อัล |
+ 36HNO 3 = 10อัล(NO 3) 3 + |
3N2 |
+18H2O |
สะดวกในการแก้ระบบนี้โดยการคูณสมการแรกด้วย 90 แล้วลบสมการแรกออกจากสมการที่สอง
x = 0.04 ซึ่งหมายถึง n Zn = 0.04 5 = 0.2 โมล
y = 0.03 ซึ่งหมายถึง n Al = 0.03 10 = 0.3 โมล
ตรวจสอบมวลของส่วนผสม:
0.2 65 + 0.3 27 = 21.1 ก.
ตอนนี้เรามาดูองค์ประกอบของการแก้ปัญหากันดีกว่า จะสะดวกในการเขียนปฏิกิริยาอีกครั้งและเขียนปริมาณของสารที่เกิดปฏิกิริยาและเกิดทั้งหมดเหนือปฏิกิริยา (ยกเว้นน้ำ):
|
0,2 |
0,48 |
0,2 |
0,03 | |
|
5Zn |
+ 12HNO3 = |
5Zn(หมายเลข 3) 2 |
+N2+ |
6H2O |
|
0,3 |
1,08 |
0,3 |
0,09 | |
|
10อัล |
+ 36HNO3 = |
10อัล(หมายเลข 3) 3 |
+3N2+ |
18H2O |
คำถามต่อไปคือ มีกรดไนตริกเหลืออยู่ในสารละลายหรือไม่ และเหลืออยู่เท่าใด
ตามสมการปฏิกิริยา ปริมาณของกรดที่ทำปฏิกิริยา:
n HNO3 = 0.48 + 1.08 = 1.56 โมล
เหล่านั้น. กรดมีมากเกินไป และคุณสามารถคำนวณส่วนที่เหลือในสารละลายได้:
n HNO3 พักผ่อน = 2 − 1.56 = 0.44 โมล
ดังนั้นใน ทางออกสุดท้ายประกอบด้วย:
ม. สังกะสี(NO3)2 = n M = 0.2 189 = 37.8 กรัม
อลูมิเนียมไนเตรตจำนวน 0.3 โมล:
ม. อัล(NO3)3 = n M = 0.3 213 = 63.9 ก
กรดไนตริกส่วนเกินในปริมาณ 0.44 โมล:
ม. HNO3 พักผ่อน = n M = 0.44 63 = 27.72 กรัม
สารละลายสุดท้ายมีมวลเท่าใด
ให้เราจำไว้ว่ามวลของสารละลายสุดท้ายประกอบด้วยส่วนประกอบที่เราผสม (สารละลายและสารต่างๆ) ลบด้วยผลิตภัณฑ์ที่ทำปฏิกิริยาที่ทิ้งสารละลายไว้ (ตะกอนและก๊าซ):
ใหม่ สารละลาย = มวลของสารละลายกรด + มวลของโลหะผสม - มวลของไนโตรเจน
ม. N2 = n M = 28 (0.03 + 0.09) = 3.36 กรัม
ใหม่ สารละลาย = 630.3 + 21.1 − 3.36 = 648.04 กรัม
ตอนนี้คุณสามารถคำนวณเศษส่วนมวลของสารในสารละลายผลลัพธ์ได้:
จากนั้นสำหรับงานของเรา:
ωAl(NO 3) 3 = m ปริมาตร / m สารละลาย = 63.9 / 648.04 = 0.0986
ω HNO3 พักผ่อน = เมตร น้ำ / เมตร สารละลาย = 27.72 / 648.04 = 0.0428
คำตอบ: ซิงค์ไนเตรต 5.83%, อลูมิเนียมไนเตรต 9.86%, กรดไนตริก 4.28%
ตัวอย่างที่ 6เมื่อผสมทองแดง เหล็ก และอลูมิเนียม 17.4 กรัมด้วยกรดไนตริกเข้มข้นมากเกินไป จะปล่อยก๊าซ (n.o.) ออกมา 4.48 ลิตร และเมื่อส่วนผสมนี้สัมผัสกับกรดไฮโดรคลอริกส่วนเกินที่มีมวลเท่ากัน จะได้ 8.96 ลิตรของ ก๊าซ (n.o.) ถูกปล่อยออกมา กำหนดองค์ประกอบของส่วนผสมเริ่มต้น (สธธ.)
เมื่อแก้ไขปัญหานี้ เราต้องจำไว้ว่า ประการแรก กรดไนตริกเข้มข้นกับโลหะที่ไม่ใช้งาน (ทองแดง) จะสร้าง NO 2 และเหล็กและอลูมิเนียมจะไม่ทำปฏิกิริยากับมัน กรดไฮโดรคลอริกไม่ทำปฏิกิริยากับทองแดง
ตอบตัวอย่างที่ 6: ทองแดง 36.8%, เหล็ก 32.2%, อลูมิเนียม 31%
ปัญหาสำหรับการแก้ปัญหาอย่างอิสระ
1. ปัญหาง่ายๆ กับส่วนผสมสองอย่าง
1-1. ส่วนผสมของทองแดงและอลูมิเนียมที่มีน้ำหนัก 20 กรัมได้รับการบำบัดด้วยสารละลายกรดไนตริก 96% และปล่อยก๊าซ (n.o.) จำนวน 8.96 ลิตร หาสัดส่วนมวลของอะลูมิเนียมในส่วนผสม
1-2. ส่วนผสมของทองแดงและสังกะสีที่มีน้ำหนัก 10 กรัมได้รับการบำบัดด้วยสารละลายอัลคาไลเข้มข้น ในกรณีนี้มีการปล่อยก๊าซ 2.24 ลิตร (ny) คำนวณเศษส่วนมวลของสังกะสีในส่วนผสมตั้งต้น.
1-3. ส่วนผสมของแมกนีเซียมและแมกนีเซียมออกไซด์ที่มีน้ำหนัก 6.4 กรัมได้รับการบำบัดด้วยกรดซัลฟิวริกเจือจางในปริมาณที่เพียงพอ ในกรณีนี้มีการปล่อยก๊าซ 2.24 ลิตร (n.s.) หาสัดส่วนมวลของแมกนีเซียมในส่วนผสม.
1-4. ส่วนผสมของสังกะสีและซิงค์ออกไซด์ที่มีน้ำหนัก 3.08 กรัมถูกละลายในกรดซัลฟิวริกเจือจาง เราได้รับซิงค์ซัลเฟตที่มีน้ำหนัก 6.44 กรัม คำนวณเศษส่วนมวลของสังกะสีในส่วนผสมดั้งเดิม
1-5. เมื่อส่วนผสมของเหล็กและผงสังกะสีที่มีน้ำหนัก 9.3 กรัมสัมผัสกับสารละลายคอปเปอร์ (II) คลอไรด์ส่วนเกิน จะเกิดทองแดงขึ้น 9.6 กรัม กำหนดองค์ประกอบของส่วนผสมเริ่มต้น
1-6. ต้องใช้สารละลายกรดไฮโดรคลอริก 20% มวลเท่าใดในการละลายส่วนผสมของสังกะสีและซิงค์ออกไซด์ 20 กรัมอย่างสมบูรณ์หากปล่อยไฮโดรเจนด้วยปริมาตร 4.48 ลิตร (n.s.)
1-7. เมื่อส่วนผสมของเหล็กและทองแดง 3.04 กรัมละลายในกรดไนตริกเจือจาง ไนโตรเจนออกไซด์ (II) จะถูกปล่อยออกมาด้วยปริมาตร 0.896 ลิตร (n.s.) กำหนดองค์ประกอบของส่วนผสมเริ่มต้น
1-8. เมื่อส่วนผสมของตะไบเหล็กและอะลูมิเนียม 1.11 กรัมละลายในสารละลายกรดไฮโดรคลอริก 16% (ρ = 1.09 กรัม/มิลลิลิตร) ไฮโดรเจน 0.672 ลิตร (n.s.) จะถูกปล่อยออกมา ค้นหาเศษส่วนมวลของโลหะในส่วนผสมและหาปริมาตรของกรดไฮโดรคลอริกที่ใช้ไป
2. งานมีความซับซ้อนมากขึ้น
2-1. ส่วนผสมของแคลเซียมและอลูมิเนียมน้ำหนัก 18.8 กรัมถูกเผาโดยไม่มีอากาศและมีผงกราไฟท์มากเกินไป ผลิตภัณฑ์ที่ทำปฏิกิริยาได้รับการบำบัดด้วยกรดไฮโดรคลอริกเจือจาง และก๊าซ 11.2 ลิตร (n.o.) ถูกปล่อยออกมา กำหนดเศษส่วนมวลของโลหะในส่วนผสม
2-2. ในการละลายโลหะผสมแมกนีเซียม-อลูมิเนียม 1.26 กรัม ให้ใช้สารละลายกรดซัลฟิวริก 19.6% 35 มล. (ρ = 1.1 กรัม/มิลลิลิตร) กรดส่วนเกินทำปฏิกิริยากับสารละลายโพแทสเซียมไบคาร์บอเนต 28.6 มิลลิลิตร ที่ความเข้มข้น 1.4 โมล/ลิตร กำหนดเศษส่วนมวลของโลหะในโลหะผสมและปริมาตรของก๊าซ (หมายเลข) ที่ปล่อยออกมาระหว่างการละลายของโลหะผสม
2-3. เมื่อส่วนผสมของเหล็กและเหล็ก (II) ออกไซด์ 27.2 กรัมถูกละลายในกรดซัลฟิวริกและสารละลายระเหยจนแห้ง จะเกิดเหล็กซัลเฟต 111.2 กรัม - เหล็ก (II) ซัลเฟตเฮปตาไฮเดรต - เกิดขึ้น กำหนดองค์ประกอบเชิงปริมาณของส่วนผสมเริ่มต้น
2-4. เมื่อเหล็กที่มีน้ำหนัก 28 กรัมทำปฏิกิริยากับคลอรีน จะเกิดส่วนผสมของเหล็ก (II) และ (III) คลอไรด์ที่มีน้ำหนัก 77.7 กรัม คำนวณมวลของเหล็ก (III) คลอไรด์ในส่วนผสมที่ได้
2-5. เศษส่วนมวลของโพแทสเซียมในการผสมกับลิเธียมคือเท่าใด หากเป็นผลมาจากการบำบัดส่วนผสมนี้ด้วยคลอรีนส่วนเกิน จะเกิดส่วนผสมขึ้นโดยที่เศษส่วนมวลของโพแทสเซียมคลอไรด์คือ 80%
2-6. หลังจากบำบัดส่วนผสมของโพแทสเซียมและแมกนีเซียมด้วยมวลรวม 10.2 กรัมด้วยโบรมีนส่วนเกินมวลของส่วนผสมที่เกิดขึ้นของของแข็งจะเท่ากับ 42.2 กรัมของผสมนี้ได้รับการบำบัดด้วยสารละลายโซเดียมไฮดรอกไซด์ที่มากเกินไปหลังจากนั้น ตะกอนจะถูกแยกออกและเผาให้มีน้ำหนักคงที่ คำนวณมวลของสารตกค้างที่เกิดขึ้น
2-7.
2-8. โลหะผสมอลูมิเนียม-เงินได้รับการบำบัดด้วยสารละลายเข้มข้นของกรดไนตริกที่มากเกินไป และสารตกค้างถูกละลายในกรดอะซิติก ปริมาตรของก๊าซที่ปล่อยออกมาในปฏิกิริยาทั้งสองซึ่งวัดภายใต้สภาวะเดียวกันนั้นมีค่าเท่ากัน คำนวณเศษส่วนมวลของโลหะในโลหะผสม
3. สามโลหะและปัญหาที่ซับซ้อน
3-1. เมื่อผสมทองแดง เหล็ก และอลูมิเนียม 8.2 กรัมด้วยกรดไนตริกเข้มข้นมากเกินไป จะปล่อยก๊าซ 2.24 ลิตร ก๊าซที่มีปริมาตรเท่ากันจะถูกปล่อยออกมาเมื่อส่วนผสมเดียวกันที่มีมวลเท่ากันได้รับการบำบัดด้วยกรดซัลฟิวริกเจือจาง (DS) ที่มากเกินไป กำหนดองค์ประกอบของส่วนผสมเริ่มต้นเป็นเปอร์เซ็นต์มวล
3-2. ส่วนผสมของเหล็ก ทองแดง และอลูมิเนียม 14.7 กรัม ทำปฏิกิริยากับกรดซัลฟิวริกเจือจางที่มากเกินไป จะปล่อยไฮโดรเจน 5.6 ลิตร (n.s.) กำหนดองค์ประกอบของส่วนผสมเป็นเปอร์เซ็นต์มวล หากคลอรีนของตัวอย่างเดียวกันของส่วนผสมต้องใช้คลอรีน 8.96 ลิตร (n.s.)
3-3. ตะไบเหล็ก สังกะสี และอลูมิเนียมผสมกันในอัตราส่วนโมล 2:4:3 (ตามลำดับที่แสดง) ของผสมนี้ 4.53 กรัมบำบัดด้วยคลอรีนส่วนเกิน ส่วนผสมที่เป็นผลลัพธ์ของคลอไรด์ถูกละลายในน้ำ 200 มิลลิลิตร กำหนดความเข้มข้นของสารในสารละลายที่ได้
3-4. โลหะผสมของทองแดง เหล็ก และสังกะสีที่มีน้ำหนัก 6 กรัม (มวลของส่วนประกอบทั้งหมดเท่ากัน) วางอยู่ในสารละลายกรดไฮโดรคลอริก 18.25% ที่มีน้ำหนัก 160 กรัม คำนวณเศษส่วนมวลของสารในสารละลายที่ได้
3-5. ส่วนผสม 13.8 กรัมซึ่งประกอบด้วยซิลิคอน อลูมิเนียม และเหล็กได้รับการบำบัดด้วยโซเดียมไฮดรอกไซด์ส่วนเกินเมื่อถูกความร้อน และปล่อยก๊าซ 11.2 ลิตร (n.s.) เมื่อมวลของส่วนผสมสัมผัสกับกรดไฮโดรคลอริกส่วนเกิน จะปล่อยก๊าซ 8.96 ลิตร (n.s.) กำหนดมวลของสารในส่วนผสมดั้งเดิม
3-6. เมื่อผสมสังกะสี ทองแดง และเหล็กด้วยสารละลายอัลคาไลเข้มข้นมากเกินไป ก๊าซจะถูกปล่อยออกมาและมวลของสารตกค้างที่ไม่ละลายน้ำจะน้อยกว่ามวลของส่วนผสมดั้งเดิมถึง 2 เท่า สารตกค้างนี้ได้รับการบำบัดด้วยกรดไฮโดรคลอริกส่วนเกิน ปริมาตรของก๊าซที่ปล่อยออกมาจะเท่ากับปริมาตรของก๊าซที่ปล่อยออกมาในกรณีแรก (ปริมาตรถูกวัดภายใต้เงื่อนไขเดียวกัน) คำนวณเศษส่วนมวลของโลหะในส่วนผสมเริ่มต้น
3-7. มีส่วนผสมของแคลเซียม แคลเซียมออกไซด์ และแคลเซียมคาร์ไบด์ โดยมีอัตราส่วนโมลาร์ของส่วนประกอบ 3:2:5 (ตามลำดับที่ระบุไว้) ปริมาตรน้ำขั้นต่ำที่สามารถเกิดปฏิกิริยาเคมีกับส่วนผสมดังกล่าวที่มีน้ำหนัก 55.2 กรัมคือเท่าใด
3-8. ส่วนผสมของโครเมียม สังกะสี และเงินที่มีมวลรวม 7.1 กรัมได้รับการบำบัดด้วยกรดไฮโดรคลอริกเจือจาง มวลของสารตกค้างที่ไม่ละลายกลายเป็น 3.2 กรัม หลังจากแยกตะกอนแล้วสารละลายจะได้รับการบำบัดด้วยโบรมีนในตัวกลางที่เป็นด่าง และเมื่อสิ้นสุดปฏิกิริยาจะได้รับการบำบัดด้วยแบเรียมไนเตรตส่วนเกิน มวลของตะกอนที่เกิดขึ้นจะเท่ากับ 12.65 กรัม คำนวณเศษส่วนมวลของโลหะในส่วนผสมเริ่มต้น
คำตอบและความคิดเห็นต่อปัญหาเพื่อการแก้ปัญหาอย่างอิสระ
1-1. 36% (อลูมิเนียมไม่ทำปฏิกิริยากับกรดไนตริกเข้มข้น);
1-2. 65% (เฉพาะโลหะแอมโฟเทอริก - สังกะสี - ละลายในอัลคาไล);
1-5. 30.1% Fe (เหล็ก, แทนที่ทองแดง, เข้าสู่สถานะออกซิเดชัน +2);
1-7. 36.84% Fe (ธาตุเหล็กในกรดไนตริกไปที่ +3);
1-8. 75.68% Fe (เหล็กทำปฏิกิริยากับกรดไฮโดรคลอริกถึง +2) สารละลาย HCl 12.56 มล.
2-1. 42.55% Ca (แคลเซียมและอลูมิเนียมที่มีกราไฟท์ (คาร์บอน) ก่อตัวเป็นคาร์ไบด์ CaC 2 และ Al 4 C 3 เมื่อไฮโดรไลซ์ด้วยน้ำหรือ HCl อะเซทิลีน C 2 H 2 และมีเทน CH 4 จะถูกปล่อยออกมาตามลำดับ)
2-3. 61.76% Fe (เฟอรัสซัลเฟตเฮปตาไฮเดรต - FeSO 4 · 7H 2 O);
2-7. 5.9% Li 2 SO 4, 22.9% Na 2 SO 4, 5.47% H 2 O 2 (เมื่อลิเธียมถูกออกซิไดซ์กับออกซิเจนจะเกิดออกไซด์ของมันและเมื่อโซเดียมถูกออกซิไดซ์จะเกิด Na 2 O 2 เปอร์ออกไซด์ซึ่งไฮโดรไลซ์ใน น้ำเป็นไฮโดรเจนเปอร์ออกไซด์และด่าง)
3-1. 39% ลูกบาศก์เมตร, 3.4% อัล;
3-2. 38.1% เฟ, 43.5% ลูกบาศ์ก;
3-3. 1.53% FeCl 3, 2.56% ZnCl 2, 1.88% AlCl 3 (เหล็กทำปฏิกิริยากับคลอรีนถึงสถานะออกซิเดชัน +3);
3-4. 2.77% FeCl 2, 2.565% ZnCl 2, 14.86% HCl (อย่าลืมว่าทองแดงไม่ทำปฏิกิริยากับกรดไฮโดรคลอริกดังนั้นมวลจึงไม่รวมอยู่ในมวลของสารละลายใหม่)
3-5. 2.8 g Si, 5.4 g Al, 5.6 g Fe (ซิลิคอนเป็นอโลหะทำปฏิกิริยากับสารละลายอัลคาไลทำให้เกิดโซเดียมซิลิเกตและไฮโดรเจนมันไม่ทำปฏิกิริยากับกรดไฮโดรคลอริก)
3-6. 6.9% Cu, 43.1% Fe, 50% สังกะสี;
3-8. 45.1% Ag, 36.6% Cr, 18.3% Zn (โครเมียม เมื่อละลายในกรดไฮโดรคลอริก จะเปลี่ยนเป็นโครเมียม (II) คลอไรด์ ซึ่งเมื่อสัมผัสกับโบรมีนในตัวกลางที่เป็นด่าง จะเปลี่ยนเป็นโครเมต เมื่อเติมเกลือแบเรียม จะไม่ละลาย โครเมตเกิดเป็นแบเรียม)
บล็อกทดสอบ
ส่วน ก
1. ทรายและเกลือหมายถึง:
ก. สารธรรมดา
ข. สารประกอบทางเคมี
ค. ระบบที่เป็นเนื้อเดียวกัน
ง. ระบบที่ต่างกัน
2. หมอกหมายถึง:
ก. ละอองลอย
บีอิมัลชัน
ค. สารละลาย
ง. การระงับ
3. เพื่อให้ได้น้ำมันเบนซินจากน้ำมันธรรมชาติให้ใช้วิธีดังต่อไปนี้:
ก. การสังเคราะห์
บีระเหิด
ค. การกรอง
ง. การกลั่น
4. ระบุวิธีการที่เหมาะสมที่สุดในการแยกส่วนผสมของน้ำมันเบนซินและน้ำ:
ก. การกรอง
ข. การกลั่น
ค. การระเหิด
ง. การปักหลัก
5. การแยกส่วนผสมของน้ำมันและน้ำขึ้นอยู่กับ:
ก. ความแตกต่างของความหนาแน่นของของเหลวทั้งสองชนิด
ข. ความสามารถในการละลายของของเหลวชนิดหนึ่งในของเหลวอีกชนิดหนึ่ง
ค. ความแตกต่างของสี
ง. สถานะการรวมตัวของของเหลวคล้ายกัน
6. สามารถแยกส่วนผสมของตะไบทองแดงและเหล็กได้:
ก. การกรอง
ข. โดยการกระทำของแม่เหล็ก
ค. โครมาโตกราฟี
ง. การกลั่น (การกลั่น)
7. สารบริสุทธิ์ซึ่งตรงข้ามกับสารผสมคืออะไร:
และเหล็กหล่อ
ในส่วนผสมอาหาร
จากทางอากาศ
ง. น้ำทะเล
8.สิ่งที่ใช้กับสารผสมต่างกัน:
มีส่วนผสมของออกซิเจนและไนโตรเจน
ในน้ำในแม่น้ำที่เป็นโคลน
ด้วยเปลือกหิมะ
9.ส่วนผสมที่เป็นของแข็งคืออะไร:
สารละลายกลูโคส
ด้วยสารละลายแอลกอฮอล์
D สารละลายโพแทสเซียมซัลเฟต
10.วิธีการทำให้สารผสมต่างกันบริสุทธิ์มีชื่อว่าอะไร:
และการกลั่น
ในการกรอง
ด้วยการระเหย
เครื่องทำความร้อนเจลลี่
ส่วนบี
1. สร้างลำดับที่ถูกต้องสำหรับการแยกส่วนผสมของเกลือแกงและทรายแม่น้ำ:
ก) ตัวกรอง
B) ประกอบอุปกรณ์กรอง
B) ละลายในน้ำ
D) ระเหยสารละลาย
D) ประกอบอุปกรณ์ระเหย
2. เลือกจำนวนคู่สารที่ต้องการแยก
1) การระเหย
2) การกรอง
ก) ทรายและน้ำในแม่น้ำ
B) น้ำตาลและน้ำ
B) เหล็กและกำมะถัน
D) น้ำและแอลกอฮอล์
3. เชื่อมโยงตัวอย่างที่เสนอของสารผสมกับกลุ่มใดกลุ่มหนึ่ง (หมอก, ควัน, เครื่องดื่มเป็นฟอง, ตะกอนแม่น้ำและทะเล, ครก, ครีม, มาสคาร่า, ลิปสติก, โลหะผสม, แร่ธาตุ) โดยกรอกตาราง:
|
สถานะรวมของสาร |
ตัวอย่างของสารผสม |
|
ยากยาก | |
|
ของแข็งของเหลว | |
|
ของแข็งก๊าซ | |
|
ของเหลวของเหลว | |
|
ของเหลวแข็ง | |
|
ก๊าซเหลว | |
|
ก๊าซก๊าซ | |
|
ก๊าซของเหลว | |
|
ก๊าซของแข็ง |
บล็อกงานทดสอบ
|
1. ภารกิจที่ 1. กรอกตาราง |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
คำตอบ: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
2. แก้ปริศนาอักษรไขว้ คำตอบในคอลัมน์แนวตั้ง - วิธีแยกส่วนผสมที่ระบุ
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
คำตอบ: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
3. แนะนำหลายวิธีในการทำให้น้ำธรรมชาติบริสุทธิ์ในสภาพแคมป์ปิ้ง |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
คำตอบ: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
4. แอนนาแกรมจัดเรียงตัวอักษรในคำใหม่เพื่อสร้างคำศัพท์หลักของบทเรียนนี้ เขียนคำศัพท์เหล่านี้ลงในคำตอบของคุณ มีสเซ่, กงรีปา, ซูเพนซิยาส, ทาโซชิ, ริโฟลิฟานเต
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
คำตอบ: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
5. แบ่งแนวคิดที่เสนอออกเป็น 2 กลุ่ม อากาศ น้ำทะเล แอลกอฮอล์ ออกซิเจน เหล็ก เหล็ก ป้อนคำตอบของคุณในตาราง ตั้งชื่อให้กับคอลัมน์
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
คำตอบ: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
6. เคมีเยี่ยม ในเทพนิยายที่มีชื่อเสียง แม่เลี้ยงหรือวิญญาณชั่วร้ายอื่น ๆ บังคับให้นางเอกแยกส่วนผสมบางอย่างออกเป็นส่วนประกอบแยกกัน คุณจำได้ไหมว่าส่วนผสมเหล่านี้คืออะไรและแยกจากกันด้วยวิธีใด จำนิทาน 2-3 เรื่องก็เพียงพอแล้ว |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
คำตอบ: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
7. ตอบคำถามสั้นๆ 1. เมื่อแร่ถูกบดที่โรงงานเหมืองแร่และแปรรูป ชิ้นส่วนของเครื่องมือเหล็กจะตกลงไป พวกมันสามารถสกัดได้จากแร่ได้อย่างไร? 2. เครื่องดูดฝุ่นดูดอากาศที่มีฝุ่นและปล่อยอากาศที่สะอาดออกมา ทำไม 3. น้ำหลังล้างรถในโรงรถขนาดใหญ่มีน้ำมันเครื่องปนเปื้อน ก่อนระบายลงท่อระบายน้ำควรทำอย่างไร? 4. ร่อนแป้งออกจากรำข้าว ทำไมพวกเขาถึงทำเช่นนี้? |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
คำตอบ: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
หากอนุภาคที่กระจัดกระจายถูกปล่อยออกมาอย่างช้าๆ จากตัวกลางหรือจำเป็นต้องทำให้ระบบที่ต่างกันชัดเจนล่วงหน้า วิธีการต่างๆ เช่น การตกตะกอน การลอยอยู่ในน้ำ การจำแนกประเภท การแข็งตัว ฯลฯ จะถูกนำมาใช้
การแข็งตัวเป็นกระบวนการของการยึดเกาะของอนุภาคในระบบคอลลอยด์ (อิมัลชันหรือสารแขวนลอย) ด้วยการก่อตัวของมวลรวม การยึดเกาะเกิดขึ้นเนื่องจากการชนกันของอนุภาคระหว่างการเคลื่อนที่แบบบราวเนียน การแข็งตัวหมายถึงกระบวนการที่เกิดขึ้นเองซึ่งมีแนวโน้มที่จะเข้าสู่สภาวะที่มีพลังงานอิสระต่ำกว่า เกณฑ์การแข็งตัวคือความเข้มข้นขั้นต่ำของสารที่ให้ซึ่งทำให้เกิดการแข็งตัว โดยธรรมชาติแล้ว การแข็งตัวของเลือดสามารถเร่งได้โดยการเพิ่มสารพิเศษ - ตัวจับตัวเป็นก้อน - ในระบบคอลลอยด์ เช่นเดียวกับการใช้สนามไฟฟ้ากับระบบ (การแข็งตัวของเลือดด้วยไฟฟ้า) การกระทำทางกล (การสั่นสะเทือน การกวน) เป็นต้น
ในระหว่างการแข็งตัวมักจะเติมสารเคมีตกตะกอนลงในส่วนผสมที่ต่างกันซึ่งแยกจากกันซึ่งจะทำลายเปลือกโซลเวตในขณะที่ลดส่วนการแพร่กระจายของชั้นไฟฟ้าสองชั้นซึ่งอยู่ที่พื้นผิวของอนุภาค สิ่งนี้อำนวยความสะดวกในการรวมตัวกันของอนุภาคและการก่อตัวของมวลรวม ดังนั้น เนื่องจากการก่อตัวของเศษส่วนที่มากขึ้นของเฟสที่กระจัดกระจาย การสะสมของอนุภาคจึงถูกเร่ง เกลือของเหล็ก อลูมิเนียม หรือเกลือของโลหะโพลีวาเลนต์อื่นๆ ถูกใช้เป็นตัวตกตะกอน
การเปปไทเซชันเป็นกระบวนการย้อนกลับของการแข็งตัว ซึ่งเป็นการสลายตัวของมวลรวมให้เป็นอนุภาคปฐมภูมิ การทำให้เป็นเปปไทด์ทำได้โดยการเติมสารที่ทำให้เป็นเปปไทซิ่งลงในตัวกลางการกระจายตัว กระบวนการนี้ส่งเสริมการแยกตัวของสารออกเป็นอนุภาคปฐมภูมิ สารเปปไทซิ่งสามารถเป็นสารลดแรงตึงผิวหรืออิเล็กโทรไลต์ เช่น กรดฮิวมิกหรือเฟอร์ริกคลอไรด์ กระบวนการทำให้เป็นเพปไทเซชันใช้เพื่อให้ได้ระบบที่กระจายของเหลวจากเพสต์หรือผง
ในทางกลับกันการตกตะกอนคือการแข็งตัวชนิดหนึ่ง ในกระบวนการนี้ อนุภาคขนาดเล็กที่ถูกแขวนลอยในตัวกลางก๊าซหรือของเหลวจะก่อตัวเป็นก้อนรวมตัวตกตะกอนที่เรียกว่าฟล็อค โพลีเมอร์ที่ละลายน้ำได้ เช่น โพลีอิเล็กโตรไลต์ ถูกใช้เป็นสารตกตะกอน สารที่ก่อตัวเป็นก้อนในระหว่างการจับตัวเป็นก้อนสามารถกำจัดออกได้อย่างง่ายดายโดยการกรองหรือตกตะกอน การตกตะกอนใช้ในการบำบัดน้ำและการแยกสารที่มีคุณค่าออกจากน้ำเสีย ตลอดจนเพื่อเพิ่มคุณค่าของแร่ธาตุ ในกรณีของการบำบัดน้ำ จะใช้สารตกตะกอนในปริมาณความเข้มข้นต่ำ (ตั้งแต่ 0.1 ถึง 5 มก./ลิตร)
เพื่อทำลายมวลรวมในระบบของเหลว มีการใช้สารเติมแต่งเพื่อกระตุ้นประจุบนอนุภาคที่ป้องกันไม่ให้เข้าใกล้กัน ผลกระทบนี้สามารถทำได้โดยการเปลี่ยนค่า pH ของสิ่งแวดล้อม วิธีนี้เรียกว่าการไล่ตะกอน
การลอยอยู่ในน้ำเป็นกระบวนการแยกอนุภาคที่ไม่ชอบน้ำที่เป็นของแข็งออกจากเฟสต่อเนื่องของของเหลวโดยการเลือกตรึงไว้ที่ส่วนต่อประสานระหว่างเฟสของเหลวและก๊าซ (พื้นผิวสัมผัสของของเหลวและก๊าซหรือพื้นผิวของฟองในเฟสของเหลว) อนุภาคของแข็งและการรวมก๊าซจะถูกลบออกจากพื้นผิวของเฟสของเหลว กระบวนการนี้ใช้ไม่เพียงแต่เพื่อกำจัดอนุภาคที่อยู่ในเฟสที่กระจัดกระจายเท่านั้น แต่ยังใช้เพื่อแยกอนุภาคต่างๆ เนื่องจากความสามารถในการเปียกน้ำที่แตกต่างกัน ในกระบวนการนี้ อนุภาคที่ไม่ชอบน้ำจะถูกจับจ้องอยู่ที่ส่วนต่อประสานและแยกออกจากอนุภาคที่ชอบน้ำซึ่งตกลงไปที่ด้านล่าง ผลลัพธ์การลอยอยู่ในน้ำที่ดีที่สุดเกิดขึ้นเมื่อขนาดอนุภาคอยู่ระหว่าง 0.1 ถึง 0.04 มม.
การลอยอยู่ในน้ำมีหลายประเภท: โฟม น้ำมัน ฟิล์ม ฯลฯ ที่พบบ่อยที่สุดคือการลอยฟอง กระบวนการนี้ช่วยให้อนุภาคที่บำบัดด้วยรีเอเจนต์สามารถถูกพาขึ้นสู่ผิวน้ำโดยใช้ฟองอากาศ สิ่งนี้ทำให้เกิดชั้นโฟมซึ่งควบคุมความเสถียรโดยใช้โฟมเข้มข้น
การจำแนกประเภทใช้ในอุปกรณ์ที่มีหน้าตัดแบบแปรผัน ด้วยความช่วยเหลือทำให้สามารถแยกอนุภาคขนาดเล็กจำนวนหนึ่งออกจากผลิตภัณฑ์หลักซึ่งประกอบด้วยอนุภาคขนาดใหญ่ได้ การจำแนกประเภทดำเนินการโดยใช้เครื่องหมุนเหวี่ยงและไฮโดรไซโคลนเนื่องจากผลของแรงเหวี่ยง
การแยกสารแขวนลอยโดยใช้การบำบัดด้วยแม่เหล็กของระบบเป็นวิธีการที่มีแนวโน้มดีมาก น้ำที่ได้รับการบำบัดในสนามแม่เหล็กจะคงคุณสมบัติที่เปลี่ยนแปลงไว้เป็นเวลานาน เช่น ความสามารถในการทำให้เปียกลดลง กระบวนการนี้ทำให้สามารถแยกสารแขวนลอยให้เข้มข้นขึ้นได้
ต่างกัน (ต่างกัน) |
เป็นเนื้อเดียวกัน (เป็นเนื้อเดียวกัน) |
|
สารผสมที่ต่างกันคือสารที่สามารถระบุส่วนต่อประสานระหว่างส่วนประกอบดั้งเดิมได้ด้วยตาเปล่าหรือใต้แว่นขยายหรือกล้องจุลทรรศน์: |
สารในสารผสมดังกล่าวผสมกันมากที่สุดเท่าที่จะเป็นไปได้ในระดับโมเลกุล ในสารผสมดังกล่าว เป็นไปไม่ได้ที่จะตรวจจับส่วนต่อประสานระหว่างส่วนประกอบดั้งเดิมแม้จะใช้กล้องจุลทรรศน์: |
| ตัวอย่าง | |
|
ระบบกันสะเทือน (ของแข็ง + ของเหลว) อิมัลชัน (ของเหลว + ของเหลว) ควัน (ของแข็ง + แก๊ส) ส่วนผสมผงแข็ง (ของแข็ง+ของแข็ง) |
สารละลายที่แท้จริง (เช่น สารละลายเกลือแกงในน้ำ สารละลายแอลกอฮอล์ในน้ำ) สารละลายที่เป็นของแข็ง (โลหะผสม เกลือที่เป็นผลึกไฮเดรต) สารละลายแก๊ส (ส่วนผสมของก๊าซที่ไม่ทำปฏิกิริยากัน) |
วิธีการแยกสารผสม
ส่วนผสมที่ต่างกันของประเภทก๊าซ-ของเหลว, ของเหลว-ของแข็ง, ของแข็งก๊าซ-ของแข็ง จะไม่เสถียรในเวลาภายใต้อิทธิพลของแรงโน้มถ่วง ในสารผสมดังกล่าว ส่วนประกอบที่มีความหนาแน่นต่ำกว่าจะค่อยๆ เพิ่มขึ้น (ลอย) และเมื่อมีความหนาแน่นมากขึ้น ส่วนประกอบก็จะจมลง (ตกตะกอน) กระบวนการแยกสารผสมที่เกิดขึ้นเองตามเวลานี้เรียกว่า ปกป้อง- ตัวอย่างเช่น ส่วนผสมของทรายละเอียดและน้ำค่อนข้างเร็วจะแบ่งออกเป็นสองส่วนโดยธรรมชาติ:
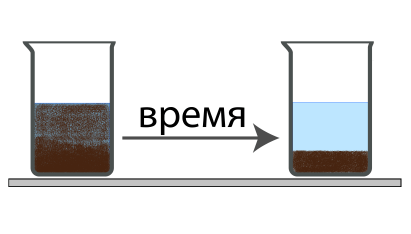
เพื่อเร่งกระบวนการสะสมของสารที่มีความหนาแน่นสูงกว่าจากของเหลวในสภาพห้องปฏิบัติการ พวกเขามักจะใช้วิธีการตกตะกอนในเวอร์ชันขั้นสูงกว่า - การหมุนเหวี่ยง- บทบาทของแรงโน้มถ่วงในเครื่องหมุนเหวี่ยงนั้นเล่นโดยแรงเหวี่ยงซึ่งมักเกิดขึ้นระหว่างการหมุน เนื่องจากแรงเหวี่ยงหนีศูนย์กลางขึ้นอยู่กับความเร็วของการหมุนโดยตรง จึงสามารถสร้างแรงได้มากกว่าแรงโน้มถ่วงหลายเท่าเพียงแค่เพิ่มจำนวนรอบการหมุนเหวี่ยงต่อหนึ่งหน่วยเวลา ด้วยเหตุนี้จึงสามารถแยกส่วนผสมได้เร็วกว่ามากเมื่อเทียบกับการตกตะกอน
หลังจากการตกตะกอนหรือการหมุนเหวี่ยง สามารถแยกส่วนลอยเหนือตะกอนออกจากตะกอนได้โดยใช้วิธีนี้ การแยกน้ำ— โดยค่อยๆ ระบายของเหลวออกจากตะกอนอย่างระมัดระวัง
คุณสามารถแยกส่วนผสมของของเหลวสองชนิดที่ไม่ละลายซึ่งกันและกัน (หลังจากตกตะกอน) โดยใช้กรวยแยก ซึ่งมีหลักการทำงานที่ชัดเจนจากภาพประกอบต่อไปนี้:
เพื่อแยกสารผสมที่มีสถานะการรวมกลุ่มต่างกัน นอกเหนือจากการตกตะกอนและการหมุนเหวี่ยงแล้ว การกรองยังถูกนำมาใช้อย่างกว้างขวางอีกด้วย วิธีการนี้ประกอบด้วยข้อเท็จจริงที่ว่าตัวกรองมีปริมาณงานที่แตกต่างกันโดยสัมพันธ์กับส่วนประกอบของส่วนผสม ส่วนใหญ่มักเกิดจากขนาดอนุภาคที่แตกต่างกัน แต่ก็อาจเป็นเพราะว่าส่วนประกอบแต่ละส่วนของส่วนผสมมีปฏิกิริยารุนแรงกับพื้นผิวตัวกรองมากขึ้น ( ถูกดูดซับพวกเขา).
ตัวอย่างเช่น สามารถแยกสารแขวนลอยของผงที่ไม่ละลายน้ำที่เป็นของแข็งกับน้ำได้โดยใช้ตัวกรองกระดาษที่มีรูพรุน ของแข็งยังคงอยู่บนตัวกรอง และน้ำไหลผ่านและรวบรวมไว้ในภาชนะที่อยู่ใต้ตัวกรอง:
ในบางกรณี ส่วนผสมที่ต่างกันสามารถแยกออกได้เนื่องจากคุณสมบัติทางแม่เหล็กที่แตกต่างกันของส่วนประกอบ ตัวอย่างเช่น ส่วนผสมของผงกำมะถันและผงเหล็กโลหะสามารถแยกออกได้โดยใช้แม่เหล็ก อนุภาคเหล็กต่างจากอนุภาคซัลเฟอร์ที่ถูกดึงดูดและยึดไว้ด้วยแม่เหล็ก:

การแยกส่วนประกอบของส่วนผสมโดยใช้สนามแม่เหล็กเรียกว่า การแยกแม่เหล็ก.
ถ้าส่วนผสมเป็นสารละลายของของแข็งทนไฟในของเหลว สารนี้สามารถแยกออกจากของเหลวได้โดยการระเหยสารละลาย:
หากต้องการแยกของผสมที่เป็นเนื้อเดียวกันของของเหลวออก วิธีการที่เรียกว่า การกลั่นหรือ การกลั่น- วิธีนี้มีหลักการทำงานคล้ายกับการระเหย แต่ช่วยให้คุณแยกไม่เพียงแต่ส่วนประกอบที่ระเหยออกจากส่วนประกอบที่ไม่ระเหยเท่านั้น แต่ยังรวมถึงสารที่มีจุดเดือดค่อนข้างใกล้ด้วย หนึ่งในตัวเลือกที่ง่ายที่สุดสำหรับอุปกรณ์การกลั่นแสดงในรูปด้านล่าง:
ความหมายของกระบวนการกลั่นก็คือ เมื่อส่วนผสมของของเหลวเดือด ไอระเหยของส่วนประกอบที่มีจุดเดือดน้อยกว่าจะระเหยไปก่อน ไอของสารนี้หลังจากผ่านตู้เย็นจะควบแน่นและไหลเข้าสู่ตัวรับ วิธีการกลั่นมีการใช้กันอย่างแพร่หลายในอุตสาหกรรมน้ำมันในระหว่างการกลั่นน้ำมันเบื้องต้นเพื่อแยกน้ำมันออกเป็นเศษส่วน (น้ำมันเบนซิน น้ำมันก๊าด ดีเซล ฯลฯ)
วิธีการกลั่นยังทำให้น้ำบริสุทธิ์จากสิ่งเจือปน (โดยหลักคือเกลือ) น้ำที่ผ่านการทำให้บริสุทธิ์โดยการกลั่นเรียกว่า น้ำกลั่น.






 หมู่บ้านร้างในภูมิภาคมอสโก
หมู่บ้านร้างในภูมิภาคมอสโก เรียงความเกี่ยวกับผลงานของ S
เรียงความเกี่ยวกับผลงานของ S เรื่องราวของชีวิต - กุหลาบสีทอง
เรื่องราวของชีวิต - กุหลาบสีทอง