กลุ่มของสารที่กรดอะมิโนสามารถทำปฏิกิริยาได้ คุณสมบัติทางเคมีของกรดอะมิโน
กรดอะมิโน โปรตีน และเปปไทด์เป็นตัวอย่างของสารประกอบที่อธิบายไว้ด้านล่าง โมเลกุลที่มีฤทธิ์ทางชีวภาพจำนวนมากประกอบด้วยกลุ่มฟังก์ชันที่แตกต่างกันทางเคมีหลายกลุ่ม ซึ่งสามารถโต้ตอบระหว่างกันและกับกลุ่มฟังก์ชันของกันและกันได้
กรดอะมิโน
กรดอะมิโน- สารประกอบอินทรีย์สองฟังก์ชันซึ่งรวมถึงหมู่คาร์บอกซิล - สหประชาชาติและกลุ่มอะมิโนก็คือ เอ็น.เอช. 2 .
แยก α และ β - กรดอะมิโน:
ส่วนใหญ่พบในธรรมชาติ α -กรด โปรตีนประกอบด้วยกรดอะมิโน 19 ตัวและกรดอิมิโน 1 ตัว ( ค 5 ชม. 9เลขที่ 2 ):


ที่ง่ายที่สุด กรดอะมิโน- ไกลซีน กรดอะมิโนที่เหลือสามารถแบ่งออกเป็นกลุ่มหลักได้ดังต่อไปนี้:
1) ความคล้ายคลึงกันของไกลซีน - อะลานีน, วาลีน, ลิวซีน, ไอโซลิวซีน
การได้รับกรดอะมิโน
คุณสมบัติทางเคมีของกรดอะมิโน
กรดอะมิโน- พวกนี้เป็นสารประกอบแอมโฟเทริกเพราะว่า มีหมู่ฟังก์ชันตรงข้ามกัน 2 หมู่ คือ หมู่อะมิโน และหมู่ไฮดรอกซิล ดังนั้นพวกมันจึงทำปฏิกิริยากับทั้งกรดและด่าง:
การเปลี่ยนแปลงของกรด-เบสสามารถแสดงได้ดังนี้:
คุณสมบัติของกรดอะมิโนสามารถแบ่งออกเป็นสองกลุ่ม: เคมีและกายภาพ
คุณสมบัติทางเคมีของกรดอะมิโน
กรดอะมิโนสามารถแสดงคุณสมบัติที่แตกต่างกันได้ขึ้นอยู่กับสารประกอบ
ปฏิกิริยาระหว่างกรดอะมิโน:
กรดอะมิโนเป็นสารประกอบแอมโฟเทอริก ก่อตัวเป็นเกลือที่มีทั้งกรดและด่าง
เนื่องจากกรดคาร์บอกซิลิก กรดอะมิโนจึงก่อให้เกิดอนุพันธ์เชิงฟังก์ชัน ได้แก่ เกลือ เอสเทอร์ เอไมด์
ปฏิกิริยาและคุณสมบัติของกรดอะมิโนด้วย เหตุผล:
เกลือจะเกิดขึ้น:
NH 2 -CH 2 -COOH + NaOH NH 2 -CH 2 -COONa + H2O
เกลือโซเดียม + กรด 2-อะมิโนอะซิติก เกลือโซเดียมของกรดอะมิโนอะซิติก (ไกลซีน) + น้ำ
การมีปฏิสัมพันธ์กับ แอลกอฮอล์:
กรดอะมิโนสามารถทำปฏิกิริยากับแอลกอฮอล์เมื่อมีก๊าซไฮโดรเจนคลอไรด์เปลี่ยนเป็น เอสเทอร์- กรดอะมิโนเอสเทอร์ไม่มีโครงสร้างไบโพลาร์และเป็นสารประกอบระเหยได้
NH 2 -CH 2 -COOH + CH 3 OH NH 2 -CH 2 -COOCH 3 + H 2 O.
เมทิลเอสเทอร์ / กรด 2-อะมิโนอะซิติก /
การมีปฏิสัมพันธ์กับ แอมโมเนีย:
เอไมด์จะเกิดขึ้น:
NH 2 -CH(R)-COOH + H-NH 2 = NH 2 -CH(R)-CONH 2 + H 2 O
ปฏิกิริยาระหว่างกรดอะมิโนกับ กรดแก่:
เราได้รับเกลือ:
HOOC-CH 2 -NH 2 + HCl → Cl (หรือ HOOC-CH 2 -NH 2 *HCl)
นี่เป็นคุณสมบัติทางเคมีพื้นฐานของกรดอะมิโน
คุณสมบัติทางกายภาพของกรดอะมิโน
ให้เราแสดงคุณสมบัติทางกายภาพของกรดอะมิโน:
- ไม่มีสี
- มีรูปแบบเป็นผลึก
- กรดอะมิโนส่วนใหญ่มีรสหวาน แต่ขึ้นอยู่กับอนุมูล (R) อาจมีรสขมหรือรสจืด
- ละลายได้ง่ายในน้ำ แต่ละลายได้ไม่ดีในตัวทำละลายอินทรีย์หลายชนิด
- กรดอะมิโนมีคุณสมบัติของกิจกรรมทางแสง
- ละลายโดยสลายตัวที่อุณหภูมิสูงกว่า 200°C
- ไม่ระเหย
- สารละลายกรดอะมิโนที่เป็นน้ำในสภาพแวดล้อมที่เป็นกรดและด่างนำกระแสไฟฟ้า

ในบรรดาสารอินทรีย์ที่มีไนโตรเจนนั้นมีสารประกอบที่มีฟังก์ชันคู่อยู่ สิ่งสำคัญอย่างยิ่งคือ กรดอะมิโน.
กรดอะมิโนประมาณ 300 ชนิดพบได้ในเซลล์และเนื้อเยื่อของสิ่งมีชีวิต แต่มีเพียง 20 ชนิดเท่านั้น ( กรดอะมิโน ) ของพวกเขาทำหน้าที่เป็นหน่วย (โมโนเมอร์) ซึ่งสร้างเปปไทด์และโปรตีนของสิ่งมีชีวิตทั้งหมด (ดังนั้นจึงเรียกว่ากรดอะมิโนโปรตีน) ลำดับตำแหน่งของกรดอะมิโนเหล่านี้ในโปรตีนถูกเข้ารหัสในลำดับนิวคลีโอไทด์ของยีนที่เกี่ยวข้อง กรดอะมิโนที่เหลือพบได้ทั้งในรูปของโมเลกุลอิสระและในรูปพันธะ กรดอะมิโนจำนวนมากพบได้ในสิ่งมีชีวิตบางชนิดเท่านั้น และยังมีกรดอื่นๆ ที่พบในสิ่งมีชีวิตชนิดใดชนิดหนึ่งที่บรรยายไว้เท่านั้น จุลินทรีย์และพืชส่วนใหญ่สังเคราะห์กรดอะมิโนที่ต้องการ สัตว์และมนุษย์ไม่สามารถผลิตสิ่งที่เรียกว่ากรดอะมิโนจำเป็นที่ได้จากอาหารได้ กรดอะมิโนมีส่วนร่วมในการเผาผลาญโปรตีนและคาร์โบไฮเดรตในการก่อตัวของสารประกอบที่สำคัญสำหรับสิ่งมีชีวิต (เช่นเบสพิวรีนและไพริมิดีนซึ่งเป็นส่วนสำคัญของกรดนิวคลีอิก) พวกมันเป็นส่วนหนึ่งของฮอร์โมน วิตามิน อัลคาลอยด์ เม็ดสี , สารพิษ, ยาปฏิชีวนะ ฯลฯ ; กรดอะมิโนบางชนิดทำหน้าที่เป็นตัวกลางในการส่งกระแสประสาท
กรดอะมิโน- สารประกอบแอมโฟเทอริกอินทรีย์ซึ่งรวมถึงกลุ่มคาร์บอกซิล - COOH และกลุ่มอะมิโน -NH 2 .
กรดอะมิโน ถือได้ว่าเป็นกรดคาร์บอกซิลิกในโมเลกุลที่อะตอมไฮโดรเจนในอนุมูลจะถูกแทนที่ด้วยหมู่อะมิโน
การจำแนกประเภท
กรดอะมิโนแบ่งตามลักษณะโครงสร้าง1. ขึ้นอยู่กับตำแหน่งสัมพัทธ์ของกลุ่มอะมิโนและคาร์บอกซิล กรดอะมิโนจะถูกแบ่งออกเป็น α-, β-, γ-, δ-, ε- ฯลฯ
2. ขึ้นอยู่กับจำนวนกลุ่มฟังก์ชันจะแยกแยะกลุ่มที่เป็นกรดเป็นกลางและพื้นฐานได้
3. พวกมันแยกแยะตามลักษณะของอนุมูลไฮโดรคาร์บอน อะลิฟาติก(อ้วน), มีกลิ่นหอมประกอบด้วยกำมะถันและ เฮเทอโรไซคลิกกรดอะมิโน กรดอะมิโนข้างต้นอยู่ในกลุ่มไขมัน
ตัวอย่างของกรดอะมิโนอะโรมาติกคือกรดพารา-อะมิโนเบนโซอิก:
ตัวอย่างของกรดอะมิโนเฮเทอโรไซคลิกคือทริปโตเฟน ซึ่งเป็นกรด α-อะมิโนที่จำเป็น
ระบบการตั้งชื่อ
ตามระบบการตั้งชื่อตามระบบชื่อของกรดอะมิโนนั้นถูกสร้างขึ้นจากชื่อของกรดที่เกี่ยวข้องโดยการเพิ่มคำนำหน้า อะมิโนและระบุตำแหน่งของหมู่อะมิโนสัมพันธ์กับหมู่คาร์บอกซิล การกำหนดหมายเลขโซ่คาร์บอนจากอะตอมคาร์บอนของกลุ่มคาร์บอกซิล
ตัวอย่างเช่น:
อีกวิธีหนึ่งในการสร้างชื่อของกรดอะมิโนก็มักจะใช้ตามที่เพิ่มคำนำหน้าให้กับชื่อเล็กน้อยของกรดคาร์บอกซิลิก อะมิโนระบุตำแหน่งของหมู่อะมิโนด้วยตัวอักษรกรีก
ตัวอย่าง:
สำหรับกรด α-อะมิโนR-CH(NH2)COOH
ซึ่งมีบทบาทสำคัญในกระบวนการชีวิตของสัตว์และพืชจึงมีการใช้ชื่อเล็กน้อย
โต๊ะ.
|
กรดอะมิโน |
ย่อ การกำหนด |
โครงสร้างของราก (R) |
|
ไกลซีน |
กลี |
ชม- |
|
อลานิน |
อาล่า (อาล่า) |
ช 3 - |
|
วาลิน |
วาล |
(ช่อง 3) 2 ช่อง - |
|
ลิวซีน |
เล่ย (เล่ย) |
(ช 3) 2 ช – ช 2 - |
|
เซริน |
เซอร์ |
โอ้-CH2- |
|
ไทโรซีน |
ไทร์ (สนามยิงปืน) |
HO – C 6 H 4 – CH 2 - |
|
กรดแอสปาร์ติก |
งูเห่า (ASP) |
HOOC – CH 2 - |
|
กรดกลูตามิก |
กลู |
HOOC – CH 2 – CH 2 - |
|
ซีสเตอีน |
ซิส (ซิส) |
HS – CH 2 - |
|
แอสพาราจีน |
อาสน์ (อาสน์) |
โอ = ค – CH 2 – │ เอ็นเอช 2 |
|
ไลซีน |
ลิส (ลิซ) |
NH 2 – CH 2 - CH 2 – CH 2 - |
|
ฟีนิลอะลานีน |
เพ็ญ |
ค 6 ชั่วโมง 5 – CH 2 - |
หากโมเลกุลของกรดอะมิโนมีกลุ่มอะมิโนสองกลุ่มก็จะใช้คำนำหน้าในชื่อของมันไดอามิโน-, กลุ่ม NH 2 สามกลุ่ม – ไตรอามิโน-ฯลฯ
ตัวอย่าง:
การมีอยู่ของกลุ่มคาร์บอกซิลสองหรือสามกลุ่มนั้นสะท้อนให้เห็นในชื่อด้วยคำต่อท้าย –ไดวี่หรือ -กรดไตรอิก:
ไอโซเมเรีย
1. ไอโซเมอริซึมของโครงกระดูกคาร์บอน
2. ไอโซเมอริซึมของตำแหน่งของหมู่ฟังก์ชัน
3. ไอโซเมอร์เชิงแสง
กรดα-อะมิโน ยกเว้นไกลซีน NH 2 -CH 2 -COOH
คุณสมบัติทางกายภาพ
กรดอะมิโนเป็นสารผลึกที่มีจุดหลอมเหลวสูง (สูงกว่า 250°C) ซึ่งมีความแตกต่างกันเล็กน้อยในกรดอะมิโนแต่ละตัว ดังนั้นจึงไม่มีลักษณะเฉพาะ การหลอมละลายจะมาพร้อมกับการสลายตัวของสาร กรดอะมิโนละลายได้สูงในน้ำและไม่ละลายในตัวทำละลายอินทรีย์ ซึ่งทำให้คล้ายกับสารประกอบอนินทรีย์ กรดอะมิโนหลายชนิดมีรสหวาน
การรับ
3. การสังเคราะห์ทางจุลชีววิทยา เป็นที่ทราบกันดีว่าจุลินทรีย์ในระหว่างกระบวนการชีวิตของพวกมันจะผลิตกรดα - กรดอะมิโนของโปรตีน
คุณสมบัติทางเคมี
กรดอะมิโนเป็นสารประกอบอินทรีย์แบบแอมโฟเทอริก โดยมีคุณสมบัติเป็นกรด-เบส
ฉัน . คุณสมบัติทั่วไป
1. การวางตัวเป็นกลางภายในโมเลกุล → เกิดสวิตเตอร์ไอออนแบบไบโพลาร์:
สารละลายที่เป็นน้ำเป็นสื่อกระแสไฟฟ้า คุณสมบัติเหล่านี้อธิบายได้จากข้อเท็จจริงที่ว่าโมเลกุลของกรดอะมิโนมีอยู่ในรูปของเกลือภายในซึ่งเกิดขึ้นจากการถ่ายโอนโปรตอนจากคาร์บอกซิลไปยังกลุ่มอะมิโน:
สวิตเตอร์
สารละลายที่เป็นน้ำของกรดอะมิโนมีสภาพแวดล้อมที่เป็นกลาง เป็นกรด หรือเป็นด่าง ขึ้นอยู่กับจำนวนหมู่ฟังก์ชัน
แอปพลิเคชัน
1) กรดอะมิโนมีการกระจายอย่างกว้างขวางในธรรมชาติ
2) โมเลกุลของกรดอะมิโนเป็นหน่วยการสร้างโปรตีนจากพืชและสัตว์ทั้งหมด มนุษย์และสัตว์ได้รับกรดอะมิโนที่จำเป็นสำหรับการสร้างโปรตีนในร่างกายซึ่งเป็นส่วนหนึ่งของโปรตีนในอาหาร
3) กรดอะมิโนถูกกำหนดไว้สำหรับการอ่อนเพลียอย่างรุนแรงหลังการผ่าตัดที่รุนแรง
4) ใช้เลี้ยงคนป่วย
5) กรดอะมิโนเป็นสิ่งจำเป็นในการรักษาโรคบางชนิด (เช่นกรดกลูตามิกใช้สำหรับโรคทางประสาท, ฮิสติดีนสำหรับแผลในกระเพาะอาหาร)
6) กรดอะมิโนบางชนิดใช้ในการเกษตรเพื่อเป็นอาหารสัตว์ซึ่งมีผลดีต่อการเจริญเติบโตของพวกมัน
7) มีความสำคัญทางเทคนิค: กรด aminocaproic และ aminoenanthic ก่อให้เกิดเส้นใยสังเคราะห์ - capron และ enanth
เกี่ยวกับบทบาทของกรดอะมิโน
การเกิดขึ้นตามธรรมชาติและบทบาททางชีวภาพของกรดอะมิโน
การค้นพบในธรรมชาติและบทบาททางชีวภาพของกรดอะมิโน
กรดอะมิโนเป็นสารประกอบที่ทำหน้าที่ต่างกันซึ่งจำเป็นต้องมีกลุ่มฟังก์ชันสองกลุ่ม: กลุ่มอะมิโน - NH 2 และกลุ่มคาร์บอกซิล - COOH ที่เกี่ยวข้องกับอนุมูลไฮโดรคาร์บอน สามารถเขียนสูตรทั่วไปของกรดอะมิโนที่ง่ายที่สุดได้ดังนี้:
![]()
เนื่องจากกรดอะมิโนมีหมู่ฟังก์ชันที่แตกต่างกันสองหมู่ที่มีอิทธิพลซึ่งกันและกัน ปฏิกิริยาลักษณะเฉพาะจึงแตกต่างจากปฏิกิริยาของกรดคาร์บอกซิลิกและเอมีน
คุณสมบัติของกรดอะมิโน
กลุ่มอะมิโน - NH 2 กำหนดคุณสมบัติพื้นฐานของกรดอะมิโนเนื่องจากสามารถยึดไฮโดรเจนไอออนบวกเข้ากับตัวมันเองผ่านกลไกผู้บริจาคและตัวรับเนื่องจากมีคู่อิเล็กตรอนอิสระอยู่ที่อะตอมไนโตรเจน
กลุ่ม -COOH (กลุ่มคาร์บอกซิล) กำหนดคุณสมบัติที่เป็นกรดของสารประกอบเหล่านี้ ดังนั้นกรดอะมิโนจึงเป็นสารประกอบอินทรีย์แบบแอมโฟเทอริก พวกมันทำปฏิกิริยากับด่างเป็นกรด:
ด้วยกรดแก่ - คล้ายเบส - เอมีน:
นอกจากนี้ หมู่อะมิโนในกรดอะมิโนยังทำปฏิกิริยากับหมู่คาร์บอกซิลทำให้เกิดเกลือภายใน:

การแตกตัวเป็นไอออนของโมเลกุลกรดอะมิโนขึ้นอยู่กับลักษณะที่เป็นกรดหรือด่างของสิ่งแวดล้อม:

เนื่องจากกรดอะมิโนในสารละลายในน้ำมีพฤติกรรมเหมือนสารประกอบแอมโฟเทอริกทั่วไป ในสิ่งมีชีวิตพวกมันจึงมีบทบาทเป็นสารบัฟเฟอร์ที่รักษาความเข้มข้นของไฮโดรเจนไอออนไว้
กรดอะมิโนเป็นสารผลึกไม่มีสีที่ละลายและสลายตัวที่อุณหภูมิสูงกว่า 200 °C ละลายได้ในน้ำและไม่ละลายในอีเทอร์ อาจมีรสหวาน ขม หรือไม่มีรส ทั้งนี้ขึ้นอยู่กับ R- Radical
กรดอะมิโนแบ่งออกเป็นตามธรรมชาติ (พบในสิ่งมีชีวิต) และสังเคราะห์ ในบรรดากรดอะมิโนธรรมชาติ (ประมาณ 150 ตัว) กรดอะมิโนที่เป็นโปรตีน (ประมาณ 20 ตัว) มีความโดดเด่นซึ่งเป็นส่วนหนึ่งของโปรตีน เป็นรูปตัว L ประมาณครึ่งหนึ่งของกรดอะมิโนเหล่านี้คือ ไม่สามารถถูกแทนที่ได้เพราะไม่ได้สังเคราะห์ขึ้นในร่างกายมนุษย์ กรดจำเป็นได้แก่ วาลีน, ลิวซีน, ไอโซลิวซีน, ฟีนิลอะลานีน, ไลซีน, ทรีโอนีน, ซีสเตอีน, เมไทโอนีน, ฮิสติดีน, ทริปโตเฟน สารเหล่านี้เข้าสู่ร่างกายมนุษย์พร้อมกับอาหาร หากปริมาณในอาหารไม่เพียงพอ การพัฒนาและการทำงานของร่างกายมนุษย์จะหยุดชะงัก ในโรคบางชนิด ร่างกายไม่สามารถสังเคราะห์กรดอะมิโนอื่นๆ ได้ ดังนั้นในฟีนิลคีโตนูเรีย ไทโรซีนจึงไม่สังเคราะห์ขึ้น คุณสมบัติที่สำคัญที่สุดของกรดอะมิโนคือความสามารถในการเข้าสู่การควบแน่นของโมเลกุลด้วยการปล่อยน้ำและการก่อตัวของกลุ่มเอไมด์ -NH-CO- เช่น:


สารประกอบโมเลกุลสูงที่ได้รับจากปฏิกิริยานี้มีชิ้นส่วนเอไมด์จำนวนมากจึงถูกเรียกว่า ใยสังเคราะห์
นอกเหนือจากเส้นใยไนลอนสังเคราะห์ที่กล่าวถึงข้างต้นแล้ว ยังรวมถึง ตัวอย่างเช่น เอแนนต์ ที่เกิดขึ้นระหว่างการควบแน่นของกรดอะมิโนอีแนนติก กรดอะมิโนที่มีหมู่อะมิโนและคาร์บอกซิลที่ปลายโมเลกุลเหมาะสำหรับการผลิตเส้นใยสังเคราะห์
โพลีเอไมด์ของกรดอะมิโนอัลฟ่า เรียกว่า เปปไทด์- ขึ้นอยู่กับจำนวนของกรดอะมิโนที่ตกค้าง ไดเปปไทด์, ไตรเปปไทด์, โพลีเปปไทด์- ในสารประกอบดังกล่าว หมู่ -NH-CO- เรียกว่าหมู่เปปไทด์
ไอโซเมอริซึมและการตั้งชื่อของกรดอะมิโน
ไอโซเมอริซึมของกรดอะมิโนถูกกำหนดโดยโครงสร้างที่แตกต่างกันของสายโซ่คาร์บอนและตำแหน่งของหมู่อะมิโน ตัวอย่างเช่น

ชื่อของกรดอะมิโนก็แพร่หลายเช่นกันซึ่งตำแหน่งของหมู่อะมิโนจะถูกระบุด้วยตัวอักษรของอักษรกรีก: α, β, y เป็นต้น ดังนั้นกรด 2-aminobutanoic จึงสามารถเรียกว่ากรดα-amino : :

วิธีการได้รับกรดอะมิโน

กรดอะมิโนเป็นสารประกอบอินทรีย์ที่มีหมู่ฟังก์ชันในโมเลกุล ได้แก่ อะมิโนและคาร์บอกซิล
การตั้งชื่อกรดอะมิโน ตามระบบการตั้งชื่อตามระบบ ชื่อของกรดอะมิโนนั้นเกิดขึ้นจากชื่อของกรดคาร์บอกซิลิกที่เกี่ยวข้องและการเติมคำว่า "อะมิโน" ตำแหน่งของกลุ่มอะมิโนระบุด้วยตัวเลข การนับจะดำเนินการจากคาร์บอนของกลุ่มคาร์บอกซิล
ไอโซเมอริซึมของกรดอะมิโน ไอโซเมอริซึมของโครงสร้างถูกกำหนดโดยตำแหน่งของหมู่อะมิโนและโครงสร้างของอนุมูลคาร์บอน ขึ้นอยู่กับตำแหน่งของหมู่ NH 2, กรดอะมิโน -, - และ -มีความโดดเด่น

โมเลกุลโปรตีนถูกสร้างขึ้นจากกรดα-อะมิโน
พวกมันยังมีลักษณะเฉพาะด้วยไอโซเมอริซึมของกลุ่มฟังก์ชัน (ไอโซเมอร์ระหว่างคลาสของกรดอะมิโนสามารถเป็นเอสเทอร์ของกรดอะมิโนหรือเอไมด์ของกรดไฮดรอกซี) ตัวอย่างเช่น สำหรับกรด 2-อะมิโนโพรพาโนอิก CH 3 – CH(NH) 2 – COOH ไอโซเมอร์ต่อไปนี้เป็นไปได้

คุณสมบัติทางกายภาพของกรดα-อะมิโน
กรดอะมิโนเป็นสารผลึกไม่มีสี ไม่ระเหย (ความดันไออิ่มตัวต่ำ) ละลายโดยมีการสลายตัวที่อุณหภูมิสูง ส่วนใหญ่ละลายได้ในน้ำสูงและละลายได้ไม่ดีในตัวทำละลายอินทรีย์
สารละลายที่เป็นน้ำของกรดอะมิโนโมโนเบสิกมีปฏิกิริยาที่เป็นกลาง -กรดอะมิโนถือได้ว่าเป็นเกลือภายใน (ไบโพลาร์ไอออน): + NH 3 ช.2 ซีโอโอ . ในสภาพแวดล้อมที่เป็นกรด พวกมันจะมีพฤติกรรมเหมือนแคตไอออน ในสภาพแวดล้อมที่เป็นด่าง พวกมันจะมีพฤติกรรมเหมือนแอนไอออน กรดอะมิโนเป็นสารประกอบแอมโฟเทอริกที่มีคุณสมบัติเป็นกรดและเบส
วิธีการได้รับกรด α-อะมิโน
1. ผลของแอมโมเนียต่อเกลือของกรดคลอรีน
Cl
ช.2
คูน 4 + NH 3  เอ็นเอช 2
CH2COOH
เอ็นเอช 2
CH2COOH
2. ผลของแอมโมเนียและกรดไฮโดรไซยานิกต่ออัลดีไฮด์

3. การย่อยโปรตีนจะผลิตกรดอะมิโน 25 ชนิด การแยกพวกมันออกจากกันไม่ใช่เรื่องง่าย
วิธีการได้รับ -กรดอะมิโน
1. การเติมแอมโมเนียลงในกรดคาร์บอกซิลิกที่ไม่อิ่มตัว
ช.2 = ช COOH + 2NH 3 NH 2 ช.2 ช.2 คูนห์ 4.
2. การสังเคราะห์ขึ้นอยู่กับกรด dibasic malonic
คุณสมบัติทางเคมีของกรดอะมิโน
1. ปฏิกิริยาต่อหมู่คาร์บอกซิล
1.1. การก่อตัวของอีเทอร์โดยการกระทำของแอลกอฮอล์
2.ปฏิกิริยาที่หมู่อะมิโน
2.1. ปฏิกิริยากับกรดแร่
เอ็นเอช 2 CH 2 COOH + HCl H 3 N + ช.2 COOH + Cl
2.2. ปฏิกิริยากับกรดไนตรัส
เอ็นเอช 2 CH 2 COOH + HNO 2 H O ช.2 COOH + N 2 + H 2 O
3. การแปลงกรดอะมิโนเมื่อถูกความร้อน
3 .1.-กรดอะมิโนก่อตัวเป็นไซคลิกเอไมด์
.1.-กรดอะมิโนก่อตัวเป็นไซคลิกเอไมด์
3![]() .2.-กรดอะมิโนจะกำจัดหมู่อะมิโนและอะตอมไฮโดรเจนของอะตอมคาร์บอน y
.2.-กรดอะมิโนจะกำจัดหมู่อะมิโนและอะตอมไฮโดรเจนของอะตอมคาร์บอน y
ตัวแทนรายบุคคล
ไกลซีน NH 2 CH 2 COOH (ไกลโคคอล) กรดอะมิโนชนิดหนึ่งที่พบมากที่สุดในโปรตีน ภายใต้สภาวะปกติ - ผลึกไม่มีสีที่มี Tm = 232236С ละลายได้ง่ายในน้ำ ไม่ละลายในแอลกอฮอล์และอีเทอร์สัมบูรณ์ ดัชนีไฮโดรเจนของสารละลายในน้ำ6.8; พีเค ก = 1.510 10; рК в = 1.710 12.
α-อะลานีน – กรดอะมิโนโพรพิโอนิก
กระจายอยู่ทั่วไปในธรรมชาติ พบได้ฟรีในพลาสมาในเลือดและในโปรตีนส่วนใหญ่ T pl = 295296С, ละลายได้สูงในน้ำ, ละลายได้ไม่ดีในเอธานอล, ไม่ละลายในอีเทอร์ pK และ (COOH) = 2.34; พีเคเอ (NH  )
= 9,69.
)
= 9,69.
-อะลานีน NH 2 CH 2 CH 2 COOH – ผลึกขนาดเล็กที่มีอุณหภูมิหลอมละลาย = 200°C ละลายได้ดีในน้ำ มีเอธานอลต่ำ ไม่ละลายในอีเทอร์และอะซิโตน pK และ (COOH) = 3.60; พีเคเอ (NH  ) = 10.19; ขาดโปรตีน
) = 10.19; ขาดโปรตีน
คอมเพล็กซ์ คำนี้ใช้เพื่อตั้งชื่อชุดของกรด α-อะมิโนที่มีหมู่คาร์บอกซิลสองหรือสามหมู่ ง่ายที่สุด:

เอ็น  คอมเพล็กซ์ที่พบมากที่สุดคือกรดเอทิลีนไดเอมีนเตตราอะซิติก
คอมเพล็กซ์ที่พบมากที่สุดคือกรดเอทิลีนไดเอมีนเตตราอะซิติก
เกลือไดโซเดียม Trilon B ถูกนำมาใช้กันอย่างแพร่หลายในเคมีวิเคราะห์
พันธะระหว่างสารตกค้างของกรด α-อะมิโนเรียกว่าพันธะเปปไทด์ และสารประกอบที่เกิดในตัวมันเองเรียกว่าเปปไทด์
สารตกค้างของกรดα-amino สองตัวก่อให้เกิดไดเปปไทด์, สาม - ไตรเปปไทด์ สารตกค้างจำนวนมากก่อตัวเป็นโพลีเปปไทด์ โพลีเปปไทด์ก็เหมือนกับกรดอะมิโนที่เป็นแอมโฟเทอริก โดยแต่ละชนิดมีจุดไอโซอิเล็กทริกของตัวเอง โปรตีนเป็นโพลีเปปไทด์
 สมการลอการิทึม
สมการลอการิทึม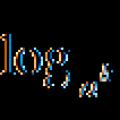 เทคนิคการแก้สมการลอการิทึม
เทคนิคการแก้สมการลอการิทึม การวิเคราะห์ตนเองของครูนักบำบัดการพูด
การวิเคราะห์ตนเองของครูนักบำบัดการพูด