สูตรทางเคมีของโครงสร้างหลักของโปรตีน คุณสมบัติทางเคมีฟิสิกส์ของโปรตีน
>> เคมี: โปรตีน
โปรตีนหรือสารโปรตีนเป็นโพลีเมอร์ธรรมชาติที่มีโมเลกุลสูง (น้ำหนักโมเลกุลแตกต่างกันไปตั้งแต่ 5-10 พันถึง 1 ล้านหรือมากกว่า) โพลีเมอร์ตามธรรมชาติ ซึ่งโมเลกุลเหล่านี้สร้างขึ้นจากสารตกค้างของกรดอะมิโนที่เชื่อมต่อกันด้วยพันธะเอไมด์ (เปปไทด์)
โปรตีนเรียกอีกอย่างว่าโปรตีน (จากภาษากรีก "โปรโตส" - อันแรกที่สำคัญ) จำนวนกรดอะมิโนตกค้างในโมเลกุลโปรตีนแตกต่างกันอย่างมากและบางครั้งก็ถึงหลายพัน โปรตีนแต่ละชนิดมีลำดับของกรดอะมิโนตกค้างอยู่ในตัว
โปรตีนทำหน้าที่ทางชีวภาพที่หลากหลาย: ตัวเร่งปฏิกิริยา (เอนไซม์), การควบคุม (ฮอร์โมน), โครงสร้าง (คอลลาเจน, ไฟโบรอิน), มอเตอร์ (ไมโอซิน), การขนส่ง (เฮโมโกลบิน, ไมโอโกลบิน), การป้องกัน (อิมมูโนโกลบูลิน, อินเตอร์เฟอรอน), สารสำรอง (เคซีน, อัลบูมิน, gliadin) และอื่น ๆ ในบรรดาโปรตีนมียาปฏิชีวนะและสารที่เป็นพิษ
โปรตีนเป็นพื้นฐานของไบโอแมมเบรน ซึ่งเป็นส่วนที่สำคัญที่สุดของเซลล์และส่วนประกอบของเซลล์ พวกมันมีบทบาทสำคัญในชีวิตของเซลล์ซึ่งก่อตัวเป็นพื้นฐานทางวัตถุของกิจกรรมทางเคมี
คุณสมบัติพิเศษของโปรตีนคือการจัดระเบียบตัวเองของโครงสร้าง กล่าวคือ ความสามารถในการสร้างโครงสร้างเชิงพื้นที่ที่เฉพาะเจาะจงโดยธรรมชาติเฉพาะกับโปรตีนที่กำหนดเท่านั้น โดยพื้นฐานแล้ว กิจกรรมทั้งหมดของร่างกาย (การพัฒนา การเคลื่อนไหว การทำงานของหน้าที่ต่างๆ และอีกมากมาย) เกี่ยวข้องกับสารโปรตีน (รูปที่ 36) เป็นไปไม่ได้ที่จะจินตนาการถึงชีวิตที่ปราศจากโปรตีน
โปรตีนเป็นส่วนประกอบที่สำคัญที่สุดของอาหารมนุษย์และสัตว์ ซึ่งเป็นซัพพลายเออร์ของกรดอะมิโนที่พวกเขาต้องการ
โครงสร้าง
ในโครงสร้างเชิงพื้นที่ของโปรตีน ลักษณะของอนุมูล (สารตกค้าง) R- ในโมเลกุลกรดอะมิโนมีความสำคัญอย่างยิ่ง อนุมูลของกรดอะมิโนที่ไม่มีขั้วมักจะอยู่ภายในโมเลกุลโปรตีนขนาดใหญ่และทำให้เกิดปฏิกิริยาที่ไม่ชอบน้ำ (ดูด้านล่าง) อนุมูลเชิงขั้วที่มีหมู่ไอออนิก (ที่ก่อตัวเป็นไอออน) มักจะอยู่บนผิวของโมเลกุลโปรตีนขนาดใหญ่และแสดงลักษณะปฏิกิริยาของปฏิกิริยาไฟฟ้าสถิต (ไอออนิก) อนุมูลแบบไม่มีขั้ว (เช่น ที่มีกลุ่ม OH แอลกอฮอล์ กลุ่มเอไมด์) สามารถอยู่ได้ทั้งบนพื้นผิวและภายในโมเลกุลโปรตีน พวกเขามีส่วนร่วมในการก่อตัวของพันธะไฮโดรเจน
ในโมเลกุลโปรตีน กรดเอ-อะมิโนเชื่อมต่อกันด้วยพันธะเปปไทด์ (-CO-NH-) ดังนี้
สายโพลีเปปไทด์ที่สร้างขึ้นในลักษณะนี้หรือแต่ละส่วนภายในสายพอลิเปปไทด์ ในบางกรณี สามารถเชื่อมต่อกันเพิ่มเติมได้ด้วยพันธะไดซัลไฟด์ (-S-S-) หรือที่มักเรียกว่าสะพานไดซัลไฟด์
บทบาทสำคัญในการสร้างโครงสร้างของโปรตีนนั้นเล่นโดยพันธะไอออนิก (เกลือ) และไฮโดรเจน เช่นเดียวกับปฏิกิริยาที่ไม่ชอบน้ำ ซึ่งเป็นการสัมผัสพิเศษระหว่างส่วนประกอบที่ไม่ชอบน้ำของโมเลกุลโปรตีนในตัวกลางที่เป็นน้ำ พันธะเหล่านี้มีจุดแข็งต่างกันและก่อให้เกิดโมเลกุลโปรตีนขนาดใหญ่ที่ซับซ้อน
แม้จะมีความแตกต่างในโครงสร้างและหน้าที่ของสารโปรตีน แต่องค์ประกอบขององค์ประกอบจะผันผวนเล็กน้อย (ใน% ของมวลแห้ง): คาร์บอน - 51-53; ออกซิเจน - 21.5-23.5; ไนโตรเจน - 16.8-18.4; ไฮโดรเจน - 6.5-7.3; กำมะถัน - 0.3-2.5 โปรตีนบางชนิดมีฟอสฟอรัส ซีลีเนียม และองค์ประกอบอื่นๆ ในปริมาณเล็กน้อย
ลำดับของการเชื่อมต่อสารตกค้างของกรดอะมิโนในสายโซ่โพลีเปปไทด์เรียกว่าโครงสร้างหลักของโปรตีน (รูปที่ 37)
โมเลกุลโปรตีนอาจประกอบด้วยสายพอลิเปปไทด์หนึ่งสายหรือมากกว่า ซึ่งแต่ละสายมีเรซิดิวกรดอะมิโนจำนวนต่างกัน เมื่อพิจารณาจากจำนวนส่วนผสมที่เป็นไปได้แล้ว อาจกล่าวได้ว่าความหลากหลายของโปรตีนนั้นแทบจะไร้ขีดจำกัด แต่ก็ไม่ได้มีอยู่ในธรรมชาติทั้งหมด จำนวนโปรตีนประเภทต่าง ๆ ทั้งหมดในสิ่งมีชีวิตทุกประเภทคือ 10 10 -10 12 . สำหรับโปรตีนที่มีโครงสร้างซับซ้อนมาก นอกเหนือจากโปรตีนปฐมภูมิแล้ว ยังมีการจำแนกระดับโครงสร้างที่สูงกว่า: โครงสร้างรอง ตติยภูมิ และบางครั้งเป็นสี่ส่วน (ตารางที่ 9) โปรตีนส่วนใหญ่มีโครงสร้างรอง แม้ว่าจะไม่ได้ตลอดทั้งสายของพอลิเปปไทด์ทั้งหมดก็ตาม โซ่โพลีเปปไทด์ที่มีโครงสร้างรองบางอย่างสามารถจัดเรียงในช่องว่างต่างกันได้
การจัดเรียงเชิงพื้นที่นี้เรียกว่าโครงสร้างตติยภูมิ (รูปที่ 39)
ในการก่อตัวของโครงสร้างตติยภูมินอกเหนือจากพันธะไฮโดรเจนแล้วปฏิกิริยาของไอออนิกและไม่ชอบน้ำก็มีบทบาทสำคัญ โดยธรรมชาติของ "การบรรจุ" ของโมเลกุลโปรตีน โปรตีนทรงกลมหรือทรงกลมและไฟบริลลาร์หรือเส้นใย
สำหรับโปรตีนทรงกลม โครงสร้าง a-helical นั้นมีลักษณะเฉพาะมากกว่า ส่วนเฮลิซนั้นโค้ง "พับ" โมเลกุลขนาดใหญ่มีรูปทรงกลม พวกมันละลายในน้ำและสารละลายน้ำเกลือเพื่อสร้างระบบคอลลอยด์ โปรตีนจากสัตว์ พืช และจุลินทรีย์ส่วนใหญ่เป็นโปรตีนทรงกลม 
สำหรับโปรตีนไฟบริลลาร์ โครงสร้างเส้นใยมีลักษณะเฉพาะมากกว่า โดยทั่วไปจะไม่ละลายในน้ำ โปรตีนไฟบริลลาร์มักจะทำหน้าที่สร้างโครงสร้าง คุณสมบัติ (ความแข็งแรง ความสามารถในการยืดตัว) ขึ้นอยู่กับวิธีการบรรจุสายโซ่โพลีเปปไทด์ ตัวอย่างของโปรตีนไฟบริลลาร์ ได้แก่ โปรตีนจากเนื้อเยื่อของกล้ามเนื้อ (ไมโอซิน) เคราติน (เนื้อเยื่อที่มีเขา) ในบางกรณี หน่วยย่อยของโปรตีนแต่ละหน่วยจะสร้างกลุ่มที่ซับซ้อนด้วยความช่วยเหลือของพันธะไฮโดรเจน ไฟฟ้าสถิต และปฏิกิริยาอื่นๆ ในกรณีนี้จะเกิดโครงสร้างสี่ส่วนของโปรตีน
อย่างไรก็ตาม ควรสังเกตอีกครั้งว่าโครงสร้างหลักมีบทบาทพิเศษในการจัดระเบียบโครงสร้างโปรตีนที่สูงขึ้น 
การจำแนกประเภท
โปรตีนมีหลายประเภท ขึ้นอยู่กับลักษณะที่แตกต่างกัน:
ระดับความยาก (ง่ายและซับซ้อน);
รูปร่างของโมเลกุล (โปรตีนทรงกลมและไฟบริลลาร์);
ความสามารถในการละลายในตัวทำละลายแต่ละตัว (ละลายได้ในน้ำ, ละลายได้ในสารละลายน้ำเกลือเจือจาง - อัลบูมิน, ที่ละลายในแอลกอฮอล์ - โปรลามิน, ละลายในด่างเจือจางและกรด - กลูเตลิน);
ทำหน้าที่ (เช่น เก็บโปรตีน โครงกระดูก ฯลฯ)
คุณสมบัติ
โปรตีนเป็นอิเล็กโทรไลต์แอมโฟเทอริก ที่ค่า pH ของตัวกลาง (เรียกว่าจุดไอโซอิเล็กทริก) จำนวนประจุบวกและลบในโมเลกุลโปรตีนจะเท่ากัน นี่เป็นหนึ่งในคุณสมบัติหลักของโปรตีน โปรตีน ณ จุดนี้เป็นกลางทางไฟฟ้า และความสามารถในการละลายในน้ำจะต่ำที่สุด ความสามารถของโปรตีนในการลดความสามารถในการละลายเมื่อโมเลกุลของพวกมันกลายเป็นกลางทางไฟฟ้านั้นถูกใช้เพื่อแยกพวกมันออกจากสารละลาย เช่น ในเทคโนโลยีเพื่อให้ได้ผลิตภัณฑ์ที่เป็นโปรตีน
ไฮเดรชั่น
กระบวนการให้ความชุ่มชื้นหมายถึงการจับกันของน้ำโดยโปรตีน ในขณะที่พวกมันมีคุณสมบัติที่ชอบน้ำ: บวม มวลและปริมาตรเพิ่มขึ้น อาการบวมของโปรตีนจะมาพร้อมกับการละลายบางส่วน ความชอบน้ำของโปรตีนแต่ละชนิดขึ้นอยู่กับโครงสร้าง hydrophilic amide (-CO-NH-, พันธะเปปไทด์), amine (NH2) และ carboxyl (COOH) ที่มีอยู่ในองค์ประกอบและตั้งอยู่บนพื้นผิวของโมเลกุลโปรตีนขนาดใหญ่ดึงดูดโมเลกุลของน้ำโดยปรับทิศทางบนพื้นผิวของโมเลกุลอย่างเคร่งครัด . เปลือกการให้ความชุ่มชื้น (น้ำ) ที่ล้อมรอบโปรตีนทรงกลมป้องกันการรวมกลุ่มและการตกตะกอน และด้วยเหตุนี้ มีส่วนทำให้เกิดความเสถียรของสารละลายโปรตีน ที่จุดไอโซอิเล็กทริก โปรตีนมีความสามารถในการจับน้ำน้อยที่สุด เปลือกไฮเดรชั่นรอบๆ โมเลกุลโปรตีนจะถูกทำลาย ดังนั้นพวกมันจึงรวมกันเป็นก้อนขนาดใหญ่ การรวมตัวของโมเลกุลโปรตีนยังเกิดขึ้นเมื่อพวกมันถูกทำให้แห้งด้วยตัวทำละลายอินทรีย์บางชนิด เช่น เอทิลแอลกอฮอล์ สิ่งนี้นำไปสู่การตกตะกอนของโปรตีน เมื่อ pH ของตัวกลางเปลี่ยนแปลง โมเลกุลของโปรตีนจะกลายเป็นประจุ และความสามารถในการให้ความชุ่มชื้นของมันจะเปลี่ยนไป
ด้วยอาการบวมที่จำกัด สารละลายโปรตีนเข้มข้นจะสร้างระบบที่ซับซ้อนที่เรียกว่าเยลลี่ เยลลี่ไม่เป็นของเหลว ยืดหยุ่น มีความเป็นพลาสติก มีความแข็งแรงทางกลบางอย่าง และสามารถรักษารูปร่างได้ โปรตีนทรงกลมสามารถให้ความชุ่มชื้นได้อย่างสมบูรณ์โดยการละลายในน้ำ (เช่น โปรตีนนม) ทำให้เกิดสารละลายที่มีความเข้มข้นต่ำ คุณสมบัติที่ชอบน้ำของโปรตีน เช่น ความสามารถในการบวม สร้างเยลลี่ สารแขวนลอยที่คงตัว อิมัลชันและโฟม มีความสำคัญอย่างยิ่งในด้านชีววิทยาและอุตสาหกรรมอาหาร เจลลี่ที่เคลื่อนที่ได้มากซึ่งสร้างขึ้นจากโมเลกุลโปรตีนเป็นหลักคือไซโตพลาสซึม - เนื้อหากึ่งของเหลวของเซลล์ เยลลี่ไฮเดรทสูง - กลูเตนดิบที่แยกได้จากแป้งสาลี มีน้ำมากถึง 65% ความชอบน้ำที่แตกต่างกันของโปรตีนกลูเตนเป็นหนึ่งในสัญญาณที่บ่งบอกถึงคุณภาพของเมล็ดข้าวสาลีและแป้งที่ได้จากมัน (ที่เรียกว่าข้าวสาลีที่แข็งแรงและอ่อนแอ) ความชอบน้ำของโปรตีนจากเมล็ดพืชและแป้งมีบทบาทสำคัญในการจัดเก็บและการแปรรูปเมล็ดพืชในการอบ แป้งที่ได้จากอุตสาหกรรมการอบเป็นโปรตีนที่บวมในน้ำ ซึ่งเป็นเยลลี่เข้มข้นที่มีเมล็ดแป้ง
การเสื่อมสภาพของโปรตีน
ในระหว่างการเปลี่ยนสภาพภายใต้อิทธิพลของปัจจัยภายนอก (อุณหภูมิ การกระทำทางกล การกระทำของสารเคมี และปัจจัยอื่นๆ อีกจำนวนหนึ่ง) การเปลี่ยนแปลงเกิดขึ้นในโครงสร้างรอง ระดับอุดมศึกษา และควอเทอร์นารีของโมเลกุลโปรตีน กล่าวคือ ต้นกำเนิดของมัน โครงสร้างเชิงพื้นที่ โครงสร้างหลักและองค์ประกอบทางเคมีของโปรตีนจึงไม่เปลี่ยนแปลง การเปลี่ยนแปลงคุณสมบัติทางกายภาพ: ความสามารถในการละลายลดลง ความสามารถในการให้น้ำ สูญเสียกิจกรรมทางชีวภาพ รูปร่างของโมเลกุลโปรตีนเปลี่ยนไปการรวมกลุ่มเกิดขึ้น ในเวลาเดียวกัน กิจกรรมของหมู่เคมีบางกลุ่มเพิ่มขึ้น ผลของเอนไซม์โปรตีโอไลติกต่อโปรตีนก็ได้รับการอำนวยความสะดวก และทำให้ไฮโดรไลซ์ง่ายขึ้น
ในเทคโนโลยีการอาหาร การลดทอนสภาพด้วยความร้อนของโปรตีนมีความสำคัญในทางปฏิบัติเป็นพิเศษ โดยระดับที่ขึ้นอยู่กับอุณหภูมิ ระยะเวลาในการให้ความร้อนและความชื้น สิ่งนี้จะต้องจำไว้เมื่อพัฒนาโหมดการอบชุบด้วยความร้อนของวัตถุดิบอาหาร ผลิตภัณฑ์กึ่งสำเร็จรูป และผลิตภัณฑ์สำเร็จรูปในบางครั้ง กระบวนการเปลี่ยนสภาพด้วยความร้อนมีบทบาทพิเศษในการลวกวัตถุดิบผัก การอบแห้งเมล็ดพืช การอบขนมปัง และการทำพาสต้า การเปลี่ยนสภาพของโปรตีนอาจเกิดจากการกระทำทางกล (แรงกด การถู การเขย่า อัลตราซาวนด์) ในที่สุด การกระทำของสารเคมี (กรด ด่าง แอลกอฮอล์ อะซิโตน) นำไปสู่การเสียสภาพของโปรตีน เทคนิคเหล่านี้ใช้กันอย่างแพร่หลายในด้านอาหารและเทคโนโลยีชีวภาพ
เกิดฟอง
กระบวนการทำให้เกิดฟองเป็นที่เข้าใจกันว่าความสามารถของโปรตีนในการสร้างระบบก๊าซเหลวที่มีความเข้มข้นสูงเรียกว่าโฟม ความคงตัวของโฟมซึ่งโปรตีนเป็นตัวเป่า ไม่เพียงขึ้นอยู่กับธรรมชาติและความเข้มข้นเท่านั้น แต่ยังขึ้นอยู่กับอุณหภูมิด้วย โปรตีนเป็นสารทำให้เกิดฟองมีการใช้กันอย่างแพร่หลายในอุตสาหกรรมขนม (ขนมหวาน มาร์ชเมลโล่ ซูเฟล่) โครงสร้างของโฟมมีขนมปังซึ่งส่งผลต่อคุณสมบัติด้านรสชาติ
โมเลกุลของโปรตีนภายใต้อิทธิพลของปัจจัยหลายประการสามารถถูกทำลายหรือโต้ตอบกับสารอื่นๆ เพื่อสร้างผลิตภัณฑ์ใหม่ได้ สำหรับอุตสาหกรรมอาหาร กระบวนการที่สำคัญมากสามารถแยกแยะได้สองกระบวนการ: 1) การไฮโดรไลซิสของโปรตีนภายใต้การกระทำของเอนไซม์และ 2) ปฏิกิริยาระหว่างกลุ่มอะมิโนของโปรตีนหรือกรดอะมิโนกับกลุ่มคาร์บอนิลของน้ำตาลรีดิวซ์ ภายใต้อิทธิพลของโปรตีเอส - เอ็นไซม์ที่เร่งปฏิกิริยาไฮโดรไลติกแตกแยกของโปรตีน ตัวหลังแตกตัวเป็นผลิตภัณฑ์ที่ง่ายกว่า (โพลี- และไดเปปไทด์) และสุดท้ายกลายเป็นกรดอะมิโน อัตราการไฮโดรไลซิสของโปรตีนขึ้นอยู่กับองค์ประกอบ โครงสร้างโมเลกุล กิจกรรมของเอนไซม์ และสภาวะ
โปรตีนไฮโดรไลซิส
ปฏิกิริยาไฮโดรไลซิสกับการก่อตัวของกรดอะมิโนในแง่ทั่วไปสามารถเขียนได้ดังนี้: 
การเผาไหม้
4. ปฏิกิริยาอะไรที่สามารถใช้เพื่อจำแนกโปรตีนได้?
5. โปรตีนมีบทบาทอย่างไรในชีวิตของสิ่งมีชีวิต?
6. เรียกคืนจากหลักสูตรชีววิทยาทั่วไปซึ่งโปรตีนกำหนดคุณสมบัติภูมิคุ้มกันของสิ่งมีชีวิต
7. บอกเราเกี่ยวกับโรคเอดส์และการป้องกันโรคร้ายนี้
8. จะรู้จักผลิตภัณฑ์ที่ทำจากขนสัตว์ธรรมชาติและเส้นใยประดิษฐ์ได้อย่างไร?
9. เขียนสมการปฏิกิริยาสำหรับการไฮโดรไลซิสของโปรตีนด้วยสูตรทั่วไป (-NH-CH-CO-) n
l
R
กระบวนการนี้มีความสำคัญทางชีววิทยาอย่างไรและมีการใช้ในอุตสาหกรรมอย่างไร
10. เขียนสมการปฏิกิริยาที่สามารถนำมาใช้เพื่อสร้างการเปลี่ยนแปลงต่อไปนี้: อีเทน -> เอทิลแอลกอฮอล์ -> อะซิติกอัลดีไฮด์ -> กรดอะซิติก -> กรดคลอโรอะซิติก -> กรดอะมิโนอะซิติก -> โพลีเปปไทด์
กรณีเคมี งานและวิธีแก้ปัญหา บันทึกบทเรียน
โปรตีน (โปรตีน) คลาสของสารประกอบที่ประกอบด้วยไนโตรเจนเชิงซ้อน ซึ่งเป็นส่วนประกอบที่มีลักษณะเฉพาะและสำคัญที่สุด (พร้อมกับกรดนิวคลีอิก) ของสิ่งมีชีวิต โปรตีนทำหน้าที่หลายอย่างและหลากหลาย โปรตีนส่วนใหญ่เป็นเอนไซม์ที่กระตุ้นปฏิกิริยาเคมี ฮอร์โมนหลายชนิดที่ควบคุมกระบวนการทางสรีรวิทยาก็เป็นโปรตีนเช่นกัน โปรตีนโครงสร้างเช่นคอลลาเจนและเคราตินเป็นส่วนประกอบหลักของเนื้อเยื่อกระดูก ผมและเล็บ โปรตีนที่หดตัวของกล้ามเนื้อมีความสามารถในการเปลี่ยนความยาวโดยใช้พลังงานเคมีเพื่อทำงานทางกล โปรตีนเป็นแอนติบอดีที่ยึดเกาะและทำให้สารพิษเป็นกลาง โปรตีนบางชนิดที่สามารถตอบสนองต่ออิทธิพลภายนอก (แสง กลิ่น) ทำหน้าที่เป็นตัวรับในอวัยวะรับความรู้สึกที่รับรู้การระคายเคือง โปรตีนหลายชนิดที่อยู่ภายในเซลล์และบนเยื่อหุ้มเซลล์ทำหน้าที่ควบคุมในช่วงครึ่งแรกของศตวรรษที่ 19 นักเคมีหลายคนและในหมู่พวกเขาโดยหลักแล้ว J. von Liebig ค่อยๆสรุปว่าโปรตีนเป็นสารประกอบไนโตรเจนประเภทพิเศษ ชื่อ "โปรตีน" (จากภาษากรีก.
โปรโตส ครั้งแรก) ถูกเสนอในปี 1840 โดยนักเคมีชาวดัตช์ G. Mulder คุณสมบัติทางกายภาพ โปรตีนมีสีขาวในสถานะของแข็ง แต่ไม่มีสีในสารละลาย เว้นแต่จะมีกลุ่มโครโมฟอร์ (สี) บางกลุ่ม เช่น เฮโมโกลบิน ความสามารถในการละลายน้ำของโปรตีนที่แตกต่างกันนั้นแตกต่างกันอย่างมาก นอกจากนี้ยังแตกต่างกันไปตาม pH และความเข้มข้นของเกลือในสารละลาย เพื่อให้สามารถเลือกสภาวะที่โปรตีนตัวหนึ่งจะตกตะกอนอย่างเฉพาะเจาะจงเมื่อมีโปรตีนอื่นอยู่ วิธีการ "เกลือออก" นี้ใช้กันอย่างแพร่หลายในการแยกและทำให้โปรตีนบริสุทธิ์ โปรตีนบริสุทธิ์มักจะตกตะกอนจากสารละลายเป็นผลึกเมื่อเปรียบเทียบกับสารประกอบอื่น น้ำหนักโมเลกุลของโปรตีนมีขนาดใหญ่มาก ตั้งแต่หลายพันถึงหลายล้านดัลตัน ดังนั้นในระหว่างการปั่นแยกด้วยความเข้มข้นสูง โปรตีนจะถูกตกตะกอนและยิ่งไปกว่านั้นในอัตราที่ต่างกัน เนื่องจากการปรากฏตัวของกลุ่มที่มีประจุบวกและลบในโมเลกุลโปรตีน พวกมันจึงเคลื่อนที่ด้วยความเร็วที่แตกต่างกันในสนามไฟฟ้า นี่เป็นพื้นฐานของอิเล็กโตรโฟรีซิส ซึ่งเป็นวิธีการที่ใช้ในการแยกโปรตีนแต่ละชนิดออกจากสารผสมที่ซับซ้อน การทำให้โปรตีนบริสุทธิ์ยังดำเนินการโดยโครมาโตกราฟี
คุณสมบัติทางเคมี โครงสร้าง. โปรตีนเป็นโพลีเมอร์ กล่าวคือ โมเลกุลที่สร้างขึ้นเหมือนสายโซ่จากหน่วยโมโนเมอร์ที่ทำซ้ำหรือหน่วยย่อยตามบทบาทของพวกมัน เอ -กรดอะมิโน. สูตรทั่วไปของกรดอะมิโนที่ไหน R อะตอมไฮโดรเจนหรือหมู่อินทรีย์บางกลุ่มโมเลกุลโปรตีน (สายโพลีเปปไทด์) อาจประกอบด้วยกรดอะมิโนจำนวนค่อนข้างน้อยหรือโมโนเมอร์หลายพันหน่วย การเชื่อมโยงของกรดอะมิโนในสายโซ่เป็นไปได้เพราะแต่ละกลุ่มมีกลุ่มเคมีที่แตกต่างกันสองกลุ่ม: กลุ่มอะมิโนที่มีคุณสมบัติพื้นฐาน
NH2 และหมู่คาร์บอกซิลที่เป็นกรด COOH ทั้งสองกลุ่มนี้มีความเกี่ยวข้องกับ เอ - อะตอมของคาร์บอน หมู่คาร์บอกซิลของกรดอะมิโนหนึ่งตัวสามารถสร้างพันธะเอไมด์ (เปปไทด์) กับหมู่อะมิโนของกรดอะมิโนอื่น: หลังจากที่กรดอะมิโนสองชนิดเชื่อมต่อกันในลักษณะนี้แล้ว สามารถขยายสายโซ่ได้โดยการเพิ่มหนึ่งในสามของกรดอะมิโนที่สอง และอื่นๆ ดังที่เห็นได้จากสมการข้างต้น เมื่อเกิดพันธะเปปไทด์ โมเลกุลของน้ำจะถูกปลดปล่อยออกมา เมื่อมีกรด ด่าง หรือเอนไซม์โปรตีโอไลติก ปฏิกิริยาจะเกิดขึ้นในทิศทางตรงกันข้าม: สายโซ่โพลีเปปไทด์จะถูกแยกออกเป็นกรดอะมิโนด้วยการเติมน้ำ ปฏิกิริยานี้เรียกว่าไฮโดรไลซิส ไฮโดรไลซิสเกิดขึ้นเองตามธรรมชาติ และจำเป็นต้องใช้พลังงานในการรวมกรดอะมิโนเข้าเป็นสายพอลิเปปไทด์
หลังจากที่กรดอะมิโนสองชนิดเชื่อมต่อกันในลักษณะนี้แล้ว สามารถขยายสายโซ่ได้โดยการเพิ่มหนึ่งในสามของกรดอะมิโนที่สอง และอื่นๆ ดังที่เห็นได้จากสมการข้างต้น เมื่อเกิดพันธะเปปไทด์ โมเลกุลของน้ำจะถูกปลดปล่อยออกมา เมื่อมีกรด ด่าง หรือเอนไซม์โปรตีโอไลติก ปฏิกิริยาจะเกิดขึ้นในทิศทางตรงกันข้าม: สายโซ่โพลีเปปไทด์จะถูกแยกออกเป็นกรดอะมิโนด้วยการเติมน้ำ ปฏิกิริยานี้เรียกว่าไฮโดรไลซิส ไฮโดรไลซิสเกิดขึ้นเองตามธรรมชาติ และจำเป็นต้องใช้พลังงานในการรวมกรดอะมิโนเข้าเป็นสายพอลิเปปไทด์ หมู่คาร์บอกซิลและหมู่เอไมด์ (หรือหมู่อิไมด์ที่คล้ายกันในกรณีของโพรลีนกรดอะมิโน) มีอยู่ในกรดอะมิโนทั้งหมด แต่ความแตกต่างระหว่างกรดอะมิโนถูกกำหนดโดยธรรมชาติของกลุ่มนั้น หรือ "สายข้าง" ซึ่งระบุไว้ข้างต้นด้วยตัวอักษร
R . บทบาทของสายโซ่ด้านข้างสามารถเล่นได้โดยอะตอมไฮโดรเจนหนึ่งอะตอม เช่นเดียวกับในไกลซีนของกรดอะมิโน หรือโดยกลุ่มที่เทอะทะ เช่น ฮิสทิดีนและทริปโตเฟน โซ่ข้างบางชนิดมีความเฉื่อยทางเคมี ในขณะที่บางประเภทมีปฏิกิริยาตอบสนองสูงสามารถสังเคราะห์กรดอะมิโนได้หลายพันชนิด และกรดอะมิโนหลายชนิดเกิดขึ้นในธรรมชาติ แต่มีกรดอะมิโนเพียง 20 ชนิดเท่านั้นที่ใช้สำหรับการสังเคราะห์โปรตีน ได้แก่ อะลานีน อาร์จินีน แอสปาราจีน กรดแอสปาร์ติก วาลีน ฮิสทิดีน ไกลซีน กลูตามีน กลูตามิก กรด, ไอโซลิวซีน, ลิวซีน, ไลซีน , เมไทโอนีน, โพรลีน, ซีรีน, ไทโรซีน, ทรีโอนีน, ทริปโตเฟน, ฟีนิลอะลานีน และซิสเทอีน (ในโปรตีน ซิสเทอีนอาจปรากฏเป็นไดเมอร์
ซีสทีน) จริงอยู่ ในโปรตีนบางชนิดมีกรดอะมิโนอื่นๆ นอกเหนือไปจากกรดอะมิโน 20 ชนิดที่เกิดขึ้นเป็นประจำ แต่เกิดขึ้นจากการดัดแปลงใดๆ ใน 20 ชนิดที่ระบุไว้หลังจากที่รวมเข้ากับโปรตีนแล้วกิจกรรมทางแสง กรดอะมิโนทั้งหมด ยกเว้นไกลซีน เอ อะตอมของคาร์บอนมีสี่กลุ่มที่ต่างกัน ในแง่ของเรขาคณิต สี่กลุ่มที่แตกต่างกันสามารถติดได้สองวิธี และด้วยเหตุนี้จึงมีการกำหนดค่าที่เป็นไปได้สองแบบ หรือสองไอโซเมอร์ที่เกี่ยวข้องกันเป็นวัตถุกับภาพสะท้อนของมัน กล่าวคือ เหมือนมือซ้ายไปขวา การกำหนดค่าหนึ่งเรียกว่าซ้ายหรือมือซ้าย (หลี่ ) และสิทธิอื่น ๆ หรือ dextrorotatory (ดี ) เนื่องจากไอโซเมอร์สองตัวดังกล่าวต่างกันในทิศทางการหมุนของระนาบของแสงโพลาไรซ์ พบเฉพาะในโปรตีนหลี่ -กรดอะมิโน (ข้อยกเว้นคือไกลซีน มันสามารถแสดงได้ในรูปแบบเดียวเท่านั้น เนื่องจากสองในสี่กลุ่มนั้นเหมือนกัน) และพวกมันทั้งหมดมีกิจกรรมทางแสง (เนื่องจากมีไอโซเมอร์เพียงตัวเดียว)ดี - กรดอะมิโนหายากในธรรมชาติ พบได้ในยาปฏิชีวนะบางชนิดและผนังเซลล์ของแบคทีเรียลำดับของกรดอะมิโน กรดอะมิโนในสายโซ่โพลีเปปไทด์ไม่ได้จัดเรียงแบบสุ่ม แต่อยู่ในลำดับที่แน่นอน และลำดับนี้กำหนดหน้าที่และคุณสมบัติของโปรตีน โดยการเรียงลำดับกรดอะมิโน 20 ชนิด คุณจะได้โปรตีนที่แตกต่างกันจำนวนมาก เช่นเดียวกับที่คุณสร้างข้อความต่างๆ มากมายจากตัวอักษรของตัวอักษรในอดีต การกำหนดลำดับกรดอะมิโนของโปรตีนมักใช้เวลาหลายปี การกำหนดโดยตรงยังคงเป็นงานที่ค่อนข้างลำบาก แม้ว่าจะมีการสร้างอุปกรณ์ที่อนุญาตให้ดำเนินการได้โดยอัตโนมัติ มักจะง่ายกว่าที่จะกำหนดลำดับนิวคลีโอไทด์ของยีนที่สอดคล้องกันและรับลำดับกรดอะมิโนของโปรตีนจากยีนนั้น จนถึงปัจจุบัน มีการกำหนดลำดับกรดอะมิโนของโปรตีนหลายร้อยชนิดแล้ว โดยปกติแล้วจะทราบหน้าที่ของโปรตีนถอดรหัส และช่วยให้จินตนาการถึงหน้าที่ที่เป็นไปได้ของโปรตีนที่คล้ายคลึงกันซึ่งก่อตัวขึ้น เช่น ในเนื้องอกที่เป็นมะเร็ง
โปรตีนที่ซับซ้อน โปรตีนที่ประกอบด้วยกรดอะมิโนเท่านั้นเรียกว่าง่าย อย่างไรก็ตาม บ่อยครั้ง อะตอมของโลหะหรือสารประกอบทางเคมีบางชนิดที่ไม่ใช่กรดอะมิโนติดอยู่กับสายโพลีเปปไทด์ โปรตีนดังกล่าวเรียกว่าซับซ้อน ตัวอย่างคือเฮโมโกลบิน: ประกอบด้วยธาตุเหล็กพอร์ไฟริน ซึ่งทำให้มีสีแดงและทำหน้าที่เป็นตัวพาออกซิเจนชื่อของโปรตีนที่ซับซ้อนที่สุดมีตัวบ่งชี้ถึงลักษณะของกลุ่มที่แนบมา: น้ำตาลมีอยู่ในไกลโคโปรตีน, ไขมันในไลโปโปรตีน หากการเร่งปฏิกิริยาของเอนไซม์ขึ้นอยู่กับกลุ่มที่แนบมา เรียกว่า กลุ่มเทียม บ่อยครั้ง วิตามินบางชนิดมีบทบาทในกลุ่มเทียมหรือเป็นส่วนหนึ่งของมัน ตัวอย่างเช่น วิตามินเอที่ติดอยู่กับโปรตีนตัวใดตัวหนึ่งของเรตินา เป็นตัวกำหนดความไวต่อแสง
โครงสร้างระดับตติยภูมิ สิ่งที่สำคัญไม่ใช่ลำดับกรดอะมิโนของโปรตีน (โครงสร้างหลัก) มากนัก แต่วิธีการวางในช่องว่าง ตลอดความยาวทั้งหมดของสายพอลิเปปไทด์ ไอออนของไฮโดรเจนจะก่อตัวเป็นพันธะไฮโดรเจนแบบปกติ ซึ่งทำให้มีรูปร่างเป็นเกลียวหรือชั้น (โครงสร้างทุติยภูมิ) จากการรวมกันของเกลียวและชั้นดังกล่าวรูปแบบที่กะทัดรัดของลำดับถัดไปเกิดขึ้น - โครงสร้างระดับอุดมศึกษาของโปรตีน รอบพันธะที่ยึดตัวเชื่อมแบบโมโนเมอร์ของโซ่ สามารถหมุนผ่านมุมเล็กๆ ได้ ดังนั้น จากมุมมองทางเรขาคณิตล้วนๆ จำนวนของโครงแบบที่เป็นไปได้สำหรับสายพอลิเปปไทด์ใดๆ จึงมีขนาดใหญ่อย่างไม่สิ้นสุด ในความเป็นจริง โปรตีนแต่ละชนิดมีอยู่ในรูปแบบเดียวเท่านั้น กำหนดโดยลำดับกรดอะมิโนของมัน โครงสร้างนี้ไม่แข็งกระด้างเหมือนเดิม « หายใจ” ผันผวนรอบการกำหนดค่าเฉลี่ยบางอย่าง โซ่ถูกพับเป็นรูปแบบที่พลังงานอิสระ (ความสามารถในการทำงาน) น้อยที่สุด เช่นเดียวกับสปริงที่ปล่อยออกมาจะถูกบีบอัดให้อยู่ในสถานะที่สอดคล้องกับพลังงานอิสระขั้นต่ำเท่านั้น บ่อยครั้ง ส่วนหนึ่งของสายโซ่เชื่อมโยงอย่างแน่นหนากับไดซัลไฟด์อีกตัวหนึ่ง (เอสเอส) พันธะระหว่างสองซิสเทอีนตกค้าง นี่เป็นส่วนหนึ่งที่ว่าทำไมซิสเทอีนในกรดอะมิโนจึงมีบทบาทสำคัญอย่างยิ่งความซับซ้อนของโครงสร้างของโปรตีนนั้นยิ่งใหญ่มากจนยังไม่สามารถคำนวณโครงสร้างระดับอุดมศึกษาของโปรตีนได้ แม้ว่าจะทราบลำดับกรดอะมิโนของโปรตีนก็ตาม แต่ถ้าเป็นไปได้ที่จะได้ผลึกโปรตีน โครงสร้างระดับอุดมศึกษาสามารถกำหนดได้โดยการเลี้ยวเบนของรังสีเอกซ์
ในโครงสร้าง หดตัว และโปรตีนอื่น ๆ โซ่จะยาวและโซ่พับเล็กน้อยหลายเส้นวางเรียงต่อกันเป็นเส้นใย ในทางกลับกันเส้นใยจะพับเป็นเส้นใยขนาดใหญ่ขึ้น อย่างไรก็ตาม โปรตีนส่วนใหญ่ในสารละลายมีลักษณะเป็นทรงกลม: โซ่จะพันเป็นทรงกลม เหมือนเส้นด้ายในลูกบอล พลังงานอิสระที่มีการกำหนดค่านี้มีน้อยมาก เนื่องจากกรดอะมิโนที่ไม่ชอบน้ำ ("การกันน้ำ") ถูกซ่อนอยู่ภายในทรงกลม และกรดอะมิโนที่ชอบน้ำ ("ดึงดูดน้ำ") อยู่บนผิวของมัน
โปรตีนหลายชนิดเป็นสารประกอบเชิงซ้อนของสายโซ่โพลีเปปไทด์หลายสาย โครงสร้างนี้เรียกว่าโครงสร้างควอเทอร์นารีของโปรตีน ตัวอย่างเช่น โมเลกุลของเฮโมโกลบินประกอบด้วยหน่วยย่อยสี่หน่วย ซึ่งแต่ละหน่วยเป็นโปรตีนทรงกลม
โปรตีนที่มีโครงสร้างเนื่องจากโครงร่างเชิงเส้นของพวกมันสร้างเส้นใยซึ่งมีความต้านทานแรงดึงสูงมาก ในขณะที่โครงแบบทรงกลมช่วยให้โปรตีนเข้าสู่ปฏิกิริยาจำเพาะกับสารประกอบอื่นๆ บนพื้นผิวของทรงกลมด้วยการวางโซ่ที่ถูกต้องฟันผุของรูปร่างบางอย่างจะปรากฏขึ้นซึ่งมีกลุ่มเคมีปฏิกิริยาอยู่ หากโปรตีนที่กำหนดเป็นเอนไซม์ โมเลกุลของสารบางชนิดซึ่งปกติแล้วจะมีขนาดเล็กกว่าจะเข้าสู่โพรงดังกล่าว เช่นเดียวกับที่กุญแจเข้าสู่ตัวล็อค ในกรณีนี้ โครงร่างของเมฆอิเล็กตรอนของโมเลกุลจะเปลี่ยนแปลงภายใต้อิทธิพลของกลุ่มเคมีที่อยู่ในโพรง และสิ่งนี้บังคับให้มันทำปฏิกิริยาในทางใดทางหนึ่ง ด้วยวิธีนี้เอนไซม์จะเร่งปฏิกิริยา โมเลกุลของแอนติบอดียังมีโพรงซึ่งสารแปลกปลอมต่างๆ จับตัวกันและด้วยเหตุนี้จึงทำให้ไม่มีอันตราย โมเดล "กุญแจและล็อค" ซึ่งอธิบายปฏิสัมพันธ์ของโปรตีนกับสารประกอบอื่นๆ ทำให้สามารถเข้าใจความจำเพาะของเอนไซม์และแอนติบอดี กล่าวคือ ความสามารถในการทำปฏิกิริยากับสารประกอบบางชนิดเท่านั้น
โปรตีนในสิ่งมีชีวิตประเภทต่างๆ โปรตีนที่ทำหน้าที่เหมือนกันในพืชและสัตว์ต่างชนิดกัน ดังนั้นจึงมีชื่อเดียวกันก็มีรูปแบบที่คล้ายคลึงกัน อย่างไรก็ตาม พวกมันแตกต่างกันบ้างในลำดับกรดอะมิโน เมื่อสปีชีส์แยกตัวจากบรรพบุรุษร่วมกัน กรดอะมิโนบางตัวในบางตำแหน่งจะถูกแทนที่ด้วยการกลายพันธุ์ด้วยกรดอะมิโนอื่นๆ การกลายพันธุ์ที่เป็นอันตรายซึ่งทำให้เกิดโรคทางพันธุกรรมจะถูกละทิ้งโดยการคัดเลือกโดยธรรมชาติ แต่สามารถรักษาสิ่งที่เป็นประโยชน์หรืออย่างน้อยก็เป็นกลางได้ ยิ่งสปีชีส์ทางชีวภาพใกล้กันมากเท่าไร โปรตีนของพวกมันก็จะยิ่งมีความแตกต่างกันน้อยลงเท่านั้นโปรตีนบางชนิดเปลี่ยนแปลงได้ค่อนข้างเร็ว ส่วนโปรตีนบางชนิดค่อนข้างอนุรักษ์นิยม หลังรวมถึงตัวอย่างเช่น cytochrome กับเอ็นไซม์ระบบทางเดินหายใจที่พบในสิ่งมีชีวิตส่วนใหญ่ ในมนุษย์และลิงชิมแปนซี มีลำดับกรดอะมิโนเหมือนกัน และในไซโตโครม กับข้าวสาลีมีเพียง 38% ของกรดอะมิโนที่เปลี่ยนไป แม้แต่การเปรียบเทียบมนุษย์กับแบคทีเรีย ความคล้ายคลึงของไซโตโครม กับ(ความแตกต่างนี้ส่งผลต่อกรดอะมิโน 65% ที่นี่) ยังคงมองเห็นได้ แม้ว่าบรรพบุรุษร่วมกันของแบคทีเรียและมนุษย์จะอาศัยอยู่บนโลกเมื่อประมาณสองพันล้านปีก่อน ทุกวันนี้ การเปรียบเทียบลำดับกรดอะมิโนมักถูกใช้เพื่อสร้างต้นไม้สายวิวัฒนาการ (ลำดับวงศ์ตระกูล) ที่สะท้อนถึงความสัมพันธ์เชิงวิวัฒนาการระหว่างสิ่งมีชีวิตต่างๆ
การเสื่อมสภาพ โมเลกุลโปรตีนสังเคราะห์ที่พับเก็บได้มาซึ่งโครงร่างของมันเอง อย่างไรก็ตาม การกำหนดค่านี้สามารถทำลายได้ด้วยการให้ความร้อน โดยการเปลี่ยนค่า pH โดยการกระทำของตัวทำละลายอินทรีย์ และแม้กระทั่งโดยการกวนสารละลายจนเกิดฟองอากาศปรากฏขึ้นบนพื้นผิว โปรตีนที่เปลี่ยนแปลงในลักษณะนี้เรียกว่า denatured; มันสูญเสียกิจกรรมทางชีวภาพและมักจะไม่ละลายน้ำ ตัวอย่างที่รู้จักกันดีของโปรตีนที่ทำให้เสียสภาพ ได้แก่ ไข่ต้มหรือวิปครีม โปรตีนขนาดเล็กที่มีกรดอะมิโนเพียงร้อยตัวเท่านั้นที่สามารถสร้างขึ้นใหม่ได้ กล่าวคือ รับการกำหนดค่าเดิมอีกครั้ง แต่โปรตีนส่วนใหญ่นั้นถูกแปลงสภาพเป็นมวลของสายโซ่โพลีเปปไทด์ที่พันกันและไม่คืนค่าโครงสร้างเดิมของพวกมันปัญหาหลักประการหนึ่งในการแยกโปรตีนที่ออกฤทธิ์คือความไวสูงต่อการเสียสภาพ คุณสมบัติของโปรตีนพบว่ามีประโยชน์ในการถนอมผลิตภัณฑ์อาหาร: อุณหภูมิสูงจะทำให้เอนไซม์ของจุลินทรีย์เปลี่ยนแปลงสภาพไปอย่างถาวร และจุลินทรีย์ก็ตาย
การสังเคราะห์โปรตีน สำหรับการสังเคราะห์โปรตีน สิ่งมีชีวิตต้องมีระบบของเอ็นไซม์ที่สามารถเชื่อมกรดอะมิโนตัวหนึ่งเข้ากับอีกตัวหนึ่งได้ จำเป็นต้องมีแหล่งข้อมูลเพื่อกำหนดกรดอะมิโนที่ควรเชื่อมต่อ เนื่องจากมีโปรตีนหลายพันชนิดในร่างกาย และแต่ละชนิดประกอบด้วยกรดอะมิโนหลายร้อยชนิดโดยเฉลี่ย ข้อมูลที่ต้องการจึงต้องมีปริมาณมหาศาลอย่างแท้จริง มันถูกเก็บไว้ (คล้ายกับวิธีที่บันทึกถูกเก็บไว้ในเทปแม่เหล็ก) ในโมเลกุลของกรดนิวคลีอิกที่ประกอบขึ้นเป็นยีน ซม . พันธุกรรมด้วย; กรดนิวคลีอิก.การกระตุ้นเอนไซม์ สายโซ่โพลีเปปไทด์ที่สังเคราะห์จากกรดอะมิโนไม่ใช่โปรตีนในรูปแบบสุดท้ายเสมอไป เอนไซม์จำนวนมากถูกสังเคราะห์ขึ้นเป็นครั้งแรกในฐานะสารตั้งต้นที่ไม่ใช้งานและจะทำงานได้ก็ต่อเมื่อเอ็นไซม์อื่นกำจัดกรดอะมิโนสองสามตัวออกจากปลายด้านหนึ่งของสายโซ่เท่านั้น เอนไซม์ย่อยอาหารบางชนิด เช่น ทริปซิน ถูกสังเคราะห์ในรูปแบบที่ไม่ใช้งานนี้ เอนไซม์เหล่านี้ถูกกระตุ้นในทางเดินอาหารอันเป็นผลมาจากการกำจัดส่วนปลายของโซ่ ฮอร์โมนอินซูลิน ซึ่งโมเลกุลในรูปแบบแอคทีฟประกอบด้วยสายสั้นสองสาย ถูกสังเคราะห์ในรูปของสายโซ่เดียวที่เรียกว่า อินซูลิน จากนั้นส่วนตรงกลางของสายโซ่นี้จะถูกลบออกและชิ้นส่วนที่เหลือจะเกาะติดกันสร้างโมเลกุลของฮอร์โมนที่ใช้งานอยู่ โปรตีนเชิงซ้อนจะเกิดขึ้นหลังจากที่กลุ่มเคมีบางกลุ่มยึดติดกับโปรตีนเท่านั้นและสิ่งที่แนบมานี้มักต้องใช้เอนไซม์ด้วยการไหลเวียนของเมตาบอลิ หลังจากให้อาหารสัตว์ด้วยกรดอะมิโนที่ติดฉลากด้วยไอโซโทปกัมมันตภาพรังสีของคาร์บอน ไนโตรเจน หรือไฮโดรเจน ฉลากจะถูกรวมเข้ากับโปรตีนอย่างรวดเร็ว หากกรดอะมิโนที่ติดฉลากหยุดเข้าสู่ร่างกาย ปริมาณของฉลากในโปรตีนจะเริ่มลดลง การทดลองเหล่านี้แสดงให้เห็นว่าโปรตีนที่เกิดขึ้นจะไม่ถูกเก็บไว้ในร่างกายจนกว่าจะสิ้นสุดชีวิต ทั้งหมดมีข้อยกเว้นบางประการ อยู่ในสถานะไดนามิก สลายตัวเป็นกรดอะมิโนอย่างต่อเนื่อง แล้วสังเคราะห์ใหม่อีกครั้งโปรตีนบางชนิดสลายตัวเมื่อเซลล์ตายและถูกทำลาย สิ่งนี้เกิดขึ้นตลอดเวลา ตัวอย่างเช่น กับเซลล์เม็ดเลือดแดงและเซลล์เยื่อบุผิวที่บุผิวด้านในของลำไส้ นอกจากนี้ การสลายและการสังเคราะห์โปรตีนยังเกิดขึ้นในเซลล์ที่มีชีวิตอีกด้วย น่าแปลกที่ไม่มีใครรู้เกี่ยวกับการสลายโปรตีนมากกว่าเรื่องการสังเคราะห์ อย่างไรก็ตาม สิ่งที่ชัดเจนก็คือ เอ็นไซม์โปรตีโอไลติกมีส่วนในการสลาย คล้ายกับเอนไซม์ที่สลายโปรตีนให้เป็นกรดอะมิโนในทางเดินอาหาร
ครึ่งชีวิตของโปรตีนที่แตกต่างกันนั้นแตกต่างกันไปตั้งแต่หลายชั่วโมงจนถึงหลายเดือน ข้อยกเว้นเพียงอย่างเดียวคือโมเลกุลคอลลาเจน เมื่อก่อตัวแล้วจะคงตัวและไม่มีการต่ออายุหรือเปลี่ยนใหม่ อย่างไรก็ตาม เมื่อเวลาผ่านไป คุณสมบัติบางอย่าง โดยเฉพาะอย่างยิ่ง ความยืดหยุ่น การเปลี่ยนแปลง และเนื่องจากไม่มีการต่ออายุ การเปลี่ยนแปลงบางอย่างที่เกี่ยวข้องกับอายุเป็นผลมาจากสิ่งนี้ ตัวอย่างเช่น การปรากฏตัวของริ้วรอยบนผิวหนัง
โปรตีนสังเคราะห์ นักเคมีได้เรียนรู้วิธีผสมกรดอะมิโนมานานแล้ว แต่กรดอะมิโนจะรวมกันแบบสุ่ม เพื่อให้ผลิตภัณฑ์ของโพลิเมอไรเซชันดังกล่าวมีความคล้ายคลึงกับกรดตามธรรมชาติเพียงเล็กน้อย จริงอยู่ เป็นไปได้ที่จะรวมกรดอะมิโนตามลำดับที่กำหนด ซึ่งทำให้สามารถรับโปรตีนที่ออกฤทธิ์ทางชีวภาพได้ โดยเฉพาะอย่างยิ่งอินซูลิน กระบวนการนี้ค่อนข้างซับซ้อน และด้วยวิธีนี้ เป็นไปได้ที่จะได้รับเฉพาะโปรตีนที่มีโมเลกุลประกอบด้วยกรดอะมิโนประมาณร้อยตัวเท่านั้น เป็นที่พึงประสงค์แทนที่จะสังเคราะห์หรือแยกลำดับนิวคลีโอไทด์ของยีนที่สอดคล้องกับลำดับกรดอะมิโนที่ต้องการ และจากนั้นนำเข้ายีนนี้ไปในแบคทีเรีย ซึ่งจะผลิตขึ้นโดยการทำซ้ำผลิตภัณฑ์ที่ต้องการเป็นจำนวนมาก อย่างไรก็ตาม วิธีนี้ก็มีข้อเสียเช่นกัน ซม . ดูเพิ่มเติมที่ พันธุวิศวกรรม โปรตีนและโภชนาการ เมื่อโปรตีนในร่างกายแตกตัวเป็นกรดอะมิโน กรดอะมิโนเหล่านี้สามารถนำกลับมาใช้ใหม่สำหรับการสังเคราะห์โปรตีนได้ ในเวลาเดียวกัน กรดอะมิโนเองก็อาจสลายตัวได้ เพื่อที่จะได้ใช้ประโยชน์ไม่เต็มที่ เป็นที่ชัดเจนว่าในระหว่างการเจริญเติบโต การตั้งครรภ์ และการรักษาบาดแผล การสังเคราะห์โปรตีนจะต้องเกินการย่อยสลาย ร่างกายสูญเสียโปรตีนบางส่วนอย่างต่อเนื่อง เหล่านี้คือโปรตีนของเส้นผม เล็บ และชั้นผิวของผิวหนัง ดังนั้นการสังเคราะห์โปรตีนแต่ละสิ่งมีชีวิตจะต้องได้รับกรดอะมิโนจากอาหาร พืชสีเขียวสังเคราะห์จากCO 2 น้ำและแอมโมเนียหรือไนเตรตล้วนเป็นกรดอะมิโน 20 ชนิดที่พบในโปรตีน แบคทีเรียจำนวนมากยังสามารถสังเคราะห์กรดอะมิโนเมื่อมีน้ำตาล (หรือเทียบเท่า) และไนโตรเจนคงที่ แต่สุดท้ายแล้วน้ำตาลก็มาจากพืชสีเขียว ในสัตว์ ความสามารถในการสังเคราะห์กรดอะมิโนมีจำกัด พวกเขาได้รับกรดอะมิโนจากการกินพืชสีเขียวหรือสัตว์อื่นๆ ในทางเดินอาหารโปรตีนที่ดูดซึมจะถูกแบ่งออกเป็นกรดอะมิโนส่วนหลังจะถูกดูดซึมและลักษณะโปรตีนของสิ่งมีชีวิตที่กำหนดนั้นถูกสร้างขึ้นจากพวกมัน ไม่มีโปรตีนที่ดูดซึมรวมอยู่ในโครงสร้างของร่างกายเช่นนี้ ข้อยกเว้นเพียงอย่างเดียวคือในสัตว์เลี้ยงลูกด้วยนมหลายชนิด ส่วนหนึ่งของแอนติบอดีของมารดาสามารถส่งผ่านรกไปยังระบบไหลเวียนของทารกในครรภ์ได้ครบถ้วน และผ่านน้ำนมมารดา (โดยเฉพาะในสัตว์เคี้ยวเอื้อง) ไปยังทารกแรกเกิดทันทีหลังคลอดต้องการโปรตีน. เป็นที่ชัดเจนว่าเพื่อรักษาชีวิต ร่างกายจะต้องได้รับโปรตีนจากอาหารจำนวนหนึ่ง อย่างไรก็ตาม ขนาดของความต้องการนี้ขึ้นอยู่กับปัจจัยหลายประการ ร่างกายต้องการอาหารทั้งเป็นแหล่งพลังงาน (แคลอรี) และเป็นวัสดุในการสร้างโครงสร้าง ประการแรกคือความต้องการพลังงาน ซึ่งหมายความว่าเมื่อมีคาร์โบไฮเดรตและไขมันเพียงเล็กน้อยในอาหาร โปรตีนในอาหารจะไม่ถูกนำมาใช้เพื่อการสังเคราะห์โปรตีนของตัวเอง แต่เป็นแหล่งของแคลอรี ด้วยการอดอาหารเป็นเวลานาน แม้แต่โปรตีนของคุณเองก็ยังถูกใช้เพื่อตอบสนองความต้องการพลังงาน หากอาหารมีคาร์โบไฮเดรตเพียงพอ ปริมาณโปรตีนจะลดลงความสมดุลของไนโตรเจน โดยเฉลี่ยประมาณ 16% ของมวลโปรตีนทั้งหมดคือไนโตรเจน เมื่อกรดอะมิโนที่ประกอบเป็นโปรตีนถูกทำลายลง ไนโตรเจนที่มีอยู่ในกรดจะถูกขับออกจากร่างกายในปัสสาวะและ (ในระดับที่น้อยกว่า) ในอุจจาระในรูปของสารประกอบไนโตรเจนต่างๆ ดังนั้นจึงสะดวกที่จะใช้ตัวบ่งชี้เช่นสมดุลไนโตรเจนเพื่อประเมินคุณภาพของสารอาหารโปรตีนเช่น ความแตกต่าง (เป็นกรัม) ระหว่างปริมาณไนโตรเจนที่เข้าสู่ร่างกายและปริมาณไนโตรเจนที่ขับออกมาต่อวัน ด้วยโภชนาการปกติในผู้ใหญ่ ปริมาณเหล่านี้จะเท่ากัน ในสิ่งมีชีวิตที่กำลังเติบโต ปริมาณไนโตรเจนที่ขับออกมาจะน้อยกว่าปริมาณที่เข้ามา กล่าวคือ ยอดคงเหลือเป็นบวก ด้วยการขาดโปรตีนในอาหาร ความสมดุลจึงเป็นลบ หากอาหารมีแคลอรีเพียงพอ แต่ไม่มีโปรตีนอยู่ในนั้น ร่างกายก็จะเก็บโปรตีนไว้ ในขณะเดียวกัน เมแทบอลิซึมของโปรตีนก็ช้าลง และการนำกรดอะมิโนกลับมาใช้ใหม่ในการสังเคราะห์โปรตีนก็ดำเนินไปอย่างมีประสิทธิภาพมากที่สุด อย่างไรก็ตามการสูญเสียเป็นสิ่งที่หลีกเลี่ยงไม่ได้และสารประกอบไนโตรเจนยังคงถูกขับออกทางปัสสาวะและบางส่วนในอุจจาระ ปริมาณไนโตรเจนที่ขับออกจากร่างกายต่อวันในช่วงที่ขาดโปรตีนสามารถทำหน้าที่เป็นตัววัดการขาดโปรตีนในแต่ละวัน เป็นเรื่องปกติที่จะสันนิษฐานว่าโดยการแนะนำปริมาณโปรตีนที่เทียบเท่ากับการขาดสารอาหารนี้เข้าไปในอาหาร เป็นไปได้ที่จะฟื้นฟูสมดุลของไนโตรเจน อย่างไรก็ตามมันไม่ใช่ เมื่อได้รับโปรตีนในปริมาณนี้ ร่างกายจะเริ่มใช้กรดอะมิโนอย่างมีประสิทธิภาพน้อยลง ดังนั้นจึงจำเป็นต้องมีโปรตีนเพิ่มเติมเพื่อคืนความสมดุลของไนโตรเจนหากปริมาณโปรตีนในอาหารเกินความจำเป็นในการรักษาสมดุลของไนโตรเจน ดูเหมือนว่าจะไม่มีอันตรายจากสิ่งนี้ กรดอะมิโนที่มากเกินไปนั้นถูกใช้เป็นแหล่งพลังงานเพียงอย่างเดียว ตัวอย่างที่โดดเด่นเป็นพิเศษคือชาวเอสกิโมซึ่งกินคาร์โบไฮเดรตเพียงเล็กน้อยและมีโปรตีนมากกว่าที่จำเป็นเพื่อรักษาสมดุลของไนโตรเจนประมาณสิบเท่า อย่างไรก็ตาม ในกรณีส่วนใหญ่ การใช้โปรตีนเป็นแหล่งพลังงานไม่เป็นประโยชน์ เนื่องจากคุณสามารถได้รับแคลอรีจากคาร์โบไฮเดรตในปริมาณที่กำหนดมากกว่าโปรตีนในปริมาณเท่ากัน ในประเทศยากจน ประชากรจะได้รับแคลอรี่ที่จำเป็นจากคาร์โบไฮเดรตและบริโภคโปรตีนในปริมาณที่น้อยที่สุด
หากร่างกายได้รับแคลอรี่ตามจำนวนที่ต้องการในรูปของผลิตภัณฑ์ที่ไม่ใช่โปรตีน ปริมาณโปรตีนขั้นต่ำที่ช่วยรักษาสมดุลของไนโตรเจนจะอยู่ที่ประมาณ 30 กรัมต่อวัน ในขนมปังสี่ชิ้นหรือนม 0.5 ลิตรมีโปรตีนอยู่ประมาณเท่าๆ กัน ปริมาณที่มากกว่าเล็กน้อยมักจะถือว่าเหมาะสมที่สุด แนะนำตั้งแต่ 50 ถึง 70 กรัม
กรดอะมิโนที่จำเป็น จนถึงปัจจุบันนี้ถือว่าโปรตีนโดยรวมแล้ว ในขณะเดียวกัน เพื่อให้เกิดการสังเคราะห์โปรตีน กรดอะมิโนที่จำเป็นทั้งหมดต้องมีอยู่ในร่างกาย กรดอะมิโนบางชนิดที่ร่างกายของสัตว์สามารถสังเคราะห์ได้ พวกเขาถูกเรียกว่าทดแทนได้เนื่องจากไม่จำเป็นต้องมีอยู่ในอาหาร เป็นสิ่งสำคัญเท่านั้นโดยทั่วไปการบริโภคโปรตีนเป็นแหล่งไนโตรเจนก็เพียงพอแล้ว เมื่อขาดกรดอะมิโนที่จำเป็น ร่างกายสามารถสังเคราะห์กรดอะมิโนเหล่านี้ได้โดยใช้ค่ากรดอะมิโนที่มากเกินไป กรดอะมิโน "จำเป็น" ที่เหลืออยู่ไม่สามารถสังเคราะห์ได้และต้องกินเข้าไปพร้อมกับอาหาร สิ่งจำเป็นสำหรับมนุษย์ ได้แก่ วาลีน ลิวซีน ไอโซลิวซีน ทรีโอนีน เมไทโอนีน ฟีนิลอะลานีน ทริปโตเฟน ฮิสทิดีน ไลซีน และอาร์จินีน (แม้ว่าอาร์จินีนสามารถสังเคราะห์ในร่างกายได้ แต่ก็ถือว่าเป็นกรดอะมิโนที่จำเป็น เนื่องจากทารกแรกเกิดและเด็กที่กำลังเติบโตผลิตในปริมาณที่ไม่เพียงพอ ในทางกลับกัน สำหรับผู้ที่มีอายุมากแล้ว การบริโภคกรดอะมิโนเหล่านี้บางส่วนจากอาหาร อาจเป็นทางเลือก)รายชื่อกรดอะมิโนที่จำเป็นนี้มีความใกล้เคียงกันในสัตว์มีกระดูกสันหลังอื่นๆ และแม้แต่ในแมลง คุณค่าทางโภชนาการของโปรตีนมักจะถูกกำหนดโดยการให้อาหารแก่หนูที่กำลังเติบโตและการติดตามน้ำหนักที่เพิ่มขึ้นของสัตว์
คุณค่าทางโภชนาการของโปรตีน คุณค่าทางโภชนาการของโปรตีนถูกกำหนดโดยกรดอะมิโนที่จำเป็นซึ่งขาดมากที่สุด ลองอธิบายสิ่งนี้ด้วยตัวอย่าง โปรตีนในร่างกายของเรามีค่าเฉลี่ยประมาณ ทริปโตเฟน 2% (โดยน้ำหนัก) สมมติว่าอาหารประกอบด้วยโปรตีน 10 กรัมที่มีทริปโตเฟน 1% และมีกรดอะมิโนที่จำเป็นอื่นๆ เพียงพอ ในกรณีของเรา โปรตีนที่มีข้อบกพร่อง 10 กรัมนี้เทียบเท่ากับโปรตีนที่สมบูรณ์ 5 กรัม ส่วนที่เหลืออีก 5 กรัมสามารถทำหน้าที่เป็นแหล่งพลังงานเท่านั้น โปรดทราบว่าเนื่องจากกรดอะมิโนไม่ได้ถูกเก็บไว้ในร่างกาย และเพื่อให้เกิดการสังเคราะห์โปรตีน กรดอะมิโนทั้งหมดจะต้องมีอยู่พร้อม ๆ กัน ผลของการบริโภคกรดอะมิโนที่จำเป็นจะถูกตรวจพบก็ต่อเมื่อพวกมันทั้งหมดเข้าสู่ ร่างกายไปพร้อม ๆ กัน. องค์ประกอบโดยเฉลี่ยของโปรตีนจากสัตว์ส่วนใหญ่นั้นใกล้เคียงกับองค์ประกอบโดยเฉลี่ยของโปรตีนในร่างกายมนุษย์ ดังนั้นเราจึงไม่น่าจะเผชิญกับการขาดกรดอะมิโนหากอาหารของเราอุดมไปด้วยอาหาร เช่น เนื้อสัตว์ ไข่ นม และชีส อย่างไรก็ตาม มีโปรตีน เช่น เจลาติน (ผลิตภัณฑ์จากการเสื่อมสภาพของคอลลาเจน) ซึ่งมีกรดอะมิโนที่จำเป็นน้อยมาก โปรตีนจากพืชแม้ว่าจะดีกว่าเจลาตินในแง่นี้ แต่ก็มีกรดอะมิโนที่จำเป็นต่ำเช่นกัน โดยเฉพาะอย่างยิ่งไลซีนและทริปโตเฟนเพียงเล็กน้อย อย่างไรก็ตาม การรับประทานอาหารมังสวิรัติล้วนไม่เป็นอันตรายเลย เว้นแต่จะกินโปรตีนจากพืชในปริมาณที่มากกว่าเล็กน้อย ซึ่งเพียงพอที่จะให้กรดอะมิโนที่จำเป็นแก่ร่างกาย โปรตีนส่วนใหญ่พบได้ในพืชในเมล็ดพืช โดยเฉพาะในเมล็ดข้าวสาลีและพืชตระกูลถั่วต่างๆ หน่ออ่อน เช่น หน่อไม้ฝรั่ง ก็อุดมไปด้วยโปรตีนเช่นกันโปรตีนสังเคราะห์ในอาหาร การเพิ่มกรดอะมิโนจำเป็นสังเคราะห์หรือโปรตีนที่อุดมไปด้วยโปรตีนในปริมาณเล็กน้อยลงในโปรตีนที่ไม่สมบูรณ์ เช่น โปรตีนจากข้าวโพด ทำให้สามารถเพิ่มคุณค่าทางโภชนาการของโปรตีนชนิดหลังได้อย่างมีนัยสำคัญ กล่าวคือ จึงเป็นการเพิ่มปริมาณโปรตีนที่บริโภค ความเป็นไปได้อีกประการหนึ่งคือการปลูกแบคทีเรียหรือยีสต์บนปิโตรเลียมไฮโดรคาร์บอนด้วยการเติมไนเตรตหรือแอมโมเนียเป็นแหล่งไนโตรเจน โปรตีนจุลินทรีย์ที่ได้จากวิธีนี้สามารถใช้เป็นอาหารสำหรับสัตว์ปีกหรือปศุสัตว์ หรือมนุษย์สามารถบริโภคได้โดยตรง วิธีที่สามที่ใช้กันอย่างแพร่หลายใช้สรีรวิทยาของสัตว์เคี้ยวเอื้อง ในสัตว์เคี้ยวเอื้องในตอนต้นของกระเพาะที่เรียกว่า กระเพาะรูเมนเป็นที่อยู่อาศัยของแบคทีเรียและโปรโตซัวรูปแบบพิเศษที่เปลี่ยนโปรตีนจากพืชที่บกพร่องให้กลายเป็นโปรตีนจุลินทรีย์ที่สมบูรณ์มากขึ้น และในทางกลับกัน หลังจากการย่อยและการดูดซึมจะกลายเป็นโปรตีนจากสัตว์ ยูเรียซึ่งเป็นสารประกอบที่มีไนโตรเจนสังเคราะห์ราคาถูกสามารถเติมลงในอาหารปศุสัตว์ได้ จุลินทรีย์ที่อาศัยอยู่ในกระเพาะรูเมนใช้ยูเรียไนโตรเจนเพื่อเปลี่ยนคาร์โบไฮเดรต (ซึ่งมีมากกว่าในอาหาร) ให้เป็นโปรตีน ประมาณหนึ่งในสามของไนโตรเจนทั้งหมดในอาหารปศุสัตว์สามารถมาในรูปของยูเรียซึ่งในสาระสำคัญหมายถึงการสังเคราะห์โปรตีนทางเคมีในระดับหนึ่ง ในสหรัฐอเมริกา วิธีนี้มีบทบาทสำคัญในการได้รับโปรตีนวิธีหนึ่งวรรณกรรม เมอร์เรย์ อาร์, เกรนเนอร์ ดี, เมเยส พี, ร็อดเวลล์ ดับเบิลยู ชีวเคมีของมนุษย์, ท. 12. ม., 1993Alberts B. , Bray D. , Lewis J. และคณะ อณูชีววิทยาของเซลล์, ท. 13. ม., 1994
ท่ามกลางอินทรียวัตถุ กระรอก, หรือ โปรตีนเป็นพอลิเมอร์ชีวภาพที่มีจำนวนมากที่สุด หลากหลายที่สุด และมีความสำคัญสูงสุด พวกเขาบัญชีสำหรับ 50 - 80% น้ำหนักแห้งของเซลล์
โมเลกุลของโปรตีนมีขนาดใหญ่จึงเรียกว่า โมเลกุลขนาดใหญ่. นอกจากคาร์บอน ออกซิเจน ไฮโดรเจน และไนโตรเจน โปรตีนยังสามารถประกอบด้วยกำมะถัน ฟอสฟอรัส และเหล็ก โปรตีนแตกต่างกันในจำนวน (จากหนึ่งแสนถึงหลายพัน) องค์ประกอบและลำดับของโมโนเมอร์ โมโนเมอร์ของโปรตีนคือกรดอะมิโน (รูปที่ 1)
โปรตีนที่หลากหลายไม่มีที่สิ้นสุดถูกสร้างขึ้นจากการผสมผสานของทุกสิ่งที่แตกต่างกัน 20 กรดอะมิโน. กรดอะมิโนแต่ละชนิดมีชื่อ โครงสร้างและคุณสมบัติพิเศษเป็นของตัวเอง สูตรทั่วไปสามารถแสดงได้ดังนี้:

โมเลกุลของกรดอะมิโนประกอบด้วยสองส่วนที่เหมือนกันสำหรับกรดอะมิโนทั้งหมด หนึ่งในนั้นคือหมู่อะมิโน ( -NH2) ด้วยคุณสมบัติพื้นฐานอีกชนิดหนึ่งที่มีหมู่คาร์บอกซิล ( -COOH) ที่มีคุณสมบัติเป็นกรด ส่วนของโมเลกุลที่เรียกว่าอนุมูล ( R) กรดอะมิโนที่แตกต่างกันมีโครงสร้างที่แตกต่างกัน การปรากฏตัวของหมู่เบสและกรดในโมเลกุลกรดอะมิโนหนึ่งตัวกำหนดปฏิกิริยาสูงของพวกมัน ผ่านกลุ่มเหล่านี้กรดอะมิโนเชื่อมต่อกันเป็นโปรตีน ในกรณีนี้ โมเลกุลของน้ำปรากฏขึ้น และอิเล็กตรอนที่ปล่อยออกมาจะสร้างพันธะเปปไทด์ นั่นคือเหตุผลที่เรียกว่าโปรตีน โพลีเปปไทด์.
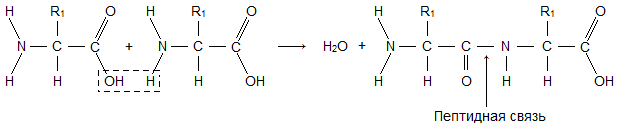
โมเลกุลของโปรตีนสามารถมีรูปแบบเชิงพื้นที่ที่แตกต่างกัน และโครงสร้างโครงสร้างสี่ระดับมีความโดดเด่นในโครงสร้าง
ลำดับของกรดอะมิโนในสายพอลิเปปไทด์คือ โครงสร้างหลักกระรอก. มีลักษณะเฉพาะของโปรตีนทุกชนิด และเป็นตัวกำหนดรูปร่าง คุณสมบัติ และหน้าที่ของโปรตีน
โปรตีนส่วนใหญ่มีรูปร่างเป็นเกลียวอันเป็นผลมาจากการก่อตัวของพันธะไฮโดรเจนระหว่าง -CO-และ -เอ็นเอช-กลุ่มของกรดอะมิโนตกค้างต่าง ๆ ของสายพอลิเปปไทด์ พันธะไฮโดรเจนมีความอ่อนแอ แต่เมื่อรวมกันแล้วจะมีโครงสร้างที่แข็งแรงพอสมควร เกลียวนี้คือ โครงสร้างรองกระรอก.
โครงสร้างตติยภูมิ- "การบรรจุ" เชิงพื้นที่สามมิติของสายโซ่โพลีเปปไทด์ เป็นผลให้เกิดการกำหนดค่าที่แปลกประหลาด แต่เฉพาะสำหรับโปรตีนแต่ละตัว - ลูกกลม. ความแข็งแรงของโครงสร้างตติยภูมินั้นมาจากพันธะต่างๆ ที่เกิดขึ้นระหว่างอนุมูลของกรดอะมิโน
โครงสร้างควอเทอร์นารีไม่ธรรมดาสำหรับโปรตีนทุกชนิด มันเกิดขึ้นจากการรวมกันของโมเลกุลขนาดใหญ่หลายตัวที่มีโครงสร้างตติยภูมิกลายเป็นคอมเพล็กซ์ที่ซับซ้อน ตัวอย่างเช่น ฮีโมโกลบินในเลือดของมนุษย์เป็นคอมเพล็กซ์ของโมเลกุลโปรตีนสี่โมเลกุล
ความซับซ้อนของโครงสร้างของโมเลกุลโปรตีนนี้สัมพันธ์กับหน้าที่ที่หลากหลายซึ่งมีอยู่ในไบโอโพลีเมอร์เหล่านี้
การละเมิดโครงสร้างตามธรรมชาติของโปรตีนเรียกว่า การทำให้เสียสภาพ. สามารถเกิดขึ้นได้ภายใต้อิทธิพลของอุณหภูมิ สารเคมี พลังงานการแผ่รังสี และปัจจัยอื่นๆ ด้วยแรงกระแทกที่อ่อนแอ เฉพาะโครงสร้างควอเทอร์นารีเท่านั้นที่จะสลายตัว โดยที่โครงสร้างที่แข็งแรงกว่า แบบที่สาม และแบบรอง และโปรตีนยังคงอยู่ในรูปของสายโซ่โพลีเปปไทด์
กระบวนการนี้สามารถย้อนกลับได้บางส่วน: หากโครงสร้างหลักไม่ถูกรบกวน โปรตีนที่แปลงสภาพแล้วจะสามารถฟื้นฟูโครงสร้างได้ เป็นไปตามที่คุณสมบัติทั้งหมดของโครงสร้างของโมเลกุลโปรตีนถูกกำหนดโดยโครงสร้างหลักของมัน
ยกเว้น โปรตีนอย่างง่ายซึ่งประกอบด้วยกรดอะมิโนเท่านั้นก็ยังมี โปรตีนที่ซับซ้อน
กระรอกเป็นสารประกอบอินทรีย์น้ำหนักโมเลกุลสูงที่สร้างขึ้นจากสารตกค้างของกรดอะมิโน 20 ชนิด ตามโครงสร้าง พวกมันเป็นของพอลิเมอร์ โมเลกุลของพวกมันอยู่ในรูปของสายโซ่ยาวซึ่งประกอบด้วยโมเลกุลที่ทำซ้ำ - โมโนเมอร์ ในการก่อรูปโมเลกุลโพลีเมอร์ โมโนเมอร์แต่ละตัวต้องมีพันธะปฏิกิริยาอย่างน้อยสองพันธะกับโมโนเมอร์อื่น
โปรตีนมีโครงสร้างคล้ายกับโพลีเมอร์ไนลอน: โพลีเมอร์ทั้งสองเป็นสายโซ่ของโมโนเมอร์ แต่มีความแตกต่างที่สำคัญระหว่างพวกเขา ไนลอนประกอบด้วยโมโนเมอร์สองประเภท ในขณะที่โปรตีนประกอบด้วยโมโนเมอร์ 20 ชนิดที่เรียกว่ากรดอะมิโน ขึ้นอยู่กับลำดับของการสลับของโมโนเมอร์ โปรตีนหลายชนิดจะเกิดขึ้น
สูตรทั่วไปสำหรับกรดอะมิโนที่ประกอบเป็นโปรตีนคือ:
สูตรนี้แสดงให้เห็นว่าสี่กลุ่มต่าง ๆ ติดอยู่กับอะตอมของคาร์บอนกลาง สามในนั้น - อะตอมไฮโดรเจน H, หมู่อัลคาไลน์อะมิโน H N และกลุ่มคาร์บอกซิล COOH - เหมือนกันสำหรับกรดอะมิโนทั้งหมด ตามองค์ประกอบและโครงสร้างของกลุ่มที่สี่กำหนด
R กรดอะมิโนต่างกัน ในกรณีที่ง่ายที่สุด ในโมเลกุลกลีเซอรอล - กลุ่มดังกล่าวคืออะตอมไฮโดรเจน ในโมเลกุลอะลานีน - CH เป็นต้นพันธะเคมี (- CO -
NH -) เชื่อมหมู่อะมิโนของกรดอะมิโนหนึ่งกับหมู่คาร์บอกซิลของอีกกลุ่มหนึ่งในโมเลกุลโปรตีนเรียกว่า พันธะเปปไทด์(ดูรูปที่ 7.5)
สิ่งมีชีวิตที่ทำงานอยู่ทั้งหมด ไม่ว่าจะเป็นพืช สัตว์ แบคทีเรีย หรือไวรัส มีโปรตีนที่สร้างจากกรดอะมิโนตัวเดียวกัน ดังนั้นอาหารทุกประเภทจึงมีกรดอะมิโนเหมือนกันซึ่งเป็นส่วนหนึ่งของโปรตีนของสิ่งมีชีวิตที่กินอาหาร
คำจำกัดความ "โปรตีนเป็นโพลีเมอร์ที่สร้างขึ้นจากกรดอะมิโน 20 ชนิด" มีลักษณะเฉพาะของโปรตีนที่ไม่สมบูรณ์ ภายใต้สภาวะของห้องปฏิบัติการ การหาพันธะเปปไทด์ในสารละลายของกรดอะมิโนนั้นไม่ใช่เรื่องยาก ดังนั้นจึงเกิดเป็นสายโมเลกุลยาว อย่างไรก็ตาม ในสายโซ่ดังกล่าว การจัดเรียงของกรดอะมิโนจะไม่เป็นระเบียบ และโมเลกุลที่ได้จะแตกต่างกัน ในเวลาเดียวกัน ในโปรตีนธรรมชาติแต่ละชนิด การจัดเรียงกรดอะมิโนแต่ละชนิดจะเหมือนกันเสมอ และนี่หมายความว่าในระหว่างการสังเคราะห์โปรตีนในระบบที่มีชีวิต ข้อมูลจะถูกใช้ ซึ่งสอดคล้องกับลำดับกรดอะมิโนที่กำหนดไว้อย่างดีสำหรับโปรตีนแต่ละชนิด
ลำดับของกรดอะมิโนในโปรตีนเป็นตัวกำหนดโครงสร้างเชิงพื้นที่ โปรตีนส่วนใหญ่ทำหน้าที่เป็นตัวเร่งปฏิกิริยา ในโครงสร้างเชิงพื้นที่มีจุดศูนย์กลางในรูปแบบของความกดอากาศที่มีรูปร่างที่กำหนดไว้อย่างดี โมเลกุลซึ่งการเปลี่ยนแปลงซึ่งถูกกระตุ้นโดยโปรตีนนี้เข้าสู่ศูนย์กลางดังกล่าว โปรตีนซึ่งในกรณีนี้ทำหน้าที่เป็นเอนไซม์ สามารถกระตุ้นปฏิกิริยาได้ก็ต่อเมื่อรูปร่างของโมเลกุลที่เปลี่ยนรูปและศูนย์กลางที่แอคทีฟตรงกัน สิ่งนี้เป็นตัวกำหนดความสามารถในการคัดเลือกโปรตีนเอนไซม์สูง
ศูนย์กลางที่แอคทีฟของเอ็นไซม์สามารถเกิดขึ้นได้จากการพับส่วนของสายโซ่โปรตีนที่อยู่ไกลกันมาก ดังนั้นการแทนที่กรดอะมิโนตัวหนึ่งเป็นอีกตัวหนึ่ง แม้จะอยู่ห่างจากจุดออกฤทธิ์เพียงเล็กน้อย ก็อาจส่งผลต่อการคัดเลือกของเอนไซม์หรือทำลายไซต์ทั้งหมดได้ ด้วยการสร้างลำดับกรดอะมิโนที่แตกต่างกัน คุณจะได้รับศูนย์แอคทีฟที่หลากหลาย นี่เป็นหนึ่งในคุณสมบัติที่สำคัญที่สุดของโปรตีนที่ทำหน้าที่เป็นเอนไซม์
เนื้อหาของบทความ
โปรตีน (ข้อ 1)- กลุ่มของโพลิเมอร์ชีวภาพที่มีอยู่ในทุกสิ่งมีชีวิต ด้วยการมีส่วนร่วมของโปรตีน กระบวนการหลักที่รับรองกิจกรรมที่สำคัญของร่างกายเกิดขึ้น: การหายใจ การย่อยอาหาร การหดตัวของกล้ามเนื้อ การส่งกระแสประสาท การก่อตัวของเนื้อเยื่อกระดูก ผิวหนัง ผม เขาของสิ่งมีชีวิตประกอบด้วยโปรตีน สำหรับสัตว์เลี้ยงลูกด้วยนมส่วนใหญ่ การเจริญเติบโตและการพัฒนาของสิ่งมีชีวิตเกิดขึ้นเนื่องจากผลิตภัณฑ์ที่มีโปรตีนเป็นส่วนประกอบอาหาร บทบาทของโปรตีนในร่างกายและโครงสร้างจึงมีความหลากหลายมาก
องค์ประกอบของโปรตีน
โปรตีนทั้งหมดเป็นโพลีเมอร์ซึ่งเป็นสายโซ่ที่ประกอบขึ้นจากชิ้นส่วนของกรดอะมิโน กรดอะมิโนเป็นสารประกอบอินทรีย์ที่ประกอบด้วยหมู่อะมิโน NH 2 และกรดอินทรีย์ในองค์ประกอบ (ตามชื่อ) คาร์บอกซิล กลุ่ม COOH จากความหลากหลายของกรดอะมิโนที่มีอยู่ทั้งหมด (ตามหลักวิชา จำนวนกรดอะมิโนที่เป็นไปได้นั้นไม่จำกัด) เฉพาะกรดอะมิโนที่มีอะตอมของคาร์บอนเพียงอะตอมเดียวระหว่างกลุ่มอะมิโนและกลุ่มคาร์บอกซิลเท่านั้นที่มีส่วนร่วมในการก่อตัวของโปรตีน โดยทั่วไป กรดอะมิโนที่เกี่ยวข้องกับการก่อตัวของโปรตีนสามารถแสดงแทนด้วยสูตร: H 2 N–CH(R)–COOH กลุ่ม R ที่ติดอยู่กับอะตอมของคาร์บอน (กลุ่มหนึ่งระหว่างกลุ่มอะมิโนและคาร์บอกซิล) กำหนดความแตกต่างระหว่างกรดอะมิโนที่ประกอบเป็นโปรตีน กลุ่มนี้สามารถประกอบด้วยอะตอมของคาร์บอนและไฮโดรเจนเท่านั้น แต่มักประกอบด้วยกลุ่มการทำงานต่างๆ (สามารถแปลงเพิ่มเติม) นอกเหนือจาก C และ H ได้ เช่น H2O- H 2 N- เป็นต้น นอกจากนี้ยังมี ตัวเลือกเมื่อ R \u003d H.
สิ่งมีชีวิตของสิ่งมีชีวิตประกอบด้วยกรดอะมิโนที่แตกต่างกันมากกว่า 100 ชนิด อย่างไรก็ตาม ไม่ใช่ทั้งหมดที่ใช้ในการสร้างโปรตีน แต่มีเพียง 20 ชนิดเท่านั้นที่เรียกว่า "พื้นฐาน" ในตาราง. 1 แสดงชื่อ (ชื่อส่วนใหญ่มีการพัฒนาตามประวัติศาสตร์) สูตรโครงสร้าง และคำย่อที่ใช้กันอย่างแพร่หลาย สูตรโครงสร้างทั้งหมดถูกจัดเรียงในตารางเพื่อให้ส่วนหลักของกรดอะมิโนอยู่ทางด้านขวา
| ชื่อ | โครงสร้าง | การกำหนด |
| ไกลซีน | GLI | |
| อะลานิน | อะลา | |
| วาลิน | เพลา | |
| ลูซิเน่ | LEI | |
| ISOLEUCINE | ILE | |
| SERIN | SER | |
| ทรีโอนีน | TRE | |
| CYSTEINE | CIS | |
| เมทิโอนีน | MET | |
| ไลซีน | ลิซ | |
| อาร์จินีน | ARG | |
| กรดแอสพาราจิก | ASN | |
| แอสพาราจิน | ASN | |
| กรดกลูตามิก | GLU | |
| กลูตามีน | GLN | |
| ฟีนิลอะลานีน | เครื่องเป่าผม | |
| ไทโรซีน | TIR | |
| ทริปโตเฟน | สาม | |
| ฮิสติดีน | GIS | |
| PROLINE | มือโปร | |
| ในทางปฏิบัติระหว่างประเทศ การกำหนดชื่อย่อของกรดอะมิโนที่อยู่ในรายการโดยใช้ตัวย่อสามตัวอักษรละตินหรือตัวย่อหนึ่งตัวอักษรภาษาละตินเป็นที่ยอมรับ เช่น ไกลซีน - Gly หรือ G อะลานีน - Ala หรือ A | ||
ในบรรดากรดอะมิโน 20 ชนิด (ตารางที่ 1) มีเพียงโพรลีนเท่านั้นที่มีหมู่ NH (แทนที่จะเป็น NH 2) ถัดจากกลุ่มคาร์บอกซิลของ COOH เนื่องจากเป็นส่วนหนึ่งของไซคลิก
กรดอะมิโนแปดตัว (วาลีน, ลิวซีน, ไอโซลิวซีน, ธรีโอนีน, เมไทโอนีน, ไลซีน, ฟีนิลอะลานีนและทริปโตเฟน) ถูกเรียกวางไว้บนโต๊ะบนพื้นหลังสีเทา เนื่องจากร่างกายต้องได้รับอาหารโปรตีนอย่างต่อเนื่องเพื่อการเจริญเติบโตและพัฒนาการตามปกติ
โมเลกุลโปรตีนเกิดขึ้นจากการเชื่อมต่อตามลำดับของกรดอะมิโนในขณะที่กลุ่มคาร์บอกซิลของกรดหนึ่งมีปฏิสัมพันธ์กับกลุ่มอะมิโนของโมเลกุลที่อยู่ใกล้เคียง เป็นผลให้เกิดพันธะ –CO–NH– เปปไทด์และน้ำ โมเลกุลจะถูกปล่อยออกมา ในรูป 1 แสดงการเชื่อมต่อแบบอนุกรมของอะลานีน วาลีน และไกลซีน
ข้าว. หนึ่ง การเชื่อมต่อแบบอนุกรมของกรดอะมิโนในระหว่างการก่อตัวของโมเลกุลโปรตีน เส้นทางจากขั้วอะมิโนกลุ่ม H 2 N ไปยังขั้วกลุ่มคาร์บอกซิล COOH ได้รับเลือกให้เป็นทิศทางหลักของสายโซ่โพลีเมอร์
เพื่ออธิบายโครงสร้างของโมเลกุลโปรตีนอย่างกระชับ จะใช้ตัวย่อของกรดอะมิโน (ตารางที่ 1 คอลัมน์ที่สาม) ที่เกี่ยวข้องกับการก่อตัวของสายโซ่โพลีเมอร์ ชิ้นส่วนของโมเลกุลที่แสดงในรูปที่ 1 เขียนดังนี้: H 2 N-ALA-VAL-GLY-COOH
โมเลกุลของโปรตีนประกอบด้วยกรดอะมิโนตกค้าง 50 ถึง 1500 ตัว (สายที่สั้นกว่าเรียกว่าพอลิเปปไทด์) ลักษณะเฉพาะของโปรตีนถูกกำหนดโดยชุดของกรดอะมิโนที่ประกอบเป็นสายโซ่โพลีเมอร์ และที่สำคัญไม่น้อยไปกว่านั้น โดยลำดับของการสลับกันไปตามสายโซ่ ตัวอย่างเช่น โมเลกุลอินซูลินประกอบด้วยกรดอะมิโนตกค้าง 51 ชนิด (เป็นโปรตีนสายโซ่ที่สั้นที่สุดชนิดหนึ่ง) และประกอบด้วยสายโซ่คู่ขนานที่เชื่อมต่อถึงกันสองสายซึ่งมีความยาวไม่เท่ากัน ลำดับของชิ้นส่วนกรดอะมิโนแสดงไว้ในรูปที่ 2.
ข้าว. 2 โมเลกุลอินซูลินสร้างขึ้นจากสารตกค้างของกรดอะมิโน 51 ชนิด ชิ้นส่วนของกรดอะมิโนชนิดเดียวกันจะถูกทำเครื่องหมายด้วยสีพื้นหลังที่สอดคล้องกัน สารตกค้างของกรดอะมิโนซิสเทอีน (ชื่อย่อ CIS) ที่มีอยู่ในสะพานไดซัลไฟด์รูปลูกโซ่ -S-S- ซึ่งเชื่อมโยงโมเลกุลโพลีเมอร์สองโมเลกุลหรือสร้างจัมเปอร์ภายในสายเดียว
โมเลกุลของกรดอะมิโนซิสเทอีน (ตารางที่ 1) ประกอบด้วยกลุ่มซัลไฟด์ปฏิกิริยา -SH ซึ่งมีปฏิสัมพันธ์ซึ่งกันและกันทำให้เกิดสะพานไดซัลไฟด์ -S-S- บทบาทของซิสเทอีนในโลกของโปรตีนนั้นพิเศษด้วยการมีส่วนร่วมของมันทำให้เกิดการเชื่อมโยงข้ามระหว่างโมเลกุลโปรตีนโพลีเมอร์
การเชื่อมโยงของกรดอะมิโนเข้ากับสายโซ่พอลิเมอร์เกิดขึ้นในสิ่งมีชีวิตภายใต้การควบคุมของกรดนิวคลีอิกซึ่งให้ลำดับการประกอบที่เข้มงวดและควบคุมความยาวคงที่ของโมเลกุลพอลิเมอร์ ( ซม. กรดนิวคลีอิก).
โครงสร้างของโปรตีน
องค์ประกอบของโมเลกุลโปรตีนที่นำเสนอในรูปแบบของการตกค้างของกรดอะมิโน (รูปที่ 2) เรียกว่าโครงสร้างหลักของโปรตีน พันธะไฮโดรเจนเกิดขึ้นระหว่างหมู่อิมิโน HN ที่มีอยู่ในสายพอลิเมอร์และหมู่คาร์บอนิล CO ( ซม. HYDROGEN BOND) เป็นผลให้โมเลกุลของโปรตีนได้รับรูปร่างเชิงพื้นที่ที่เรียกว่าโครงสร้างทุติยภูมิ ที่พบมากที่สุดคือโครงสร้างรองสองประเภทในโปรตีน
ตัวเลือกแรกที่เรียกว่า α-helix ถูกนำมาใช้โดยใช้พันธะไฮโดรเจนภายในโมเลกุลพอลิเมอร์หนึ่งโมเลกุล พารามิเตอร์ทางเรขาคณิตของโมเลกุลซึ่งกำหนดโดยความยาวของพันธะและมุมของพันธะนั้นทำให้การก่อตัวของพันธะไฮโดรเจนเป็นไปได้สำหรับกลุ่ม HN และ C=O ซึ่งมีเปปไทด์สองชิ้น H-N-C=O (รูปที่ 3) .
องค์ประกอบของสายโพลีเปปไทด์ที่แสดงในรูปที่ 3 เขียนในรูปแบบย่อดังนี้:
H 2 N-ALA VAL-ALA-LEY-ALA-ALA-ALA-ALA-VAL-ALA-ALA-ALA-COOH.
อันเป็นผลมาจากการหดตัวของพันธะไฮโดรเจน โมเลกุลจึงอยู่ในรูปของเกลียว - ที่เรียกว่า α-helix ซึ่งแสดงเป็นริบบิ้นเกลียวโค้งที่เคลื่อนผ่านอะตอมที่สร้างสายโซ่พอลิเมอร์ (รูปที่ 4)
ข้าว. สี่ โมเดล 3 มิติของโมเลกุลโปรตีนในรูปของเกลียว α พันธะไฮโดรเจนจะแสดงเป็นเส้นประสีเขียว รูปทรงกระบอกของเกลียวสามารถมองเห็นได้ในมุมการหมุนที่แน่นอน (ไม่แสดงอะตอมไฮโดรเจนในรูป) สีของอะตอมแต่ละอะตอมถูกกำหนดตามกฎสากล ซึ่งแนะนำสีดำสำหรับอะตอมคาร์บอน สีฟ้าสำหรับไนโตรเจน สีแดงสำหรับออกซิเจน และสีเหลืองสำหรับกำมะถัน (แนะนำให้ใช้สีขาวสำหรับอะตอมไฮโดรเจนที่ไม่แสดงในภาพ ในกรณีนี้ โครงสร้างทั้งหมดแสดงบนพื้นหลังสีเข้ม)
โครงสร้างรองอีกรูปแบบหนึ่งที่เรียกว่าโครงสร้าง β ยังเกิดขึ้นได้ด้วยการมีส่วนร่วมของพันธะไฮโดรเจน ความแตกต่างก็คือกลุ่ม H-N และ C=O ของสายโซ่โพลีเมอร์สองสายหรือมากกว่านั้นอยู่ในปฏิสัมพันธ์แบบคู่ขนาน เนื่องจากสายโซ่โพลีเปปไทด์มีทิศทาง (รูปที่ 1) ตัวแปรจึงเป็นไปได้เมื่อทิศทางของโซ่เหมือนกัน (โครงสร้าง β แบบขนาน รูปที่ 5) หรืออยู่ตรงข้าม (โครงสร้าง β ที่ต้านขนานกัน รูปที่ 6) .
โซ่โพลีเมอร์ขององค์ประกอบต่าง ๆ สามารถมีส่วนร่วมในการก่อตัวของโครงสร้าง β ในขณะที่กลุ่มอินทรีย์ที่อยู่ในกรอบของสายโซ่โพลีเมอร์ (Ph, CH 2 OH เป็นต้น) ในกรณีส่วนใหญ่มีบทบาทรอง การจัดเรียงร่วมกันของ HN และ C =กลุ่ม O เด็ดขาด เนื่องจากกลุ่ม HN และ C=O ถูกชี้นำในทิศทางที่ต่างกันเมื่อเทียบกับสายโซ่โพลีเมอร์ (ขึ้นและลงในรูป) จึงเป็นไปได้ที่สายโซ่ตั้งแต่สามสายขึ้นไปจะมีปฏิสัมพันธ์พร้อมกัน
องค์ประกอบของสายโซ่โพลีเปปไทด์แรกในรูปที่ 5:
H 2 N-LEI-ALA-FEN-GLI-ALA-ALA-COOH
องค์ประกอบของสายโซ่ที่สองและสาม:
H 2 N-GLY-ALA-SER-GLY-TRE-ALA-COOH
องค์ประกอบของสายโพลีเปปไทด์ที่แสดงในรูปที่ 6 เหมือนในรูป 5 ข้อแตกต่างคือโซ่ที่สองมีทิศทางตรงกันข้าม (เทียบกับรูปที่ 5)
เป็นไปได้ที่จะสร้างโครงสร้าง β ภายในโมเลกุลเดียว เมื่อชิ้นส่วนลูกโซ่ในส่วนใดส่วนหนึ่งหมุนได้ 180° ในกรณีนี้ กิ่งสองกิ่งของโมเลกุลหนึ่งมีทิศทางตรงกันข้าม อันเป็นผลให้มีลักษณะตรงกันข้าม โครงสร้าง β ถูกสร้างขึ้น (รูปที่ 7)
โครงสร้างที่แสดงในรูปที่ 7 ในภาพแบนแสดงในรูปที่ 8 ในรูปแบบของแบบจำลองสามมิติ ส่วนของโครงสร้าง β มักจะแสดงในลักษณะที่ง่ายขึ้นด้วยริบบิ้นหยักแบนที่ไหลผ่านอะตอมที่ก่อตัวเป็นสายโซ่โพลีเมอร์
ในโครงสร้างของโปรตีนหลายชนิด ส่วนของ α-helix และโครงสร้าง β ที่คล้ายริบบิ้นจะสลับกัน เช่นเดียวกับสายโซ่โพลีเปปไทด์เดี่ยว การจัดเรียงและการสลับกันของพวกมันในสายโซ่โพลีเมอร์เรียกว่าโครงสร้างระดับอุดมศึกษาของโปรตีน
วิธีการแสดงโครงสร้างของโปรตีนแสดงไว้ด้านล่างโดยใช้ตัวอย่างโปรตีนจากพืช สูตรโครงสร้างของโปรตีนซึ่งมักประกอบด้วยชิ้นส่วนของกรดอะมิโนหลายร้อยชิ้น มีความซับซ้อน ยุ่งยาก และเข้าใจยาก ดังนั้นบางครั้งจึงใช้สูตรโครงสร้างแบบง่าย - โดยไม่มีสัญลักษณ์ขององค์ประกอบทางเคมี (รูปที่ 9 ตัวเลือก A) แต่ในขณะเดียวกัน เวลาที่พวกเขารักษาสีของจังหวะวาเลนซ์ตามกฎสากล (รูปที่ 4) ในกรณีนี้ สูตรจะไม่ถูกนำเสนอในลักษณะแบนราบ แต่เป็นภาพเชิงพื้นที่ซึ่งสอดคล้องกับโครงสร้างที่แท้จริงของโมเลกุล วิธีนี้ทำให้สามารถแยกแยะความแตกต่างระหว่างไดซัลไฟด์บริดจ์ (คล้ายกับที่พบในอินซูลิน, รูปที่ 2), กลุ่มฟีนิลในกรอบด้านข้างของโซ่ ฯลฯ ภาพของโมเลกุลในรูปแบบสามมิติ โมเดล (ลูกที่เชื่อมต่อด้วยแท่ง) ค่อนข้างชัดเจน (รูปที่ 9 ตัวเลือก B) อย่างไรก็ตาม ทั้งสองวิธีไม่อนุญาตให้แสดงโครงสร้างตติยภูมิ ดังนั้น Jane Richardson นักชีวฟิสิกส์ชาวอเมริกันจึงเสนอให้พรรณนาโครงสร้าง α เป็นริบบิ้นบิดเป็นเกลียว (ดูรูปที่ 4) โครงสร้าง β เป็นริบบิ้นหยักแบน (รูปที่ 8) และการเชื่อมต่อ โซ่เดี่ยว - ในรูปแบบของมัดบาง ๆ โครงสร้างแต่ละประเภทมีสีของตัวเอง วิธีการแสดงโครงสร้างระดับตติยภูมิของโปรตีนนี้ใช้กันอย่างแพร่หลายในปัจจุบัน (รูปที่ 9 ตัวแปร B) บางครั้ง สำหรับเนื้อหาข้อมูลที่มากขึ้น โครงสร้างระดับอุดมศึกษาและสูตรโครงสร้างแบบง่ายจะแสดงร่วมกัน (รูปที่ 9 ตัวแปร D) นอกจากนี้ยังมีการปรับเปลี่ยนวิธีการที่เสนอโดย Richardson: α-helices ถูกวาดเป็นทรงกระบอกและโครงสร้างβอยู่ในรูปของลูกศรแบนที่ระบุทิศทางของห่วงโซ่ (รูปที่ 9 ตัวเลือก E) วิธีที่พบได้น้อยกว่าคือวิธีการที่โมเลกุลทั้งหมดถูกวาดเป็นมัด ซึ่งโครงสร้างที่ไม่เท่ากันนั้นโดดเด่นด้วยสีที่ต่างกัน และสะพานไดซัลไฟด์จะแสดงเป็นสะพานสีเหลือง (รูปที่ 9 ตัวแปร E)
ตัวเลือก B เป็นวิธีที่สะดวกที่สุดสำหรับการรับรู้เมื่อไม่ได้ระบุลักษณะโครงสร้างของโปรตีน (ชิ้นส่วนของกรดอะมิโน, ลำดับการสลับ, พันธะไฮโดรเจน) เมื่อแสดงโครงสร้างระดับตติยภูมิในขณะที่สันนิษฐานว่าโปรตีนทั้งหมดมี "รายละเอียด" นำมาจากชุดมาตรฐานของกรดอะมิโน 20 ชนิด ( ตารางที่ 1) งานหลักในการวาดภาพโครงสร้างระดับอุดมศึกษาคือการแสดงการจัดเรียงเชิงพื้นที่และการสลับโครงสร้างรอง
ข้าว. 9 รุ่นต่างๆ ของภาพโครงสร้างของโปรตีน CRUMBIN.
A เป็นสูตรโครงสร้างในรูปเชิงพื้นที่
B - โครงสร้างในรูปแบบของแบบจำลองสามมิติ
B คือโครงสร้างระดับอุดมศึกษาของโมเลกุล
G - การรวมกันของตัวเลือก A และ B
E - ภาพที่ง่ายขึ้นของโครงสร้างระดับอุดมศึกษา
E - โครงสร้างตติยภูมิพร้อมสะพานไดซัลไฟด์
วิธีที่สะดวกที่สุดสำหรับการรับรู้คือโครงสร้างตติยภูมิสามมิติ (ตัวเลือก B) ที่ปราศจากรายละเอียดของสูตรโครงสร้าง
โมเลกุลโปรตีนที่มีโครงสร้างระดับตติยภูมิตามกฎแล้วจะมีการกำหนดค่าบางอย่างซึ่งเกิดขึ้นจากปฏิกิริยาเชิงขั้ว (ไฟฟ้าสถิต) และพันธะไฮโดรเจน เป็นผลให้โมเลกุลอยู่ในรูปของขดลวดขนาดกะทัดรัด - โปรตีนทรงกลม (ทรงกลม, lat. ลูก) หรือเส้นใย - โปรตีนไฟบริล (fibra, lat. ไฟเบอร์)
ตัวอย่างของโครงสร้างทรงกลมคือโปรตีนอัลบูมิน โปรตีนของไข่ไก่อยู่ในกลุ่มของอัลบูมิน โซ่โพลีเมอร์ของอัลบูมินส่วนใหญ่ประกอบขึ้นจากอะลานีน กรดแอสปาร์ติก ไกลซีน และซิสเทอีน สลับกันในลำดับที่แน่นอน โครงสร้างตติยภูมิประกอบด้วย α-helices ที่เชื่อมต่อกันด้วยโซ่เดี่ยว (รูปที่ 10)
ข้าว. สิบ โครงสร้างระดับโลกของ ALBUMIN
ตัวอย่างของโครงสร้างไฟบริลคือโปรตีนไฟโบรอิน ประกอบด้วยไกลซีน, อะลานีนและซีรีนตกค้างจำนวนมาก (ทุกวินาทีของกรดอะมิโนคือไกลซีน); ซิสเทอีนตกค้างที่มีกลุ่มซัลไฟด์ขาดหายไป ไฟโบรอินซึ่งเป็นส่วนประกอบหลักของไหมธรรมชาติและใยแมงมุม ประกอบด้วยโครงสร้าง β ที่เชื่อมต่อกันด้วยโซ่เดี่ยว (รูปที่ 11)
ข้าว. สิบเอ็ด FIBRILLARY โปรตีน FIBROIN
ความเป็นไปได้ในการสร้างโครงสร้างระดับอุดมศึกษาของบางชนิดนั้นมีอยู่ในโครงสร้างหลักของโปรตีนนั่นคือ กำหนดล่วงหน้าโดยลำดับการสลับของกรดอะมิโนตกค้าง จากชุดของสารตกค้างบางชุด α-helices ส่วนใหญ่เกิดขึ้น (มีชุดดังกล่าวค่อนข้างมาก) ชุดอื่นนำไปสู่การปรากฏตัวของโครงสร้าง β โซ่เดี่ยวมีลักษณะโดยองค์ประกอบ
โมเลกุลโปรตีนบางชนิด ในขณะที่ยังคงโครงสร้างระดับตติยภูมิไว้ สามารถรวมกันเป็นมวลรวมซุปเปอร์โมเลกุลขนาดใหญ่ ในขณะที่พวกมันถูกยึดเข้าด้วยกันโดยปฏิกิริยาเชิงขั้ว เช่นเดียวกับพันธะไฮโดรเจน การก่อตัวดังกล่าวเรียกว่าโครงสร้างควอเทอร์นารีของโปรตีน ตัวอย่างเช่น โปรตีนเฟอร์ริติน ซึ่งส่วนใหญ่ประกอบด้วยลิวซีน กรดกลูตามิก กรดแอสปาร์ติก และฮิสทิดีน (เฟอริซินมีกรดอะมิโนตกค้างทั้งหมด 20 ชนิดในปริมาณที่แตกต่างกัน) ก่อให้เกิดโครงสร้างระดับอุดมศึกษาของ α-helices ที่วางขนานกันสี่ตัว เมื่อโมเลกุลรวมกันเป็นชุดเดียว (รูปที่ 12) จะเกิดโครงสร้างควอเทอร์นารี ซึ่งสามารถรวมโมเลกุลเฟอร์ริตินได้มากถึง 24 โมเลกุล
รูปที่ 12 การก่อตัวของโครงสร้างควอเทอร์นารีของโกลบอลโปรตีนเฟอริติน
อีกตัวอย่างหนึ่งของการก่อตัวของซุปเปอร์โมเลกุลคือโครงสร้างของคอลลาเจน เป็นโปรตีนไฟบริลลาร์ซึ่งมีสายโซ่หลักเป็นไกลซีนสลับกับโพรลีนและไลซีน โครงสร้างประกอบด้วยโซ่เดี่ยว α-helices สามตัว สลับกับโครงสร้าง β คล้ายริบบิ้นที่ซ้อนกันเป็นมัดแบบขนาน (รูปที่ 13)
รูปที่ 13 โครงสร้างระดับโมเลกุลของคอลลาเจนไฟบริลลารีโปรตีน
คุณสมบัติทางเคมีของโปรตีน
ภายใต้การกระทำของตัวทำละลายอินทรีย์ ของเสียจากแบคทีเรียบางชนิด (การหมักกรดแลคติก) หรืออุณหภูมิที่เพิ่มขึ้น โครงสร้างทุติยภูมิและตติยภูมิถูกทำลายโดยไม่ทำลายโครงสร้างหลัก ส่งผลให้โปรตีนสูญเสียความสามารถในการละลายและสูญเสียกิจกรรมทางชีวภาพ กระบวนการที่เรียกว่า denaturation นั่นคือการสูญเสียคุณสมบัติทางธรรมชาติเช่นการทำให้นมเปรี้ยวทำให้เป็นก้อนโปรตีนจับตัวเป็นก้อนของไข่ไก่ต้ม ที่อุณหภูมิสูง โปรตีนของสิ่งมีชีวิต (โดยเฉพาะจุลินทรีย์) จะเสื่อมสภาพอย่างรวดเร็ว โปรตีนดังกล่าวไม่สามารถมีส่วนร่วมในกระบวนการทางชีวภาพ ส่งผลให้จุลินทรีย์ตาย จึงสามารถเก็บนมต้ม (หรือพาสเจอร์ไรส์) ได้นานขึ้น
พันธะเปปไทด์ H-N-C=O ก่อตัวเป็นสายโซ่พอลิเมอร์ของโมเลกุลโปรตีน ถูกไฮโดรไลซ์เมื่อมีกรดหรือด่าง และสายโซ่โพลีเมอร์จะแตกออก ซึ่งท้ายที่สุดจะนำไปสู่กรดอะมิโนดั้งเดิมได้ พันธะเปปไทด์ที่รวมอยู่ใน α-helices หรือโครงสร้าง β มีความทนทานต่อการไฮโดรไลซิสและการโจมตีทางเคมีต่างๆ มากกว่า (เมื่อเทียบกับพันธะเดียวกันในสายโซ่เดี่ยว) การแยกชิ้นส่วนของโมเลกุลโปรตีนที่ละเอียดอ่อนยิ่งขึ้นไปเป็นกรดอะมิโนที่เป็นส่วนประกอบนั้นจะดำเนินการในตัวกลางที่ปราศจากน้ำโดยใช้ไฮดราซีน H 2 N–NH 2 ในขณะที่ชิ้นส่วนกรดอะมิโนทั้งหมด ยกเว้นชิ้นสุดท้าย ก่อให้เกิดสิ่งที่เรียกว่ากรดคาร์บอกซิลิกไฮดราไซด์ที่มี ส่วน C (O)–HN–NH 2 ( รูปที่ 14)
ข้าว. สิบสี่ โพลิเปปไทด์แตกแยก
การวิเคราะห์ดังกล่าวสามารถให้ข้อมูลเกี่ยวกับองค์ประกอบกรดอะมิโนของโปรตีน แต่สิ่งสำคัญกว่าคือต้องทราบลำดับของพวกมันในโมเลกุลโปรตีน วิธีหนึ่งที่ใช้กันอย่างแพร่หลายเพื่อจุดประสงค์นี้คือการกระทำของ phenylisothiocyanate (FITC) บนสายโซ่โพลีเปปไทด์ ซึ่งในตัวกลางที่เป็นด่างจะเกาะติดกับพอลิเปปไทด์ (จากปลายที่มีหมู่อะมิโน) และเมื่อปฏิกิริยาของตัวกลางเปลี่ยนไป เป็นกรด มันจะหลุดออกจากสายโซ่ นำชิ้นส่วนของกรดอะมิโนหนึ่งตัวไปด้วย (รูปที่ 15)
ข้าว. สิบห้า ความแตกแยกของโพลิเปปไทด์ตามลำดับ
มีการพัฒนาวิธีการพิเศษมากมายสำหรับการวิเคราะห์ดังกล่าว รวมถึงวิธีการต่างๆ ที่เริ่ม "แยกส่วนประกอบ" ของโมเลกุลโปรตีนออกเป็นส่วนประกอบต่างๆ โดยเริ่มจากส่วนปลายของคาร์บอกซิล
สะพานข้ามไดซัลไฟด์ SS (เกิดขึ้นจากปฏิกิริยาของซิสเทอีนตกค้าง รูปที่ 2 และ 9) ถูกแยกออก ทำให้กลายเป็นกลุ่ม HS โดยการกระทำของสารรีดิวซ์ต่างๆ การกระทำของสารออกซิไดซ์ (ออกซิเจนหรือไฮโดรเจนเปอร์ออกไซด์) นำไปสู่การก่อตัวของสะพานไดซัลไฟด์อีกครั้ง (รูปที่ 16)
ข้าว. 16. ความแตกแยกของสะพานไดซัลไฟด์
ในการสร้างการเชื่อมโยงข้ามเพิ่มเติมในโปรตีนจะใช้ปฏิกิริยาของหมู่อะมิโนและคาร์บอกซิล สามารถเข้าถึงได้มากขึ้นสำหรับปฏิสัมพันธ์ที่หลากหลายคือหมู่อะมิโนที่อยู่ในกรอบด้านข้างของสายโซ่ - ชิ้นส่วนของไลซีน, แอสปาราจีน, ไลซีน, โพรลีน (ตารางที่ 1) เมื่อหมู่อะมิโนดังกล่าวมีปฏิกิริยากับฟอร์มาลดีไฮด์ กระบวนการของการควบแน่นจะเกิดขึ้นและสะพานข้าม –NH–CH2–NH– ปรากฏขึ้น (รูปที่ 17)
ข้าว. 17 การสร้างสะพานข้ามขวางเพิ่มเติมระหว่างโมเลกุลโปรตีน.
โปรตีนกลุ่มขั้วคาร์บอกซิลสามารถทำปฏิกิริยากับสารประกอบเชิงซ้อนของโลหะพอลิวาเลนต์บางชนิดได้ (มักใช้สารประกอบโครเมียมมากกว่า) และการเกิดพันธะขวางก็เกิดขึ้นเช่นกัน กระบวนการทั้งสองนี้ใช้ในการฟอกหนัง
บทบาทของโปรตีนในร่างกาย
บทบาทของโปรตีนในร่างกายมีความหลากหลาย
เอนไซม์(การหมัก lat. - การหมัก) อีกชื่อหนึ่งคือ เอ็นไซม์ (en zumh กรีก. - ในยีสต์) - เหล่านี้เป็นโปรตีนที่มีฤทธิ์เร่งปฏิกิริยา สามารถเพิ่มความเร็วของกระบวนการทางชีวเคมีได้หลายพันครั้ง ภายใต้การกระทำของเอ็นไซม์ ส่วนประกอบที่เป็นส่วนประกอบของอาหาร ได้แก่ โปรตีน ไขมัน และคาร์โบไฮเดรตจะถูกแยกย่อยเป็นสารประกอบที่ง่ายกว่า จากนั้นจึงสังเคราะห์โมเลกุลขนาดใหญ่ขึ้นใหม่ ซึ่งจำเป็นสำหรับร่างกายบางประเภท เอนไซม์ยังมีส่วนร่วมในกระบวนการสังเคราะห์ทางชีวเคมีหลายอย่าง เช่น ในการสังเคราะห์โปรตีน (โปรตีนบางชนิดช่วยในการสังเคราะห์โปรตีนอื่นๆ) ซม. เอนไซม์
เอ็นไซม์ไม่เพียงแต่เป็นตัวเร่งปฏิกิริยาที่มีประสิทธิภาพสูงเท่านั้น แต่ยังรวมถึงการคัดเลือกด้วย (ควบคุมปฏิกิริยาอย่างเคร่งครัดในทิศทางที่กำหนด) ปฏิกิริยาเกิดขึ้นได้เกือบ 100% โดยปราศจากการก่อตัวของผลพลอยได้ และในขณะเดียวกัน สภาพการไหลก็ไม่รุนแรง นั่นคือ ความดันบรรยากาศปกติและอุณหภูมิของสิ่งมีชีวิต สำหรับการเปรียบเทียบ การสังเคราะห์แอมโมเนียจากไฮโดรเจนและไนโตรเจนต่อหน้าตัวเร่งปฏิกิริยาเหล็กกระตุ้นจะดำเนินการที่ 400–5000°C และความดัน 30 MPa ผลผลิตของแอมโมเนียอยู่ที่ 15–25% ต่อรอบ เอนไซม์ถือเป็นตัวเร่งปฏิกิริยาที่ไม่มีใครเทียบได้
การศึกษาเอนไซม์อย่างเข้มข้นเริ่มขึ้นในกลางศตวรรษที่ 19 ขณะนี้มีการศึกษาเอนไซม์ต่างๆ มากกว่า 2,000 ชนิด ซึ่งเป็นโปรตีนประเภทที่มีความหลากหลายมากที่สุด
ชื่อของเอ็นไซม์มีดังนี้: ชื่อของรีเอเจนต์ที่เอ็นไซม์โต้ตอบหรือชื่อของปฏิกิริยาเร่งปฏิกิริยา ถูกเติมด้วยตอนจบ -aza เช่น อาร์จิเนสสลายอาร์จินีน (ตารางที่ 1), decarboxylase catalyzes decarboxylation เช่น. การกำจัด CO 2 ออกจากกลุ่มคาร์บอกซิล:
– COOH → – CH + CO 2
บ่อยครั้ง เพื่อให้ระบุบทบาทของเอนไซม์ได้แม่นยำยิ่งขึ้น ทั้งวัตถุและประเภทของปฏิกิริยาจะถูกระบุในชื่อของมัน ตัวอย่างเช่น แอลกอฮอล์ดีไฮโดรจีเนสเป็นเอนไซม์ที่ทำให้ดีไฮโดรจีเนตแอลกอฮอล์
สำหรับเอ็นไซม์บางตัวที่ค้นพบเมื่อนานมาแล้ว ชื่อทางประวัติศาสตร์ (โดยไม่ลงท้ายด้วย -aza) ก็ถูกรักษาไว้ เช่น เปปซิน (เป๊ปซี่ กรีก. การย่อยอาหาร) และทริปซิน (thrypsis กรีก. การทำให้เหลว) เอ็นไซม์เหล่านี้จะสลายโปรตีน
สำหรับการจัดระบบ เอ็นไซม์จะถูกรวมเป็นคลาสขนาดใหญ่ การจำแนกประเภทขึ้นอยู่กับประเภทของปฏิกิริยา คลาสจะถูกตั้งชื่อตามหลักการทั่วไป - ชื่อของปฏิกิริยาและจุดสิ้นสุด - aza บางส่วนของชั้นเรียนเหล่านี้มีการระบุไว้ด้านล่าง
Oxidoreductaseเป็นเอนไซม์ที่กระตุ้นปฏิกิริยารีดอกซ์ ดีไฮโดรจีเนสที่รวมอยู่ในคลาสนี้ดำเนินการถ่ายโอนโปรตอน ตัวอย่างเช่น แอลกอฮอล์ดีไฮโดรจีเนส (ADH) ออกซิไดซ์แอลกอฮอล์ไปเป็นอัลดีไฮด์ การออกซิเดชันที่ตามมาของอัลดีไฮด์ไปยังกรดคาร์บอกซิลิกจะถูกเร่งปฏิกิริยาโดยอัลดีไฮด์ ดีไฮโดรจีเนส (ALDH) กระบวนการทั้งสองเกิดขึ้นในร่างกายระหว่างกระบวนการแปรรูปเอทานอลให้เป็นกรดอะซิติก (รูปที่ 18)
ข้าว. สิบแปด ออกซิเดชันสองขั้นตอนของเอทานอลเป็นกรดอะซิติก
ไม่ใช่เอธานอลที่มีฤทธิ์เสพติด แต่อะซีตัลดีไฮด์ผลิตภัณฑ์ขั้นกลางยิ่งกิจกรรมของเอนไซม์ ALDH ต่ำลงเท่าใดระยะที่สองก็จะผ่านไปช้า - การเกิดออกซิเดชันของอะซิตัลดีไฮด์เป็นกรดอะซิติกและยิ่งนานขึ้นและแข็งแรงขึ้นจากการกลืนกิน ของเอทานอล การวิเคราะห์แสดงให้เห็นว่ามากกว่า 80% ของตัวแทนของเผ่าพันธุ์สีเหลืองมีกิจกรรมที่ค่อนข้างต่ำของ ALDH ดังนั้นจึงมีความทนทานต่อแอลกอฮอล์ที่รุนแรงขึ้นอย่างเห็นได้ชัด สาเหตุของการออกฤทธิ์ที่ลดลงโดยธรรมชาติของ ALDH คือส่วนหนึ่งของกรดกลูตามิกเรซิดิวในโมเลกุล ALDH ที่ “ถูกทำให้อ่อนฤทธิ์” ถูกแทนที่ด้วยชิ้นส่วนไลซีน (ตารางที่ 1)
โอน- เอ็นไซม์ที่กระตุ้นการถ่ายโอนหมู่ฟังก์ชัน เช่น ทรานซิมิเนส กระตุ้นการถ่ายโอนของหมู่อะมิโน
ไฮโดรเลสเป็นเอ็นไซม์ที่เร่งปฏิกิริยาไฮโดรไลซิส ทริปซินและเปปซินไฮโดรไลซ์เปปไทด์ที่กล่าวถึงก่อนหน้านี้และไลเปสแยกพันธะเอสเทอร์ในไขมัน:
–RC(O)OR 1 + H 2 O → –RC(O)OH + HOR 1
Liase- เอ็นไซม์ที่กระตุ้นปฏิกิริยาที่เกิดขึ้นในลักษณะที่ไม่ใช่ไฮโดรไลติก อันเป็นผลมาจากปฏิกิริยาดังกล่าว พันธะ C-C, C-O, C-N จะแตกออกและเกิดพันธะใหม่ขึ้น เอนไซม์ดีคาร์บอกซิเลสอยู่ในคลาสนี้
ไอโซเมอเรส- เอ็นไซม์ที่เร่งปฏิกิริยาไอโซเมอไรเซชัน เช่น การเปลี่ยนกรดมาลิกเป็นกรดฟูมาริก (รูปที่ 19) นี่คือตัวอย่างของซิสทรานส์ไอโซเมอไรเซชัน (ดู ISOMERIA)
ข้าว. 19. การแยกตัวของกรดมาลิกเป็นกรดฟูมาริกต่อหน้าเอนไซม์
ในการทำงานของเอ็นไซม์นั้น หลักการทั่วไปนั้นสังเกตได้ ตามที่มีโครงสร้างสัมพันธ์กันระหว่างเอ็นไซม์และรีเอเจนต์ของปฏิกิริยาเร่งเสมอ จากการแสดงออกที่เป็นรูปเป็นร่างของหนึ่งในผู้ก่อตั้งหลักคำสอนของเอนไซม์ อี. ฟิชเชอร์ รีเอเจนต์เข้าใกล้เอ็นไซม์เหมือนกุญแจไขกุญแจ ในเรื่องนี้ เอนไซม์แต่ละตัวกระตุ้นปฏิกิริยาเคมีบางอย่างหรือกลุ่มของปฏิกิริยาประเภทเดียวกัน บางครั้งเอนไซม์สามารถทำหน้าที่กับสารประกอบเดี่ยว เช่น ยูรีเอส (uron กรีก. - ปัสสาวะ) กระตุ้นเฉพาะการไฮโดรไลซิสของยูเรีย:
(H 2 N) 2 C \u003d O + H 2 O \u003d CO 2 + 2NH 3
การคัดเลือกที่ดีที่สุดนั้นแสดงให้เห็นโดยเอนไซม์ที่แยกความแตกต่างระหว่างแอนติพอดที่ออกฤทธิ์ทางแสง - ไอโซเมอร์มือซ้ายและมือขวา L-arginase ทำหน้าที่เฉพาะกับ levorotatory arginine และไม่ส่งผลต่อ dextrorotatory isomer L-lactate dehydrogenase ทำหน้าที่เฉพาะกับเอสเทอร์ levorotatory ของกรดแลคติคที่เรียกว่า lactates (lactis lat. นม) ในขณะที่ D-lactate dehydrogenase จะสลาย D-lactates เท่านั้น
เอ็นไซม์ส่วนใหญ่ไม่ได้ทำหน้าที่หนึ่ง แต่กับกลุ่มของสารประกอบที่เกี่ยวข้อง ตัวอย่างเช่น ทริปซิน "ชอบ" ที่จะแยกพันธะเปปไทด์ที่เกิดจากไลซีนและอาร์จินีน (ตารางที่ 1)
คุณสมบัติการเร่งปฏิกิริยาของเอนไซม์บางชนิด เช่น ไฮโดรเลส ถูกกำหนดโดยโครงสร้างของโมเลกุลโปรตีนเองเท่านั้น เอนไซม์อีกประเภทหนึ่ง - ออกซิโดเรดักเตส (เช่น แอลกอฮอล์ดีไฮโดรจีเนส) สามารถทำงานได้เฉพาะเมื่อมีโมเลกุลที่ไม่ใช่โปรตีนที่เกี่ยวข้องกับ พวกเขา - วิตามินที่กระตุ้น Mg, Ca, Zn, Mn และชิ้นส่วนของกรดนิวคลีอิก (รูปที่ 20)
ข้าว. ยี่สิบ แอลกอฮอล์ดีไฮโดรเจเนสโมเลกุล
โปรตีนขนส่งจับและขนส่งโมเลกุลหรือไอออนต่างๆ ผ่านเยื่อหุ้มเซลล์ (ทั้งภายในและภายนอกเซลล์) รวมทั้งจากอวัยวะหนึ่งไปยังอีกอวัยวะหนึ่ง
ตัวอย่างเช่น ฮีโมโกลบินจับออกซิเจนเมื่อเลือดไหลผ่านปอดและส่งไปยังเนื้อเยื่อต่างๆ ของร่างกาย ที่ซึ่งออกซิเจนจะถูกปล่อยออกมาและนำไปใช้ในการออกซิไดซ์ส่วนประกอบอาหาร กระบวนการนี้ทำหน้าที่เป็นแหล่งพลังงาน (บางครั้งใช้คำว่า "การเผาไหม้" อาหารในร่างกาย)
นอกจากส่วนโปรตีนแล้ว เฮโมโกลบินยังมีสารประกอบเชิงซ้อนของธาตุเหล็กที่มีโมเลกุลพอร์ไฟรินแบบไซคลิก (porphyros กรีก. - สีม่วง) ซึ่งกำหนดสีแดงของเลือด คอมเพล็กซ์นี้ (รูปที่ 21 ซ้าย) ที่ทำหน้าที่เป็นตัวพาออกซิเจน ในเฮโมโกลบิน ธาตุเหล็กพอร์ไฟรินเชิงซ้อนจะอยู่ภายในโมเลกุลโปรตีนและถูกคงไว้โดยปฏิกิริยาเชิงขั้ว เช่นเดียวกับพันธะประสานกับไนโตรเจนในฮิสทิดีน (ตารางที่ 1) ซึ่งเป็นส่วนหนึ่งของโปรตีน โมเลกุล O2 ซึ่งฮีโมโกลบินพาไป จะถูกยึดติดผ่านพันธะประสานกับอะตอมของเหล็กจากด้านตรงข้ามกับที่ติดฮิสทิดีน (รูปที่ 21, ขวา)
ข้าว. 21 โครงสร้างของเหล็กคอมเพล็กซ์
โครงสร้างของคอมเพล็กซ์แสดงทางด้านขวาในรูปแบบของแบบจำลองสามมิติ คอมเพล็กซ์ถูกเก็บไว้ในโมเลกุลโปรตีนโดยพันธะประสาน (เส้นประสีน้ำเงิน) ระหว่างอะตอม Fe และอะตอม N ในฮิสทิดีน ซึ่งเป็นส่วนหนึ่งของโปรตีน โมเลกุล O 2 ซึ่งบรรทุกโดยเฮโมโกลบิน ประสานกัน (เส้นประสีแดง) กับอะตอม Fe จากประเทศตรงข้ามของคอมเพล็กซ์ระนาบ
เฮโมโกลบินเป็นหนึ่งในโปรตีนที่มีการศึกษามากที่สุด ประกอบด้วย a-helices ที่เชื่อมต่อกันด้วยโซ่เดี่ยวและมีธาตุเหล็กสี่ชนิด ดังนั้นเฮโมโกลบินจึงเปรียบเสมือนแพ็คเกจขนาดใหญ่สำหรับการถ่ายโอนโมเลกุลออกซิเจนสี่ตัวในคราวเดียว รูปแบบของเฮโมโกลบินสอดคล้องกับโปรตีนทรงกลม (รูปที่ 22)
ข้าว. 22 รูปทรงกลมของฮีโมโกลบิน
"ข้อได้เปรียบ" หลักของเฮโมโกลบินคือการเติมออกซิเจนและการแยกตัวออกในภายหลังระหว่างการส่งผ่านไปยังเนื้อเยื่อและอวัยวะต่างๆ เกิดขึ้นอย่างรวดเร็ว คาร์บอนมอนอกไซด์ CO (คาร์บอนมอนอกไซด์) จะจับกับ Fe ในเฮโมโกลบินได้เร็วยิ่งขึ้นไปอีก แต่ต่างจาก O 2 ที่ก่อตัวเป็นสารประกอบเชิงซ้อนที่ย่อยสลายยาก เป็นผลให้ฮีโมโกลบินดังกล่าวไม่สามารถจับ O 2 ซึ่งทำให้ (เมื่อสูดดมคาร์บอนมอนอกไซด์จำนวนมาก) ไปสู่ความตายของร่างกายจากการหายใจไม่ออก
หน้าที่ที่สองของเฮโมโกลบินคือการถ่ายโอน CO 2 ที่หายใจออก แต่ไม่ใช่อะตอมของเหล็ก แต่ H 2 ของกลุ่ม N ของโปรตีนเกี่ยวข้องกับกระบวนการจับคาร์บอนไดออกไซด์ชั่วคราว
"ประสิทธิภาพ" ของโปรตีนขึ้นอยู่กับโครงสร้างของพวกมัน ตัวอย่างเช่น การแทนที่กรดอะมิโนที่ตกค้างเพียงตัวเดียวของกรดกลูตามิกในสายพอลิเปปไทด์ของเฮโมโกลบินด้วยสารตกค้างวาลีน (ความผิดปกติแต่กำเนิดที่ไม่ค่อยสังเกตพบ) นำไปสู่โรคที่เรียกว่าโรคโลหิตจางชนิดเคียว
นอกจากนี้ยังมีการลำเลียงโปรตีนที่สามารถจับไขมัน กลูโคส กรดอะมิโน และขนส่งได้ทั้งภายในและภายนอกเซลล์
โปรตีนขนส่งชนิดพิเศษไม่ได้นำพาสารเอง แต่ทำหน้าที่เป็น "ตัวควบคุมการขนส่ง" โดยส่งสารบางชนิดผ่านเมมเบรน (ผนังด้านนอกของเซลล์) โปรตีนดังกล่าวมักเรียกว่าโปรตีนเมมเบรน พวกมันมีรูปร่างเป็นทรงกระบอกกลวงและฝังอยู่ในผนังเมมเบรนทำให้แน่ใจได้ว่าการเคลื่อนที่ของโมเลกุลขั้วหรือไอออนเข้าไปในเซลล์ ตัวอย่างของโปรตีนเมมเบรนคือ porin (รูปที่ 23)
ข้าว. 23 โปรตีนโพริน
โปรตีนจากอาหารและการเก็บรักษาตามชื่อหมายถึงเป็นแหล่งโภชนาการภายในซึ่งบ่อยขึ้นสำหรับตัวอ่อนของพืชและสัตว์ตลอดจนในระยะแรกของการพัฒนาสิ่งมีชีวิตเล็ก โปรตีนในอาหาร ได้แก่ อัลบูมิน (รูปที่ 10) ซึ่งเป็นส่วนประกอบหลักของไข่ขาว เช่นเดียวกับเคซีน ซึ่งเป็นโปรตีนหลักของนม ภายใต้การกระทำของเอนไซม์เปปซิน เคซีนทำให้แข็งตัวในกระเพาะอาหาร ซึ่งช่วยให้คงอยู่ในระบบทางเดินอาหารและดูดซึมได้อย่างมีประสิทธิภาพ เคซีนประกอบด้วยชิ้นส่วนของกรดอะมิโนทั้งหมดที่ร่างกายต้องการ
ในเฟอร์ริติน (รูปที่ 12) ซึ่งมีอยู่ในเนื้อเยื่อของสัตว์จะมีการเก็บไอออนของเหล็กไว้
Myoglobin ยังเป็นโปรตีนในการจัดเก็บซึ่งคล้ายกับเฮโมโกลบินในองค์ประกอบและโครงสร้าง Myoglobin มีความเข้มข้นส่วนใหญ่ในกล้ามเนื้อบทบาทหลักคือการจัดเก็บออกซิเจนซึ่งเฮโมโกลบินมอบให้ ออกซิเจนอิ่มตัวอย่างรวดเร็ว (เร็วกว่าฮีโมโกลบินมาก) แล้วค่อยๆ ถ่ายโอนไปยังเนื้อเยื่อต่างๆ
โปรตีนโครงสร้างทำหน้าที่ป้องกัน (ผิวหนัง) หรือรองรับ - พวกมันยึดร่างกายไว้ด้วยกันและให้ความแข็งแรง (กระดูกอ่อนและเอ็น) ส่วนประกอบหลักของพวกเขาคือโปรตีนคอลลาเจนไฟบริลลาร์ (รูปที่ 11) ซึ่งเป็นโปรตีนที่พบมากที่สุดในโลกของสัตว์ ในร่างกายของสัตว์เลี้ยงลูกด้วยนม คิดเป็นสัดส่วนเกือบ 30% ของมวลโปรตีนทั้งหมด คอลลาเจนมีความต้านทานแรงดึงสูง (เป็นที่ทราบกันดีว่าความแข็งแรงของผิวหนัง) แต่เนื่องจากคอลลาเจนของผิวหนังมี cross-links ต่ำ หนังสัตว์จึงไม่เหมาะมากในรูปแบบดิบสำหรับการผลิตผลิตภัณฑ์ต่างๆ เพื่อลดอาการบวมของผิวหนังในน้ำ การหดตัวระหว่างการอบแห้ง เช่นเดียวกับการเพิ่มความแข็งแรงในสภาวะที่มีน้ำและเพิ่มความยืดหยุ่นในคอลลาเจน จึงมีการสร้าง cross-links เพิ่มเติม (รูปที่ 15a) นี่คือสิ่งที่เรียกว่า กระบวนการฟอกหนัง
ในสิ่งมีชีวิต โมเลกุลคอลลาเจนที่เกิดขึ้นในกระบวนการของการเจริญเติบโตและการพัฒนาของสิ่งมีชีวิตจะไม่ได้รับการปรับปรุงและไม่ได้ถูกแทนที่ด้วยโมเลกุลที่สังเคราะห์ขึ้นใหม่ เมื่อร่างกายมีอายุมากขึ้น จำนวนของการเชื่อมขวางในคอลลาเจนจะเพิ่มขึ้น ซึ่งทำให้ความยืดหยุ่นลดลง และเนื่องจากการต่ออายุไม่เกิดขึ้น การเปลี่ยนแปลงที่เกี่ยวข้องกับอายุจึงปรากฏขึ้น - ความเปราะบางของกระดูกอ่อนและเส้นเอ็นเพิ่มขึ้น ริ้วรอยบนผิวหนัง
เอ็นข้อต่อประกอบด้วยอีลาสติน ซึ่งเป็นโปรตีนโครงสร้างที่ยืดออกเป็นสองมิติได้ง่าย โปรตีนเรซินซึ่งอยู่ที่จุดยึดของปีกของแมลงบางชนิดมีความยืดหยุ่นมากที่สุด
การก่อตัวของเขา - ผม เล็บ ขน ซึ่งประกอบด้วยโปรตีนเคราตินเป็นส่วนใหญ่ (รูปที่ 24) ความแตกต่างที่สำคัญคือเนื้อหาของซิสเทอีนที่ตกค้างซึ่งก่อให้เกิดสะพานไดซัลไฟด์ซึ่งให้ความยืดหยุ่นสูง (ความสามารถในการฟื้นฟูรูปร่างเดิมหลังจากการเสียรูป) ให้กับเส้นผมและผ้าขนสัตว์
ข้าว. 24. ชิ้นส่วนของโปรตีน FIBRILLAR เคราติน
สำหรับการเปลี่ยนแปลงรูปร่างของวัตถุเคราตินที่ไม่สามารถย้อนกลับได้ ก่อนอื่นคุณต้องทำลายสะพานไดซัลไฟด์ด้วยความช่วยเหลือของตัวรีดิวซ์ สร้างรูปร่างใหม่ จากนั้นสร้างสะพานไดซัลไฟด์ขึ้นใหม่ด้วยความช่วยเหลือของตัวออกซิไดซ์ (รูปที่ . 16) นี่เป็นวิธีการเช่นการดัดผม
ด้วยการเพิ่มขึ้นของเนื้อหาของซิสเทอีนในเคราตินและด้วยเหตุนี้การเพิ่มจำนวนของสะพานไดซัลไฟด์ความสามารถในการเปลี่ยนรูปจะหายไป แต่มีความแข็งแรงสูงปรากฏขึ้นในเวลาเดียวกัน (แตรของกีบและเปลือกเต่ามีมากถึง 18% ของชิ้นส่วนซิสเทอีน) สัตว์เลี้ยงลูกด้วยนมมีเคราตินถึง 30 ชนิด
โปรตีนไฟบริลที่เกี่ยวข้องกับเคราตินที่ถูกขับออกมาจากตัวหนอนไหมในระหว่างการม้วนผมของรังไหม เช่นเดียวกับแมงมุมในระหว่างการทอผ้า มีเพียงโครงสร้าง β ที่เชื่อมต่อกันด้วยสายโซ่เดียว (รูปที่ 11) ไฟโบรอินไม่มีสะพานไดซัลไฟด์ตามขวาง ซึ่งแตกต่างจากเคราติน แต่มีความต้านทานแรงดึงสูงมาก (ความแข็งแรงต่อหน่วยหน้าตัดของตัวอย่างใยบางตัวจะสูงกว่าสายเคเบิลเหล็ก) เนื่องจากไม่มีการเชื่อมโยงขวาง ไฟโบรอินจึงไม่ยืดหยุ่น (เป็นที่ทราบกันดีอยู่แล้วว่าผ้าขนสัตว์นั้นแทบจะลบไม่ออก และผ้าไหมจะมีรอยย่นได้ง่าย)
โปรตีนควบคุม
โปรตีนควบคุม หรือที่เรียกกันทั่วไปว่าฮอร์โมน มีส่วนเกี่ยวข้องกับกระบวนการทางสรีรวิทยาต่างๆ ตัวอย่างเช่น ฮอร์โมนอินซูลิน (รูปที่ 25) ประกอบด้วย α-chains สองสายที่เชื่อมต่อกันด้วยไดซัลไฟด์บริดจ์ อินซูลินควบคุมกระบวนการเผาผลาญที่เกี่ยวข้องกับกลูโคส การไม่มีอินซูลินทำให้เกิดโรคเบาหวาน
ข้าว. 25 โปรตีนอินซูลิน
ต่อมใต้สมองของสมองสังเคราะห์ฮอร์โมนที่ควบคุมการเจริญเติบโตของร่างกาย มีโปรตีนควบคุมที่ควบคุมการสังเคราะห์ทางชีวสังเคราะห์ของเอนไซม์ต่างๆ ในร่างกาย
โปรตีนที่หดตัวและมอเตอร์ทำให้ร่างกายสามารถหดตัว เปลี่ยนรูปร่าง และเคลื่อนไหว โดยหลักแล้ว เรากำลังพูดถึงกล้ามเนื้อ 40% ของมวลของโปรตีนทั้งหมดที่มีอยู่ในกล้ามเนื้อคือไมโอซิน (mys, myos, กรีก. - กล้ามเนื้อ). โมเลกุลของมันมีทั้งไฟบริลลาร์และส่วนทรงกลม (รูปที่ 26)
ข้าว. 26 ไมโอซิน โมเลกุล
โมเลกุลดังกล่าวรวมกันเป็นมวลรวมขนาดใหญ่ที่มีโมเลกุล 300–400
เมื่อความเข้มข้นของแคลเซียมไอออนเปลี่ยนแปลงไปในช่องว่างรอบ ๆ เส้นใยกล้ามเนื้อ จะเกิดการเปลี่ยนแปลงโครงสร้างของโมเลกุลแบบย้อนกลับได้ ซึ่งเป็นการเปลี่ยนแปลงรูปร่างของสายโซ่เนื่องจากการหมุนของชิ้นส่วนแต่ละชิ้นรอบๆ พันธะเวเลนซ์ สิ่งนี้นำไปสู่การหดตัวของกล้ามเนื้อและการผ่อนคลาย สัญญาณการเปลี่ยนแปลงความเข้มข้นของแคลเซียมไอออนมาจากปลายประสาทในเส้นใยกล้ามเนื้อ การหดตัวของกล้ามเนื้อเทียมอาจเกิดจากการกระทำของแรงกระตุ้นไฟฟ้า ซึ่งนำไปสู่การเปลี่ยนแปลงอย่างรวดเร็วในความเข้มข้นของแคลเซียมไอออน ซึ่งเป็นพื้นฐานในการกระตุ้นกล้ามเนื้อหัวใจเพื่อฟื้นฟูการทำงานของหัวใจ
โปรตีนป้องกันช่วยให้คุณปกป้องร่างกายจากการบุกรุกของแบคทีเรียโจมตีไวรัสและจากการรุกของโปรตีนต่างประเทศ (ชื่อทั่วไปของสิ่งแปลกปลอมคือแอนติเจน) บทบาทของโปรตีนป้องกันดำเนินการโดยอิมมูโนโกลบูลิน (ชื่ออื่นคือแอนติบอดี) พวกเขารู้จักแอนติเจนที่แทรกซึมเข้าสู่ร่างกายและผูกมัดกับพวกมันอย่างแน่นหนา ในร่างกายของสัตว์เลี้ยงลูกด้วยนมรวมถึงมนุษย์มีอิมมูโนโกลบูลินห้าประเภท: M, G, A, D และ E โครงสร้างของพวกเขาเป็นทรงกลมนอกจากนี้พวกมันทั้งหมดถูกสร้างขึ้นในลักษณะที่คล้ายกัน การจัดเรียงโมเลกุลของแอนติบอดีแสดงไว้ด้านล่างโดยใช้คลาส G อิมมูโนโกลบูลินเป็นตัวอย่าง (รูปที่ 27) โมเลกุลประกอบด้วยสายโซ่โพลีเปปไทด์สี่สายที่เชื่อมต่อกันด้วยสะพานไดซัลไฟด์ SS สามสาย (ในรูปที่ 27 แสดงด้วยพันธะวาเลนซ์ที่หนาขึ้นและสัญลักษณ์ S ขนาดใหญ่) นอกจากนี้ สายโซ่โพลีเมอร์แต่ละสายยังมีสะพานไดซัลไฟด์ภายในสายโซ่ สายโพลีเมอร์ขนาดใหญ่สองสาย (เน้นด้วยสีน้ำเงิน) มีกรดอะมิโนตกค้าง 400–600 อีกสองสาย (เน้นด้วยสีเขียว) มีความยาวเกือบครึ่งหนึ่ง โดยมีกรดอะมิโนตกค้างอยู่ประมาณ 220 ตัว โซ่ทั้งสี่อยู่ในลักษณะที่กลุ่ม H 2 N ของเทอร์มินัลถูกชี้ไปในทิศทางเดียว
ข้าว. 27 แผนผังของโครงสร้างของอิมมูโนโกลบูลิน
หลังจากที่ร่างกายสัมผัสกับโปรตีนแปลกปลอม (แอนติเจน) เซลล์ของระบบภูมิคุ้มกันจะเริ่มผลิตอิมมูโนโกลบูลิน (แอนติบอดี) ซึ่งสะสมอยู่ในซีรัมในเลือด ในขั้นตอนแรก งานหลักจะทำโดยส่วนลูกโซ่ที่มีขั้ว H 2 N (ในรูปที่ 27 ส่วนที่เกี่ยวข้องจะถูกทำเครื่องหมายด้วยสีน้ำเงินอ่อนและสีเขียวอ่อน) เหล่านี้เป็นไซต์การจับแอนติเจน ในกระบวนการสังเคราะห์อิมมูโนโกลบูลิน ไซต์เหล่านี้ถูกสร้างขึ้นในลักษณะที่โครงสร้างและการกำหนดค่าของพวกมันสอดคล้องกับโครงสร้างของแอนติเจนที่ใกล้เข้ามามากที่สุด (เช่นกุญแจล็อคเช่นเอนไซม์ แต่งานในกรณีนี้คือ แตกต่าง). ดังนั้น สำหรับแอนติเจนแต่ละตัว แอนติบอดีแต่ละตัวจึงถูกสร้างขึ้นเพื่อตอบสนองต่อภูมิคุ้มกัน ไม่ใช่โปรตีนที่รู้จักเพียงชนิดเดียวที่สามารถเปลี่ยนโครงสร้างของมันได้ ดังนั้น "พลาสติก" ขึ้นอยู่กับปัจจัยภายนอก นอกเหนือจากอิมมูโนโกลบูลิน เอ็นไซม์แก้ปัญหาความสอดคล้องของโครงสร้างกับรีเอเจนต์ด้วยวิธีที่แตกต่าง - ด้วยความช่วยเหลือของชุดเอ็นไซม์ขนาดมหึมาสำหรับกรณีที่เป็นไปได้ทั้งหมด และอิมมูโนโกลบูลินในแต่ละครั้งจะสร้าง "เครื่องมือการทำงาน" ขึ้นใหม่ นอกจากนี้ บริเวณบานพับของอิมมูโนโกลบูลิน (รูปที่ 27) จัดให้มีบริเวณการจับสองบริเวณที่มีการเคลื่อนย้ายที่เป็นอิสระ ส่งผลให้โมเลกุลอิมมูโนโกลบุลินสามารถ "ค้นหา" บริเวณที่สะดวกที่สุดสองบริเวณสำหรับการดักจับในแอนติเจนในทันที เพื่อให้สามารถตรึงได้อย่างปลอดภัย มันคล้ายกับการกระทำของสัตว์จำพวกครัสเตเชียน
ถัดไปห่วงโซ่ของปฏิกิริยาต่อเนื่องของระบบภูมิคุ้มกันของร่างกายถูกเปิดใช้งาน อิมมูโนโกลบูลินของคลาสอื่นเชื่อมต่อกัน ส่งผลให้โปรตีนจากต่างประเทศถูกปิดใช้งาน จากนั้นแอนติเจน (จุลินทรีย์หรือสารพิษจากต่างประเทศ) จะถูกทำลายและกำจัดออก
หลังจากสัมผัสกับแอนติเจน ความเข้มข้นสูงสุดของอิมมูโนโกลบูลินจะถึง (ขึ้นอยู่กับลักษณะของแอนติเจนและลักษณะเฉพาะของสิ่งมีชีวิต) ภายในเวลาไม่กี่ชั่วโมง (บางครั้งเป็นเวลาหลายวัน) ร่างกายยังคงความทรงจำของการสัมผัสดังกล่าวและเมื่อถูกโจมตีอีกครั้งด้วยแอนติเจนเดียวกันอิมมูโนโกลบูลินจะสะสมในเลือดเร็วขึ้นมากและในปริมาณที่มากขึ้น - ภูมิคุ้มกันที่ได้มาจะเกิดขึ้น
การจำแนกประเภทโปรตีนข้างต้นเป็นไปตามเงื่อนไขในระดับหนึ่ง ตัวอย่างเช่น โปรตีนทรอมบินที่กล่าวถึงในหมู่โปรตีนป้องกัน โดยพื้นฐานแล้วเป็นเอนไซม์ที่เร่งปฏิกิริยาไฮโดรไลซิสของพันธะเปปไทด์ กล่าวคือ อยู่ในคลาสของโปรตีเอส
โปรตีนป้องกันมักถูกเรียกว่าโปรตีนพิษงูและโปรตีนที่เป็นพิษของพืชบางชนิด เนื่องจากหน้าที่ของพวกมันคือปกป้องร่างกายจากความเสียหาย
มีโปรตีนที่ทำหน้าที่เฉพาะตัวจนยากต่อการจำแนก ตัวอย่างเช่น โปรตีนโมเนลลินที่พบในพืชแอฟริกามีรสหวานมากและเป็นหัวข้อของการศึกษาว่าเป็นสารปลอดสารพิษที่สามารถใช้แทนน้ำตาลเพื่อป้องกันโรคอ้วนได้ พลาสมาในเลือดของปลาแอนตาร์กติกบางชนิดมีโปรตีนที่มีคุณสมบัติป้องกันการแข็งตัวที่ทำให้เลือดของปลาเหล่านี้ไม่แข็งตัว
การสังเคราะห์โปรตีนประดิษฐ์
การควบแน่นของกรดอะมิโนที่นำไปสู่สายโซ่โพลีเปปไทด์เป็นกระบวนการที่มีการศึกษามาเป็นอย่างดี เป็นไปได้ที่จะดำเนินการ ตัวอย่างเช่น การควบแน่นของกรดอะมิโนตัวใดตัวหนึ่งหรือของผสมของกรด และรับพอลิเมอร์ที่มีหน่วยเดียวกันหรือหน่วยต่างกัน ตามลำดับแบบสุ่ม โพลีเมอร์ดังกล่าวมีความคล้ายคลึงกับโพลีเปปไทด์ธรรมชาติเพียงเล็กน้อยและไม่มีฤทธิ์ทางชีวภาพ งานหลักคือการเชื่อมต่อกรดอะมิโนในลำดับที่กำหนดไว้ล่วงหน้าอย่างเคร่งครัด เพื่อสร้างลำดับของกรดอะมิโนตกค้างในโปรตีนธรรมชาติ นักวิทยาศาสตร์ชาวอเมริกัน Robert Merrifield เสนอวิธีการดั้งเดิมที่ทำให้สามารถแก้ปัญหาดังกล่าวได้ สาระสำคัญของวิธีการนี้คือ กรดอะมิโนตัวแรกติดอยู่กับเจลพอลิเมอร์ที่ไม่ละลายน้ำซึ่งมีกลุ่มปฏิกิริยาที่สามารถรวมกับ –COOH – กลุ่มของกรดอะมิโนได้ พอลิสไตรีนเชื่อมขวางกับหมู่คลอโรเมทิลที่นำเข้ามาถูกนำไปใช้เป็นสารตั้งต้นที่เป็นโพลีเมอร์ดังกล่าว เพื่อให้กรดอะมิโนที่นำมาทำปฏิกิริยาไม่ทำปฏิกิริยากับตัวเองและเพื่อไม่ให้รวมกลุ่ม H 2 N กับสารตั้งต้น กลุ่มอะมิโนของกรดนี้จะถูกบล็อกล่วงหน้าด้วยหมู่แทนที่ขนาดใหญ่ [(C 4 H 9) 3] 3 OS (O) - กลุ่ม หลังจากที่กรดอะมิโนยึดติดกับตัวรองรับโพลีเมอร์แล้ว กลุ่มที่ปิดกั้นจะถูกลบออกและกรดอะมิโนอีกตัวหนึ่งจะถูกนำเข้าไปในส่วนผสมของปฏิกิริยา ซึ่งก่อนหน้านี้กลุ่ม H 2 N ก็ถูกบล็อกเช่นกัน ในระบบดังกล่าว เป็นไปได้เฉพาะการทำงานร่วมกันของกลุ่ม H 2 N ของกรดอะมิโนตัวแรกและกลุ่ม –COOH ของกรดที่สองเท่านั้น ซึ่งดำเนินการต่อหน้าตัวเร่งปฏิกิริยา (เกลือฟอสโฟเนียม) จากนั้นทำซ้ำโครงร่างทั้งหมดโดยแนะนำกรดอะมิโนตัวที่สาม (รูปที่ 28)
ข้าว. 28. โครงการสังเคราะห์ของโซ่โพลีเปปไทด์
ในขั้นตอนสุดท้าย สายโพลีเปปไทด์ที่เป็นผลลัพธ์จะถูกแยกออกจากส่วนรองรับโพลีสไตรีน ตอนนี้กระบวนการทั้งหมดเป็นแบบอัตโนมัติ มีเครื่องสังเคราะห์เปปไทด์อัตโนมัติที่ทำงานตามรูปแบบที่อธิบายไว้ เปปไทด์จำนวนมากที่ใช้ในยาและการเกษตรได้รับการสังเคราะห์ด้วยวิธีนี้ นอกจากนี้ยังเป็นไปได้ที่จะได้รับอะนาลอกที่ปรับปรุงแล้วของเปปไทด์ธรรมชาติด้วยการกระทำแบบคัดเลือกและเพิ่มประสิทธิภาพ มีการสังเคราะห์โปรตีนขนาดเล็กบางชนิด เช่น ฮอร์โมนอินซูลินและเอนไซม์บางชนิด
นอกจากนี้ยังมีวิธีการสังเคราะห์โปรตีนที่ทำซ้ำกระบวนการทางธรรมชาติ: พวกเขาสังเคราะห์ชิ้นส่วนของกรดนิวคลีอิกที่กำหนดค่าไว้เพื่อผลิตโปรตีนบางชนิด จากนั้นชิ้นส่วนเหล่านี้จะถูกแทรกเข้าไปในสิ่งมีชีวิต (เช่น ในแบคทีเรีย) หลังจากนั้นร่างกายจะเริ่มผลิต โปรตีนที่ต้องการ ด้วยวิธีนี้ โปรตีนและเปปไทด์ที่เข้าถึงยากจำนวนมากรวมถึงอะนาลอกของพวกมันได้รับมาในขณะนี้
โปรตีนเป็นแหล่งอาหาร
โปรตีนในสิ่งมีชีวิตจะถูกย่อยสลายเป็นกรดอะมิโนดั้งเดิมอย่างต่อเนื่อง (ด้วยการมีส่วนร่วมของเอนไซม์ที่ขาดไม่ได้) กรดอะมิโนบางตัวจะผ่านไปยังส่วนอื่น จากนั้นโปรตีนจะถูกสังเคราะห์อีกครั้ง (ด้วยการมีส่วนร่วมของเอนไซม์) เช่น ร่างกายมีการต่ออายุตัวเองอย่างต่อเนื่อง โปรตีนบางชนิด (คอลลาเจนของผิวหนัง เส้นผม) ไม่ได้รับการสร้างใหม่ ร่างกายจะสูญเสียพวกมันไปอย่างต่อเนื่องและสังเคราะห์ขึ้นใหม่แทน โปรตีนที่เป็นแหล่งอาหารมีหน้าที่หลัก 2 ประการคือ ทำหน้าที่จัดหาวัสดุก่อสร้างสำหรับการสังเคราะห์โมเลกุลโปรตีนใหม่และให้พลังงานแก่ร่างกาย (แหล่งแคลอรี)
สัตว์เลี้ยงลูกด้วยนมที่กินเนื้อเป็นอาหาร (รวมทั้งมนุษย์) ได้รับโปรตีนที่จำเป็นจากอาหารจากพืชและสัตว์ ไม่มีโปรตีนใดที่ได้จากอาหารถูกรวมเข้ากับร่างกายในรูปแบบที่ไม่เปลี่ยนแปลง ในทางเดินอาหาร โปรตีนที่ดูดซึมทั้งหมดจะถูกย่อยสลายเป็นกรดอะมิโน และโปรตีนที่จำเป็นสำหรับสิ่งมีชีวิตบางชนิดก็ถูกสร้างขึ้นจากพวกมันแล้ว ในขณะที่อีก 12 ตัวสามารถสังเคราะห์ได้จากกรดจำเป็น 8 ชนิด (ตารางที่ 1) ในร่างกายหากไม่ใช่ ให้อาหารในปริมาณที่เพียงพอ แต่ต้องให้กรดที่จำเป็นกับอาหารโดยไม่ล้มเหลว ร่างกายได้รับอะตอมของกำมะถันในซิสเทอีนด้วยเมไทโอนีนกรดอะมิโนที่จำเป็น โปรตีนบางส่วนสลายตัว ปล่อยพลังงานที่จำเป็นต่อการดำรงชีวิต และไนโตรเจนที่บรรจุอยู่ภายในจะถูกขับออกจากร่างกายด้วยปัสสาวะ โดยปกติร่างกายมนุษย์จะสูญเสียโปรตีน 25-30 กรัมต่อวัน ดังนั้นอาหารที่มีโปรตีนจะต้องอยู่ในปริมาณที่เหมาะสมเสมอ ความต้องการโปรตีนขั้นต่ำต่อวันสำหรับผู้ชายคือ 37 กรัมและ 29 กรัมสำหรับผู้หญิง แต่ปริมาณที่แนะนำนั้นสูงเกือบสองเท่า ในการประเมินอาหาร การพิจารณาคุณภาพโปรตีนเป็นสิ่งสำคัญ ในกรณีที่ไม่มีกรดอะมิโนจำเป็นหรือมีปริมาณต่ำ โปรตีนจะถือว่ามีคุณค่าต่ำ ดังนั้นควรบริโภคโปรตีนดังกล่าวในปริมาณที่มากขึ้น ดังนั้น โปรตีนจากพืชตระกูลถั่วจึงมีเมไทโอนีนน้อย และโปรตีนจากข้าวสาลีและข้าวโพดมีไลซีนต่ำ (กรดอะมิโนทั้งสองจำเป็น) โปรตีนจากสัตว์ (ไม่รวมคอลลาเจน) จัดเป็นอาหารที่สมบูรณ์ ชุดของกรดที่จำเป็นทั้งหมดประกอบด้วยเคซีนนม เช่นเดียวกับคอทเทจชีสและชีสที่เตรียมจากมัน ดังนั้นอาหารมังสวิรัติหากเข้มงวดมาก เช่น “ปราศจากนม” ต้องการการบริโภคพืชตระกูลถั่ว ถั่ว และเห็ดเพิ่มขึ้น เพื่อให้ร่างกายได้รับกรดอะมิโนที่จำเป็นในปริมาณที่เหมาะสม
กรดอะมิโนและโปรตีนสังเคราะห์ยังใช้เป็นผลิตภัณฑ์อาหาร โดยเพิ่มลงในอาหารซึ่งมีกรดอะมิโนที่จำเป็นในปริมาณเล็กน้อย มีแบคทีเรียที่สามารถแปรรูปและดูดซึมน้ำมันไฮโดรคาร์บอน ในกรณีนี้ สำหรับการสังเคราะห์โปรตีนอย่างเต็มรูปแบบ พวกมันจะต้องได้รับสารอาหารที่มีไนโตรเจนเป็นส่วนประกอบ (แอมโมเนียหรือไนเตรต) โปรตีนที่ได้จากวิธีนี้ใช้เป็นอาหารสำหรับปศุสัตว์และสัตว์ปีก ชุดของเอนไซม์ คาร์โบไฮเดรต มักถูกเติมลงในอาหารสัตว์ ซึ่งกระตุ้นการไฮโดรไลซิสของส่วนประกอบอาหารคาร์โบไฮเดรตที่ย่อยสลายได้ยาก (ผนังเซลล์ของเมล็ดพืช) อันเป็นผลมาจากการที่อาหารจากพืชดูดซึมได้เต็มที่กว่า
มิคาอิล เลวิตสกี้
โปรตีน (ข้อ 2)
(โปรตีน) คลาสของสารประกอบที่ประกอบด้วยไนโตรเจนเชิงซ้อน ซึ่งเป็นส่วนประกอบที่มีลักษณะเฉพาะและสำคัญที่สุด (พร้อมกับกรดนิวคลีอิก) ของสิ่งมีชีวิต โปรตีนทำหน้าที่หลายอย่างและหลากหลาย โปรตีนส่วนใหญ่เป็นเอนไซม์ที่กระตุ้นปฏิกิริยาเคมี ฮอร์โมนหลายชนิดที่ควบคุมกระบวนการทางสรีรวิทยาก็เป็นโปรตีนเช่นกัน โปรตีนโครงสร้างเช่นคอลลาเจนและเคราตินเป็นส่วนประกอบหลักของเนื้อเยื่อกระดูก ผมและเล็บ โปรตีนที่หดตัวของกล้ามเนื้อมีความสามารถในการเปลี่ยนความยาวโดยใช้พลังงานเคมีเพื่อทำงานทางกล โปรตีนเป็นแอนติบอดีที่ยึดเกาะและทำให้สารพิษเป็นกลาง โปรตีนบางชนิดที่สามารถตอบสนองต่ออิทธิพลภายนอก (แสง กลิ่น) ทำหน้าที่เป็นตัวรับในอวัยวะรับความรู้สึกที่รับรู้การระคายเคือง โปรตีนหลายชนิดที่อยู่ภายในเซลล์และบนเยื่อหุ้มเซลล์ทำหน้าที่ควบคุม
ในช่วงครึ่งแรกของศตวรรษที่ 19 นักเคมีหลายคนและในหมู่พวกเขาโดยหลักแล้ว J. von Liebig ค่อยๆสรุปว่าโปรตีนเป็นสารประกอบไนโตรเจนประเภทพิเศษ ชื่อ "โปรตีน" (มาจากภาษากรีกโปรโตส - ตัวแรก) ถูกเสนอในปี พ.ศ. 2383 โดยนักเคมีชาวดัตช์ G. Mulder
คุณสมบัติทางกายภาพ
โปรตีนมีสีขาวในสถานะของแข็ง แต่ไม่มีสีในสารละลาย เว้นแต่จะมีกลุ่มโครโมฟอร์ (สี) บางกลุ่ม เช่น เฮโมโกลบิน ความสามารถในการละลายน้ำของโปรตีนที่แตกต่างกันนั้นแตกต่างกันอย่างมาก นอกจากนี้ยังแตกต่างกันไปตาม pH และความเข้มข้นของเกลือในสารละลาย เพื่อให้สามารถเลือกสภาวะที่โปรตีนตัวหนึ่งจะตกตะกอนอย่างเฉพาะเจาะจงเมื่อมีโปรตีนอื่นอยู่ วิธีการ "เกลือออก" นี้ใช้กันอย่างแพร่หลายในการแยกและทำให้โปรตีนบริสุทธิ์ โปรตีนบริสุทธิ์มักจะตกตะกอนจากสารละลายเป็นผลึก
เมื่อเปรียบเทียบกับสารประกอบอื่น น้ำหนักโมเลกุลของโปรตีนมีขนาดใหญ่มาก ตั้งแต่หลายพันถึงหลายล้านดัลตัน ดังนั้นในระหว่างการปั่นแยกด้วยความเข้มข้นสูง โปรตีนจะถูกตกตะกอนและยิ่งไปกว่านั้นในอัตราที่ต่างกัน เนื่องจากการปรากฏตัวของกลุ่มที่มีประจุบวกและลบในโมเลกุลโปรตีน พวกมันจึงเคลื่อนที่ด้วยความเร็วที่แตกต่างกันในสนามไฟฟ้า นี่เป็นพื้นฐานของอิเล็กโตรโฟรีซิส ซึ่งเป็นวิธีการที่ใช้ในการแยกโปรตีนแต่ละชนิดออกจากสารผสมที่ซับซ้อน การทำให้โปรตีนบริสุทธิ์ยังดำเนินการโดยโครมาโตกราฟี
คุณสมบัติทางเคมี
โครงสร้าง.
โปรตีนเป็นโพลีเมอร์ กล่าวคือ โมเลกุลที่สร้างขึ้นเหมือนสายโซ่จากหน่วยมอนอเมอร์ซ้ำ หรือหน่วยย่อย ซึ่งมีบทบาทเล่นโดยกรดอัลฟา-อะมิโน สูตรทั่วไปของกรดอะมิโน
โดยที่ R คืออะตอมไฮโดรเจนหรือหมู่อินทรีย์บางกลุ่ม
โมเลกุลโปรตีน (สายโพลีเปปไทด์) อาจประกอบด้วยกรดอะมิโนจำนวนค่อนข้างน้อยหรือโมโนเมอร์หลายพันหน่วย การเชื่อมโยงของกรดอะมิโนในสายโซ่เป็นไปได้เนื่องจากแต่ละกลุ่มมีกลุ่มเคมีที่แตกต่างกันสองกลุ่ม: กลุ่มอะมิโนที่มีคุณสมบัติพื้นฐาน NH2 และกลุ่มคาร์บอกซิลที่เป็นกรด COOH ทั้งสองกลุ่มนี้ยึดติดกับอะตอมของคาร์บอน หมู่คาร์บอกซิลของกรดอะมิโนหนึ่งตัวสามารถสร้างพันธะเอไมด์ (เปปไทด์) กับหมู่อะมิโนของกรดอะมิโนอื่น:
หลังจากที่กรดอะมิโนสองชนิดเชื่อมต่อกันในลักษณะนี้แล้ว สามารถขยายสายโซ่ได้โดยการเพิ่มหนึ่งในสามของกรดอะมิโนที่สอง และอื่นๆ ดังที่เห็นได้จากสมการข้างต้น เมื่อเกิดพันธะเปปไทด์ โมเลกุลของน้ำจะถูกปลดปล่อยออกมา เมื่อมีกรด ด่าง หรือเอนไซม์โปรตีโอไลติก ปฏิกิริยาจะเกิดขึ้นในทิศทางตรงกันข้าม: สายโซ่โพลีเปปไทด์จะถูกแยกออกเป็นกรดอะมิโนด้วยการเติมน้ำ ปฏิกิริยานี้เรียกว่าไฮโดรไลซิส ไฮโดรไลซิสเกิดขึ้นเองตามธรรมชาติ และจำเป็นต้องใช้พลังงานในการรวมกรดอะมิโนเข้าเป็นสายพอลิเปปไทด์
หมู่คาร์บอกซิลและหมู่เอไมด์ (หรือหมู่อิไมด์ที่คล้ายกัน - ในกรณีของกรดอะมิโนโพรลีน) มีอยู่ในกรดอะมิโนทั้งหมด ในขณะที่ความแตกต่างระหว่างกรดอะมิโนจะถูกกำหนดโดยธรรมชาติของกลุ่มนั้นหรือ "ข้างเคียง" chain" ซึ่งแสดงไว้ด้านบนด้วยตัวอักษร R บทบาทของสายโซ่ด้านข้างสามารถเล่นได้โดยอะตอมของไฮโดรเจนหนึ่งอะตอม เช่น กรดอะมิโนไกลซีน และการจัดกลุ่มที่เทอะทะ เช่น ฮิสทิดีนและทริปโตเฟน โซ่ข้างบางชนิดมีความเฉื่อยทางเคมี ในขณะที่บางประเภทมีปฏิกิริยาตอบสนองสูง
สามารถสังเคราะห์กรดอะมิโนได้หลายพันชนิด และกรดอะมิโนหลายชนิดเกิดขึ้นในธรรมชาติ แต่มีกรดอะมิโนเพียง 20 ชนิดเท่านั้นที่ใช้สำหรับการสังเคราะห์โปรตีน ได้แก่ อะลานีน อาร์จินีน แอสปาราจีน กรดแอสปาร์ติก วาลีน ฮิสทิดีน ไกลซีน กลูตามีน กลูตามิก กรด, ไอโซลิวซีน, ลิวซีน, ไลซีน , เมไทโอนีน, โพรลีน, ซีรีน, ไทโรซีน, ทรีโอนีน, ทริปโตเฟน, ฟีนิลอะลานีนและซิสเทอีน (ในโปรตีน ซิสเทอีนอาจปรากฏเป็นไดเมอร์ - ซีสตีน) จริงอยู่ ในโปรตีนบางชนิดมีกรดอะมิโนอื่นๆ นอกเหนือไปจากกรดอะมิโน 20 ชนิดที่เกิดขึ้นเป็นประจำ แต่เกิดขึ้นจากการดัดแปลงใดๆ ใน 20 ชนิดที่ระบุไว้หลังจากที่รวมเข้ากับโปรตีนแล้ว
กิจกรรมทางแสง
กรดอะมิโนทั้งหมด ยกเว้นไกลซีน มีกลุ่มที่แตกต่างกันสี่กลุ่มติดอยู่กับอะตอม α-คาร์บอน ในแง่ของเรขาคณิต สี่กลุ่มที่แตกต่างกันสามารถติดได้สองวิธี และด้วยเหตุนี้จึงมีการกำหนดค่าที่เป็นไปได้สองแบบ หรือสองไอโซเมอร์ที่เกี่ยวข้องกันเป็นวัตถุกับภาพสะท้อนของมัน กล่าวคือ เหมือนมือซ้ายไปขวา การกำหนดค่าหนึ่งเรียกว่าซ้ายหรือมือซ้าย (L) และอีกรูปแบบหนึ่งคือมือขวาหรือมือขวา (D) เนื่องจากไอโซเมอร์ทั้งสองนั้นต่างกันในทิศทางการหมุนของระนาบของแสงโพลาไรซ์ กรดแอล-อะมิโนเท่านั้นที่เกิดขึ้นในโปรตีน (ยกเว้นไกลซีน มันสามารถแสดงได้ในรูปแบบเดียวเท่านั้น เนื่องจากสองกลุ่มจากสี่กลุ่มนั้นเหมือนกัน) และพวกมันทั้งหมดมีกิจกรรมทางแสง (เนื่องจากมีไอโซเมอร์เพียงตัวเดียว) กรด D-amino นั้นหายากในธรรมชาติ พบได้ในยาปฏิชีวนะบางชนิดและผนังเซลล์ของแบคทีเรีย
ลำดับของกรดอะมิโน
กรดอะมิโนในสายโซ่โพลีเปปไทด์ไม่ได้จัดเรียงแบบสุ่ม แต่อยู่ในลำดับที่แน่นอน และลำดับนี้กำหนดหน้าที่และคุณสมบัติของโปรตีน โดยการเรียงลำดับกรดอะมิโน 20 ชนิด คุณจะได้โปรตีนที่แตกต่างกันจำนวนมาก เช่นเดียวกับที่คุณสร้างข้อความต่างๆ มากมายจากตัวอักษรของตัวอักษร
ในอดีต การกำหนดลำดับกรดอะมิโนของโปรตีนมักใช้เวลาหลายปี การกำหนดโดยตรงยังคงเป็นงานที่ค่อนข้างลำบาก แม้ว่าจะมีการสร้างอุปกรณ์ที่อนุญาตให้ดำเนินการได้โดยอัตโนมัติ มักจะง่ายกว่าที่จะกำหนดลำดับนิวคลีโอไทด์ของยีนที่สอดคล้องกันและรับลำดับกรดอะมิโนของโปรตีนจากยีนนั้น จนถึงปัจจุบัน มีการกำหนดลำดับกรดอะมิโนของโปรตีนหลายร้อยชนิดแล้ว โดยปกติแล้วจะทราบหน้าที่ของโปรตีนถอดรหัส และช่วยให้จินตนาการถึงหน้าที่ที่เป็นไปได้ของโปรตีนที่คล้ายคลึงกันซึ่งก่อตัวขึ้น เช่น ในเนื้องอกที่เป็นมะเร็ง
โปรตีนที่ซับซ้อน
โปรตีนที่ประกอบด้วยกรดอะมิโนเท่านั้นเรียกว่าง่าย อย่างไรก็ตาม บ่อยครั้ง อะตอมของโลหะหรือสารประกอบทางเคมีบางชนิดที่ไม่ใช่กรดอะมิโนติดอยู่กับสายโพลีเปปไทด์ โปรตีนดังกล่าวเรียกว่าซับซ้อน ตัวอย่างคือเฮโมโกลบิน: ประกอบด้วยธาตุเหล็กพอร์ไฟริน ซึ่งทำให้มีสีแดงและทำหน้าที่เป็นตัวพาออกซิเจน
ชื่อของโปรตีนที่ซับซ้อนที่สุดมีตัวบ่งชี้ถึงลักษณะของกลุ่มที่แนบมา: น้ำตาลมีอยู่ในไกลโคโปรตีน, ไขมันในไลโปโปรตีน หากการเร่งปฏิกิริยาของเอนไซม์ขึ้นอยู่กับกลุ่มที่แนบมา เรียกว่า กลุ่มเทียม บ่อยครั้ง วิตามินบางชนิดมีบทบาทในกลุ่มเทียมหรือเป็นส่วนหนึ่งของมัน ตัวอย่างเช่น วิตามินเอที่ติดอยู่กับโปรตีนตัวใดตัวหนึ่งของเรตินา เป็นตัวกำหนดความไวต่อแสง
โครงสร้างระดับตติยภูมิ
สิ่งที่สำคัญไม่ใช่ลำดับกรดอะมิโนของโปรตีน (โครงสร้างหลัก) มากนัก แต่วิธีการวางในช่องว่าง ตลอดความยาวทั้งหมดของสายพอลิเปปไทด์ ไอออนของไฮโดรเจนจะก่อตัวเป็นพันธะไฮโดรเจนแบบปกติ ซึ่งทำให้มีรูปร่างเป็นเกลียวหรือชั้น (โครงสร้างทุติยภูมิ) จากการรวมกันของเกลียวและชั้นดังกล่าวรูปแบบที่กะทัดรัดของลำดับถัดไปเกิดขึ้น - โครงสร้างระดับอุดมศึกษาของโปรตีน รอบพันธะที่ยึดตัวเชื่อมแบบโมโนเมอร์ของโซ่ สามารถหมุนผ่านมุมเล็กๆ ได้ ดังนั้น จากมุมมองทางเรขาคณิตล้วนๆ จำนวนของโครงแบบที่เป็นไปได้สำหรับสายพอลิเปปไทด์ใดๆ จึงมีขนาดใหญ่อย่างไม่สิ้นสุด ในความเป็นจริง โปรตีนแต่ละชนิดมีอยู่ในรูปแบบเดียวเท่านั้น กำหนดโดยลำดับกรดอะมิโนของมัน โครงสร้างนี้ไม่แข็งกระด้าง ดูเหมือนว่าจะ "หายใจ" - มันแกว่งไปมารอบ ๆ การกำหนดค่าเฉลี่ยบางอย่าง โซ่ถูกพับเป็นรูปแบบที่พลังงานอิสระ (ความสามารถในการทำงาน) น้อยที่สุด เช่นเดียวกับสปริงที่ปล่อยออกมาจะถูกบีบอัดให้อยู่ในสถานะที่สอดคล้องกับพลังงานอิสระขั้นต่ำเท่านั้น บ่อยครั้ง ส่วนหนึ่งของห่วงโซ่เชื่อมโยงอย่างแน่นหนากับอีกส่วนหนึ่งโดยพันธะไดซัลไฟด์ (–S–S–) ระหว่างซิสเตอีนตกค้างสองตัว นี่เป็นส่วนหนึ่งที่ว่าทำไมซิสเทอีนในกรดอะมิโนจึงมีบทบาทสำคัญอย่างยิ่ง
ความซับซ้อนของโครงสร้างของโปรตีนนั้นยิ่งใหญ่มากจนยังไม่สามารถคำนวณโครงสร้างระดับอุดมศึกษาของโปรตีนได้ แม้ว่าจะทราบลำดับกรดอะมิโนของโปรตีนก็ตาม แต่ถ้าเป็นไปได้ที่จะได้ผลึกโปรตีน โครงสร้างระดับอุดมศึกษาสามารถกำหนดได้โดยการเลี้ยวเบนของรังสีเอกซ์
ในโครงสร้าง หดตัว และโปรตีนอื่น ๆ โซ่จะยาวและโซ่พับเล็กน้อยหลายเส้นวางเรียงต่อกันเป็นเส้นใย ในทางกลับกันเส้นใยก็พับเป็นรูปแบบที่ใหญ่ขึ้น - เส้นใย อย่างไรก็ตาม โปรตีนส่วนใหญ่ในสารละลายมีลักษณะเป็นทรงกลม: โซ่จะพันเป็นทรงกลม เหมือนเส้นด้ายในลูกบอล พลังงานอิสระที่มีการกำหนดค่านี้มีน้อยมาก เนื่องจากกรดอะมิโนที่ไม่ชอบน้ำ ("การกันน้ำ") ถูกซ่อนอยู่ภายในทรงกลม และกรดอะมิโนที่ชอบน้ำ ("ดึงดูดน้ำ") อยู่บนผิวของมัน
โปรตีนหลายชนิดเป็นสารประกอบเชิงซ้อนของสายโซ่โพลีเปปไทด์หลายสาย โครงสร้างนี้เรียกว่าโครงสร้างควอเทอร์นารีของโปรตีน ตัวอย่างเช่น โมเลกุลของเฮโมโกลบินประกอบด้วยหน่วยย่อยสี่หน่วย ซึ่งแต่ละหน่วยเป็นโปรตีนทรงกลม
โปรตีนที่มีโครงสร้างเนื่องจากโครงร่างเชิงเส้นของพวกมันสร้างเส้นใยซึ่งมีความต้านทานแรงดึงสูงมาก ในขณะที่โครงแบบทรงกลมช่วยให้โปรตีนเข้าสู่ปฏิกิริยาจำเพาะกับสารประกอบอื่นๆ บนพื้นผิวของทรงกลมด้วยการวางโซ่ที่ถูกต้องฟันผุของรูปร่างบางอย่างจะปรากฏขึ้นซึ่งมีกลุ่มเคมีปฏิกิริยาอยู่ หากโปรตีนนี้เป็นเอ็นไซม์ โมเลกุลของสารบางชนิดที่ปกติแล้วจะมีขนาดเล็กกว่าจะเข้าสู่โพรงดังกล่าว เช่นเดียวกับที่กุญแจเข้าสู่ตัวล็อค ในกรณีนี้ โครงร่างของเมฆอิเล็กตรอนของโมเลกุลจะเปลี่ยนแปลงภายใต้อิทธิพลของกลุ่มเคมีที่อยู่ในโพรง และสิ่งนี้บังคับให้มันทำปฏิกิริยาในทางใดทางหนึ่ง ด้วยวิธีนี้เอนไซม์จะเร่งปฏิกิริยา โมเลกุลของแอนติบอดียังมีโพรงซึ่งสารแปลกปลอมต่างๆ จับตัวกันและด้วยเหตุนี้จึงทำให้ไม่มีอันตราย โมเดล "กุญแจและล็อค" ซึ่งอธิบายปฏิสัมพันธ์ของโปรตีนกับสารประกอบอื่นๆ ทำให้สามารถเข้าใจความจำเพาะของเอนไซม์และแอนติบอดี กล่าวคือ ความสามารถในการทำปฏิกิริยากับสารประกอบบางชนิดเท่านั้น
โปรตีนในสิ่งมีชีวิตประเภทต่างๆ
โปรตีนที่ทำหน้าที่เหมือนกันในพืชและสัตว์ต่างชนิดกัน ดังนั้นจึงมีชื่อเดียวกันก็มีรูปแบบที่คล้ายคลึงกัน อย่างไรก็ตาม พวกมันแตกต่างกันบ้างในลำดับกรดอะมิโน เมื่อสปีชีส์แยกตัวจากบรรพบุรุษร่วมกัน กรดอะมิโนบางตัวในบางตำแหน่งจะถูกแทนที่ด้วยการกลายพันธุ์ด้วยกรดอะมิโนอื่นๆ การกลายพันธุ์ที่เป็นอันตรายซึ่งทำให้เกิดโรคทางพันธุกรรมจะถูกละทิ้งโดยการคัดเลือกโดยธรรมชาติ แต่สามารถรักษาสิ่งที่เป็นประโยชน์หรืออย่างน้อยก็เป็นกลางได้ ยิ่งสปีชีส์ทางชีวภาพใกล้กันมากเท่าไร โปรตีนของพวกมันก็จะยิ่งมีความแตกต่างกันน้อยลงเท่านั้น
โปรตีนบางชนิดเปลี่ยนแปลงได้ค่อนข้างเร็ว ส่วนโปรตีนบางชนิดค่อนข้างอนุรักษ์นิยม อย่างหลังรวมถึงตัวอย่างเช่น cytochrome c ซึ่งเป็นเอ็นไซม์ระบบทางเดินหายใจที่พบในสิ่งมีชีวิตส่วนใหญ่ ในมนุษย์และลิงชิมแปนซี ลำดับกรดอะมิโนของมันจะเหมือนกัน ในขณะที่ในไซโตโครมซีของข้าวสาลี มีกรดอะมิโนเพียง 38% เท่านั้นที่มีความแตกต่างกัน แม้เมื่อเปรียบเทียบมนุษย์กับแบคทีเรีย ความคล้ายคลึงของไซโตโครมกับ (ความแตกต่างในที่นี้ส่งผลต่อกรดอะมิโน 65%) ยังคงมองเห็นได้ แม้ว่าบรรพบุรุษร่วมกันของแบคทีเรียและมนุษย์จะอาศัยอยู่บนโลกเมื่อประมาณสองพันล้านปีก่อน ทุกวันนี้ การเปรียบเทียบลำดับกรดอะมิโนมักถูกใช้เพื่อสร้างต้นไม้สายวิวัฒนาการ (ลำดับวงศ์ตระกูล) ที่สะท้อนถึงความสัมพันธ์เชิงวิวัฒนาการระหว่างสิ่งมีชีวิตต่างๆ
การเสื่อมสภาพ
โมเลกุลโปรตีนสังเคราะห์ที่พับเก็บได้มาซึ่งโครงร่างของมันเอง อย่างไรก็ตาม การกำหนดค่านี้สามารถทำลายได้ด้วยการให้ความร้อน โดยการเปลี่ยนค่า pH โดยการกระทำของตัวทำละลายอินทรีย์ และแม้กระทั่งโดยการกวนสารละลายจนเกิดฟองอากาศปรากฏขึ้นบนพื้นผิว โปรตีนที่เปลี่ยนแปลงในลักษณะนี้เรียกว่า denatured; มันสูญเสียกิจกรรมทางชีวภาพและมักจะไม่ละลายน้ำ ตัวอย่างที่รู้จักกันดีของโปรตีนที่ทำให้เสียสภาพ ได้แก่ ไข่ต้มหรือวิปครีม โปรตีนขนาดเล็กที่มีกรดอะมิโนเพียงร้อยตัวเท่านั้นที่สามารถสร้างขึ้นใหม่ได้ กล่าวคือ รับการกำหนดค่าเดิมอีกครั้ง แต่โปรตีนส่วนใหญ่นั้นถูกแปลงสภาพเป็นมวลของสายโซ่โพลีเปปไทด์ที่พันกันและไม่คืนค่าโครงสร้างเดิมของพวกมัน
ปัญหาหลักประการหนึ่งในการแยกโปรตีนที่ออกฤทธิ์คือความไวสูงต่อการเสียสภาพ คุณสมบัติของโปรตีนพบว่ามีประโยชน์ในการถนอมผลิตภัณฑ์อาหาร: อุณหภูมิสูงจะทำให้เอนไซม์ของจุลินทรีย์เปลี่ยนแปลงสภาพไปอย่างถาวร และจุลินทรีย์ก็ตาย
การสังเคราะห์โปรตีน
สำหรับการสังเคราะห์โปรตีน สิ่งมีชีวิตต้องมีระบบของเอ็นไซม์ที่สามารถเชื่อมกรดอะมิโนตัวหนึ่งเข้ากับอีกตัวหนึ่งได้ จำเป็นต้องมีแหล่งข้อมูลเพื่อกำหนดกรดอะมิโนที่ควรเชื่อมต่อ เนื่องจากมีโปรตีนหลายพันชนิดในร่างกาย และแต่ละชนิดประกอบด้วยกรดอะมิโนหลายร้อยชนิดโดยเฉลี่ย ข้อมูลที่ต้องการจึงต้องมีปริมาณมหาศาลอย่างแท้จริง มันถูกเก็บไว้ (คล้ายกับวิธีที่บันทึกถูกเก็บไว้ในเทปแม่เหล็ก) ในโมเลกุลของกรดนิวคลีอิกที่ประกอบขึ้นเป็นยีน
การกระตุ้นเอนไซม์
สายโซ่โพลีเปปไทด์ที่สังเคราะห์จากกรดอะมิโนไม่ใช่โปรตีนในรูปแบบสุดท้ายเสมอไป เอนไซม์จำนวนมากถูกสังเคราะห์ขึ้นเป็นครั้งแรกในฐานะสารตั้งต้นที่ไม่ใช้งานและจะทำงานได้ก็ต่อเมื่อเอ็นไซม์อื่นกำจัดกรดอะมิโนสองสามตัวออกจากปลายด้านหนึ่งของสายโซ่เท่านั้น เอนไซม์ย่อยอาหารบางชนิด เช่น ทริปซิน ถูกสังเคราะห์ในรูปแบบที่ไม่ใช้งานนี้ เอนไซม์เหล่านี้ถูกกระตุ้นในทางเดินอาหารอันเป็นผลมาจากการกำจัดส่วนปลายของโซ่ ฮอร์โมนอินซูลิน ซึ่งโมเลกุลในรูปแบบแอคทีฟประกอบด้วยสายสั้นสองสาย ถูกสังเคราะห์ในรูปของสายโซ่เดียวที่เรียกว่า อินซูลิน จากนั้นส่วนตรงกลางของสายโซ่นี้จะถูกลบออกและชิ้นส่วนที่เหลือจะเกาะติดกันสร้างโมเลกุลของฮอร์โมนที่ใช้งานอยู่ โปรตีนเชิงซ้อนจะเกิดขึ้นหลังจากที่กลุ่มเคมีบางกลุ่มยึดติดกับโปรตีนเท่านั้นและสิ่งที่แนบมานี้มักต้องใช้เอนไซม์ด้วย
การไหลเวียนของเมตาบอลิ
หลังจากให้อาหารสัตว์ด้วยกรดอะมิโนที่ติดฉลากด้วยไอโซโทปกัมมันตภาพรังสีของคาร์บอน ไนโตรเจน หรือไฮโดรเจน ฉลากจะถูกรวมเข้ากับโปรตีนอย่างรวดเร็ว หากกรดอะมิโนที่ติดฉลากหยุดเข้าสู่ร่างกาย ปริมาณของฉลากในโปรตีนจะเริ่มลดลง การทดลองเหล่านี้แสดงให้เห็นว่าโปรตีนที่เกิดขึ้นจะไม่ถูกเก็บไว้ในร่างกายจนกว่าจะสิ้นสุดชีวิต ทั้งหมดมีข้อยกเว้นบางประการ อยู่ในสถานะไดนามิก สลายตัวเป็นกรดอะมิโนอย่างต่อเนื่อง แล้วสังเคราะห์ใหม่อีกครั้ง
โปรตีนบางชนิดสลายตัวเมื่อเซลล์ตายและถูกทำลาย สิ่งนี้เกิดขึ้นตลอดเวลา ตัวอย่างเช่น กับเซลล์เม็ดเลือดแดงและเซลล์เยื่อบุผิวที่บุผิวด้านในของลำไส้ นอกจากนี้ การสลายและการสังเคราะห์โปรตีนยังเกิดขึ้นในเซลล์ที่มีชีวิตอีกด้วย น่าแปลกที่ไม่มีใครรู้เกี่ยวกับการสลายโปรตีนมากกว่าเรื่องการสังเคราะห์ อย่างไรก็ตาม สิ่งที่ชัดเจนก็คือ เอ็นไซม์โปรตีโอไลติกมีส่วนในการสลาย คล้ายกับเอนไซม์ที่สลายโปรตีนให้เป็นกรดอะมิโนในทางเดินอาหาร
ครึ่งชีวิตของโปรตีนต่างกัน - จากหลายชั่วโมงถึงหลายเดือน ข้อยกเว้นเพียงอย่างเดียวคือโมเลกุลคอลลาเจน เมื่อก่อตัวแล้วจะคงตัวและไม่มีการต่ออายุหรือเปลี่ยนใหม่ อย่างไรก็ตาม เมื่อเวลาผ่านไป คุณสมบัติบางอย่าง โดยเฉพาะอย่างยิ่ง ความยืดหยุ่น การเปลี่ยนแปลง และเนื่องจากไม่มีการต่ออายุ การเปลี่ยนแปลงบางอย่างที่เกี่ยวข้องกับอายุเป็นผลมาจากสิ่งนี้ ตัวอย่างเช่น การปรากฏตัวของริ้วรอยบนผิวหนัง
โปรตีนสังเคราะห์
นักเคมีได้เรียนรู้วิธีผสมกรดอะมิโนมานานแล้ว แต่กรดอะมิโนจะรวมกันแบบสุ่ม เพื่อให้ผลิตภัณฑ์ของโพลิเมอไรเซชันดังกล่าวมีความคล้ายคลึงกับกรดตามธรรมชาติเพียงเล็กน้อย จริงอยู่ เป็นไปได้ที่จะรวมกรดอะมิโนตามลำดับที่กำหนด ซึ่งทำให้สามารถรับโปรตีนที่ออกฤทธิ์ทางชีวภาพได้ โดยเฉพาะอย่างยิ่งอินซูลิน กระบวนการนี้ค่อนข้างซับซ้อน และด้วยวิธีนี้ เป็นไปได้ที่จะได้รับเฉพาะโปรตีนที่มีโมเลกุลประกอบด้วยกรดอะมิโนประมาณร้อยตัวเท่านั้น เป็นที่พึงประสงค์แทนที่จะสังเคราะห์หรือแยกลำดับนิวคลีโอไทด์ของยีนที่สอดคล้องกับลำดับกรดอะมิโนที่ต้องการ และจากนั้นนำเข้ายีนนี้ไปในแบคทีเรีย ซึ่งจะผลิตขึ้นโดยการทำซ้ำผลิตภัณฑ์ที่ต้องการเป็นจำนวนมาก อย่างไรก็ตาม วิธีนี้ก็มีข้อเสียเช่นกัน
โปรตีนและโภชนาการ
เมื่อโปรตีนในร่างกายแตกตัวเป็นกรดอะมิโน กรดอะมิโนเหล่านี้สามารถนำกลับมาใช้ใหม่สำหรับการสังเคราะห์โปรตีนได้ ในเวลาเดียวกัน กรดอะมิโนเองก็อาจสลายตัวได้ เพื่อที่จะได้ใช้ประโยชน์ไม่เต็มที่ เป็นที่ชัดเจนว่าในระหว่างการเจริญเติบโต การตั้งครรภ์ และการรักษาบาดแผล การสังเคราะห์โปรตีนจะต้องเกินการย่อยสลาย ร่างกายสูญเสียโปรตีนบางส่วนอย่างต่อเนื่อง เหล่านี้คือโปรตีนของเส้นผม เล็บ และชั้นผิวของผิวหนัง ดังนั้นการสังเคราะห์โปรตีนแต่ละสิ่งมีชีวิตจะต้องได้รับกรดอะมิโนจากอาหาร
แหล่งของกรดอะมิโน
พืชสีเขียวสังเคราะห์กรดอะมิโนทั้งหมด 20 ชนิดที่พบในโปรตีนจากคาร์บอนไดออกไซด์ น้ำ และแอมโมเนียหรือไนเตรต แบคทีเรียจำนวนมากยังสามารถสังเคราะห์กรดอะมิโนเมื่อมีน้ำตาล (หรือเทียบเท่า) และไนโตรเจนคงที่ แต่สุดท้ายแล้วน้ำตาลก็มาจากพืชสีเขียว ในสัตว์ ความสามารถในการสังเคราะห์กรดอะมิโนมีจำกัด พวกเขาได้รับกรดอะมิโนจากการกินพืชสีเขียวหรือสัตว์อื่นๆ ในทางเดินอาหารโปรตีนที่ดูดซึมจะถูกแบ่งออกเป็นกรดอะมิโนส่วนหลังจะถูกดูดซึมและลักษณะโปรตีนของสิ่งมีชีวิตที่กำหนดนั้นถูกสร้างขึ้นจากพวกมัน ไม่มีโปรตีนที่ดูดซึมรวมอยู่ในโครงสร้างของร่างกายเช่นนี้ ข้อยกเว้นเพียงอย่างเดียวคือในสัตว์เลี้ยงลูกด้วยนมหลายชนิด ส่วนหนึ่งของแอนติบอดีของมารดาสามารถส่งผ่านรกไปยังระบบไหลเวียนของทารกในครรภ์ได้ครบถ้วน และผ่านน้ำนมมารดา (โดยเฉพาะในสัตว์เคี้ยวเอื้อง) ไปยังทารกแรกเกิดทันทีหลังคลอด
ต้องการโปรตีน.
เป็นที่ชัดเจนว่าเพื่อรักษาชีวิต ร่างกายจะต้องได้รับโปรตีนจากอาหารจำนวนหนึ่ง อย่างไรก็ตาม ขนาดของความต้องการนี้ขึ้นอยู่กับปัจจัยหลายประการ ร่างกายต้องการอาหารทั้งเป็นแหล่งพลังงาน (แคลอรี) และเป็นวัสดุในการสร้างโครงสร้าง ประการแรกคือความต้องการพลังงาน ซึ่งหมายความว่าเมื่อมีคาร์โบไฮเดรตและไขมันเพียงเล็กน้อยในอาหาร โปรตีนในอาหารจะไม่ถูกนำมาใช้เพื่อการสังเคราะห์โปรตีนของตัวเอง แต่เป็นแหล่งของแคลอรี ด้วยการอดอาหารเป็นเวลานาน แม้แต่โปรตีนของคุณเองก็ยังถูกใช้เพื่อตอบสนองความต้องการพลังงาน หากอาหารมีคาร์โบไฮเดรตเพียงพอ ปริมาณโปรตีนจะลดลง
ความสมดุลของไนโตรเจน
โดยเฉลี่ยประมาณ 16% ของมวลโปรตีนทั้งหมดคือไนโตรเจน เมื่อกรดอะมิโนที่ประกอบเป็นโปรตีนถูกทำลายลง ไนโตรเจนที่มีอยู่ในกรดจะถูกขับออกจากร่างกายในปัสสาวะและ (ในระดับที่น้อยกว่า) ในอุจจาระในรูปของสารประกอบไนโตรเจนต่างๆ ดังนั้นจึงสะดวกที่จะใช้ตัวบ่งชี้เช่นสมดุลไนโตรเจนเพื่อประเมินคุณภาพของสารอาหารโปรตีนเช่น ความแตกต่าง (เป็นกรัม) ระหว่างปริมาณไนโตรเจนที่เข้าสู่ร่างกายและปริมาณไนโตรเจนที่ขับออกมาต่อวัน ด้วยโภชนาการปกติในผู้ใหญ่ ปริมาณเหล่านี้จะเท่ากัน ในสิ่งมีชีวิตที่กำลังเติบโต ปริมาณไนโตรเจนที่ขับออกมาจะน้อยกว่าปริมาณที่เข้ามา กล่าวคือ ยอดคงเหลือเป็นบวก ด้วยการขาดโปรตีนในอาหาร ความสมดุลจึงเป็นลบ หากอาหารมีแคลอรีเพียงพอ แต่ไม่มีโปรตีนอยู่ในนั้น ร่างกายก็จะเก็บโปรตีนไว้ ในขณะเดียวกัน เมแทบอลิซึมของโปรตีนก็ช้าลง และการนำกรดอะมิโนกลับมาใช้ใหม่ในการสังเคราะห์โปรตีนก็ดำเนินไปอย่างมีประสิทธิภาพมากที่สุด อย่างไรก็ตามการสูญเสียเป็นสิ่งที่หลีกเลี่ยงไม่ได้และสารประกอบไนโตรเจนยังคงถูกขับออกทางปัสสาวะและบางส่วนในอุจจาระ ปริมาณไนโตรเจนที่ขับออกจากร่างกายต่อวันในช่วงที่ขาดโปรตีนสามารถทำหน้าที่เป็นตัววัดการขาดโปรตีนในแต่ละวัน เป็นเรื่องปกติที่จะสันนิษฐานว่าโดยการแนะนำปริมาณโปรตีนที่เทียบเท่ากับการขาดสารอาหารนี้เข้าไปในอาหาร เป็นไปได้ที่จะฟื้นฟูสมดุลของไนโตรเจน อย่างไรก็ตามมันไม่ใช่ เมื่อได้รับโปรตีนในปริมาณนี้ ร่างกายจะเริ่มใช้กรดอะมิโนอย่างมีประสิทธิภาพน้อยลง ดังนั้นจึงจำเป็นต้องมีโปรตีนเพิ่มเติมเพื่อคืนความสมดุลของไนโตรเจน
หากปริมาณโปรตีนในอาหารเกินความจำเป็นในการรักษาสมดุลของไนโตรเจน ดูเหมือนว่าจะไม่มีอันตรายจากสิ่งนี้ กรดอะมิโนที่มากเกินไปนั้นถูกใช้เป็นแหล่งพลังงานเพียงอย่างเดียว ตัวอย่างที่โดดเด่นเป็นพิเศษคือชาวเอสกิโมซึ่งกินคาร์โบไฮเดรตเพียงเล็กน้อยและมีโปรตีนมากกว่าที่จำเป็นเพื่อรักษาสมดุลของไนโตรเจนประมาณสิบเท่า อย่างไรก็ตาม ในกรณีส่วนใหญ่ การใช้โปรตีนเป็นแหล่งพลังงานไม่เป็นประโยชน์ เนื่องจากคุณสามารถได้รับแคลอรีจากคาร์โบไฮเดรตในปริมาณที่กำหนดมากกว่าโปรตีนในปริมาณเท่ากัน ในประเทศยากจน ประชากรจะได้รับแคลอรี่ที่จำเป็นจากคาร์โบไฮเดรตและบริโภคโปรตีนในปริมาณที่น้อยที่สุด
หากร่างกายได้รับแคลอรี่ตามจำนวนที่ต้องการในรูปของผลิตภัณฑ์ที่ไม่ใช่โปรตีน ปริมาณโปรตีนขั้นต่ำที่ช่วยรักษาสมดุลของไนโตรเจนจะอยู่ที่ประมาณ 30 กรัมต่อวัน ในขนมปังสี่ชิ้นหรือนม 0.5 ลิตรมีโปรตีนอยู่ประมาณเท่าๆ กัน ปริมาณที่มากกว่าเล็กน้อยมักจะถือว่าเหมาะสมที่สุด แนะนำตั้งแต่ 50 ถึง 70 กรัม
กรดอะมิโนที่จำเป็น
จนถึงปัจจุบันนี้ถือว่าโปรตีนโดยรวมแล้ว ในขณะเดียวกัน เพื่อให้เกิดการสังเคราะห์โปรตีน กรดอะมิโนที่จำเป็นทั้งหมดต้องมีอยู่ในร่างกาย กรดอะมิโนบางชนิดที่ร่างกายของสัตว์สามารถสังเคราะห์ได้ พวกเขาเรียกว่าแทนกันได้เนื่องจากไม่จำเป็นต้องมีอยู่ในอาหาร - เป็นสิ่งสำคัญเท่านั้นโดยทั่วไปการบริโภคโปรตีนเป็นแหล่งไนโตรเจนก็เพียงพอแล้ว เมื่อขาดกรดอะมิโนที่จำเป็น ร่างกายสามารถสังเคราะห์กรดอะมิโนเหล่านี้ได้โดยใช้ค่ากรดอะมิโนที่มากเกินไป กรดอะมิโน "จำเป็น" ที่เหลืออยู่ไม่สามารถสังเคราะห์ได้และต้องกินเข้าไปพร้อมกับอาหาร สิ่งจำเป็นสำหรับมนุษย์ ได้แก่ วาลีน ลิวซีน ไอโซลิวซีน ทรีโอนีน เมไทโอนีน ฟีนิลอะลานีน ทริปโตเฟน ฮิสทิดีน ไลซีน และอาร์จินีน (แม้ว่าอาร์จินีนสามารถสังเคราะห์ในร่างกายได้ แต่ก็ถือว่าเป็นกรดอะมิโนที่จำเป็น เนื่องจากทารกแรกเกิดและเด็กที่กำลังเติบโตผลิตในปริมาณที่ไม่เพียงพอ ในทางกลับกัน สำหรับผู้ที่มีอายุมากแล้ว การบริโภคกรดอะมิโนเหล่านี้บางส่วนจากอาหาร อาจเป็นทางเลือก)
รายชื่อกรดอะมิโนที่จำเป็นนี้มีความใกล้เคียงกันในสัตว์มีกระดูกสันหลังอื่นๆ และแม้แต่ในแมลง คุณค่าทางโภชนาการของโปรตีนมักจะถูกกำหนดโดยการให้อาหารแก่หนูที่กำลังเติบโตและการติดตามน้ำหนักที่เพิ่มขึ้นของสัตว์
คุณค่าทางโภชนาการของโปรตีน
คุณค่าทางโภชนาการของโปรตีนถูกกำหนดโดยกรดอะมิโนที่จำเป็นซึ่งขาดมากที่สุด ลองอธิบายสิ่งนี้ด้วยตัวอย่าง โปรตีนในร่างกายของเรามีค่าเฉลี่ยประมาณ ทริปโตเฟน 2% (โดยน้ำหนัก) สมมติว่าอาหารประกอบด้วยโปรตีน 10 กรัมที่มีทริปโตเฟน 1% และมีกรดอะมิโนที่จำเป็นอื่นๆ เพียงพอ ในกรณีของเรา โปรตีนที่มีข้อบกพร่อง 10 กรัมนี้เทียบเท่ากับโปรตีนที่สมบูรณ์ 5 กรัม ส่วนที่เหลืออีก 5 กรัมสามารถทำหน้าที่เป็นแหล่งพลังงานเท่านั้น โปรดทราบว่าเนื่องจากกรดอะมิโนไม่ได้ถูกเก็บไว้ในร่างกาย และเพื่อให้เกิดการสังเคราะห์โปรตีน กรดอะมิโนทั้งหมดจะต้องมีอยู่พร้อม ๆ กัน ผลของการบริโภคกรดอะมิโนที่จำเป็นสามารถตรวจพบได้ก็ต่อเมื่อทั้งหมดเข้าสู่ ร่างกายไปพร้อม ๆ กัน
องค์ประกอบโดยเฉลี่ยของโปรตีนจากสัตว์ส่วนใหญ่นั้นใกล้เคียงกับองค์ประกอบโดยเฉลี่ยของโปรตีนในร่างกายมนุษย์ ดังนั้นเราจึงไม่น่าจะเผชิญกับการขาดกรดอะมิโนหากอาหารของเราอุดมไปด้วยอาหาร เช่น เนื้อสัตว์ ไข่ นม และชีส อย่างไรก็ตาม มีโปรตีน เช่น เจลาติน (ผลิตภัณฑ์จากการเสื่อมสภาพของคอลลาเจน) ซึ่งมีกรดอะมิโนที่จำเป็นน้อยมาก โปรตีนจากพืชแม้ว่าจะดีกว่าเจลาตินในแง่นี้ แต่ก็มีกรดอะมิโนที่จำเป็นต่ำเช่นกัน โดยเฉพาะอย่างยิ่งไลซีนและทริปโตเฟนเพียงเล็กน้อย อย่างไรก็ตาม การรับประทานอาหารมังสวิรัติล้วนไม่เป็นอันตรายเลย เว้นแต่จะกินโปรตีนจากพืชในปริมาณที่มากกว่าเล็กน้อย ซึ่งเพียงพอที่จะให้กรดอะมิโนที่จำเป็นแก่ร่างกาย โปรตีนส่วนใหญ่พบได้ในพืชในเมล็ดพืช โดยเฉพาะในเมล็ดข้าวสาลีและพืชตระกูลถั่วต่างๆ หน่ออ่อน เช่น หน่อไม้ฝรั่ง ก็อุดมไปด้วยโปรตีนเช่นกัน
โปรตีนสังเคราะห์ในอาหาร
การเพิ่มกรดอะมิโนจำเป็นสังเคราะห์หรือโปรตีนที่อุดมไปด้วยโปรตีนในปริมาณเล็กน้อยลงในโปรตีนที่ไม่สมบูรณ์ เช่น โปรตีนจากข้าวโพด ทำให้สามารถเพิ่มคุณค่าทางโภชนาการของโปรตีนชนิดหลังได้อย่างมีนัยสำคัญ กล่าวคือ จึงเป็นการเพิ่มปริมาณโปรตีนที่บริโภค ความเป็นไปได้อีกประการหนึ่งคือการปลูกแบคทีเรียหรือยีสต์บนปิโตรเลียมไฮโดรคาร์บอนด้วยการเติมไนเตรตหรือแอมโมเนียเป็นแหล่งไนโตรเจน โปรตีนจุลินทรีย์ที่ได้จากวิธีนี้สามารถใช้เป็นอาหารสำหรับสัตว์ปีกหรือปศุสัตว์ หรือมนุษย์สามารถบริโภคได้โดยตรง วิธีที่สามที่ใช้กันอย่างแพร่หลายใช้สรีรวิทยาของสัตว์เคี้ยวเอื้อง ในสัตว์เคี้ยวเอื้องในตอนต้นของกระเพาะที่เรียกว่า กระเพาะรูเมนเป็นที่อยู่อาศัยของแบคทีเรียและโปรโตซัวรูปแบบพิเศษที่เปลี่ยนโปรตีนจากพืชที่บกพร่องให้กลายเป็นโปรตีนจุลินทรีย์ที่สมบูรณ์มากขึ้น และในทางกลับกัน หลังจากการย่อยและการดูดซึม จะกลายเป็นโปรตีนจากสัตว์ ยูเรียซึ่งเป็นสารประกอบที่มีไนโตรเจนสังเคราะห์ราคาถูกสามารถเติมลงในอาหารปศุสัตว์ได้ จุลินทรีย์ที่อาศัยอยู่ในกระเพาะรูเมนใช้ยูเรียไนโตรเจนเพื่อเปลี่ยนคาร์โบไฮเดรต (ซึ่งมีมากกว่าในอาหาร) ให้เป็นโปรตีน ประมาณหนึ่งในสามของไนโตรเจนทั้งหมดในอาหารปศุสัตว์สามารถมาในรูปของยูเรียซึ่งในสาระสำคัญหมายถึงการสังเคราะห์โปรตีนทางเคมีในระดับหนึ่ง
 ลุงวันยา พล็อตเรื่อง “ลุงอีวาน ทัศนคติต่ออาจารย์ของผู้อื่น
ลุงวันยา พล็อตเรื่อง “ลุงอีวาน ทัศนคติต่ออาจารย์ของผู้อื่น Tsakhes น้อยชื่อเล่น Zinnober
Tsakhes น้อยชื่อเล่น Zinnober Maikov, Apollon Nikolaevich - ชีวประวัติสั้น
Maikov, Apollon Nikolaevich - ชีวประวัติสั้น