สมการน้ำแมงกานีส. สูตรเคมีโครงสร้างแมงกานีส
แมงกานีสเป็นโลหะที่มีคุณค่าสำหรับมนุษย์
คุณสมบัติทางเคมีของแมงกานีสเป็นตัวกำหนดการใช้อย่างแพร่หลายในฐานะวัตถุดิบสำหรับการผลิตโลหะผสมคุณภาพสูงในเชิงอุตสาหกรรม สารประกอบของธาตุใช้ในการแพทย์และการเกษตร
สมบัติทางกายภาพและเคมีของโลหะ
- เป็นครั้งแรกที่นักเคมีชาวสวีเดนค้นพบองค์ประกอบทางเคมีในแร่เหล็ก มันถูกสกัดโดยการให้ความร้อนส่วนผสมของวัสดุแร่กับถ่านหิน เป็นผลให้ได้ชิ้นส่วนโลหะกลับคืนมา ซึ่งได้ชื่อมาจากคำภาษาเยอรมันที่แปลว่า "แร่แมงกานีส"
- องค์ประกอบทางเคมีอยู่ในกลุ่มหัวเปลี่ยนผ่านจำนวนหนึ่งและสามารถสร้างสารประกอบที่มีอะตอมในสถานะออกซิเดชัน 0 เมื่อได้รับความร้อน จะแสดงคุณสมบัติในการแทนที่ไฮโดรเจนและสลายตัวของน้ำ
- โดยธรรมชาติแล้ว โลหะที่เปราะนี้มีลักษณะสีเงิน พบได้เฉพาะในสารประกอบเท่านั้น สกัดจากวัตถุดิบแร่ ซึ่งพบได้ทั่วไปในประเภทต่อไปนี้: ไพโรลูไซต์ แมงกาไนต์ ไซโลเมเลน บราวไนต์
- โลหะนี้พบในก้อนแมงกานีสที่ก้นมหาสมุทร เทคโนโลยีในการสกัดจากด้านล่างเกี่ยวข้องกับการใช้อุปกรณ์พิเศษและไม่ใช่ลักษณะทางอุตสาหกรรม
- แมงกานีสก่อตัวเป็นออกไซด์ได้ง่ายอันเป็นผลมาจากปฏิกิริยาออกซิเดชั่นในอากาศ ขึ้นอยู่กับการเปลี่ยนแปลงของการไล่ระดับอุณหภูมิระหว่างการให้ความร้อน มันทำปฏิกิริยากับไนโตรเจน กำมะถัน ซิลิกอน เมื่อไฮโดรเจนถูกดูดซับ แมงกานีสจะสร้างสารละลายที่เป็นของแข็ง
- ยากที่จะละลายในน้ำที่อุณหภูมิห้องธรรมดา ในกรดเข้มข้น จะละลายเมื่อถูกความร้อน เกิดเป็นเกลือ
- องค์ประกอบทางเคมีหมายเลข 25 นั้นแตกต่างจากกิจกรรมในกระบวนการของปฏิกิริยาการลดโลหะจากออกไซด์ มันแทนที่โลหะโดยสร้างสารประกอบด้วยออกซิเจน
เทคโนโลยีการสกัดองค์ประกอบทางเคมี
ผู้ผลิตและซัพพลายเออร์หลักสำหรับโลหะสู่ตลาดโลก ได้แก่ บราซิล ออสเตรเลีย แอฟริกาใต้ และยูเครน ในประเทศเหล่านี้มีแหล่งแร่สำรองซึ่งคิดเป็นเกือบ 73% ของโลก
การผลิตโลหะเหล็กในระดับอุตสาหกรรมเริ่มต้นด้วยการสกัดแร่และการเพิ่มคุณค่า และขึ้นอยู่กับสารประกอบโลหะกับองค์ประกอบอื่นๆ ตัวอย่างเช่น แร่คาร์บอเนตทั่วไปจะถูกเผาล่วงหน้า ในบางกรณี มันถูกชะล้างโดยใช้กรดซัลฟิวริก ตามด้วยการลดความร้อนด้วยถ่านโค้ก บางครั้งใช้อะลูมิเนียมหรือซิลิกอนเพื่อคืนสภาพโลหะ

กระบวนการทางเคมีในการสกัดแมงกานีส
โลหะบริสุทธิ์ถูกสกัดด้วยอิเล็กโทรลิซิสจากสารละลายที่เป็นน้ำของแมงกานีสซัลเฟต
การใช้แมงกานีสในอุตสาหกรรมการผลิต
- ส่วนหลักของโลหะถูกใช้สำหรับความต้องการของโลหะเหล็กเป็นสารเติมแต่ง และในระดับโลก ปริมาณการบริโภคอยู่ในอันดับที่ 4 รองจากวัตถุดิบหลัก ได้แก่ เหล็ก อะลูมิเนียม และทองแดง แมงกานีสเป็นองค์ประกอบสำคัญที่มีอยู่ในเหล็กหล่อและเหล็กกล้าทุกประเภท คุณสมบัติเฉพาะของแมงกานีสในการสร้างโลหะผสมกับโลหะส่วนใหญ่ใช้ทำ:
- เหล็กแมงกานีสเกรดต่างๆ
- แมงกานีส (โลหะผสมที่ไม่มีเหล็ก)

การใช้งานโลหะอื่นๆ
คุณสมบัติขององค์ประกอบทางเคมีและสารประกอบนั้นใช้ในการผลิตทางอุตสาหกรรม:
- เป็นตัวเร่งปฏิกิริยาสำหรับปฏิกิริยาอินทรีย์
- สำหรับการสลายตัวของเกลืออนินทรีย์
- สำหรับการผลิตแก้ว
- เมื่อเคลือบพื้นผิวโลหะ
- ในอุตสาหกรรมเซรามิกสำหรับเคลือบสีและเคลือบฟัน
- สำหรับการดูดซับสารอันตราย
- สำหรับฟอกวัสดุธรรมชาติ (ผ้าลินิน, ผ้าขนสัตว์)
ของเสียที่ได้จากการแปรรูปวัตถุดิบโลหะด้วยการมีส่วนร่วมของแมงกานีสถูกนำมาใช้ในการเกษตรเพื่อเพิ่มคุณค่าให้กับดินสำหรับพืชผลที่มีองค์ประกอบที่มีคุณค่า
เคมีขององค์ประกอบนี้มีบทบาทสำคัญในการแพทย์
เกลือแมงกานีสถูกใช้เพื่อสร้างน้ำยาฆ่าเชื้อเพื่อล้างแผลและรักษาแผลไฟไหม้
องค์ประกอบทางเคมีหมายเลข 25 จำเป็นต่อการทำงานปกติของร่างกาย การควบคุมระดับน้ำตาลในเลือด การป้องกันโรคเบาหวาน และทำให้การทำงานของตับอ่อนเป็นปกติ
การขาดแมงกานีสในร่างกายมนุษย์อาจทำให้เกิดโรคได้ ความต้องการของมนุษย์ในแต่ละวันสำหรับธาตุสำคัญคือเกือบ 10 มก. แหล่งที่มาของร่างกายคืออาหาร:

แมลงและพืชบางชนิดสามารถรวมองค์ประกอบทางเคมีนี้ไว้ได้ ซึ่งช่วยให้มั่นใจได้ถึงการกระตุ้นการทำงานของเอนไซม์ที่เกี่ยวข้องกับกระบวนการหายใจและการสังเคราะห์ด้วยแสง
องค์ประกอบนี้ในรูปของไพโรลูไซต์ (แมงกานีสไดออกไซด์, MnO 2 ) ถูกใช้โดยศิลปินถ้ำยุคก่อนประวัติศาสตร์ที่ถ้ำลาสโกซ์ ประเทศฝรั่งเศส เมื่อ 30,000 ปีก่อน ในอียิปต์โบราณไม่นานมานี้ ผู้ผลิตแก้วใช้แร่ธาตุที่มีโลหะนี้เพื่อขจัดคราบสีเขียวอ่อนของแก้วธรรมชาติ
แร่ที่ยอดเยี่ยมถูกพบในแคว้นแมกนีเซีย ซึ่งอยู่ทางตอนเหนือของกรีซ ทางตอนใต้ของมาซิโดเนีย และนั่นคือจุดเริ่มต้นของความสับสนกับชื่อ แร่ต่างๆ จากภูมิภาคที่มีทั้งแมกนีเซียมและแมงกานีสเรียกง่ายๆ ว่าแมกนีเซีย ในศตวรรษที่ 17 คำว่า Magnesia alba หรือ White Magnesia ถูกนำมาใช้สำหรับแร่ธาตุแมกนีเซียม ในขณะที่ชื่อ Black Magnesia ใช้สำหรับออกไซด์ที่มีสีเข้มกว่าของแมงกานีส
อย่างไรก็ตาม แร่ธาตุแม่เหล็กที่มีชื่อเสียงที่พบในภูมิภาคนี้เรียกว่าหินแมกนีเซีย ซึ่งในที่สุดก็กลายเป็นแม่เหล็กในปัจจุบัน ความสับสนดำเนินไประยะหนึ่งจนกระทั่งปลายศตวรรษที่ 18 นักเคมีชาวสวีเดนกลุ่มหนึ่งลงความเห็นว่าแมงกานีสเป็นธาตุที่แยกจากกัน ในปี พ.ศ. 2317 สมาชิกคนหนึ่งของกลุ่มได้นำเสนอการค้นพบนี้ต่อ Stockholm Academy และในปีเดียวกัน Johan Gottlieb Hahn กลายเป็นบุคคลแรกที่ได้รับแมงกานีสบริสุทธิ์และพิสูจน์แล้วว่า ว่าเป็นองค์ประกอบที่แยกจากกัน.
แมงกานีส - องค์ประกอบทางเคมี ลักษณะของแมงกานีส
 เป็นโลหะหนักสีขาวเงินที่ค่อยๆ มืดลงในที่โล่ง แข็งและเปราะกว่าเหล็ก มีความถ่วงจำเพาะ 7.21 และจุดหลอมเหลว 1244°C สัญลักษณ์ทางเคมี Mn น้ำหนักอะตอม 54.938 เลขอะตอม 25 ในสูตรอ่านเป็นแมงกานีส เช่น KMnO 4 - โพแทสเซียมแมงกานีสประมาณสี่ นี่เป็นองค์ประกอบที่พบได้ทั่วไปในหิน ปริมาณประมาณ 0.085% ของมวลเปลือกโลก
เป็นโลหะหนักสีขาวเงินที่ค่อยๆ มืดลงในที่โล่ง แข็งและเปราะกว่าเหล็ก มีความถ่วงจำเพาะ 7.21 และจุดหลอมเหลว 1244°C สัญลักษณ์ทางเคมี Mn น้ำหนักอะตอม 54.938 เลขอะตอม 25 ในสูตรอ่านเป็นแมงกานีส เช่น KMnO 4 - โพแทสเซียมแมงกานีสประมาณสี่ นี่เป็นองค์ประกอบที่พบได้ทั่วไปในหิน ปริมาณประมาณ 0.085% ของมวลเปลือกโลก
มีแร่ธาตุมากกว่า 300 ชนิดที่มีองค์ประกอบนี้ พบเงินฝากบนบกขนาดใหญ่ในออสเตรเลีย กาบอง แอฟริกาใต้ บราซิล และรัสเซีย แต่จะพบมากขึ้นที่พื้นมหาสมุทร ซึ่งส่วนใหญ่อยู่ที่ระดับความลึก 4 ถึง 6 กิโลเมตร ดังนั้นการขุดที่นั่นจึงไม่สามารถทำได้ในเชิงพาณิชย์
แร่ธาตุเหล็กออกซิไดซ์ (เฮมาไทต์ แมกนีไทต์ ลิโมไนต์ และไซด์ไรต์) มีธาตุนี้อยู่ 30% แหล่งที่เป็นไปได้อีกแหล่งหนึ่งคือดินเหนียวและโคลนแดงซึ่งมีก้อนมากถึง 25% แมงกานีสที่บริสุทธิ์ที่สุดได้จากการอิเล็กโทรลิซิสของสารละลายที่เป็นน้ำ
แมงกานีสและคลอรีนอยู่ในกลุ่ม VII ของตารางธาตุ แต่คลอรีนอยู่ในกลุ่มย่อยหลักและแมงกานีสอยู่ในกลุ่มรอง ซึ่งรวมถึงเทคนีเชียม Tc และรีเนียม Ke ซึ่งเป็นอะนาล็อกอิเล็กทรอนิกส์ที่สมบูรณ์ แมงกานีส Mn เทคนีเชียม Ts และรีเนียม Ke เป็นอะนาล็อกอิเล็กทรอนิกส์ที่สมบูรณ์พร้อมการกำหนดค่าของเวเลนซ์อิเล็กตรอน
องค์ประกอบนี้มีอยู่ในปริมาณน้อยและในดินเกษตร. ในโลหะผสมหลายชนิดของทองแดง อลูมิเนียม แมกนีเซียม นิกเกิล เปอร์เซ็นต์ต่างๆ ของมันทำให้มีคุณสมบัติทางกายภาพและเทคโนโลยีเฉพาะ:
- ความต้านทานการสึกหรอ
- ทนความร้อน
- ความต้านทานต่อการกัดกร่อน
- หลอมละลาย;
- ความต้านทานไฟฟ้า ฯลฯ
ค่าวาเลนซีของแมงกานีส
สถานะออกซิเดชันของแมงกานีสอยู่ระหว่าง 0 ถึง +7 ในสถานะออกซิเดชันแบบไดวาเลนต์ แมงกานีสมีลักษณะที่เป็นโลหะอย่างชัดเจนและมีแนวโน้มสูงที่จะสร้างพันธะที่ซับซ้อน ในปฏิกิริยาออกซิเดชันแบบเตตระวาเลนต์ ลักษณะที่เป็นกลางระหว่างคุณสมบัติของโลหะและอโลหะจะเหนือกว่า ในขณะที่เฮกซะวาเลนต์และเฮปทาวาเลนต์จะมีคุณสมบัติที่ไม่ใช่โลหะ
ออกไซด์:
สูตร. สี

ชีวเคมีและเภสัชวิทยา
แมงกานีสเป็นองค์ประกอบที่กระจายอยู่ทั่วไปในธรรมชาติ มีอยู่ในเนื้อเยื่อส่วนใหญ่ของพืชและสัตว์ พบความเข้มข้นสูงสุด:
- ในเปลือกส้ม
- ในองุ่น
- ในผลเบอร์รี่
- ในหน่อไม้ฝรั่ง
- ในกุ้ง;
- ในหอยทาก;
- ในประตูบานคู่
ปฏิกิริยาที่สำคัญที่สุดอย่างหนึ่งในชีววิทยา คือการสังเคราะห์ด้วยแสง ขึ้นอยู่กับองค์ประกอบนี้โดยสิ้นเชิง เป็นดาวเด่นในศูนย์กลางปฏิกิริยาของระบบภาพถ่าย II ซึ่งโมเลกุลของน้ำจะเปลี่ยนเป็นออกซิเจน หากไม่มีมัน การสังเคราะห์ด้วยแสงก็เป็นไปไม่ได้.
เป็นองค์ประกอบสำคัญในสิ่งมีชีวิตที่รู้จักทั้งหมด ตัวอย่างเช่น เอนไซม์ที่ทำหน้าที่เปลี่ยนโมเลกุลของน้ำให้เป็นออกซิเจนในระหว่างการสังเคราะห์ด้วยแสงประกอบด้วยอะตอมของแมงกานีสสี่อะตอม
ร่างกายมนุษย์โดยเฉลี่ยมีโลหะนี้ประมาณ 12 มิลลิกรัม เราได้รับประมาณ 4 มิลลิกรัมทุกวันจากอาหาร เช่น ถั่ว รำข้าว ซีเรียล ชา และผักชีฝรั่ง องค์ประกอบนี้ทำให้กระดูกของโครงกระดูกมีความทนทานมากขึ้น นอกจากนี้ยังมีความสำคัญต่อการดูดซึมวิตามินบี 1
ประโยชน์และคุณสมบัติที่เป็นอันตราย
 องค์ประกอบการติดตามนี้มีความสำคัญทางชีววิทยาอย่างยิ่ง: ทำหน้าที่เป็นตัวเร่งปฏิกิริยาในการสังเคราะห์ทางชีวภาพของพอร์ไฟริน และฮีโมโกลบินในสัตว์และคลอโรฟิลล์ในพืชสีเขียว การปรากฏตัวของมันยังเป็นเงื่อนไขที่จำเป็นสำหรับการทำงานของระบบเอนไซม์ไมโทคอนเดรียต่างๆ เอนไซม์เมแทบอลิซึมของไขมันบางชนิด และกระบวนการออกซิเดทีฟฟอสโฟรีเลชั่น
องค์ประกอบการติดตามนี้มีความสำคัญทางชีววิทยาอย่างยิ่ง: ทำหน้าที่เป็นตัวเร่งปฏิกิริยาในการสังเคราะห์ทางชีวภาพของพอร์ไฟริน และฮีโมโกลบินในสัตว์และคลอโรฟิลล์ในพืชสีเขียว การปรากฏตัวของมันยังเป็นเงื่อนไขที่จำเป็นสำหรับการทำงานของระบบเอนไซม์ไมโทคอนเดรียต่างๆ เอนไซม์เมแทบอลิซึมของไขมันบางชนิด และกระบวนการออกซิเดทีฟฟอสโฟรีเลชั่น
ไอระเหยหรือน้ำดื่มที่ปนเปื้อนด้วยเกลือของโลหะนี้นำไปสู่การเปลี่ยนแปลงที่ระคายเคืองในทางเดินหายใจ, พิษเรื้อรังที่มีแนวโน้มก้าวหน้าและกลับไม่ได้, ลักษณะความเสียหายต่อปมประสาทฐานของระบบประสาทส่วนกลาง, จากนั้นการละเมิดประเภท extrapyramidal ที่คล้ายกัน ต่อโรคพาร์กินสัน
พิษดังกล่าวมักเป็นตัวละครมืออาชีพ ผลกระทบดังกล่าวส่งผลกระทบต่อผู้ปฏิบัติงานในกระบวนการผลิตโลหะนี้และอนุพันธ์ รวมถึงคนงานในอุตสาหกรรมเคมีและโลหการ ในทางการแพทย์ มีการใช้ในรูปของโพแทสเซียมเปอร์แมงกาเนตเป็นยาสมานแผล น้ำยาฆ่าเชื้อเฉพาะที่ และยังเป็นยาแก้พิษจากสารอัลคาลอยด์ตามธรรมชาติ (มอร์ฟีน โคเดอีน อะโทรปีน ฯลฯ)
ดินบางแห่งมีธาตุนี้ในระดับต่ำ จึงนำไปใส่ปุ๋ยและเป็นอาหารเสริมสำหรับสัตว์กินหญ้า
แมงกานีส: การประยุกต์ใช้
 ในฐานะที่เป็นโลหะบริสุทธิ์ ยกเว้นการใช้งานอย่างจำกัดในด้านวิศวกรรมไฟฟ้า ส่วนประกอบนี้ไม่มีการใช้งานจริงอื่นๆ ในขณะเดียวกันก็มีการใช้กันอย่างแพร่หลายสำหรับการเตรียมโลหะผสม การผลิตเหล็ก ฯลฯ
ในฐานะที่เป็นโลหะบริสุทธิ์ ยกเว้นการใช้งานอย่างจำกัดในด้านวิศวกรรมไฟฟ้า ส่วนประกอบนี้ไม่มีการใช้งานจริงอื่นๆ ในขณะเดียวกันก็มีการใช้กันอย่างแพร่หลายสำหรับการเตรียมโลหะผสม การผลิตเหล็ก ฯลฯ
เมื่อเฮนรี เบสเซเมอร์ได้คิดค้นกรรมวิธีการทำเหล็กขึ้นในปี พ.ศ. 2399 เหล็กของเขาถูกทำลายด้วยการรีดร้อน ปัญหาได้รับการแก้ไขในปีเดียวกันเมื่อพบว่าการเติมธาตุนี้ในปริมาณเล็กน้อยลงในเหล็กหลอมเหลวช่วยแก้ปัญหาได้ ปัจจุบันแมงกานีสประมาณ 90% ถูกใช้ในการผลิตเหล็ก
คำนิยาม
แมงกานีสเป็นองค์ประกอบที่ยี่สิบห้าของตารางธาตุ การกำหนด - Mn จากภาษาละติน "manganum" อยู่ในช่วงที่ 4 กลุ่ม VIB หมายถึงโลหะ. ค่าใช้จ่ายหลักคือ 25
แมงกานีสเป็นธาตุที่พบได้ทั่วไป โดยคิดเป็น 0.1% (มวล) ของเปลือกโลก ในบรรดาสารประกอบที่มีแมงกานีส แร่ธาตุที่พบมากที่สุดคือไพโรลูไซต์ ซึ่งเป็นแมงกานีสไดออกไซด์ MnO 2 แร่ธาตุ hausmanite Mn 3 O 4 และ brownite Mn 2 O 3 ก็มีความสำคัญเช่นกัน
ในรูปของสารธรรมดา แมงกานีสเป็นโลหะแข็งเปราะสีเงินสีขาว (รูปที่ 1) ความหนาแน่นของมันคือ 7.44 g / cm 3 จุดหลอมเหลว 1245 o C
ข้าว. 1. แมงกานีส รูปร่าง.
น้ำหนักอะตอมและโมเลกุลของแมงกานีส
น้ำหนักโมเลกุลสัมพัทธ์ของสาร(M r) เป็นตัวเลขที่แสดงจำนวนครั้งที่มวลของโมเลกุลที่กำหนดมากกว่า 1/12 ของมวลของอะตอมของคาร์บอน และ มวลอะตอมสัมพัทธ์ของธาตุ(A r) - มวลเฉลี่ยของอะตอมขององค์ประกอบทางเคมีมากกว่า 1/12 ของมวลของอะตอมคาร์บอนกี่ครั้ง
เนื่องจากแมงกานีสในสถานะอิสระมีอยู่ในรูปของโมเลกุลโมนามิก Mn ค่าของมวลอะตอมและโมเลกุลจึงตรงกัน พวกเขาเท่ากับ 54.9380
Allotropy และ allotropic ดัดแปลงของแมงกานีส
เป็นที่ทราบกันดีว่าการดัดแปลงผลึกของแมงกานีสสี่แบบ ซึ่งแต่ละแบบมีความเสถียรทางอุณหพลศาสตร์ในช่วงอุณหภูมิหนึ่งๆ ต่ำกว่า 707 o C α-แมงกานีสมีความเสถียร มีโครงสร้างที่ซับซ้อน - หน่วยเซลล์ประกอบด้วยอะตอม 58 อะตอม ความซับซ้อนของโครงสร้างของแมงกานีสที่อุณหภูมิต่ำกว่า 707 o ทำให้เกิดความเปราะบาง
ไอโซโทปของแมงกานีส
เป็นที่ทราบกันว่าแมงกานีสสามารถเกิดขึ้นได้ในธรรมชาติในรูปของไอโซโทปที่เสถียรเพียง 55 Mn เลขมวลคือ 55 นิวเคลียสของอะตอมประกอบด้วยโปรตอน 25 ตัวและนิวตรอน 30 ตัว
มีไอโซโทปเทียมของแมงกานีสที่มีเลขมวลตั้งแต่ 44 ถึง 69 เช่นเดียวกับนิวเคลียสไอโซเมอริกเจ็ดสถานะ ไอโซโทปที่มีอายุยืนยาวที่สุดในบรรดาข้างต้นคือ 53 Mn โดยมีครึ่งชีวิต 3.74 ล้านปี
ไอออนแมงกานีส
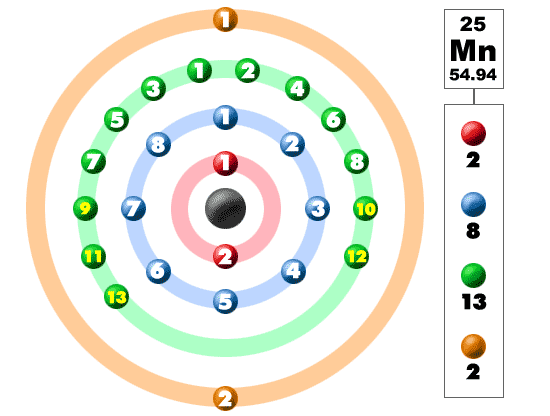
ในระดับพลังงานชั้นนอกของอะตอมแมงกานีส มีอิเล็กตรอนเจ็ดตัวที่มีวาเลนซ์:
1 วินาที 2 2 วินาที 2 2 จุด 6 3 วินาที 2 3 จุด 6 3d 5 4 วินาที 2 .
อันเป็นผลมาจากปฏิสัมพันธ์ทางเคมี แมงกานีสจึงสูญเสียเวเลนต์อิเล็กตรอนไป นั่นคือ เป็นผู้บริจาคของพวกเขาและกลายเป็นไอออนที่มีประจุบวก:
Mn 0 -2e → Mn 2+;
Mn 0 -3e → Mn 3+;
Mn 0 -4e → Mn 4+;
Mn 0 -6e → Mn 6+;
Mn 0 -7e → Mn 7+
โมเลกุลและอะตอมของแมงกานีส
ในสถานะอิสระ แมงกานีสมีอยู่ในรูปของโมเลกุล Mn เชิงเดี่ยว ต่อไปนี้คือคุณสมบัติบางอย่างที่แสดงลักษณะของอะตอมและโมเลกุลของแมงกานีส:
โลหะผสมแมงกานีส
แมงกานีสส่วนใหญ่ใช้ในการผลิตเหล็กกล้าผสม เหล็กแมงกานีสที่มี Mn สูงถึง 15% มีความแข็งและความแข็งแรงสูง ชิ้นส่วนการทำงานของเครื่องบด, โรงสีลูก, รางรถไฟทำจากมัน นอกจากนี้ แมงกานีสยังเป็นส่วนประกอบของโลหะผสมที่มีแมกนีเซียมเป็นหลัก มันเพิ่มความต้านทานต่อการกัดกร่อน โลหะผสมของทองแดงกับแมงกานีสและนิกเกิล - แมงกานีสมีค่าสัมประสิทธิ์ความต้านทานไฟฟ้าที่อุณหภูมิต่ำ แมงกานีสพบในปริมาณเล็กน้อยในโลหะผสมอลูมิเนียมหลายชนิด
ตัวอย่างการแก้ปัญหา
ตัวอย่างที่ 1
| ออกกำลังกาย | แมงกานีสผลิตโดยการลดแมงกานีส (III) ออกไซด์ด้วยซิลิกอน ออกไซด์ทางเทคนิคที่มีน้ำหนัก 20 กรัม (เศษส่วนมวลของสิ่งเจือปนเท่ากับ 5.2%) ถูกลดขนาดให้เป็นโลหะ คำนวณมวลของแมงกานีสที่ได้รับ |
| สารละลาย | เราเขียนสมการสำหรับการลดลงของแมงกานีส (III) ออกไซด์ด้วยซิลิกอนเป็นแมงกานีส: 2Mn 2 O 3 + 3Si = 3SiO 2 + 4Mn คำนวณมวลของแมงกานีส (III) ออกไซด์ที่ไม่มีสิ่งเจือปน: ω บริสุทธิ์ (Mn 2 O 3) \u003d 100% - ω สิ่งเจือปน; ω บริสุทธิ์ (Mn 2 O 3) \u003d 100% - 5.2 \u003d 94.8% \u003d 0.984 m บริสุทธิ์ (Mn 2 O 3) = m สิ่งเจือปน (Mn 2 O 3) × ω บริสุทธิ์ (Mn 2 O 3) / 100%; ม. บริสุทธิ์ (Mn 2 O 3) \u003d 20 × 0.984 \u003d 19.68 ก. ตรวจสอบปริมาณของสารแมงกานีส (III) ออกไซด์ (มวลโมลาร์ - 158 กรัม / โมล): n (Mn 2 O 3) \u003d m (Mn 2 O 3) / M (Mn 2 O 3); n (Mn 2 O 3) \u003d 19.68 / 158 \u003d 0.12 โมล ตามสมการปฏิกิริยา n (Mn 2 O 3) : n (Si) \u003d 2: 3 ซึ่งหมายความว่า n(ศรี) \u003d 3/2 × n (Mn 2 O 3) \u003d 3/2 × 0.12 \u003d 0.2 โมล จากนั้นมวลของซิลิกอนจะเท่ากับ (มวลโมลาร์ - 28 g / mol): ม. (ศรี) = n (ศรี) × ม. (ศรี); ม.(ศรี) = 0.2 × 28 = 5.6 ก. |
| คำตอบ | มวลซิลิกอน 5.6 g |
ตัวอย่างที่ 2
| ออกกำลังกาย | คำนวณมวลของโพแทสเซียมเปอร์แมงกาเนตที่จำเป็นในการออกซิไดซ์โพแทสเซียมซัลไฟต์ 7.9 กรัมในตัวกลางที่เป็นกลาง |
| สารละลาย | เราเขียนสมการสำหรับการเกิดออกซิเดชันของโพแทสเซียมซัลไฟต์ด้วยโพแทสเซียมเปอร์แมงกาเนตในตัวกลางที่เป็นกลาง: 2KMnO 4 + 3K 2 SO 3 + H 2 O \u003d 2MnO 2 + 3K 2 SO 4 + 2KOH คำนวณจำนวนโมลของโพแทสเซียมซัลไฟต์ (มวลโมลาร์ - 158 กรัม / โมล): n (K 2 SO 3) \u003d m (K 2 SO 3) / M (K 2 SO 3); n (K 2 SO 3) \u003d 7.9 / 158 \u003d 0.05 โมล ตามสมการปฏิกิริยา n (K 2 SO 3): n (KMnO 4) \u003d 3: 2 ซึ่งหมายความว่า n (KMnO 4) \u003d 2/3 × n (K 2 SO 3) \u003d 2/3 × 0.05 \u003d 0.03 โมล มวลของโพแทสเซียมเปอร์แมงกาเนตที่จำเป็นต่อการเกิดออกซิเดชันของโพแทสเซียมซัลไฟต์ในตัวกลางที่เป็นกลางคือ (มวลโมลาร์ - 158g / mol): ม. (KMnO 4) \u003d n (KMnO 4) × M (KMnO 4); ม. (KMnO 4) \u003d 0.03 × 158 \u003d 4.74 ก. |
| คำตอบ | มวลของโพแทสเซียมเปอร์แมงกาเนตคือ 4.74 กรัม |
แมงกานีสเป็นองค์ประกอบทางเคมีที่อยู่ในระบบธาตุของ Mendeleev ที่เลขอะตอม 25 ธาตุใกล้เคียงคือโครเมียมและเหล็ก ซึ่งกำหนดความคล้ายคลึงกันของคุณสมบัติทางกายภาพและทางเคมีของโลหะทั้งสามนี้ นิวเคลียสประกอบด้วยโปรตอน 25 ตัว และนิวตรอน 30 ตัว มวลอะตอมของธาตุคือ 54.938
คุณสมบัติของแมงกานีส
แมงกานีสเป็นโลหะทรานซิชันจากตระกูล d สูตรอิเล็กทรอนิกส์มีดังนี้: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 5 . ความแข็งของแมงกานีสในระดับ Mohs อยู่ที่ประมาณ 4 โลหะนั้นค่อนข้างแข็ง แต่ในขณะเดียวกันก็เปราะ ค่าการนำความร้อนคือ 0.0782 W / cm * K องค์ประกอบมีลักษณะเป็นสีขาวเงิน
มีการดัดแปลงโลหะสี่อย่างที่มนุษย์รู้จัก แต่ละตัวมีความเสถียรทางอุณหพลศาสตร์ภายใต้สภาวะอุณหภูมิที่แน่นอน ดังนั้นแมงกานีสจึงมีโครงสร้างที่ค่อนข้างซับซ้อนและแสดงความเสถียรที่อุณหภูมิต่ำกว่า 707 0 C ซึ่งเป็นตัวกำหนดความเปราะบางของมัน การดัดแปลงโลหะในเซลล์มูลฐานประกอบด้วยอะตอม 58 อะตอม
แมงกานีสสามารถมีสถานะออกซิเดชั่นที่แตกต่างกันโดยสิ้นเชิง - ตั้งแต่ 0 ถึง +7 ในขณะที่ +1 และ +5 นั้นหายากมาก เมื่อโลหะทำปฏิกิริยากับอากาศ แมงกานีสที่เป็นผงจะเผาไหม้ในออกซิเจน:
Mn+O2=MnO2
หากโลหะสัมผัสกับอุณหภูมิสูง เช่น เมื่อได้รับความร้อน มันจะสลายตัวเป็นน้ำด้วยการแทนที่ของไฮโดรเจน:
Mn+2H0O=Mn(OH)2+H2
ควรสังเกตว่าแมงกานีสไฮดรอกไซด์ซึ่งเป็นชั้นที่เกิดจากปฏิกิริยาทำให้กระบวนการเกิดปฏิกิริยาช้าลง
ไฮโดรเจนถูกดูดซับโดยโลหะ ยิ่งอุณหภูมิสูงขึ้นเท่าใดความสามารถในการละลายในแมงกานีสก็จะยิ่งสูงขึ้นเท่านั้น หากอุณหภูมิสูงเกิน 12,000C แมงกานีสจะทำปฏิกิริยากับไนโตรเจนซึ่งเป็นผลมาจากไนไตรต์ซึ่งมีองค์ประกอบแตกต่างกัน
โลหะยังมีปฏิกิริยากับคาร์บอน ผลของปฏิกิริยานี้คือการก่อตัวของคาร์ไบด์เช่นเดียวกับซิลิไซด์, บอไรด์, ฟอสไฟด์
โลหะมีความทนทานต่อสารละลายด่าง
สามารถสร้างออกไซด์ต่อไปนี้: MnO, Mn 2 O 3, MnO 2, MnO 3 ซึ่งสุดท้ายไม่ได้ถูกแยกออกในสถานะอิสระ เช่นเดียวกับแมงกานีสแอนไฮไดรด์ Mn 2 O 7 ภายใต้สภาวะปกติแมงกานีสแอนไฮไดรด์เป็นสารเหลวที่มีสีเขียวเข้มซึ่งไม่มีความเสถียรมากนัก หากอุณหภูมิเพิ่มขึ้นถึง 90 0 C การสลายตัวของแอนไฮไดรด์จะมาพร้อมกับการระเบิด ในบรรดาออกไซด์ที่แสดงความเสถียรมากที่สุดนั้น Mn 2 O 3 และ MnO 2 มีความแตกต่างกัน เช่นเดียวกับออกไซด์ที่รวมกัน Mn 3 O 4 (2MnO·MnO 2 หรือเกลือ Mn 2 MnO 4)
แมงกานีสออกไซด์:
ในระหว่างการหลอมรวมของไพโรลูไซต์และด่างกับออกซิเจนปฏิกิริยาจะเกิดขึ้นกับการก่อตัวของแมงกานีส:
2MnO 2 + 2KOH + O 2 \u003d 2K 2 MnO 4 + 2H 2 O
สารละลายแมงกานีสมีลักษณะเป็นสีเขียวเข้ม หากทำให้เป็นกรด ปฏิกิริยาจะดำเนินต่อไปด้วยการย้อมสีสารละลายเป็นสีแดงเข้ม นี่เป็นเพราะการก่อตัวของ MnO 4 − anion ซึ่งทำให้เกิดการตกตะกอนของแมงกานีสออกไซด์-ไฮดรอกไซด์ซึ่งมีสีน้ำตาล
กรดเปอร์แมงกานิกนั้นเข้มข้น แต่ไม่แสดงความเสถียรเป็นพิเศษ ดังนั้น ความเข้มข้นสูงสุดที่อนุญาตคือไม่เกิน 20% กรดเองก็เหมือนกับเกลือของมัน ทำหน้าที่เป็นตัวออกซิไดซ์ที่แรง
เกลือของแมงกานีสไม่แสดงความคงตัว ไฮดรอกไซด์มีลักษณะพื้นฐาน แมงกานีสคลอไรด์จะสลายตัวเมื่อสัมผัสกับอุณหภูมิสูง เป็นรูปแบบนี้ที่ใช้ในการรับคลอรีน

การประยุกต์ใช้แมงกานีส
โลหะนี้ไม่ได้ขาดตลาด - เป็นขององค์ประกอบทั่วไป: เนื้อหาในเปลือกโลกคือ 0.03% ของจำนวนอะตอมทั้งหมด เขาอยู่ในอันดับที่สามในการจัดอันดับโลหะหนักซึ่งรวมถึงองค์ประกอบทั้งหมดของซีรีส์ทรานซิชัน แซงหน้าเหล็กและไททาเนียม โลหะหนักคือโลหะหนักที่มีน้ำหนักอะตอมมากกว่า 40
แมงกานีสสามารถพบได้ในปริมาณเล็กน้อยในหินบางชนิด โดยทั่วไปการแปลสารประกอบออกซิเจนในรูปของแร่ไพโรลูไซต์ - MnO 2 เกิดขึ้น
แมงกานีสมีประโยชน์มากมาย เป็นสิ่งจำเป็นสำหรับการผลิตโลหะผสมและสารเคมีหลายชนิด หากไม่มีแมงกานีส การดำรงอยู่ของสิ่งมีชีวิตจะเป็นไปไม่ได้ เนื่องจากแมงกานีสทำหน้าที่เป็นธาตุที่ทำงานอยู่ และยังมีอยู่ในสิ่งมีชีวิตและสิ่งมีชีวิตในพืชเกือบทุกชนิด แมงกานีสมีผลดีต่อกระบวนการสร้างเม็ดเลือดในสิ่งมีชีวิต นอกจากนี้ยังพบในอาหารหลายชนิด

โลหะเป็นองค์ประกอบที่ขาดไม่ได้ในโลหะวิทยา เป็นแมงกานีสที่ใช้ในการกำจัดกำมะถันและออกซิเจนออกจากเหล็กในระหว่างการผลิต กระบวนการนี้ต้องใช้โลหะปริมาณมาก แต่มันก็คุ้มค่าที่จะบอกว่าไม่ได้เติมแมงกานีสบริสุทธิ์ลงในสารหลอมเหลว แต่ผสมด้วยเหล็กเรียกว่าเฟอร์โรแมงกานีส ได้มาจากกระบวนการลดปฏิกิริยาของไพโรลูไซต์กับถ่านหิน แมงกานีสยังทำหน้าที่เป็นองค์ประกอบผสมสำหรับเหล็ก ด้วยการเติมแมงกานีสลงในเหล็กกล้า ทำให้ความต้านทานการสึกหรอเพิ่มขึ้นอย่างมาก และยังไวต่อความเครียดเชิงกลน้อยลงอีกด้วย การปรากฏตัวของแมงกานีสในองค์ประกอบของโลหะที่ไม่ใช่เหล็กช่วยเพิ่มความแข็งแรงและความต้านทานต่อการกัดกร่อนได้อย่างมีนัยสำคัญ
เมทัลไดออกไซด์พบว่ามีการนำไปใช้ในปฏิกิริยาออกซิเดชันของแอมโมเนีย และยังมีส่วนร่วมในปฏิกิริยาอินทรีย์และปฏิกิริยาการสลายตัวของเกลืออนินทรีย์ ในกรณีนี้ แมงกานีสไดออกไซด์ทำหน้าที่เป็นตัวเร่งปฏิกิริยา
อุตสาหกรรมเซรามิกยังทำไม่ได้หากไม่มีแมงกานีส โดย MnO 2 ใช้เป็นสีย้อมสีดำและสีน้ำตาลเข้มสำหรับเคลือบฟันและเคลือบ แมงกานีสออกไซด์มีการกระจายตัวสูง มีความสามารถในการดูดซับที่ดีเนื่องจากสามารถขจัดสิ่งสกปรกที่เป็นอันตรายออกจากอากาศได้
แมงกานีสถูกนำไปใช้กับทองสัมฤทธิ์และทองเหลือง สารประกอบโลหะบางชนิดใช้ในการสังเคราะห์สารอินทรีย์ละเอียดและการสังเคราะห์สารอินทรีย์ทางอุตสาหกรรม แมงกานีสอาร์เซไนด์มีลักษณะพิเศษคือมีผลกระทบจากสนามแม่เหล็กขนาดมหึมา ซึ่งจะแข็งแกร่งขึ้นมากเมื่ออยู่ภายใต้ความกดดันสูง แมงกานีสเทลลูไรด์ทำหน้าที่เป็นวัสดุเทอร์โมอิเล็กทริกที่มีแนวโน้มดี
ในทางการแพทย์ควรใช้แมงกานีสหรือเกลือมากกว่า ดังนั้น สารละลายโพแทสเซียมเปอร์แมงกาเนตที่เป็นน้ำจึงถูกใช้เป็นน้ำยาฆ่าเชื้อ และพวกมันยังสามารถล้างบาดแผล บ้วนปาก หล่อลื่นแผลและแผลไฟไหม้ ในพิษบางชนิดที่มีอัลคาลอยด์และไซยาไนด์ สารละลายของมันจะถูกระบุไว้สำหรับการบริหารช่องปากด้วยซ้ำ

สำคัญ:แม้จะมีแง่บวกมากมายจากการใช้แมงกานีส แต่ในบางกรณี สารประกอบของแมงกานีสอาจส่งผลเสียต่อร่างกายมนุษย์และอาจเป็นพิษได้ ดังนั้นความเข้มข้นสูงสุดของแมงกานีสในอากาศที่อนุญาตคือ 0.3 มก./ม.3 . ในกรณีของพิษที่เด่นชัดจากสารใด ๆ ระบบประสาทของมนุษย์จะได้รับผลกระทบซึ่งเป็นลักษณะของกลุ่มอาการของแมงกานีสพาร์กินสัน
การได้รับแมงกานีส
สามารถรับโลหะได้หลายวิธี ในบรรดาวิธีที่ได้รับความนิยมมากที่สุดมีดังต่อไปนี้:
- อะลูมิเนียม แมงกานีสได้มาจากออกไซด์ Mn 2 O 3 โดยปฏิกิริยารีดักชัน ในทางกลับกันออกไซด์จะเกิดขึ้นระหว่างการเผาด้วยไพโรลูไซต์:
4MnO 2 \u003d 2Mn 2 O 3 + O 2
Mn 2 O 3 + 2Al \u003d 2Mn + Al 2 O 3
- บูรณะ แมงกานีสได้มาจากการลดโลหะด้วยโค้กจากแร่แมงกานีส ทำให้เกิดเฟอร์โรแมงกานีส (โลหะผสมของแมงกานีสและเหล็ก) วิธีนี้เป็นวิธีที่พบได้บ่อยที่สุด เนื่องจากมีการใช้โลหะจำนวนมากในการผลิตโลหะผสมต่างๆ ซึ่งส่วนประกอบหลักคือเหล็ก ด้วยเหตุนี้ แมงกานีสจึงถูกสกัดจากแร่ที่ไม่ได้อยู่ในรูปบริสุทธิ์ แต่อยู่ใน ผสมกับมัน
- อิเล็กโทรไลซิส โลหะในรูปบริสุทธิ์ได้มาจากเกลือด้วยวิธีนี้
แร่แมงกานีส โดยเฉพาะแร่ไพโรลูไซต์ เป็นที่รู้จักในสมัยโบราณ ไพโรลูไซต์ถือเป็นแร่เหล็กแม่เหล็กชนิดหนึ่งและใช้ในการหลอมแก้ว - เพื่อความชัดเจน ข้อเท็จจริงที่ว่าแร่ซึ่งแตกต่างจากแร่เหล็กแม่เหล็กจริง ๆ ไม่ได้ถูกดึงดูดโดยแม่เหล็กได้รับการอธิบายอย่างขบขัน: เชื่อกันว่าไพโรลูไซต์เป็นแร่เพศหญิงและไม่แยแสกับแม่เหล็ก
ในศตวรรษที่ 18 แมงกานีสถูกแยกออกในรูปบริสุทธิ์ และวันนี้เราจะพูดถึงรายละเอียด ดังนั้นเรามาคุยกันว่าแมงกานีสเป็นอันตรายหรือไม่ คุณสามารถซื้อได้ที่ไหน วิธีรับแมงกานีสและเป็นไปตาม GOST หรือไม่
แมงกานีสอยู่ในกลุ่ม 7 กลุ่ม 4 ที่คล้ายกัน องค์ประกอบเป็นเรื่องธรรมดา - เกิดขึ้นที่ 14
องค์ประกอบนี้เป็นของโลหะหนัก - มวลอะตอมมากกว่า 40 มันถูกส่งผ่านในอากาศ - มันถูกปกคลุมด้วยฟิล์มออกไซด์หนาแน่นที่ป้องกันไม่ให้เกิดปฏิกิริยากับออกซิเจน ต้องขอบคุณภาพยนตร์เรื่องนี้ มันไม่สามารถใช้งานได้ภายใต้สภาวะปกติ
เมื่อถูกความร้อน แมงกานีสจะทำปฏิกิริยากับสารง่าย ๆ หลายชนิด กรดและเบส เกิดเป็นสารประกอบที่มีสถานะออกซิเดชันต่างกันมาก: -1, -6, +2, +3, +4, +7 โลหะเป็นของโลหะทรานซิชัน ดังนั้นจึงแสดงทั้งคุณสมบัติรีดิวซ์และออกซิไดซ์ได้อย่างง่ายดายเท่ากัน ตัวอย่างเช่นกับโลหะทำให้เกิดสารละลายที่เป็นของแข็งโดยไม่ทำปฏิกิริยา
วิดีโอนี้จะบอกคุณว่าแมงกานีสคืออะไร:
คุณสมบัติและความแตกต่างจากวัสดุอื่นๆ
แมงกานีสเป็นโลหะสีขาวเงิน หนาแน่น แข็ง - มีโครงสร้างที่ซับซ้อนผิดปกติ อันหลังเป็นสาเหตุของความเปราะบางของสาร รู้จักการดัดแปลงแมงกานีสสี่แบบ โลหะผสมกับโลหะช่วยให้มีเสถียรภาพและได้สารละลายที่เป็นของแข็งซึ่งมีคุณสมบัติแตกต่างกันมาก
- แมงกานีสเป็นหนึ่งในธาตุที่สำคัญ สิ่งนี้ใช้กับพืชและสัตว์อย่างเท่าเทียมกัน องค์ประกอบนี้เกี่ยวข้องกับการสังเคราะห์ด้วยแสง, ในกระบวนการหายใจ, เปิดใช้งานเอนไซม์จำนวนหนึ่ง, เป็นผู้มีส่วนร่วมที่ขาดไม่ได้ในการเผาผลาญของกล้ามเนื้อและอื่น ๆ ปริมาณแมงกานีสต่อวันสำหรับมนุษย์คือ 2–9 มก. ทั้งการขาดและเกินขององค์ประกอบมีอันตรายเท่ากัน
- โลหะหนักและแข็งกว่าเหล็ก แต่ไม่มีการใช้งานจริงในรูปแบบบริสุทธิ์เนื่องจากมีความเปราะสูง แต่โลหะผสมและสารประกอบมีความสำคัญอย่างยิ่งในระบบเศรษฐกิจของประเทศ มันถูกใช้ในโลหะผสมเหล็กและอโลหะ ในการผลิตปุ๋ย วิศวกรรมไฟฟ้า ในการสังเคราะห์สารอินทรีย์อย่างละเอียด และอื่นๆ
- แมงกานีสค่อนข้างแตกต่างจากโลหะในกลุ่มย่อยของมันเอง Technetium เป็นธาตุกัมมันตภาพรังสีที่ได้มาจากการประดิษฐ์ รีเนียมหมายถึงร่องรอยและองค์ประกอบที่หายาก บอเรียมสามารถรับได้จากการประดิษฐ์เท่านั้นและไม่ได้เกิดขึ้นในธรรมชาติ กิจกรรมทางเคมีของทั้งเทคนีเชียมและรีเนียมนั้นต่ำกว่าแมงกานีสมาก การใช้งานจริง ยกเว้นนิวเคลียร์ฟิวชัน พบแมงกานีสเท่านั้น
แมงกานีส (ภาพ)

ข้อดีและข้อเสีย
คุณสมบัติทางกายภาพและทางเคมีของโลหะนั้นในทางปฏิบัติไม่ได้จัดการกับแมงกานีสเอง แต่มีสารประกอบและโลหะผสมจำนวนมาก ดังนั้นควรพิจารณาข้อดีและข้อเสียของวัสดุจากมุมมองนี้
- แมงกานีสก่อให้เกิดโลหะผสมที่หลากหลายกับโลหะเกือบทั้งหมด ซึ่งเป็นข้อดีที่แน่นอน
- ละลายร่วมกันได้อย่างสมบูรณ์นั่นคือพวกมันก่อตัวเป็นสารละลายที่เป็นของแข็งโดยมีอัตราส่วนขององค์ประกอบเป็นเนื้อเดียวกัน ในกรณีนี้โลหะผสมจะมีจุดเดือดต่ำกว่าแมงกานีสมาก
- โลหะผสมของธาตุกับคาร์บอนมีความสำคัญในทางปฏิบัติมากที่สุด โลหะผสมทั้งสองมีความสำคัญอย่างยิ่งต่ออุตสาหกรรมเหล็กกล้า
- สารประกอบแมงกานีสจำนวนมากและหลากหลายถูกนำมาใช้ในอุตสาหกรรมเคมี สิ่งทอ อุตสาหกรรมแก้ว ในการผลิตปุ๋ย และอื่นๆ พื้นฐานของความหลากหลายนี้คือกิจกรรมทางเคมีของสาร
ข้อเสียของโลหะนั้นเกี่ยวข้องกับลักษณะเฉพาะของโครงสร้างซึ่งไม่อนุญาตให้ใช้โลหะเป็นวัสดุโครงสร้าง
- สิ่งสำคัญคือความเปราะบางที่มีความแข็งสูง Mn สูงถึง +707 C ตกผลึกในโครงสร้างที่เซลล์ประกอบด้วยอะตอม 58 อะตอม
- ด้วยจุดเดือดที่ค่อนข้างสูง จึงเป็นเรื่องยากที่จะทำงานกับโลหะที่มีอัตราสูงเช่นนี้
- ค่าการนำไฟฟ้าของแมงกานีสต่ำมาก ดังนั้นการใช้แมงกานีสในวิศวกรรมไฟฟ้าจึงมีข้อจำกัดเช่นกัน
เราจะพูดถึงคุณสมบัติทางเคมีและกายภาพของแมงกานีสต่อไป
คุณสมบัติและลักษณะเฉพาะ
ลักษณะทางกายภาพของโลหะขึ้นอยู่กับอุณหภูมิอย่างชัดเจน เนื่องจากมีการแก้ไขมากถึง 4 รายการจึงไม่น่าแปลกใจ
ลักษณะสำคัญของสารมีดังนี้:
- ความหนาแน่น - ที่อุณหภูมิปกติคือ 7.45 g / cu ดู ค่านี้ขึ้นอยู่กับอุณหภูมิเล็กน้อย: ตัวอย่างเช่นเมื่อให้ความร้อนถึง 600 C ความหนาแน่นจะลดลงเพียง 7%
- จุดหลอมเหลว - 1244 C;
- จุดเดือด - 2095 C;
- ค่าการนำความร้อนที่ 25 C คือ 66.57 W / (m K) ซึ่งเป็นตัวบ่งชี้ที่ต่ำสำหรับโลหะ
- ความจุความร้อนจำเพาะ - 0.478 kJ / (kg K);
- ค่าสัมประสิทธิ์ของการขยายตัวเชิงเส้น วัดที่ 20 C เท่ากับ 22.3 10 -6 องศา -1 - ; ความจุความร้อนและการนำความร้อนของสารเพิ่มขึ้นเป็นเส้นตรงเมื่ออุณหภูมิเพิ่มขึ้น
- ความต้านทานไฟฟ้าเฉพาะ - 1.5–2.6 μm m สูงกว่าตะกั่วเพียงเล็กน้อยเท่านั้น
แมงกานีสเป็นสารพาราแมกเนติก กล่าวคือ แมงกานีสถูกทำให้เป็นแม่เหล็กในสนามแม่เหล็กภายนอกและถูกดึงดูดด้วยแม่เหล็ก โลหะจะผ่านเข้าสู่สถานะต้านคลื่นแม่เหล็กไฟฟ้าที่อุณหภูมิต่ำ และอุณหภูมิการเปลี่ยนผ่านสำหรับการดัดแปลงแต่ละครั้งจะแตกต่างกัน
โครงสร้างและองค์ประกอบของแมงกานีสได้อธิบายไว้ด้านล่าง
แมงกานีสและสารประกอบเป็นหัวข้อของวิดีโอด้านล่าง:
โครงสร้างและองค์ประกอบ
มีการอธิบายการดัดแปลงโครงสร้างของสาร 4 แบบ ซึ่งแต่ละแบบมีความเสถียรในช่วงอุณหภูมิที่แน่นอน ฟิวชั่นกับโลหะบางชนิดสามารถทำให้เฟสใดก็ได้เสถียร
- สูงถึง 707 องศาเซลเซียสการปรับเปลี่ยนมีเสถียรภาพ – ลูกบาศก์โครงร่างเป็นศูนย์กลางหน่วยเซลล์ซึ่งมี 58 อะตอม โครงสร้างดังกล่าวมีความซับซ้อนมากและทำให้สารมีความเปราะบางสูง ตัวบ่งชี้ - ความจุความร้อน, การนำความร้อน, ความหนาแน่น, เป็นคุณสมบัติของสาร
- ที่ 700–1079 ซเสถียรคือเฟส b ที่มีโครงร่างแบบเดียวกัน แต่มีโครงสร้างที่ง่ายกว่า: เซลล์มี 20 อะตอม ในระยะนี้ แมงกานีสจะมีลักษณะปั้นเป็นก้อน ความหนาแน่นของการดัดแปลง b คือ 7.26 g / cu ดู แก้ไขเฟสได้ง่าย - โดยการดับสารที่อุณหภูมิสูงกว่าอุณหภูมิเปลี่ยนเฟส
- ที่อุณหภูมิตั้งแต่ 1,079 C ถึง 1,143เฟส g มีความเสถียร ลักษณะเด่นคือโครงตาข่ายทรงลูกบาศก์ที่มีเซลล์ 4 อะตอม การดัดแปลงเป็นพลาสติก อย่างไรก็ตาม ไม่สามารถแก้ไขเฟสได้อย่างสมบูรณ์เมื่อเย็นลง ที่อุณหภูมิทรานซิชัน ความหนาแน่นของโลหะจะอยู่ที่ 6.37 ก./ลบ.ม. ซม. ที่ปกติ - 7, 21 ก. / ลบ.ม. ซม.
- สูงกว่าอุณหภูมิ 1143 C และเดือด d-phase ที่มีโครงตาข่ายลูกบาศก์อยู่ตรงกลางร่างกายนั้นเสถียร เซลล์ประกอบด้วยอะตอม 2 อะตอม ความหนาแน่นของการดัดแปลงคือ 6.28 g/cu ดู ที่น่าสนใจคือ d-Mn สามารถเข้าสู่สถานะต่อต้านคลื่นแม่เหล็กไฟฟ้าที่อุณหภูมิสูง - 303 C
การเปลี่ยนเฟสมีความสำคัญอย่างยิ่งในการได้รับโลหะผสมต่างๆ โดยเฉพาะอย่างยิ่งเนื่องจากลักษณะทางกายภาพของการดัดแปลงโครงสร้างนั้นแตกต่างกัน
การผลิตแมงกานีสมีคำอธิบายด้านล่าง
การผลิต
 โดยทั่วไป แต่ก็มีเงินฝากอิสระเช่นกัน ดังนั้นแร่แมงกานีสสำรองมากถึง 40% ของโลกจึงกระจุกตัวอยู่ในดินแดนของเงินฝาก Chiatura
โดยทั่วไป แต่ก็มีเงินฝากอิสระเช่นกัน ดังนั้นแร่แมงกานีสสำรองมากถึง 40% ของโลกจึงกระจุกตัวอยู่ในดินแดนของเงินฝาก Chiatura
ธาตุจะกระจายอยู่ในหินเกือบทั้งหมดและล้างออกง่าย เนื้อหาในน้ำทะเลมีระดับต่ำ แต่ที่ก้นมหาสมุทรรวมถึงธาตุเหล็กจะก่อตัวเป็นเนื้อเดียวกันซึ่งเนื้อหาขององค์ประกอบถึง 45% เงินฝากเหล่านี้ถือว่ามีแนวโน้มในการพัฒนาต่อไป
มีแมงกานีสสะสมจำนวนมากในรัสเซียดังนั้นสำหรับสหพันธรัฐรัสเซียจึงเป็นวัตถุดิบที่หายากมาก
แร่ที่มีชื่อเสียงที่สุดคือ ไพโรลูไซต์ แมกนีไทต์ บราวไนต์ แมงกานีสสปาร์และอื่นๆ เนื้อหาขององค์ประกอบในนั้นแตกต่างกันไปตั้งแต่ 62 ถึง 69% พวกเขาถูกขุดในเหมืองหินหรือวิธีเหมือง ตามกฎแล้วแร่จะถูกล้างล่วงหน้า
การได้รับแมงกานีสเกี่ยวข้องโดยตรงกับการใช้ ผู้บริโภคหลักคืออุตสาหกรรมเหล็กและสำหรับความต้องการนั้นไม่ใช่โลหะที่จำเป็น แต่เป็นการผสมผสานกับเหล็ก - เฟอร์โรแมงกานีส ดังนั้น เมื่อพูดถึงการผลิตแมงกานีส พวกเขามักจะหมายถึงสารประกอบที่จำเป็นในโลหะวิทยาที่เป็นเหล็ก
ก่อนหน้านี้มีการผลิตเฟอร์โรแมงกานีสในเตาหลอมเหล็ก แต่เนื่องจากการขาดแคลนโค้กและความต้องการใช้แร่แมงกานีสที่ไม่ดี ผู้ผลิตจึงเปลี่ยนมาถลุงในเตาไฟฟ้า
สำหรับการหลอมจะใช้เตาเผาแบบเปิดและปิดที่บุด้วยถ่านหิน - ด้วยวิธีนี้จะได้คาร์บอนเฟอร์โรแมงกานีส การหลอมจะดำเนินการที่แรงดันไฟฟ้า 110-160 V โดยใช้สองวิธี - ฟลักซ์และปราศจากฟลักซ์ วิธีที่สองประหยัดกว่า เนื่องจากช่วยให้สามารถสกัดธาตุได้เต็มที่มากขึ้น อย่างไรก็ตาม ด้วยปริมาณซิลิกาในแร่สูง จึงทำได้เฉพาะวิธีฟลักซ์เท่านั้น
- วิธีการปราศจากฟลักซ์- กระบวนการต่อเนื่อง ส่วนผสมของแร่แมงกานีส ถ่านโค้ก และเศษเหล็กจะถูกโหลดขณะที่หลอมใหม่ สิ่งสำคัญคือต้องแน่ใจว่าปริมาณของตัวรีดิวซ์เพียงพอ เฟอร์โรแมงกานีสและตะกรันผลิตพร้อมกัน 5-6 ครั้งต่อกะ
- ซิลิโคแมงกานีสผลิตด้วยวิธีที่คล้ายกันในเตาหลอมไฟฟ้า ค่าใช้จ่ายนอกเหนือจากแร่รวมถึงตะกรันแมงกานีส - ไม่มีฟอสฟอรัส ควอตซ์และโค้ก
- แมงกานีสโลหะได้เช่นเดียวกับการถลุงแร่เฟอร์โรแมงกานีส วัตถุดิบเป็นของเสียจากการหล่อและตัดโลหะผสม หลังจากการหลอมโลหะผสมและส่วนผสม ซิลิโคแมงกานีสจะถูกเติม และ 30 นาทีก่อนที่จะสิ้นสุดการหลอม มันถูกเป่าด้วยลมอัด
- ได้รับสารบริสุทธิ์ทางเคมี อิเล็กโทรไลซิส.
แอปพลิเคชัน
90% ของการผลิตแมงกานีสในโลกไปที่อุตสาหกรรมเหล็ก ยิ่งไปกว่านั้น โลหะส่วนใหญ่ไม่จำเป็นต้องได้รับโลหะผสมแมงกานีสเอง แต่ต้องมีและรวมถึง 1% ขององค์ประกอบ นอกจากนี้ยังสามารถแทนที่นิกเกิลได้อย่างสมบูรณ์หากเนื้อหาเพิ่มขึ้นเป็น 4–16% ความจริงก็คือแมงกานีสนั้นทำให้เฟสออสเทนไนต์เสถียรในเหล็ก
แมงกานีสเป็นโลหะที่มีความน่าสนใจไม่มากเท่ากับคุณสมบัติของสารประกอบหลายชนิด อย่างไรก็ตาม เป็นการยากที่จะประเมินค่าความสำคัญของมันสูงเกินไปในฐานะองค์ประกอบการผสม
ปฏิกิริยาของแมงกานีสออกไซด์กับอลูมิเนียมแสดงให้เห็นในวิดีโอนี้:
 "อย่าผัดผ่อนจนกว่าจะถึงพรุ่งนี้ สิ่งที่คุณเลื่อนได้จนถึงมะรืนนี้" - มาร์ก ทเวน
"อย่าผัดผ่อนจนกว่าจะถึงพรุ่งนี้ สิ่งที่คุณเลื่อนได้จนถึงมะรืนนี้" - มาร์ก ทเวน "ความลับของการเปลี่ยนแปลง คือการมุ่งเน้นไปที่การสร้างสิ่งใหม่ ไม่ใช่การต่อสู้กับสิ่งเก่า" - โสกราตีส
"ความลับของการเปลี่ยนแปลง คือการมุ่งเน้นไปที่การสร้างสิ่งใหม่ ไม่ใช่การต่อสู้กับสิ่งเก่า" - โสกราตีส การตีความ Hexagram 15 นั้นแม่นยำที่สุด
การตีความ Hexagram 15 นั้นแม่นยำที่สุด