การแก้สมการแบบกราฟิก วิธีแก้สมการแบบกราฟิก
กรดคาร์บอกซิลิกเป็นอนุพันธ์ของไฮโดรคาร์บอนที่มีหมู่คาร์บอกซิลตั้งแต่หนึ่งกลุ่มขึ้นไป
จำนวนหมู่คาร์บอกซิลบ่งบอกถึงความเป็นพื้นฐานของกรด
กรดคาร์บอกซิลิกแบ่งออกเป็นกรดคาร์บอกซิลิก monobasic (ประกอบด้วยกลุ่มคาร์บอกซิลหนึ่งกลุ่ม) ขึ้นอยู่กับจำนวนหมู่คาร์บอกซิล กรดไดเบสิก (ประกอบด้วยกลุ่มคาร์บอกซิลสองกลุ่ม) และกรดโพลีบาซิก
ขึ้นอยู่กับชนิดของอนุมูลที่เกี่ยวข้องกับกลุ่มคาร์บอกซิล กรดคาร์บอกซิลิกจะถูกแบ่งออกเป็นอิ่มตัว ไม่อิ่มตัว และอะโรมาติก กรดอิ่มตัวและไม่อิ่มตัวรวมกันภายใต้ชื่อทั่วไปของกรดอะลิฟาติกหรือกรดไขมัน
กรดคาร์บอกซิลิกโมโนเบสิก
1.1 อนุกรมที่คล้ายคลึงกันและระบบการตั้งชื่อ
อนุกรมที่คล้ายคลึงกันของกรดคาร์บอกซิลิกอิ่มตัวชนิดโมโนเบสิก (บางครั้งเรียกว่ากรดไขมัน) เริ่มต้นด้วยกรดฟอร์มิก

สูตรอนุกรมที่คล้ายคลึงกัน
ระบบการตั้งชื่อของ IUPAC ช่วยให้กรดหลายชนิดสามารถคงชื่อที่ไม่สำคัญไว้ได้ ซึ่งโดยปกติจะระบุถึงแหล่งธรรมชาติที่ใช้แยกกรดเฉพาะ เช่น ฟอร์มิก อะซิติก บิวไทริก วาเลริก เป็นต้น
สำหรับกรณีที่ซับซ้อนกว่านั้น ชื่อของกรดได้มาจากชื่อของไฮโดรคาร์บอนที่มีจำนวนอะตอมของคาร์บอนเท่ากันกับในโมเลกุลของกรดโดยเติมคำลงท้าย -ใหม่และคำพูด กรด.กรดฟอร์มิก H-COOH เรียกว่ากรดเมทาโนอิก กรดอะซิติก CH 3 -COOH เรียกว่ากรดเอทาโนอิก เป็นต้น
ดังนั้นกรดจึงถือเป็นอนุพันธ์ของไฮโดรคาร์บอน โดยหนึ่งหน่วยจะถูกแปลงเป็นคาร์บอกซิล:

เมื่อรวบรวมชื่อของกรดสายโซ่กิ่งตามระบบการตั้งชื่อที่มีเหตุผลจะถือว่าเป็นอนุพันธ์ของกรดอะซิติกในโมเลกุลที่อะตอมไฮโดรเจนถูกแทนที่ด้วยอนุมูลเช่นกรดไตรเมทิลอะซิติก (CH 3) 3 C - COOH
1.2 คุณสมบัติทางกายภาพของกรดคาร์บอกซิลิก
จากมุมมองที่เป็นทางการเท่านั้นที่สามารถพิจารณาหมู่คาร์บอกซิลเป็นการรวมกันของฟังก์ชันคาร์บอนิลและไฮดรอกซิล ในความเป็นจริงอิทธิพลซึ่งกันและกันของพวกเขาทำให้คุณสมบัติของพวกเขาเปลี่ยนแปลงไปโดยสิ้นเชิง
โพลาไรเซชันของพันธะคู่ C=0 ซึ่งตามปกติสำหรับคาร์บอนิล เพิ่มขึ้นอย่างมากเนื่องจากการหดตัวเพิ่มเติมของคู่อิเล็กตรอนอิสระจากอะตอมออกซิเจนที่อยู่ใกล้เคียงของกลุ่มไฮดรอกซิล:

ผลที่ตามมาคือการอ่อนตัวลงอย่างมีนัยสำคัญของพันธะ O-H ในไฮดรอกซิลและความง่ายในการแยกอะตอมไฮโดรเจนออกมาในรูปของโปรตอน (H +)
การปรากฏของความหนาแน่นของอิเล็กตรอนที่ลดลง (δ+) บนอะตอมคาร์บอนส่วนกลางของคาร์บอกซิลยังนำไปสู่การหดตัวของอิเล็กตรอนของพันธะ C-C ที่อยู่ใกล้เคียงกับหมู่คาร์บอกซิล และลักษณะที่ปรากฏ (เช่นในอัลดีไฮด์และคีโตน) ของการลดลง ความหนาแน่นของอิเล็กตรอน (δ +) บนอะตอมα-คาร์บอนของกรด
กรดคาร์บอกซิลิกทั้งหมดมีความเป็นกรด (ตรวจพบโดยตัวชี้วัด) และก่อตัวเป็นเกลือด้วยไฮดรอกไซด์ ออกไซด์ และคาร์บอเนตของโลหะ และกับโลหะที่ออกฤทธิ์:
กรดคาร์บอกซิลิกในกรณีส่วนใหญ่ในสารละลายที่เป็นน้ำจะถูกแยกตัวออกเพียงเล็กน้อยและเป็นกรดอ่อน ซึ่งด้อยกว่ากรดอย่างไฮโดรคลอริก ไนตริก และซัลฟิวริกอย่างมาก ดังนั้นเมื่อละลายหนึ่งโมลในน้ำ 16 ลิตรระดับการแยกตัวของกรดฟอร์มิกคือ 0.06 กรดอะซิติกคือ 0.0167 ในขณะที่กรดไฮโดรคลอริกที่มีการเจือจางดังกล่าวจะแยกตัวออกเกือบทั้งหมด สำหรับกรดคาร์บอกซิลิกชนิดโมโนเบสิกส่วนใหญ่ อาร์เค ก
= 4.8 มีเพียงกรดฟอร์มิกเท่านั้นที่มีค่า pKa ต่ำกว่า (ประมาณ 3.7) ซึ่งอธิบายได้จากการไม่มีผลกระทบจากการบริจาคอิเล็กตรอนของกลุ่มอัลคิล

ในกรดแร่ปราศจากน้ำ กรดคาร์บอกซิลิกจะถูกโปรตอนที่ออกซิเจนเพื่อสร้างคาร์โบแคต:

การเปลี่ยนแปลงความหนาแน่นของอิเล็กตรอนในโมเลกุลของกรดคาร์บอกซิลิกที่ไม่แยกออกจากกันตามที่กล่าวไว้ข้างต้น จะช่วยลดความหนาแน่นของอิเล็กตรอนบนอะตอมออกซิเจนไฮดรอกซิล และเพิ่มบนอะตอมออกซิเจนคาร์บอนิล การเปลี่ยนแปลงนี้จะเพิ่มขึ้นอีกในไอออนของกรด:
ผลลัพธ์ของการเปลี่ยนแปลงคือการทำให้ประจุในประจุลบเท่ากันอย่างสมบูรณ์ ซึ่งมีอยู่จริงในรูปแบบ A - การสั่นพ้องของประจุลบของคาร์บอกซิเลท
ตัวแทนสี่คนแรกของชุดกรดคาร์บอกซิลิกคือของเหลวเคลื่อนที่ซึ่งผสมกับน้ำได้ทุกประการ กรดซึ่งเป็นโมเลกุลที่ประกอบด้วยอะตอมของคาร์บอนตั้งแต่ห้าถึงเก้าอะตอม (เช่นเดียวกับกรดไอโซบิวทีริก) เป็นของเหลวที่มีน้ำมันความสามารถในการละลายในน้ำต่ำ
กรดฟอร์มิก อะซิติก และโพรพิโอนิกมีกลิ่นฉุน สมาชิกระดับกลางของซีรีส์มีกลิ่นอันไม่พึงประสงค์ ส่วนกรดที่สูงกว่าจะไม่มีกลิ่น

คุณสมบัติทางกายภาพของกรดคาร์บอกซิลิกได้รับผลกระทบจากความสัมพันธ์ที่มีนัยสำคัญเนื่องจากการก่อตัวของพันธะไฮโดรเจน กรดจะสร้างพันธะไฮโดรเจนที่แข็งแกร่งเนื่องจากพันธะ O-H ที่อยู่ในนั้นมีขั้วสูง 
นอกจากนี้กรดคาร์บอกซิลิกยังสามารถสร้างพันธะไฮโดรเจนโดยการมีส่วนร่วมของอะตอมออกซิเจนของไดโพลคาร์บอนิลซึ่งมีอิเล็กโตรเนกาติวีตี้อย่างมีนัยสำคัญ แท้จริงแล้วในสถานะของแข็งและของเหลว กรดคาร์บอกซิลิกส่วนใหญ่มีอยู่ในรูปของไซคลิกไดเมอร์:
โครงสร้างไดเมอร์ริกดังกล่าวจะยังคงอยู่ในระดับหนึ่งแม้ในสถานะก๊าซและในสารละลายเจือจางในตัวทำละลายที่ไม่มีขั้ว
กรดคาร์บอกซิลิกเป็นกรดอินทรีย์ พวกมันเป็นส่วนหนึ่งของสิ่งมีชีวิตและมีส่วนร่วมในการเผาผลาญ คุณสมบัติทางเคมีของกรดคาร์บอกซิลิกถูกกำหนดโดยการมีอยู่ของกลุ่มคาร์บอกซิล -COOH ซึ่งรวมถึงอะซิติก ฟอร์มิก ออกซาลิก บิวทีริก และกรดอื่นๆ อีกจำนวนหนึ่ง
คำอธิบายทั่วไป
- มีหลายวิธีในการรับกรดคาร์บอกซิลิก:
- ออกซิเดชันของแอลกอฮอล์ - C 2 H 5 OH + O2 → CH 3 COOH + H 2 O (กรดอะซิติกเกิดขึ้นจากเอทานอล)
- ออกซิเดชันของอัลดีไฮด์ - CH 3 COH + [O] → CH 3 COOH;
- ออกซิเดชันของบิวเทน - 2C 4 H 10 + 5O 2 → 4CH 3 COOH + 2H 2 O;
- แอลกอฮอล์คาร์บอเนต - CH 3 + CO → CH 3 COOH;
- การสลายตัวของกรดออกซาลิกเพื่อผลิตกรดฟอร์มิก - C 2 H 2 O 4 → HCOOH + CO 2;

ปฏิกิริยาของเกลือกับกรดซัลฟิวริกเข้มข้น - CH 3 COONa + H 2 SO 4 → CH 3 COOH + NaHSO 4
ข้าว. 1. วิธีการผลิตกรดคาร์บอกซิลิก
- คุณสมบัติทางกายภาพของกรดคาร์บอกซิลิก:
- จุดเดือดสูงกว่าของไฮโดรคาร์บอนและแอลกอฮอล์ที่เกี่ยวข้อง
- ความสามารถในการละลายที่ดีในน้ำ - ละลายเป็นไอออนบวกของไฮโดรเจนและแอนไอออนของกรดที่ตกค้าง (เป็นอิเล็กโทรไลต์อ่อน)
การเพิ่มจำนวนอะตอมของคาร์บอนจะลดความแข็งแรงของกรด
กรดคาร์บอกซิลิกมีพันธะไฮโดรเจนที่แข็งแกร่ง (แรงกว่าแอลกอฮอล์) ซึ่งเกิดจากประจุบวกสูงบนอะตอมไฮโดรเจนในกลุ่มคาร์บอกซิล
ปฏิสัมพันธ์

กรดคาร์บอกซิลิกเปลี่ยนสีของตัวบ่งชี้ สารลิตมัสและเมทิลออเรนจ์เปลี่ยนเป็นสีแดง
ข้าว. 2. การโต้ตอบกับตัวชี้วัด
|
ตารางคุณสมบัติทางเคมีของกรดคาร์บอกซิลิกอธิบายปฏิกิริยาของกรดกับสารอื่น ๆ |
ปฏิกิริยา |
ผลลัพธ์ |
|
ตัวอย่าง |
ด้วยโลหะ |
ไฮโดรเจนถูกปล่อยออกมาและเกิดเกลือขึ้น |
|
2CH 3 COOH + มก. → (CH 3 COO) 2 มก. + H 2 |
เกลือและน้ำเกิดขึ้น |
2CH 3 COOH + ZnO → (CH 3 COO) 2 Zn + H 2 O |
|
ด้วยเหตุ (การวางตัวเป็นกลาง) |
เกลือและน้ำเกิดขึ้น |
CH 3 COOH + NaOH → CH 3 COONa + H 2 O |
|
ด้วยคาร์บอเนต |
คาร์บอนไดออกไซด์และน้ำถูกปล่อยออกมา |
2CH 3 COOH + CaCO 3 → (CH 3 COO) 2 Ca + H 2 O + CO 2 |
|
ด้วยเกลือของกรดอ่อน |
กรดอนินทรีย์เกิดขึ้น |
2CH 3 COOH + นา 2 SiO 3 → 2CH 3 COONa + H 2 SiO 3 |
|
ด้วยแอมโมเนียหรือแอมโมเนียมไฮดรอกไซด์ |
แอมโมเนียมอะซิเตตเกิดขึ้น เมื่อทำปฏิกิริยากับไฮดรอกไซด์น้ำจะถูกปล่อยออกมา |
CH 3 COOH + NH 3 → CH 3 COONH 4 CH 3 COOH + NH 4 OH → CH 3 COONH 4 + H 2 O |
|
ด้วยแอลกอฮอล์ (เอสเทอริฟิเคชัน) |
เอสเทอร์จะเกิดขึ้น |
CH 3 COOH + C 2 H 5 OH → CH 3 COOC 2 H 5 + H 2 O |
|
ฮาโลเจน |
เกลือจะเกิดขึ้น |
CH 3 COOH + Br 2 → CH 2 BrCOOH |
เกลือที่เกิดจากปฏิกิริยาของสารกับกรดฟอร์มิกเรียกว่ารูปแบบและกรดอะซิติก - อะซิเตต
ดีคาร์บอกซิเลชัน
การกำจัดหมู่คาร์บอกซิลเรียกว่าดีคาร์บอกซิเลชัน ซึ่งเกิดขึ้นในกรณีต่อไปนี้:
- เมื่อให้ความร้อนเกลือต่อหน้าอัลคาไลที่เป็นของแข็งด้วยการก่อตัวของอัลเคน - RCOONa ของแข็ง + NaOH ของแข็ง → RH + Na 2 CO 3;
- เมื่อให้ความร้อนเกลือแข็ง - (CH 3 COO) 2 Ca → CH 3 -CO-CH 3 + CaCO 3;
- เมื่อเผากรดเบนโซอิก - Ph-COOH → PhH + CO 2;
- ระหว่างอิเล็กโทรไลซิสของสารละลายเกลือ - 2RCOONa + H 2 O → R-R + 2CO 2 + 2NaOH

ข้าว. 3. กระบวนการดีคาร์บอกซิเลชัน
เราได้เรียนรู้อะไรบ้าง?
จากบทเรียนชั้นประถมศึกษาปีที่ 10 เราได้เรียนรู้เกี่ยวกับคุณสมบัติทางเคมีและกายภาพพื้นฐานของกรดคาร์บอกซิลิก เกิดขึ้นระหว่างการออกซิเดชันของแอลกอฮอล์ อัลดีไฮด์ บิวเทน ระหว่างคาร์บอนิลเลชัน การสลายตัว และปฏิกิริยากับกรดซัลฟิวริก กรดละลายได้ดีในน้ำและเดือดที่อุณหภูมิสูงกว่าแอลกอฮอล์ ในระหว่างดีคาร์บอกซิเลชัน หมู่ -COOH จะถูกลบออก กรดคาร์บอกซิลิกทำปฏิกิริยากับเกลือ โลหะ ออกไซด์ ไฮดรอกไซด์ เกลือ และแอมโมเนีย
ทดสอบในหัวข้อ
การประเมินผลการรายงาน
คะแนนเฉลี่ย: 4.2. คะแนนรวมที่ได้รับ: 92
กรดคาร์บอกซิลิก (2 บรรยาย)
1. คำจำกัดความ การจำแนกประเภท
2. ไอโซเมอร์ริซึมและการตั้งชื่อของกรดคาร์บอกซิลิกโมโนเบสิก
3. คุณสมบัติทางกายภาพของกรด
4. คุณสมบัติทางเคมี โครงสร้างหมู่คาร์บอนิล
กรดคาร์บอกซิลิก – เป็นอนุพันธ์ของไฮโดรคาร์บอนที่มีหมู่คาร์บอกซิล (-COOH)
การจำแนกประเภทของกรดคาร์บอกซิลิก
กรดคาร์บอกซิลิกแบ่งตามลักษณะโครงสร้างสองประการ
1) ตามจำนวนหมู่คาร์บอกซิลของกรดแบ่งออกเป็น:
Ø ฐานเดี่ยว (โมโนคาร์บอน)
Ø โพลีเบสิก (ไดคาร์บอนิก ไตรคาร์บอนิก ฯลฯ)
. 
2) โดย ธรรมชาติของอนุมูลไฮโดรคาร์บอนกรดมีความโดดเด่น:
Ø การจำกัด (เช่น CH3CH2CH2COOH)
Ø ไม่อิ่มตัว (CH2=CHCH2COOH)
Ø อะโรเมติกส์ (RC6H4COOH)
กรดคาร์บอกซิลิกอิ่มตัวเชิงเดี่ยว
สูตรทั่วไปของกรดดังกล่าวคือ CnH2nO2 หรือ CnH2n+1COOH
ระบบการตั้งชื่อและไอโซเมอริซึมของกรดคาร์บอกซิลิก
กรดที่มีคาร์บอนน้อยกว่า 4 อะตอมจะไม่มีไอโซเมอร์ ถ้าจำนวนอะตอมเป็นสี่ กรดจะมีไอโซเมอร์สองตัว ถ้าจำนวนอะตอมเป็นห้า ก็จะมีไอโซเมอร์ห้าตัว
ระบบการตั้งชื่อประเภทต่อไปนี้ใช้ในการตั้งชื่อกรด:
ü เล็กน้อย
ü มีเหตุผล
ชื่อของกรดคาร์บอกซิลิกถูกสร้างขึ้นโดยใช้ชื่อกรดอะซิติกเป็นเบส กรดที่เหลือถือเป็นอนุพันธ์ของมันโดยแทนที่อะตอมไฮโดรเจนในกลุ่มเมทิลด้วยอนุมูลที่ซับซ้อนมากขึ้น กฎที่เหลือปฏิบัติตามกฎของการตั้งชื่ออย่างมีเหตุผลสำหรับไฮโดรคาร์บอนอย่างสมบูรณ์ (มีรายละเอียดระบุไว้ตอนต้นหลักสูตรการบรรยาย)
เมื่อเขียนชื่อของกรดคาร์บอกซิลิก จะใช้โซ่ที่ยาวที่สุดที่มีหมู่คาร์บอกซิลเป็นพื้นฐาน การกำหนดหมายเลขเริ่มต้นด้วยอะตอมคาร์บอนของกลุ่มคาร์บอกซิล (ไม่ได้ระบุหมายเลขที่ระบุตำแหน่งของหมู่ฟังก์ชัน) ส่วนต่อท้าย - ถูกเพิ่มเข้าไปในชื่อของไฮโดรคาร์บอนตามจำนวนอะตอมของคาร์บอนในสายโซ่หลัก กรดโออิก - ตัวเลขและคำนำหน้าระบุตำแหน่งและจำนวนขององค์ประกอบทดแทน
ระบบการตั้งชื่อของกรดคาร์บอกซิลิกนั้นเหมือนกับระบบการตั้งชื่อของอัลดีไฮด์ ซึ่งทำให้เข้าใจและศึกษาได้ง่ายขึ้นมาก
ชื่อของตัวแทนแต่ละคนของกรดคาร์บอกซิลิก
ชื่อจิ๊บจ๊อย | เหตุผล | ||
มด | มด | มีเทน |
|
น้ำส้มสายชู | น้ำส้มสายชู | อีเทน |
|
CH3-CH2-COOH | โพรพิโอนิก | เมทิลอะซิติก | โพรเพน |
CH3-CH2-CH2-COOH | น้ำมัน | เอทิลอะซิติก | บิวเทน |
CH3-CH2-CH2-CH2-COOH | สืบ | โพรพิลาซิติก | เพนเทน |
| กรดเมทิลเซ็กบิวทิลอะซิติก | 2,3-ไดเมทิลเพนเทน |
การเตรียมกรดคาร์บอกซิลิก
มีการกล่าวถึงวิธีการต่างๆ มากมายในการผลิตกรดโมโนบาซิกในการบรรยายครั้งก่อนๆ:
1) ออกซิเดชันของแอลกอฮอล์
2) โอโซโนไลซิสของอัลคีน
3) ออกซิเดชันของสารประกอบคาร์บอนิล (อัลดีไฮด์และคีโตน)
4) การไฮโดรไลซิสของอนุพันธ์ของ geminal trihalogen ของไฮโดรคาร์บอน (คล้ายกับการไฮโดรไลซิสของอนุพันธ์ไดฮาโลเจนในการผลิตอัลดีไฮด์วิธีที่ 5):

5) การไฮโดรไลซิสของอนุพันธ์ของกรด (อนุพันธ์ของฮาโลเจน, เอสเทอร์, ไนไตรล์)

6) คาร์บอกซิเลชันของสารประกอบออร์กาโนเมทัลลิก
นี่เป็นวิธีการสากลในการรับกรดคาร์บอกซิลิกและเป็นวิธีการในห้องปฏิบัติการ

คุณสมบัติทางกายภาพ
กรดต่ำที่มีจำนวนอะตอม C1-C3 เป็นของเหลวไม่มีสีมีกลิ่นฉุนเป็นลักษณะเฉพาะ
กรดขององค์ประกอบ C4-C9 เป็นของเหลวมันที่มีกลิ่นอันไม่พึงประสงค์ละลายในน้ำได้ไม่ดี
กรดที่มีองค์ประกอบ C10 ขึ้นไปนั้นเป็นของแข็งที่ไม่ละลายในน้ำ
ดังนั้นเมื่อน้ำหนักโมเลกุลเพิ่มขึ้น ความสามารถในการละลายของกรดในน้ำจึงลดลง
จุดเดือดของกรดสูงเกิดจากการก่อตัวของพันธะไฮโดรเจนระหว่างโมเลกุล และความสามารถในการละลายที่ดีในน้ำก็สัมพันธ์กับสิ่งนี้ (พันธะไฮโดรเจนเกิดขึ้นจากโมเลกุลของน้ำ)
https://pandia.ru/text/78/506/images/image008_0.gif" alt="990 ไบต์" width="195" height="91 src=">!}
คุณสมบัติทางเคมีของกรด
โครงสร้างหมู่คาร์บอกซิล
กลุ่มคาร์บอกซิลรวมกลุ่มฟังก์ชันสองกลุ่มเข้าด้วยกัน - คาร์บอนิลและไฮดรอกซิลซึ่งมีอิทธิพลซึ่งกันและกัน:

คุณสมบัติที่เป็นกรดของกรดคาร์บอกซิลิกค่อนข้างเด่นชัด สิ่งนี้อธิบายได้จากอิทธิพลร่วมกันของอะตอมในกลุ่มคาร์บอกซิล ความหนาแน่นของอิเล็กตรอนซึ่งถูกเลื่อนไปที่ออกซิเจนที่มีอิเลคโตรเนกาติตีมากขึ้นของกลุ่มไฮดรอกซี ซึ่งทำให้พันธะ O-H อ่อนลงและอำนวยความสะดวกในการแยกอะตอมไฮโดรเจน กล่าวคือ ช่วยให้กรดแตกตัวได้ง่ายขึ้น (เนื่องจาก +M ผลกระทบของกลุ่ม OH มีชัยเหนือเอฟเฟกต์ –I) การเคลื่อนที่ของโปรตอนที่อยู่ในตำแหน่ง α นั้นถูกกำหนดโดยโครงสร้างของกลุ่ม COOH ด้วย (คำอธิบายโดยละเอียดมีให้ในการบรรยายเรื่อง “อัลดีไฮด์และคีโตน”)
1) คุณสมบัติของกรด
การแยกตัวของกรดในสารละลายที่เป็นน้ำ กรดคาร์บอกซิลิกจะแตกตัวเป็นไอออนและมีปฏิกิริยาที่เป็นกรด สิ่งนี้สามารถตรวจพบได้โดยใช้ตัวบ่งชี้ที่พิจารณา การกำหนดคุณภาพของกรด- เช่น สารลิตมัสจะกลายเป็นสีแดง
https://pandia.ru/text/78/506/images/image011_0.gif" width="476 height=87" height="87">
โครงสร้างการสั่นพ้องขอบเขตของพันธะ C-O นั้นสอดคล้องกัน
Mesomerism เป็นปรากฏการณ์ของการทำให้ความหนาแน่นของอิเล็กตรอนเท่ากันระหว่างอะตอมออกซิเจนสองอะตอม
กรดคาร์บอกซิลิกเป็นกรดที่แรงกว่าแอลกอฮอล์
กรดฟอร์มิกมีความเข้มข้นที่สุด เนื่องจากขาดผลกระทบจากการบริจาคอิเล็กตรอนของกลุ่มอัลคิล สารทดแทนที่มีผลอุปนัยเชิงบวก (ผู้บริจาคอิเล็กตรอน - CH3, C2H5) จะลดความเป็นกรด เป็นการยากกว่าที่จะกำจัดไฮโดรเจนออกจากออกซิเจนในกลุ่ม OH
การก่อตัวของเกลือ- กรดสามารถสร้างเกลือด้วยโลหะ ออกไซด์ และไฮดรอกไซด์ของพวกมัน
ก) เมื่อทำปฏิกิริยากับโลหะ:
2RCOOH + Mg ® (RCOO)2Mg + H2
b) เมื่อทำปฏิกิริยากับไฮดรอกไซด์ของโลหะ:
2RCOOH + NaOH ® RCOONa + H2O
2) ปฏิกิริยาที่กลุ่ม OH
การก่อตัวของเอสเทอร์ (R"–COOR") เป็นปฏิกิริยาเอสเทอริฟิเคชัน นี่คือปฏิกิริยาของกรดกับแอลกอฮอล์เมื่อมีกรดแร่ ปฏิกิริยาสามารถย้อนกลับได้
กรดอะซิติก เอทิลแอลกอฮอล์ เอทิลอะซิติกกรด
กรดที่มีโครงสร้างเป็นเส้นตรง เช่น R-CH2-COOH มีแนวโน้มที่จะทำปฏิกิริยามากกว่ากรดที่มีโครงสร้างเป็นกิ่ง: R2CH-COOH, R3C-COOH บทบาทของตัวเร่งปฏิกิริยาในปฏิกิริยาเอสเทอริฟิเคชันเล่นโดยไอออน H+:

ปฏิกิริยาเกิดขึ้นตามกลไกต่อไปนี้: ออกซิเจนของกลุ่มคาร์บอนิลจับโปรตอนและก่อตัวเป็นคาร์โบเคชัน ฉัน. คาร์โบไฮเดรตนี้จะยึดโมเลกุลแอลกอฮอล์ผ่านอะตอมออกซิเจนคู่เดียวเพื่อสร้างสารเชิงซ้อน ครั้งที่สอง- ซับซ้อน ครั้งที่สองสามารถย่อยสลายและก่อตัวเป็นคาร์โบเคชันแบบพลิกกลับได้ ที่สามเมื่อแยกตัวออกจากกันซึ่งเกิดเอสเทอร์ (ตัวเร่งปฏิกิริยา - โปรตอนจึงถูกปล่อยออกมา)
สิ่งที่น่าสนใจอย่างยิ่งในปฏิกิริยานี้คือคำถามที่ว่ากรดหรือแอลกอฮอล์กำจัดไฮดรอกซิลในปฏิกิริยาการเกิดเอสเทอร์หรือไม่ การใช้ "อะตอมที่มีป้ายกำกับ" (ไอโซโทปหนัก 18O) แสดงให้เห็นว่าน้ำเกิดขึ้นเนื่องจากไฮโดรเจนของแอลกอฮอล์และกรดไฮดรอกซิล

(หากระบุว่าออกซิเจนอยู่ในแอลกอฮอล์ น้ำที่ได้ก็จะประกอบด้วยออกซิเจนธรรมดา)
ปฏิกิริยาที่มีการแทนที่หมู่ OH โดยสมบูรณ์
การเตรียมอนุพันธ์ของกรดคาร์บอกซิลิก
1) กรดเฮไลด์สามารถรับได้จากการกระทำของฟอสฟอรัสเพนตะคลอไรด์ (PCl5), ไทโอนิลคลอไรด์ (SOCl2)

2) ฮาโลเจนในกรดเฮไลด์นั้นมีปฏิกิริยาสูง ดังนั้นกรดเฮไลด์จึงถูกใช้เป็นสารอะซิเลต นี่คือวิธีการเตรียมกรดแอนไฮไดรด์

ตัวอย่างเช่น อะซิติกแอนไฮไดรด์ (R = CH3) ใช้ในการสังเคราะห์สารอินทรีย์เป็นสารกำจัดน้ำอย่างเข้มข้น
3) การก่อตัวของเอไมด์นั้นเกิดจากการกระทำของแอมโมเนีย
ไขมันในฐานะเอสเทอร์มีลักษณะเป็นปฏิกิริยาไฮโดรไลซิสแบบผันกลับได้ซึ่งเร่งปฏิกิริยาด้วยกรดแร่ ด้วยการมีส่วนร่วมของด่าง การไฮโดรไลซิสของไขมันจะเกิดขึ้นอย่างถาวร สินค้าในกรณีนี้คือ สบู่- เกลือของกรดคาร์บอกซิลิกที่สูงขึ้นและโลหะอัลคาไล
https://pandia.ru/text/78/506/images/image023_0.gif" width="103" height="53">
กรดอะคริลิกได้มาจากการสังเคราะห์ เป็นของเหลวที่มีกลิ่นฉุน พอลิเมอร์ได้ง่าย ๆ เพื่อสร้างกรดโพลีอะคริลิก
อะคริลิกแอซิดเอสเทอร์หรือผลิตภัณฑ์โพลีเมอไรเซชันมีความสำคัญในทางปฏิบัติอย่างมาก:

กรดอะคริลิกเอทิลเอสเตอร์
โพลีอะคริเลตมีความโปร่งใสและใช้ในการผลิตพลาสติกและแก้วออร์แกนิกหลายชนิด เมทาคริเลต ซึ่งเป็นเอสเทอร์ของกรดเมทาคริลิก มีความแข็งมากกว่าโพลีอะคริเลต
แก้วอินทรีย์ที่ดีที่สุดคือลูกแก้ว - กรดโพลีเมทาอะคริลิกเมทิลเอสเตอร์ Plexiglas ใช้ในการแพทย์เพื่อทำขาเทียม

กรดเมทาคริลิก เมทิลเอสเตอร์
โดยทั่วไป กรดไม่อิ่มตัวมีลักษณะเฉพาะของปฏิกิริยาหลายอย่างของอัลคีน: การเติมฮาโลเจน, ไฮโดรเจนที่พันธะพหุคูณ, ออกซิเดชันกับโพแทสเซียมเปอร์แมงกาเนต, การสังเคราะห์ไดอีน
กรดคาร์บอกซิลิก Dibasic
กรด dibasic ที่ง่ายที่สุดคือกรดออกซาลิก (พบครั้งแรกในสีน้ำตาล) หรือกรดเอเทนไดโออิก ตัวแทนต่อไปคือกรดมาโลนิกหรือโพรเพนดิโออิก กรดไดบาซิกที่มีคาร์บอน 4 อะตอมเรียกว่ากรดซัคซินิกหรือกรดบิวเทนไดโออิก
ปฏิกิริยาที่สำคัญที่สุดของกรดดังกล่าวคือการผลิตโพลีเมอร์ควบแน่น
ปฏิกิริยาเอสเทอริฟิเคชันและการผลิตเอไมด์ของกรดไดคาร์บอกซิลิกเป็นรากฐานของการผลิตทางอุตสาหกรรมที่มีความสำคัญอย่างยิ่งในทางปฏิบัติ โพลีเมอร์ควบแน่น
การควบแน่นของกรดไดคาร์บอกซิลิกและอัลเคนไดออลทำให้เกิดโพลีเอสเตอร์ โพลีเอสเตอร์ถูกนำมาใช้กันอย่างแพร่หลายในการผลิตเส้นใยสังเคราะห์
ลาฟซานเป็นหนึ่งในโพลีเอสเตอร์ที่สำคัญที่สุดซึ่งได้มาจากการควบแน่นของกรดเทเรฟทาลิกและเอทิลีนไกลคอล

การควบแน่นของกรดไดคาร์บอกซิลิกกับไดเอมีนทำให้เกิดฟอง ใยสังเคราะห์- โพลีเอไมด์ใช้ในการผลิตวัสดุสังเคราะห์ ( ขนสัตว์สังเคราะห์- โพลีเอไมด์ที่มีความสำคัญในทางปฏิบัติคือไนลอน-6,6 นั้นได้มาจากการควบแน่นของกรดอะดิปิกและเฮกซาเมทิลีนไดเอมีน

เมื่อขยายแล้วจะมีลักษณะดังนี้:

ในชื่อ "nylon-6,6" ตัวเลขแรกระบุจำนวนอะตอมของคาร์บอนในกรดไดคาร์บอกซิลิก และตัวเลขตัวที่สองระบุจำนวนอะตอมของคาร์บอนในไดเอมีน
หากส่วนผสมของกรดอะโรมาติกไดคาร์บอกซิลิก (เช่น กรดเทเรฟทาลิก) และอะโรมาติกไดเอมีนอยู่ภายใต้กระบวนการโพลีคอนเดนเซชัน จะได้วัสดุโพลีเอไมด์ที่มีความแข็งแรงเทียบเท่ากับผลิตภัณฑ์เหล็ก:
กรดคาร์บอกซิลิก กรดคาร์บอกซิลิกไม่อิ่มตัว (ไม่อิ่มตัว) เป็นสารประกอบที่มีอนุมูลไฮโดรคาร์บอนมีพันธะหลายพันธะ กรดอะคริลิก (โพรพีโนอิก) CH2=CH - COOH เป็นของเหลวที่มีกลิ่นฉุน ผสมกับน้ำได้ทุกประการ ใช้กันอย่างแพร่หลายในการผลิตโพลีเมอร์ต่างๆ กรดโอเลอิก C8H,7CH=CH - (CH^-COOH มีอยู่ในรูปของไกลด์ไรด์ในน้ำมันพืชและไขมันสัตว์ส่วนใหญ่ ได้มาจากไฮโดรไลซิส เป็นของเหลวมันไม่มีสี ออกซิไดซ์ได้ง่ายในอากาศ ละลายได้ในตัวทำละลายอินทรีย์และละลายไม่ได้ ที่มีน้ำ ใช้ในการผลิตน้ำหอมและเครื่องสำอาง โฟมทำความสะอาด สารทำให้เปียก และกรดไลโนเลอิก CH3 - (CH2)3 - (CH2 - CH - CH)2 - (CH2)7 - COOH ของกลีเซอไรด์ในน้ำมันพืช การไฮโดรไลซิส เป็นของเหลวสีเหลืองอ่อน ละลายได้ดีในตัวทำละลายอินทรีย์และไม่ละลายน้ำ ได้มาจากการไฮโดรไลซิส กรดไลโนเลอิคและกรดไลโนเลนิกไม่ได้สังเคราะห์ขึ้นในร่างกายมนุษย์และสัตว์ แต่มีความจำเป็นต่อชีวิตจึงถูกส่งเข้าสู่ร่างกายด้วยอาหารดังนั้นจึงจัดเป็นกรดไขมันจำเป็น
วิธีการได้รับ- 1. ออกซิเดชันของอัลดีไฮด์และแอลกอฮอล์ปฐมภูมิเป็นวิธีการทั่วไปในการเตรียมกรดคาร์บอกซิลิก />K M n O 4 และ K 2 C r 2 O 7 ถูกใช้เป็นตัวออกซิไดซ์
2 วิธีการทั่วไปอีกวิธีหนึ่งคือการไฮโดรไลซิสของไฮโดรคาร์บอนที่มีฮาโลเจนซึ่งมีอะตอมฮาโลเจนสามอะตอมต่ออะตอมของคาร์บอน ในกรณีนี้ จะเกิดแอลกอฮอล์ที่มีหมู่ OH บนอะตอมของคาร์บอนหนึ่งอะตอม - แอลกอฮอล์ดังกล่าวจะไม่เสถียรและแยกน้ำออกเป็นกรดคาร์บอกซิลิก:
| ซนาออน | ||||
| อาร์-ซีซีแอล 3 | → | R - COOH + H 2 O | ||
| -3โซเดียมคลอไรด์ |
3. การได้รับกรดคาร์บอกซิลิกจากไซยาไนด์ (ไนไตรล์) เป็นวิธีการสำคัญที่ช่วยให้คุณสามารถเพิ่มห่วงโซ่คาร์บอนเมื่อได้รับไซยาไนด์ดั้งเดิม อะตอมของคาร์บอนเพิ่มเติมจะถูกนำเข้าไปในโมเลกุลโดยใช้ปฏิกิริยาของการแทนที่ฮาโลเจนในโมเลกุลฮาโลคาร์บอนด้วยโซเดียมไซยาไนด์ตัวอย่างเช่น:
CH 3 -B ร + NaCN→ CH 3 - CN + NaBr.
กรดอะซิติกไนไตรล์ที่เกิดขึ้น (เมทิลไซยาไนด์) ไฮโดรไลซ์ได้ง่ายเมื่อถูกความร้อนให้กลายเป็นแอมโมเนียมอะซิเตต:
CH 3 CN + 2H 2 O → CH 3 COONH 4
เมื่อสารละลายมีความเป็นกรด กรดจะถูกปล่อยออกมา:
CH 3 COONH 4 + เอชซีแอล→ CH 3 COOH + NH 4 Cl.
4. การใช้งาน รีเอเจนต์กริกนาร์ดตามโครงการ:/>
เอช 2 โอ
ร— มก+ CO 2 → R — COO — มก→ R - COOH + มก. (OH) Br
5. การไฮโดรไลซิสของเอสเทอร์:/>
R - COOR 1 + KON → R - ปรุงอาหาร + โรห์
R - ปรุงอาหาร + เอชซีแอล → ร— ซีโอโอ+ เคซีแอล .
6. การไฮโดรไลซิสของกรดแอนไฮไดรด์:/>
(RCO) 2 O + H 2 O → 2 RCOOH
7. มีวิธีการเตรียมกรดแต่ละชนิดโดยเฉพาะ/>
กรดฟอร์มิกเตรียมโดยการให้ความร้อนคาร์บอนมอนอกไซด์ (ครั้งที่สอง ) ด้วยโซเดียมไฮดรอกไซด์ที่เป็นผงภายใต้ความดันและบำบัดรูปแบบโซเดียมที่เป็นผลลัพธ์ด้วยกรดแก่:
กรดอะซิติกผลิตโดยตัวเร่งปฏิกิริยาออกซิเดชันของบิวเทนกับออกซิเจนในบรรยากาศ:
2C 4 H 10 + 5 O 2 → 4CH 3 COOH + 2H 2 โอ
เพื่อให้ได้กรดเบนโซอิกคุณสามารถใช้การออกซิเดชันของสารเบนซีนที่คล้ายคลึงกันแบบ monosubstituted กับสารละลายที่เป็นกรดของโพแทสเซียมเปอร์แมงกาเนต:
5C 6 H 5 -CH 3 + 6 KMnO 4 + 9 H 2 SO 4 = 5C 6 H 5 COOH + 3 K 2 SO 4 + 6 มสธ 4 + 14 ชม. 2 โอ
นอกจากนี้กรดเบนโซอิกสามารถเตรียมได้จากการใช้เบนซาลดีไฮด์ ปฏิกิริยาของ Cannizzaro- ในปฏิกิริยานี้ เบนซาลดีไฮด์จะได้รับการบำบัดด้วยสารละลายโซเดียมไฮดรอกไซด์ 40-60% ที่อุณหภูมิห้อง การเกิดออกซิเดชันและการรีดักชันพร้อมกันทำให้เกิดการก่อตัว กรดเบนโซอิกและฟีนิลเมทานอล (เบนซิลแอลกอฮอล์):
คุณสมบัติทางเคมี- กรดคาร์บอกซิลิกเป็นกรดที่แรงกว่าแอลกอฮอล์ เนื่องจากอะตอมไฮโดรเจนในกลุ่มคาร์บอกซิลมีความคล่องตัวเพิ่มขึ้นเนื่องจากอิทธิพลของกลุ่ม CO ในสารละลายที่เป็นน้ำ กรดคาร์บอกซิลิกจะแยกตัวออก:
RCOOH ![]() RCOO—+H+
RCOO—+H+
อย่างไรก็ตามเนื่องจากธรรมชาติของโมเลกุลคาร์บอนเป็นโควาเลนต์ y กรด ความสมดุลของการแยกตัวข้างต้นก็เพียงพอแล้วขยับไปทางซ้ายอย่างรุนแรง ดังนั้นกรดคาร์บอกซิลิก - สิ่งเหล่านี้มักเป็นกรดอ่อน ตัวอย่างเช่น อีเทน (อะซิติก)กรดมีลักษณะเป็นค่าคงที่การแยกตัว K a = 1.7*10 -5/>
สารทดแทนที่มีอยู่ในโมเลกุลของกรดคาร์บอกซิลิกมีอิทธิพลอย่างมากต่อความเป็นกรดเนื่องจากผลกระทบที่มี ผลอุปนัย- สารทดแทน เช่น คลอรีนหรืออนุมูลฟีนิลดึงดูดความหนาแน่นของอิเล็กตรอน ดังนั้นจึงทำให้เกิดผลเชิงลบต่อการเหนี่ยวนำ (-/) การถอนความหนาแน่นของอิเล็กตรอนออกจากอะตอมไฮโดรเจนคาร์บอกซิลทำให้กรดคาร์บอกซิลิกมีความเป็นกรดเพิ่มขึ้น กรด ในทางตรงกันข้าม สารทดแทน เช่น หมู่อัลคิล มีคุณสมบัติในการบริจาคอิเล็กตรอน และสร้างผลอุปนัยเชิงบวก +I พวกเขาลดความเป็นกรด ผลของสารทดแทนต่อความเป็นกรดของกรดคาร์บอกซิลิกแสดงให้เห็นอย่างชัดเจนในค่าคงที่การแยกตัวออกจากกันเค สำหรับกรดจำนวนหนึ่ง นอกจากนี้ความแรงของกรดได้รับอิทธิพลจากการมีพันธะพหุคูณแบบคอนจูเกต
|
สูตรกรดคาร์บอกซิลิกเค |
|
โพรพิโอนิก CH 3 CH 2 COOH 1.3*10 -5 |
|
น้ำมัน CH 3 CH 2 CH 2 COOH 1.5*10 -5 |
|
อะซิติก CH 3 COOH 1.7*10 -5 |
|
เปล้า CH 3 - CH = CH - COOH 2.0 * 10 -5 |
|
ไวนิลอะซิติก CH 2 = CH-CH 2 COOH 3.8*10 -5 |
|
อะคริลิก CH 2 =CH-COOH 5.6*10 -5 |
|
ฟอร์มิค HCOOH 6.1*10 -4 |
|
เบนโซอิก C 6 H 5 COOH 1.4*10 -4 |
|
คลอโรอะซิติก CH 2 ClCOOH 2.2*10 -3 |
|
เทโทรนิค CH 3 - C ≡ C - COOH 1.3*10 -3 |
|
ไดคลอโรอะซิติก ซีเอชซีแอล 2 COOH 5.6*10 -2 |
|
ออกซาลิก HOOC - COOH 5.9*10 -2 |
|
ไตรคลอโรอะซิติกซีซีแอล 3 COOH 2.2*10 -1 |
อิทธิพลร่วมกันของอะตอมในโมเลกุลของกรดไดคาร์บอกซิลิกนำไปสู่ความจริงที่ว่าพวกมันแข็งแกร่งกว่ากรดโมโนบาซิก
2. การก่อตัวของเกลือ กรดคาร์บอกซิลิกมีคุณสมบัติเหมือนกรดธรรมดาทั้งหมด พวกมันทำปฏิกิริยากับโลหะแอคทีฟ ออกไซด์พื้นฐาน เบสและเกลือของกรดอ่อน:
2 RCOOH + M ก. → (RCOO) 2 Mg + H 2,
2 RCOOH + CaO → (RCOO) 2 Ca + H 2 O,
RCOOH+ NaOH → อาร์คูน่า+ ชม 2 โอ
RCOOH+ NaHCO 3 → อาร์คูน่า+ เอช 2 โอ + คาร์บอนไดออกไซด์ 2
กรดคาร์บอกซิลิกมีความอ่อนแอ กรดแร่เข้มข้นจึงเข้ามาแทนที่เกลือที่เกี่ยวข้อง:
ช 3 คูน่า + เอชซีแอล→ CH 3 COOH + โซเดียมคลอไรด์.
เกลือของกรดคาร์บอกซิลิกในสารละลายที่เป็นน้ำจะถูกไฮโดรไลซ์:
CH 3 ปรุงอาหาร + H 2 O ![]() CH 3 COOH + คอน
CH 3 COOH + คอน
ความแตกต่างระหว่างกรดคาร์บอกซิลิกและกรดแร่คือความเป็นไปได้ในการสร้างอนุพันธ์เชิงฟังก์ชันจำนวนหนึ่ง
3. การก่อตัวของอนุพันธ์เชิงฟังก์ชันของกรดคาร์บอกซิลิก เมื่อแทนที่หมู่ OH ในกรดคาร์บอกซิลิกด้วยหมู่ต่างๆ (/>X ) อนุพันธ์เชิงหน้าที่ของกรดเกิดขึ้นโดยมีสูตรทั่วไป R-CO-X; ที่นี่ร หมายถึงหมู่อัลคิลหรือหมู่เอริล แม้ว่าไนไตรล์จะมีสูตรทั่วไปที่แตกต่างกัน (อาร์-ซีเอ็น ) โดยปกติจะถือว่าเป็นอนุพันธ์ของกรดคาร์บอกซิลิกเนื่องจากสามารถเตรียมได้จากกรดเหล่านี้
กรดคลอไรด์เกิดจากการกระทำของฟอสฟอรัสคลอไรด์ ( V) สำหรับกรด:
R-CO-OH + PC l 5 → R-CO- แคล+ ROS l 3 + เอชซีแอล
|
ตัวอย่างการเชื่อมต่อ |
|
กรด
เอทาโนอิก (อะซิติก) กรดเบนโซอิก กรดคลอไรด์
เอทานอลคลอไรด์ เบนโซอิลคลอไรด์ (อะเซทิลคลอไรด์) กรดแอนไฮไดรด์
อีเทน (อะซิติก) เบนโซอิกแอนไฮไดรต์ แอนไฮไดรต์ เอสเทอร์
เอทิลเอทาโนเอต (เอทิลอะซิเตต) เมทิลเบนโซเอต เอไมด์ เอทานาไมด์(อะเซทาไมด์) เบนซาไมด์ ไนไตรล์ เอธานไนไตรล์ เบนโซไนไทรล์ (อะซีโตไนไตรล์) |
แอนไฮไดรด์เกิดจากกรดคาร์บอกซิลิกภายใต้การกระทำของสารกำจัดน้ำ:
2 R - CO - OH + P 2 O 5 → (R - CO -) 2 O + 2HPO 3
เอสเทอร์เกิดขึ้นจากการให้ความร้อนกรดกับแอลกอฮอล์โดยมีกรดซัลฟิวริกอยู่ด้วย (ปฏิกิริยาเอสเทอริฟิเคชันแบบผันกลับได้):
มีการสร้างกลไกของปฏิกิริยาเอสเทอริฟิเคชันแล้ว โดยวิธี "อะตอมที่มีป้ายกำกับ"
เอสเทอร์สามารถหาได้จากการทำปฏิกิริยากับกรดคลอไรด์และแอลกอฮอล์ของโลหะอัลคาไล:
R-CO-Cl + Na-O-R’ → R-CO-OR’ + NaCl
ปฏิกิริยาของกรดคาร์บอกซิลิกคลอไรด์กับแอมโมเนียทำให้เกิดเอไมด์:
CH 3 -CO-C ล + CH 3 → CH 3 -CO-CH 2 +เอชซีแอล
นอกจากนี้สามารถเตรียมเอไมด์ได้ด้วยการให้ความร้อนเกลือแอมโมเนียมของกรดคาร์บอกซิลิก:
เมื่อเอไมด์ถูกให้ความร้อนต่อหน้าสารแยกน้ำ สารเหล่านี้จะคายน้ำออกเพื่อสร้างไนไตรล์:
| อาร์ 2 0 5 | ||
| CH 3 - CO - NH 2 |
→ |
CH 3 - C ≡ N + H 2 O |
อนุพันธ์เชิงหน้าที่ของกรดต่ำกว่าคือของเหลวที่ระเหยได้ ทั้งหมดนี้ถูกไฮโดรไลซ์อย่างง่ายดายเพื่อสร้างกรดต้นกำเนิด:
R-CO-X + H 2 O → R-CO-OH + HX
ในสภาพแวดล้อมที่เป็นกรด ปฏิกิริยาเหล่านี้สามารถย้อนกลับได้ การไฮโดรไลซิสในสภาพแวดล้อมที่เป็นด่างนั้นไม่สามารถย้อนกลับได้และนำไปสู่การก่อตัวของเกลือของกรดคาร์บอกซิลิก ตัวอย่างเช่น:
R-CO-OR ' + NaOH → R-CO-ONa + R’OH
4. คุณสมบัติหลายประการของกรดคาร์บอกซิลิกเกิดจากการมีอนุมูลไฮโดรคาร์บอน ดังนั้นเมื่อฮาโลเจนทำปฏิกิริยากับกรดเมื่อมีฟอสฟอรัสแดง กรดทดแทนฮาโลเจนก็จะเกิดขึ้น และอะตอมไฮโดรเจนที่อะตอมคาร์บอน (a-อะตอม) ที่อยู่ติดกับหมู่คาร์บอกซิลจะถูกแทนที่ด้วยฮาโลเจน:
| ร cr | ||
|
CH 3 -CH 2 -COOH + Br 2 |
→ |
CH 3 -CHBr-COOH + HBr |
กรดคาร์บอกซิลิกไม่อิ่มตัวสามารถทำปฏิกิริยาเพิ่มเติมได้:
CH 2 = CH-COOH + H 2 → CH 3 -CH 2 -COOH,
CH 2 =CH-COOH + C l 2 → CH 2 C l -SHC l -COOH,
CH 2 =CH-COOH + HCl → CH 2 C l -CH 2 -COOH,
CH 2 = CH-COOH + H 2 O → HO-CH 2 -CH 2 -COOH,
ปฏิกิริยาสองประการสุดท้ายดำเนินไปโดยขัดต่อกฎของมาร์คอฟนิคอฟ
กรดคาร์บอกซิลิกไม่อิ่มตัวและอนุพันธ์ของพวกมันสามารถทำได้ ปฏิกิริยาการเกิดพอลิเมอไรเซชัน.

5. ปฏิกิริยารีดอกซ์ของกรดคาร์บอกซิลิก/>
กรดคาร์บอกซิลิกภายใต้การกระทำของสารรีดิวซ์เมื่อมีตัวเร่งปฏิกิริยาสามารถเปลี่ยนเป็นอัลดีไฮด์ แอลกอฮอล์ และแม้แต่ไฮโดรคาร์บอนได้:
กรดฟอร์มิก HCOOH มีคุณสมบัติหลายประการ เนื่องจากมีกลุ่มอัลดีไฮด์:
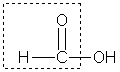
กรดฟอร์มิกเป็นตัวรีดิวซ์ที่แรงและสามารถออกซิไดซ์เป็น CO 2 ได้ง่าย เธอให้ ปฏิกิริยา "กระจกสีเงิน":
HCOOH + 2OH → 2Ag + (NH 4) 2 CO 3 + 2NH 3 + H 2 O,
หรือในรูปแบบที่เรียบง่าย:
C H 3 HCOOH + Ag 2 O → 2Аg + CO 2 + H 2 O
นอกจากนี้กรดฟอร์มิกยังถูกออกซิไดซ์ด้วยคลอรีน:
HCOOH + Cl 2 → คาร์บอนไดออกไซด์ 2 + 2เอชซีแอล
ในบรรยากาศออกซิเจน กรดคาร์บอกซิลิกจะถูกออกซิไดซ์เป็น CO 2 และ H 2 O:
CH 3 COOH + 2O 2 → 2CO 2 + 2H 2 โอ
6. ปฏิกิริยา ดีคาร์บอกซิเลชัน- กรดโมโนคาร์บอกซิลิกที่ไม่ถูกทดแทนอิ่มตัวนั้นยากต่อการแยกคาร์บอกซิเลตเมื่อถูกความร้อนเนื่องจากพันธะ C-C มีความแข็งแรงสูง ในการทำเช่นนี้จำเป็นต้องหลอมเกลือโลหะอัลคาไลของกรดคาร์บอกซิลิกกับอัลคาไล:
การปรากฏตัวของสารทดแทนที่ให้อิเล็กตรอนในอนุมูลไฮโดรคาร์บอนส่งเสริม ปฏิกิริยาดีคาร์บอกซิเลชัน:
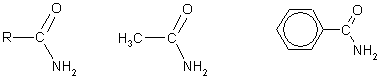
กรดคาร์บอกซิลิก Dibasic จะแยก CO 2 ออกมาได้ง่ายเมื่อถูกความร้อน:



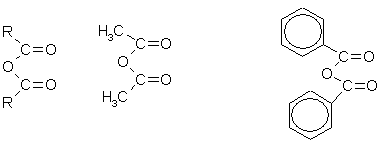

 นักศึกษาเต็มเวลาผู้ใหญ่สามารถทำงานได้กี่ชั่วโมง?
นักศึกษาเต็มเวลาผู้ใหญ่สามารถทำงานได้กี่ชั่วโมง? สรุปบทเรียนการบำบัดคำพูด "คำนำหน้าและคำบุพบท" โครงร่างของบทเรียนการบำบัดคำพูด (ชั้นประถมศึกษาปีที่ 3) ในหัวข้อ การสร้างพื้นฐานทางจิตวิทยาของการพูด
สรุปบทเรียนการบำบัดคำพูด "คำนำหน้าและคำบุพบท" โครงร่างของบทเรียนการบำบัดคำพูด (ชั้นประถมศึกษาปีที่ 3) ในหัวข้อ การสร้างพื้นฐานทางจิตวิทยาของการพูด ลิ้นบิดเพื่อแยกแยะความแตกต่าง (ความแตกต่าง) (c – b), (v-f), (b – p), (t – t), (d – d), (d – t), (k – t), (p – k), (ก – k), (k-g-x)
ลิ้นบิดเพื่อแยกแยะความแตกต่าง (ความแตกต่าง) (c – b), (v-f), (b – p), (t – t), (d – d), (d – t), (k – t), (p – k), (ก – k), (k-g-x)