ต้องใช้ความร้อนเท่าไรจึงจะได้ m กรัม การคำนวณใน Excel งานที่นำไปใช้
มนุษย์รู้จักพลังงานไม่กี่ประเภท - พลังงานกล (จลนศาสตร์และศักย์), พลังงานภายใน (ความร้อน), พลังงานสนาม (ความโน้มถ่วง, แม่เหล็กไฟฟ้าและนิวเคลียร์), เคมี มันคุ้มค่าที่จะเน้นย้ำถึงพลังของการระเบิด ...
พลังงานสูญญากาศและยังคงมีอยู่ในทฤษฎีเท่านั้น - พลังงานมืด ในบทความนี้ หัวข้อแรกในส่วน "วิศวกรรมความร้อน" ฉันจะลองใช้ภาษาที่เรียบง่ายและเข้าถึงได้ โดยใช้ตัวอย่างที่ใช้งานได้จริง เพื่อพูดคุยเกี่ยวกับรูปแบบที่สำคัญที่สุดของพลังงานในชีวิตของผู้คน - เกี่ยวกับ พลังงานความร้อนและเรื่องการคลอดบุตรทันเวลา พลังงานความร้อน.
คำสองสามคำเพื่อทำความเข้าใจสถานที่ของวิศวกรรมความร้อนเป็นสาขาของวิทยาศาสตร์ในการได้มาซึ่งการถ่ายโอนและการใช้พลังงานความร้อน วิศวกรรมความร้อนสมัยใหม่เกิดขึ้นจากอุณหพลศาสตร์ทั่วไป ซึ่งเป็นหนึ่งในสาขาวิชาฟิสิกส์ เทอร์โมไดนามิกส์มีความหมายว่า “อบอุ่น” บวกกับ “กำลัง” ดังนั้น อุณหพลศาสตร์จึงเป็นศาสตร์ของ "การเปลี่ยนแปลงของอุณหภูมิ" ของระบบ
ผลกระทบต่อระบบจากภายนอกซึ่งพลังงานภายในเปลี่ยนแปลง อาจเป็นผลมาจากการถ่ายเทความร้อน พลังงานความร้อนซึ่งระบบได้มาหรือหายไปจากการมีปฏิสัมพันธ์กับสิ่งแวดล้อมนั้นเรียกว่า ปริมาณความร้อนและวัดในระบบ SI เป็นจูล
หากคุณไม่ใช่วิศวกรความร้อนและไม่ได้จัดการกับปัญหาด้านวิศวกรรมความร้อนเป็นประจำทุกวัน เมื่อคุณเจอปัญหาเหล่านี้ บางครั้งหากไม่มีประสบการณ์ การค้นหาอย่างรวดเร็วอาจเป็นเรื่องยากมาก เป็นการยากที่จะจินตนาการถึงขนาดของค่าที่ต้องการของปริมาณความร้อนและพลังงานความร้อนโดยไม่ต้องมีประสบการณ์ ต้องใช้พลังงานกี่จูลในการทำความร้อนอากาศ 1,000 ลูกบาศก์เมตรจาก -37˚С ถึง +18˚С?.. พลังของแหล่งความร้อนที่จำเป็นในการดำเนินการนี้ใน 1 ชั่วโมงคืออะไร » ไม่ใช่วิศวกรทุกคน บางครั้งผู้เชี่ยวชาญยังจำสูตรได้ แต่มีเพียงไม่กี่คนเท่านั้นที่สามารถนำไปปฏิบัติได้!
หลังจากอ่านบทความนี้จนจบ คุณจะสามารถแก้ปัญหาการผลิตจริงและงานในครัวเรือนที่เกี่ยวข้องกับการทำความร้อนและความเย็นของวัสดุต่างๆ ได้อย่างง่ายดาย การทำความเข้าใจแก่นแท้ทางกายภาพของกระบวนการถ่ายเทความร้อนและความรู้เกี่ยวกับสูตรพื้นฐานอย่างง่ายเป็นองค์ประกอบหลักในรากฐานของความรู้ด้านวิศวกรรมความร้อน!
ปริมาณความร้อนในกระบวนการทางกายภาพต่างๆ
สารที่รู้จักส่วนใหญ่สามารถอยู่ในสถานะของแข็ง ของเหลว ก๊าซ หรือพลาสมาที่อุณหภูมิและความดันต่างกัน การเปลี่ยนแปลงจากรัฐรวมหนึ่งไปสู่อีกรัฐหนึ่ง เกิดขึ้นที่อุณหภูมิคงที่(โดยมีเงื่อนไขว่าความดันและพารามิเตอร์ด้านสิ่งแวดล้อมอื่น ๆ จะไม่เปลี่ยนแปลง) และมาพร้อมกับการดูดซับหรือการปล่อยพลังงานความร้อน แม้ว่าข้อเท็จจริงที่ว่า 99% ของสสารในจักรวาลจะอยู่ในสถานะพลาสมา แต่เราจะไม่พิจารณาสถานะของการรวมกลุ่มนี้ในบทความนี้
พิจารณากราฟที่แสดงในรูป มันแสดงให้เห็นการพึ่งพาอาศัยกันของอุณหภูมิของสาร ตู่เกี่ยวกับปริมาณความร้อน Qสรุปเป็นระบบปิดบางระบบที่มีมวลของสารหนึ่งๆ

1. ของแข็งที่มีอุณหภูมิ T1, อุ่นที่อุณหภูมิ Tm, ใช้จ่ายในกระบวนการนี้ปริมาณความร้อนเท่ากับ Q1 .
2. ต่อไป กระบวนการหลอมเหลวเริ่มต้นขึ้น ซึ่งเกิดขึ้นที่อุณหภูมิคงที่ Tpl(จุดหลอมเหลว). ในการละลายมวลทั้งหมดของของแข็ง จำเป็นต้องใช้พลังงานความร้อนในปริมาณ Q2 — Q1 .
3. ถัดไป ของเหลวที่เกิดจากการหลอมของของแข็งถูกทำให้ร้อนจนถึงจุดเดือด (การก่อตัวของก๊าซ) Tkp, ใช้จ่ายความร้อนจำนวนนี้เท่ากับ Q3-Q2 .
4. ตอนนี้อยู่ที่จุดเดือดคงที่ Tkpของเหลวเดือดและระเหยกลายเป็นแก๊ส สำหรับการเปลี่ยนมวลทั้งหมดของของเหลวเป็นก๊าซ จำเป็นต้องใช้พลังงานความร้อนในปริมาณ Q4-Q3.
5. ในขั้นตอนสุดท้าย ก๊าซจะถูกทำให้ร้อนจากอุณหภูมิ Tkpจนถึงอุณหภูมิบางส่วน T2. ในกรณีนี้ค่าใช้จ่ายของปริมาณความร้อนจะเป็น Q5-Q4. (ถ้าเราทำให้แก๊สร้อนจนถึงอุณหภูมิไอออไนเซชัน แก๊สจะกลายเป็นพลาสมา)
ดังนั้นการให้ความร้อนแก่ของแข็งดั้งเดิมจากอุณหภูมิ T1จนถึงอุณหภูมิ T2เราใช้พลังงานความร้อนในปริมาณ Q5แปลสารผ่านสามสถานะของการรวมตัว
เคลื่อนที่ไปในทิศทางตรงกันข้ามเราจะเอาความร้อนออกจากสารในปริมาณเท่ากัน Q5ผ่านขั้นตอนการควบแน่น การตกผลึก และความเย็นจากอุณหภูมิ T2จนถึงอุณหภูมิ T1. แน่นอน เรากำลังพิจารณาระบบปิดที่ไม่สูญเสียพลังงานต่อสิ่งแวดล้อมภายนอก
โปรดทราบว่าการเปลี่ยนจากสถานะของแข็งไปเป็นสถานะก๊าซเป็นไปได้ โดยผ่านเฟสของเหลว กระบวนการนี้เรียกว่าการระเหิด และกระบวนการย้อนกลับเรียกว่าการระเหิด
ดังนั้นเราจึงเข้าใจว่ากระบวนการของการเปลี่ยนแปลงระหว่างสถานะรวมของสารมีลักษณะเฉพาะโดยการใช้พลังงานที่อุณหภูมิคงที่ เมื่อสารได้รับความร้อนซึ่งอยู่ในสถานะการรวมตัวที่ไม่เปลี่ยนแปลง อุณหภูมิจะสูงขึ้นและพลังงานความร้อนก็จะถูกบริโภคไปด้วย
สูตรหลักสำหรับการถ่ายเทความร้อน
สูตรนั้นง่ายมาก
ปริมาณความร้อน Qใน J คำนวณโดยสูตร:
1. จากด้านการใช้ความร้อน กล่าวคือ จากด้านโหลด:
1.1. เมื่อให้ความร้อน (เย็น):
Q = ม * ค *(T2 -T1)
ม – มวลของสารในหน่วยกิโลกรัม
กับ -ความจุความร้อนจำเพาะของสารในหน่วย J / (kg * K)
1.2. เมื่อละลาย (แช่แข็ง):
Q = ม * λ
λ – ความร้อนจำเพาะของการหลอมเหลวและการตกผลึกของสารในหน่วย J/kg
1.3. ในระหว่างการเดือด การระเหย (ควบแน่น):
Q = ม * r
r – ความร้อนจำเพาะของการเกิดก๊าซและการควบแน่นของสสารในหน่วย J/kg
2. จากด้านการผลิตความร้อน นั่นคือ จากด้านข้างของแหล่งกำเนิด:
2.1. เมื่อเผาไหม้เชื้อเพลิง:
Q = ม * q
q – ความร้อนจำเพาะของการเผาไหม้เชื้อเพลิงใน J/kg
2.2. เมื่อแปลงไฟฟ้าเป็นพลังงานความร้อน (กฎหมาย Joule-Lenz):
Q =t *I *U =t *R *I ^2=(t .) /r)*U ^2
t – เวลาใน s
ฉัน – ค่าปัจจุบันใน A
ยู – แรงดัน rms ใน V
R – ความต้านทานโหลดเป็นโอห์ม
เราสรุปได้ว่าปริมาณความร้อนเป็นสัดส่วนโดยตรงกับมวลของสารในระหว่างการแปลงเฟสทั้งหมด และเมื่อถูกความร้อน จะเป็นสัดส่วนโดยตรงกับความแตกต่างของอุณหภูมิ ค่าสัมประสิทธิ์สัดส่วน ( ค , λ , r , q ) สำหรับแต่ละสารมีค่าของตัวเองและถูกกำหนดโดยเชิงประจักษ์ (นำมาจากหนังสืออ้างอิง)
พลังงานความร้อน นู๋ ใน W คือปริมาณความร้อนที่ถ่ายเทไปยังระบบในช่วงเวลาหนึ่ง:
N=Q/t
ยิ่งเราต้องการให้ความร้อนแก่ร่างกายเร็วขึ้นเท่าใด พลังงานควรเป็นแหล่งพลังงานความร้อนที่มากขึ้นเท่านั้น ทุกอย่างมีเหตุผล
การคำนวณในงานที่ใช้ Excel
ในชีวิตมักจะจำเป็นต้องทำการคำนวณโดยประมาณอย่างรวดเร็วเพื่อให้เข้าใจว่าเหมาะสมหรือไม่ที่จะศึกษาหัวข้อต่อไป ทำโครงการ และให้รายละเอียดการคำนวณที่ใช้แรงงานมากอย่างแม่นยำ ด้วยการคำนวณในไม่กี่นาที แม้จะแม่นยำถึง ± 30% คุณสามารถทำการตัดสินใจด้านการจัดการที่สำคัญซึ่งจะถูกกว่า 100 เท่าและเร็วกว่า 1,000 เท่า และทำให้มีประสิทธิภาพมากกว่าการคำนวณที่แม่นยำถึง 100,000 เท่า ภายในหนึ่งสัปดาห์หรือหนึ่งเดือนโดยกลุ่มผู้เชี่ยวชาญราคาแพง ...
เงื่อนไขของปัญหา:
ในสถานที่ของร้านค้าเพื่อเตรียมเหล็กแผ่นรีดขนาด 24 ม. x 15 ม. x 7 ม. เรานำเข้าเหล็กแผ่นรีดจากโกดังริมถนนจำนวน 3 ตัน เหล็กแผ่นรีดมีน้ำแข็งมวลรวม 20 กก. ภายนอก -37˚С ต้องใช้ความร้อนเท่าใดในการทำให้โลหะร้อนถึง +18˚С อุ่นน้ำแข็งละลายและอุ่นน้ำได้ถึง+18˚С; ให้ความร้อนกับปริมาตรของอากาศทั้งหมดในห้อง สมมติว่าเครื่องทำความร้อนถูกปิดโดยสมบูรณ์ก่อนหน้านั้น? ระบบทำความร้อนควรมีกำลังเท่าใดหากต้องดำเนินการทั้งหมดข้างต้นให้เสร็จภายใน 1 ชั่วโมง (เงื่อนไขที่รุนแรงและแทบไม่สมจริง - โดยเฉพาะเกี่ยวกับอากาศ!)
เราจะทำการคำนวณในโปรแกรมMS Excel หรือในโปรแกรมOo Calc.
สำหรับการจัดรูปแบบสีของเซลล์และแบบอักษร โปรดดูที่หน้า ""
ข้อมูลเบื้องต้น:
1. เราเขียนชื่อของสาร:
ไปยังเซลล์ D3: เหล็ก
ไปยังเซลล์ E3: น้ำแข็ง
ไปยังเซลล์ F3: น้ำแข็ง
ไปยังเซลล์ G3: น้ำ
ไปยังเซลล์ G3: อากาศ
2. เราป้อนชื่อของกระบวนการ:
ลงในเซลล์ D4, E4, G4, G4: ความร้อน
ไปยังเซลล์ F4: ละลาย
3. ความจุความร้อนจำเพาะของสาร คใน J / (กก. * K) เราเขียนสำหรับเหล็ก น้ำแข็ง น้ำ และอากาศ ตามลำดับ
ไปยังเซลล์ D5: 460
ไปยังเซลล์ E5: 2110
ไปยังเซลล์ G5: 4190
ไปยังเซลล์ H5: 1005
4. ความร้อนจำเพาะของการหลอมเหลวของน้ำแข็ง λ ใน J/kg enter
ไปยังเซลล์ F6: 330000
5. มวลสาร มเป็นกิโลกรัมที่เราป้อนตามลำดับสำหรับเหล็กและน้ำแข็ง
ไปยังเซลล์ D7: 3000
ไปยังเซลล์ E7: 20
เนื่องจากมวลไม่เปลี่ยนแปลงเมื่อน้ำแข็งกลายเป็นน้ำ
ในเซลล์ F7 และ G7: =E7 =20
มวลอากาศหาได้จากการคูณปริมาตรของห้องด้วยแรงโน้มถ่วงจำเพาะ
ในเซลล์ H7: =24*15*7*1.23 =3100
6. เวลาดำเนินการ tในไม่กี่นาทีเราเขียนเพียงครั้งเดียวสำหรับเหล็ก
ไปยังเซลล์ D8: 60
ค่าเวลาสำหรับการให้ความร้อนด้วยน้ำแข็ง การหลอมเหลว และความร้อนของน้ำที่ได้นั้นคำนวณจากเงื่อนไขที่กระบวนการทั้งสามนี้ต้องสรุปในเวลาเดียวกับเวลาที่กำหนดให้ทำความร้อนโลหะ เราอ่านตาม
ในเซลล์ E8: =E12/(($E$12+$F$12+$G$12)/D8) =9,7
ในเซลล์ F8: =F12/(($E$12+$F$12+$G$12)/D8) =41,0
ในเซลล์ G8: =G12/(($E$12+$F$12+$G$12)/D8) =9,4
อากาศก็ควรอุ่นขึ้นในช่วงเวลาเดียวกันเราอ่าน
ในเซลล์ H8: =D8 =60,0
7. อุณหภูมิเริ่มต้นของสารทั้งหมด ตู่1 เป็น ˚C เรา enter
ไปยังเซลล์ D9: -37
ไปยังเซลล์ E9: -37
ไปยังเซลล์ F9: 0
ไปยังเซลล์ G9: 0
ไปยังเซลล์ H9: -37
8. อุณหภูมิสุดท้ายของสารทั้งหมด ตู่2 เป็น ˚C เรา enter
ไปยังเซลล์ D10: 18
ไปยังเซลล์ E10: 0
ไปยังเซลล์ F10: 0
ไปยังเซลล์ G10: 18
ไปยังเซลล์ H10: 18
ฉันคิดว่าไม่ควรมีคำถามใดๆ ในข้อ 7 และ 8

ผลการคำนวณ:
9. ปริมาณความร้อน Qใน KJ ที่จำเป็นสำหรับแต่ละกระบวนการที่เราคำนวณ
สำหรับให้ความร้อนเหล็กในเซลล์ D12: =D7*D5*(D10-D9)/1000 =75900
สำหรับให้ความร้อนน้ำแข็งในเซลล์ E12: =E7*E5*(E10-E9)/1000 = 1561
สำหรับการละลายน้ำแข็งในเซลล์ F12: =F7*F6/1000 = 6600
สำหรับการทำน้ำร้อนในเซลล์ G12: =G7*G5*(G10-G9)/1000 = 1508
สำหรับการทำความร้อนด้วยอากาศในเซลล์ H12: =H7*H5*(H10-H9)/1000 = 171330
อ่านจำนวนพลังงานความร้อนที่จำเป็นสำหรับกระบวนการทั้งหมด
ในเซลล์ที่ผสาน D13E13F13G13H13: =SUM(D12:H12) = 256900
ในเซลล์ D14, E14, F14, G14, H14 และเซลล์ที่รวมกัน D15E15F15G15H15 ปริมาณความร้อนจะได้รับในหน่วยวัดส่วนโค้ง - ใน Gcal (เป็นกิกะแคลอรี)
10. พลังงานความร้อน นู๋หน่วยเป็นกิโลวัตต์ จำเป็นสำหรับแต่ละกระบวนการคำนวณ
สำหรับให้ความร้อนเหล็กในเซลล์ D16: =D12/(D8*60) =21,083
สำหรับให้ความร้อนน้ำแข็งในเซลล์ E16: =E12/(E8*60) = 2,686
สำหรับการละลายน้ำแข็งในเซลล์ F16: =F12/(F8*60) = 2,686
สำหรับน้ำร้อนในเซลล์ G16: =G12/(G8*60) = 2,686
สำหรับการทำความร้อนด้วยอากาศในเซลล์ H16: =H12/(H8*60) = 47,592
พลังงานความร้อนทั้งหมดที่จำเป็นในการดำเนินการทั้งหมดในเวลาเดียว tคำนวณ
ในเซลล์ที่ผสาน D17E17F17G17H17: =D13/(D8*60) = 71,361
ในเซลล์ D18, E18, F18, G18, H18 และเซลล์ที่รวมกัน D19E19F19G19H19 พลังงานความร้อนจะได้รับในหน่วยวัดส่วนโค้ง - ใน Gcal / h
เสร็จสิ้นการคำนวณใน Excel
สรุป:
โปรดทราบว่าต้องใช้พลังงานมากกว่าสองเท่าในการให้ความร้อนกับอากาศ เช่นเดียวกับการทำความร้อนในมวลเหล็กเดียวกัน
เมื่อทำน้ำร้อน ค่าใช้จ่ายด้านพลังงานจะมากเป็นสองเท่าของการทำน้ำแข็ง กระบวนการหลอมละลายใช้พลังงานมากกว่ากระบวนการให้ความร้อนหลายเท่า (โดยมีความแตกต่างของอุณหภูมิเล็กน้อย)
น้ำร้อนใช้พลังงานความร้อนมากกว่าเหล็กที่ให้ความร้อนถึงสิบเท่าและมากกว่าอากาศร้อนถึงสี่เท่า
สำหรับ รับ ข้อมูลเกี่ยวกับการเปิดตัวบทความใหม่ และสำหรับ ดาวน์โหลดไฟล์โปรแกรมที่ใช้งานได้ ฉันขอให้คุณสมัครรับข่าวสารในหน้าต่างที่อยู่ท้ายบทความหรือในหน้าต่างที่ด้านบนของหน้า
หลังจากป้อนที่อยู่อีเมลของคุณและคลิกที่ปุ่ม "รับประกาศบทความ" อย่าลืมยืนยัน สมัครสมาชิก โดยคลิกที่ลิงค์ ในจดหมายที่จะถึงคุณทันทีที่อีเมลที่ระบุ (บางครั้ง - ในโฟลเดอร์ « สแปม » )!
เราจำแนวคิดของ "ปริมาณความร้อน" และ "พลังงานความร้อน" โดยพิจารณาจากสูตรพื้นฐานสำหรับการถ่ายเทความร้อน และวิเคราะห์ตัวอย่างที่ใช้งานได้จริง ฉันหวังว่าภาษาของฉันจะเรียบง่าย เข้าใจง่าย และน่าสนใจ
ฉันหวังว่าจะได้คำถามและความคิดเห็นในบทความ!
ฉันขอ เคารพ ดาวน์โหลดไฟล์งานของผู้เขียน หลังจากสมัครสมาชิก สำหรับการประกาศบทความ
(หรือการถ่ายเทความร้อน)
ความจุความร้อนจำเพาะของสาร
ความจุความร้อนคือ ปริมาณความร้อนที่ร่างกายดูดซึมเมื่อได้รับความร้อน 1 องศา
ความจุความร้อนของร่างกายแสดงด้วยอักษรละตินตัวพิมพ์ใหญ่ จาก.
อะไรเป็นตัวกำหนดความจุความร้อนของร่างกาย? ประการแรกจากมวลของมัน เป็นที่ชัดเจนว่าการให้ความร้อน เช่น น้ำ 1 กิโลกรัม จะต้องใช้ความร้อนมากกว่าการให้ความร้อน 200 กรัม
ชนิดของสาร? มาทำการทดลองกัน ลองเอาภาชนะที่เหมือนกันสองใบแล้วเทน้ำที่มีน้ำหนัก 400 กรัมลงในหนึ่งในนั้นและน้ำมันพืชที่มีน้ำหนัก 400 กรัมในภาชนะอื่นเราจะเริ่มให้ความร้อนแก่พวกเขาด้วยความช่วยเหลือของเตาที่เหมือนกัน จากการสังเกตการอ่านเทอร์โมมิเตอร์เราจะเห็นว่าน้ำมันร้อนขึ้นอย่างรวดเร็ว หากต้องการให้น้ำร้อนและน้ำมันมีอุณหภูมิเท่ากัน จะต้องอุ่นน้ำให้นานขึ้น แต่ยิ่งเราให้ความร้อนกับน้ำนานเท่าไร ก็ยิ่งได้รับความร้อนจากเตามากขึ้นเท่านั้น
ดังนั้นเพื่อให้ความร้อนแก่มวลเดียวกันของสารต่าง ๆ จนถึงอุณหภูมิเดียวกันจึงต้องใช้ความร้อนในปริมาณที่ต่างกัน ปริมาณความร้อนที่จำเป็นในการให้ความร้อนแก่ร่างกาย และด้วยเหตุนี้ ความจุความร้อนจึงขึ้นอยู่กับชนิดของสารที่ร่างกายนี้ประกอบขึ้นเป็นองค์ประกอบ
ตัวอย่างเช่น หากต้องการเพิ่มอุณหภูมิของน้ำที่มีมวล 1 กิโลกรัม คูณ 1 ° C ต้องใช้ปริมาณความร้อนเท่ากับ 4200 J และเพื่อให้ความร้อนกับน้ำมันดอกทานตะวันมวลเดียวกัน 1 ° C จำนวน ต้องใช้ความร้อนเท่ากับ 1700 J
ปริมาณทางกายภาพที่แสดงว่าต้องใช้ความร้อนเท่าใดในการให้ความร้อนแก่สาร 1 กิโลกรัม คูณ 1 ºС เรียกว่า ความร้อนจำเพาะสารนี้
สารแต่ละชนิดมีความจุความร้อนจำเพาะของตัวเอง ซึ่งเขียนแทนด้วยตัวอักษรละติน c และวัดเป็นจูลต่อกิโลกรัม-องศา (J / (กก. ° C))
ความจุความร้อนจำเพาะของสารเดียวกันในสถานะการรวมตัวต่างกัน (ของแข็ง ของเหลว และก๊าซ) แตกต่างกัน ตัวอย่างเช่น ความจุความร้อนจำเพาะของน้ำคือ 4200 J/(กก. ºС) และความจุความร้อนจำเพาะของน้ำแข็งคือ 2100 J/(กก. ºС); อลูมิเนียมในสถานะของแข็งมีความจุความร้อนจำเพาะ 920 J/(กก. - °C) และในสถานะของเหลวคือ 1080 J/(กก. - °C)
โปรดทราบว่าน้ำมีความจุความร้อนจำเพาะสูงมาก ดังนั้นน้ำในทะเลและมหาสมุทรที่ร้อนขึ้นในฤดูร้อนจะดูดซับความร้อนจากอากาศเป็นจำนวนมาก ด้วยเหตุนี้ในสถานที่เหล่านั้นซึ่งตั้งอยู่ใกล้แหล่งน้ำขนาดใหญ่ ฤดูร้อนจึงไม่ร้อนเท่าในสถานที่ห่างไกลจากน้ำ
การคำนวณปริมาณความร้อนที่ต้องการให้ความร้อนแก่ร่างกายหรือปล่อยออกมาในระหว่างการทำความเย็น
จากที่กล่าวมาแล้ว เป็นที่ชัดเจนว่าปริมาณความร้อนที่จำเป็นในการให้ความร้อนแก่ร่างกายนั้นขึ้นอยู่กับชนิดของสารที่ร่างกายประกอบด้วย (กล่าวคือ ความจุความร้อนจำเพาะของมัน) และกับมวลของร่างกาย เป็นที่ชัดเจนว่าปริมาณความร้อนนั้นขึ้นอยู่กับว่าเราจะเพิ่มอุณหภูมิร่างกายกี่องศา
ดังนั้น ในการกำหนดปริมาณความร้อนที่ต้องการเพื่อให้ความร้อนแก่ร่างกายหรือปล่อยออกมาในระหว่างการทำความเย็น คุณต้องคูณความร้อนจำเพาะของร่างกายด้วยมวลและความแตกต่างระหว่างอุณหภูมิสุดท้ายและอุณหภูมิเริ่มต้น:
Q = ซม (t 2 - t 1 ) ,
ที่ไหน Q- ปริมาณความร้อน คคือความจุความร้อนจำเพาะ ม- มวลร่างกาย , t 1 - อุณหภูมิเริ่มต้น t 2 คืออุณหภูมิสุดท้าย
เมื่อร่างกายได้รับความร้อน t 2 > t 1 และด้วยเหตุนี้ Q > 0 . เมื่อร่างกายเย็นลง t 2และ< t 1 และด้วยเหตุนี้ Q< 0 .
ถ้าทราบความจุความร้อนของทั้งร่างกาย จาก, Qถูกกำหนดโดยสูตร:
Q \u003d C (เสื้อ 2 - t 1 ) .
ตามคำจำกัดความ แคลอรี่คือปริมาณความร้อนที่ใช้ในการทำให้น้ำหนึ่งลูกบาศก์เซนติเมตรสูงขึ้น 1 องศาเซลเซียส กิกะแคลอรีที่ใช้ในการวัดพลังงานความร้อนในวิศวกรรมพลังงานความร้อนและสาธารณูปโภค คือหนึ่งพันล้านแคลอรี 1 เมตรมี 100 เซนติเมตร ดังนั้น 1 ลูกบาศก์เมตรจึงมี 100 x 100 x 100 = 1,000,000 เซนติเมตร ดังนั้น ในการให้ความร้อนกับน้ำก้อนหนึ่งโดย
1 องศาก็จะใช้เวลาหนึ่งล้านแคลอรีหรือ 0.001 Gcal
ในเมืองของฉันราคาเครื่องทำความร้อนคือ 1132.22 rubles / Gcal และราคาของน้ำร้อนคือ 71.65 rubles / m3 ราคาของน้ำเย็นคือ 16.77 rubles / m3
ใช้ Gcal เท่าไหร่ในการต้มน้ำ 1 ลูกบาศก์เมตร?
ฉันคิดอย่างนั้น
s x 1132.22 \u003d 71.65 - 16.77 และด้วยวิธีนี้ฉันแก้สมการเพื่อหาว่า s (Gcal) เท่ากับอะไรนั่นคือมันเท่ากับ 0.0484711452 Gcal
ฉันสงสัยบางอย่าง ฉันตัดสินใจผิด
คำตอบ:
ฉันไม่พบข้อผิดพลาดใดๆ ในการคำนวณของคุณ
โดยธรรมชาติแล้ว ค่าน้ำเสีย (การกำจัดน้ำ) ไม่ควรรวมอยู่ในอัตราภาษีที่กำหนด
การคำนวณโดยประมาณสำหรับเมือง Izhevsk ตามบรรทัดฐานเก่ามีลักษณะดังนี้:
0.19 Gcal ต่อคนต่อเดือน (บรรทัดฐานนี้ถูกยกเลิกไปแล้ว แต่ไม่มีอย่างอื่นเช่นจะทำ) / 3.6 ลูกบาศก์เมตร ต่อคนต่อเดือน (อัตราการใช้น้ำร้อน) = 0.05278 Gcal ต่อ 1 ลูกบาศก์เมตร (ต้องใช้ความร้อนมากในการทำให้น้ำร้อน 1 ลูกบาศก์เมตรร้อนถึงอุณหภูมิมาตรฐานของน้ำร้อนซึ่งฉันขอเตือนคุณว่าคือ 60 องศาเซลเซียส)
สำหรับการคำนวณปริมาณพลังงานความร้อนที่แม่นยำยิ่งขึ้นสำหรับการทำน้ำร้อนโดยวิธีโดยตรงตามปริมาณทางกายภาพ (และไม่ใช่วิธีย้อนกลับตามอัตราภาษีที่ได้รับอนุมัติสำหรับการจ่ายน้ำร้อน) - ฉันแนะนำให้ใช้ แม่แบบการคำนวณอัตราค่าน้ำร้อน (REC UR). สูตรการคำนวณใช้อุณหภูมิของน้ำเย็นในฤดูร้อนและฤดูหนาว (ความร้อน) ระยะเวลาของช่วงเวลาเหล่านี้
แท็ก: กิกะแคลอรี น้ำร้อน
- เราจ่ายค่าบริการน้ำร้อนอุณหภูมิต่ำกว่ามาตรฐานมาก จะทำอย่างไร?
- ระยะเวลาการตัดการเชื่อมต่อ DHW ต่อเนื่องที่กำหนดโดยกฎไม่ผิดกฎหมาย - คำตัดสินของศาลฎีกาแห่งสหพันธรัฐรัสเซีย (2017)
- Fairer Tariff Initiative และ Hot Water Metering Methodology
- เกี่ยวกับขั้นตอนการคำนวณจำนวนเงินที่จ่ายสำหรับการทำความร้อนและการจ่ายน้ำร้อนระหว่างการปิดเครื่อง - การชี้แจงของ Rospotrebnadzor สำหรับ SD
- เกี่ยวกับการบัญชีสำหรับตัวพาความร้อนในระบบจ่ายความร้อนแบบปิด - จดหมายของกระทรวงการก่อสร้างของสหพันธรัฐรัสเซียลงวันที่ 31 มีนาคม 2558 ฉบับที่ 9116-OD / 04
- UR - เกี่ยวกับการลดการจ่ายค่าทำความร้อนและน้ำร้อน - จดหมายจากกระทรวงพลังงานของ UR ลงวันที่ 17.08.2015 ฉบับที่ 11-10 / 5661
- ระยะเวลามาตรฐานสำหรับการตรวจสอบระบบทำความร้อนในโรงเรือนทั่วไปและอุปกรณ์วัดแสงน้ำร้อนคือเท่าใด
- น้ำร้อนสกปรกจากก๊อก สมัครได้ที่ไหน?
- มาตรวัดน้ำในอพาร์ตเมนต์สามารถไขลานทางเข้าทั้งหมดได้หรือไม่? วิธีการชำระเงิน? ตัวบ่งชี้สำหรับเดือน - 42 ลูกบาศก์เมตร
- ขั้นตอนในการรักษาบัญชีแยกค่าใช้จ่ายในด้านน้ำประปาและสุขาภิบาล - คำสั่งของกระทรวงการก่อสร้างของสหพันธรัฐรัสเซียลงวันที่ 25 มกราคม 2014 ฉบับที่ 22 / pr
- ชำระค่าน้ำและค่าไฟในอพาร์ตเมนต์ที่ไม่มีที่พัก
- การคำนวณความร้อนตาม ODPU สำหรับ 1/12
- แหล่งจ่ายไฟ
- จ่ายเงินจำนวนมากสำหรับห้องพักในหอพัก (17.3 ตร.ม.)
| ความคิดเห็น: (11) | |
| คำแนะนำ: แชร์ลิงก์บนโซเชียลมีเดียหากคุณต้องการคำตอบ/ความคิดเห็นเพิ่มเติม! | |
“...- คุณมีนกแก้วกี่ตัวที่พอดีกับคุณนั่นคือความสูงของคุณ
- จำเป็นจริงๆ! ฉันจะไม่กลืนนกแก้วจำนวนมาก!…”
จาก m / f “38 นกแก้ว”
ตามกฎ SI สากล (International System of Units) ปริมาณพลังงานความร้อนหรือปริมาณความร้อนวัดเป็นจูล [J] นอกจากนี้ยังมีหน่วยกิโลจูล [kJ] = 1,000 J., MegaJoule [MJ] หลายหน่วย = 1,000,000 J, GigaJoule [ GJ] = 1,000,000,000 J. ฯลฯ หน่วยวัดพลังงานความร้อนนี้เป็นหน่วยสากลหลักและมักใช้ในการคำนวณทางวิทยาศาสตร์และทางวิทยาศาสตร์และทางเทคนิค
อย่างไรก็ตาม เราทุกคนรู้หรืออย่างน้อยก็เคยได้ยินหน่วยวัดปริมาณความร้อนอีกหน่วยหนึ่ง (หรือแค่ความร้อน) ก็คือ แคลอรี เช่นเดียวกับกิโลแคลอรี เมกะแคลอรี และกิกะแคลอรี ซึ่งหมายถึง คำนำหน้า กิโล จิกะ และเมกะ ให้ดูที่ ตัวอย่างที่มีจูลส์ด้านบน ในประเทศของเรามีการพัฒนาในอดีตเพื่อให้เมื่อคำนวณภาษีเพื่อให้ความร้อนไม่ว่าจะเป็นความร้อนด้วยไฟฟ้าก๊าซหรือหม้อไอน้ำอัดเม็ดเป็นเรื่องปกติที่จะต้องพิจารณาต้นทุนของพลังงานความร้อนหนึ่งกิกะแคลอรี
ดังนั้น Gigacalorie กิโลวัตต์กิโลวัตต์ * ชั่วโมงหรือกิโลวัตต์ / ชั่วโมงและ Joules คืออะไรและเกี่ยวข้องกันอย่างไร คุณจะได้เรียนรู้ในบทความนี้
ดังนั้นหน่วยพื้นฐานของพลังงานความร้อนก็คือจูลตามที่ได้กล่าวไปแล้ว แต่ก่อนจะพูดถึงหน่วยวัด ตามหลักการแล้ว จำเป็นต้องอธิบายในระดับครัวเรือนว่าพลังงานความร้อนคืออะไร และจะวัดได้อย่างไรและทำไม
เราทุกคนรู้ตั้งแต่วัยเด็กว่าเพื่อให้ร่างกายอบอุ่น (เพื่อให้ได้พลังงานความร้อน) คุณต้องจุดไฟ เราทุกคนจึงจุดไฟ เชื้อเพลิงแบบดั้งเดิมที่ใช้เป็นฟืนคือฟืน ดังนั้นในระหว่างการเผาไหม้เชื้อเพลิง (ใด ๆ : ฟืน, ถ่านหิน, เม็ด, ก๊าซธรรมชาติ, เชื้อเพลิงดีเซล), พลังงานความร้อน (ความร้อน) จะถูกปล่อยออกมา แต่เพื่อให้ความร้อน ตัวอย่างเช่น ปริมาณน้ำที่แตกต่างกัน ต้องใช้ฟืน (หรือเชื้อเพลิงอื่น) ปริมาณต่างกัน เป็นที่ชัดเจนว่าไฟสองสามไฟในกองไฟเพียงพอที่จะทำให้น้ำสองลิตรร้อน และในการปรุงซุปครึ่งถังสำหรับทั้งค่าย คุณต้องตุนฟืนหลายมัด เพื่อไม่ให้วัดปริมาณทางเทคนิคที่เข้มงวดเช่นปริมาณความร้อนและความร้อนของการเผาไหม้เชื้อเพลิงด้วยฟืนและถังซุป วิศวกรด้านความร้อนจึงตัดสินใจสร้างความชัดเจนและเป็นระเบียบ และตกลงที่จะประดิษฐ์หน่วยสำหรับปริมาณความร้อน เพื่อให้หน่วยนี้เหมือนกันทุกที่ ให้นิยามไว้ดังนี้ ใช้ 4,190 แคลอรี หรือ 4.19 กิโลแคลอรี ในการให้ความร้อนน้ำ 1 กิโลกรัม ขึ้น 1 องศาภายใต้สภาวะปกติ (ความดันบรรยากาศ) ดังนั้น ให้ความร้อนกับน้ำ 1 กรัม ความร้อนน้อยลงพันเท่าก็เพียงพอแล้ว - 4.19 แคลอรี
แคลอรีสัมพันธ์กับหน่วยพลังงานความร้อนสากล จูล ดังนี้
1 แคลอรี = 4.19 จูล
ดังนั้นจึงใช้พลังงานความร้อน 4.19 จูลในการทำให้น้ำ 1 กรัมร้อนขึ้น 1 องศา และใช้ความร้อน 4,190 จูลเพื่อให้ความร้อนแก่น้ำ 1 กิโลกรัม
ในเทคโนโลยีพร้อมกับหน่วยวัดพลังงานความร้อน (และอื่น ๆ ) มีหน่วยพลังงานและตามระบบสากล (SI) นี่คือวัตต์ แนวคิดเรื่องพลังงานยังใช้ได้กับอุปกรณ์ทำความร้อน หากอุปกรณ์ทำความร้อนสามารถส่งพลังงานความร้อนได้ 1 จูลใน 1 วินาที แสดงว่ากำลังไฟฟ้าอยู่ที่ 1 วัตต์ พลังงานคือความสามารถของอุปกรณ์ในการผลิต (สร้าง) พลังงานจำนวนหนึ่ง (ในกรณีของเราคือพลังงานความร้อน) ต่อหน่วยเวลา กลับไปที่ตัวอย่างของเราด้วยน้ำ ให้ความร้อนหนึ่งกิโลกรัม (หรือหนึ่งลิตรในกรณีของน้ำหนึ่งกิโลกรัมเท่ากับหนึ่งลิตร) ของน้ำหนึ่งองศาเซลเซียส (หรือเคลวินอะไรก็ได้) เราต้องการพลังงาน 1 กิโลแคลอรี หรือพลังงานความร้อน 4,190 J. เพื่อให้ความร้อนแก่น้ำหนึ่งกิโลกรัมใน 1 วินาทีของเวลา 1 องศา เราต้องการอุปกรณ์ที่มีกำลังดังต่อไปนี้:
4190 จ./1 วิ. = 4 190 ว. หรือ 4.19 กิโลวัตต์
หากเราต้องการให้ความร้อนต่อกิโลกรัมของน้ำ 25 องศาในวินาทีเดียวกัน เราก็ต้องการพลังงานเพิ่มขึ้นอีก 25 เท่า กล่าวคือ
4.19 * 25 \u003d 104.75 กิโลวัตต์
ดังนั้นเราจึงสรุปได้ว่าหม้อไอน้ำอัดเม็ดที่มีความจุ 104.75 กิโลวัตต์ อุ่นน้ำ 1 ลิตร 25 องศาในหนึ่งวินาที
เนื่องจากเราได้วัตต์และกิโลวัตต์ เราควรพูดถึงพวกเขาด้วย ดังที่ได้กล่าวไปแล้ววัตต์เป็นหน่วยของพลังงานรวมถึงพลังงานความร้อนของหม้อไอน้ำ แต่นอกเหนือจากหม้อไอน้ำเม็ดและหม้อต้มก๊าซแล้วหม้อไอน้ำไฟฟ้ายังคุ้นเคยกับมนุษยชาติซึ่งแน่นอนว่าพลังที่วัดได้ใน กิโลวัตต์เท่ากัน และไม่กินทั้งเม็ดและก๊าซ และไฟฟ้า ซึ่งวัดเป็นกิโลวัตต์-ชั่วโมง การสะกดหน่วยพลังงานที่ถูกต้องคือกิโลวัตต์ * ชั่วโมง (กล่าวคือกิโลวัตต์คูณด้วยชั่วโมงไม่หาร) การเขียนกิโลวัตต์ / ชั่วโมงเป็นความผิดพลาด!
ในหม้อต้มน้ำไฟฟ้า พลังงานไฟฟ้าจะถูกแปลงเป็นพลังงานความร้อน (ที่เรียกว่าความร้อนจูล) และหากหม้อต้มใช้ไฟฟ้า 1 กิโลวัตต์ชั่วโมง มันจะสร้างความร้อนได้เท่าไร? ในการตอบคำถามง่ายๆ นี้ คุณต้องทำการคำนวณอย่างง่าย
แปลงกิโลวัตต์เป็นกิโลจูลต่อวินาที (กิโลจูลต่อวินาที) และชั่วโมงเป็นวินาที: มี 3,600 วินาทีในหนึ่งชั่วโมงเราได้รับ:
1 kW*h =[ 1 kJ/s]*3600 s.=1,000 J *3600 s = 3,600,000 Joules หรือ 3.6 MJ
ดังนั้น,
1 kWh = 3.6 MJ.
ในทางกลับกัน 3.6 MJ / 4.19 \u003d 0.859 Mcal \u003d 859 kcal \u003d 859,000 cal พลังงาน (ความร้อน)
ตอนนี้เรามาดู Gigacalorie ซึ่งราคาสำหรับเชื้อเพลิงประเภทต่างๆ จะได้รับการพิจารณาโดยวิศวกรความร้อน
1 Gcal = 1,000,000,000 แคลอรี
1,000,000,000 แคล \u003d 4.19 * 1,000,000,000 \u003d 4,190,000,000 J. \u003d 4,190 MJ = 4.19 จ.
หรือเมื่อรู้ว่า 1 kWh = 3.6 MJ เราคำนวณใหม่ 1 กิกะแคลอรีต่อกิโลวัตต์*ชั่วโมง:
1 Gcal = 4190 MJ/3.6 MJ = 1163 kWh!
หลังจากอ่านบทความนี้แล้ว หากคุณตัดสินใจปรึกษากับผู้เชี่ยวชาญของบริษัทของเราเกี่ยวกับปัญหาใดๆ ที่เกี่ยวข้องกับการจ่ายความร้อน แสดงว่าคุณ ที่นี่!
ที่มา: heat-en.ru
730. เหตุใดจึงใช้น้ำเพื่อทำให้กลไกบางอย่างเย็นลง?
น้ำมีความจุความร้อนจำเพาะสูง ซึ่งมีส่วนช่วยในการระบายความร้อนออกจากกลไกได้ดี
731. ในกรณีใดควรใช้พลังงานมากขึ้น: เพื่อให้ความร้อนน้ำหนึ่งลิตร 1 ° C หรือเพื่อให้ความร้อนแก่น้ำหนึ่งร้อยกรัมโดย 1 ° C?
ในการต้มน้ำหนึ่งลิตรให้ร้อน เนื่องจากยิ่งมวลมากเท่าไร ก็ยิ่งต้องใช้พลังงานมากขึ้นเท่านั้น
732. ส้อมคิวโปรนิกเกิลและเงินที่มีมวลเท่ากันจุ่มลงในน้ำร้อน พวกเขาได้รับความร้อนจากน้ำในปริมาณเท่ากันหรือไม่?
ส้อมคิวโปรนิกเกิลจะได้รับความร้อนมากกว่า เนื่องจากความร้อนจำเพาะของคิวโปรนิกเกิลมีค่ามากกว่าความร้อนของเงิน
733 ตะกั่วชิ้นหนึ่งและเหล็กหล่อชิ้นหนึ่งที่มีมวลเท่ากันถูกค้อนขนาดใหญ่ทุบสามครั้ง ส่วนไหนร้อนกว่ากัน?
ตะกั่วจะร้อนขึ้นเนื่องจากความจุความร้อนจำเพาะน้อยกว่าเหล็กหล่อ และใช้พลังงานน้อยลงในการให้ความร้อนแก่ตะกั่ว
734. ขวดหนึ่งบรรจุน้ำ ส่วนอีกขวดบรรจุน้ำมันก๊าดที่มีมวลและอุณหภูมิเท่ากัน ก้อนเหล็กร้อนเท่ากันถูกโยนลงในขวดแต่ละขวด อะไรจะทำให้อุณหภูมิสูงขึ้น - น้ำหรือน้ำมันก๊าด?
น้ำมันก๊าด.
735. เหตุใดอุณหภูมิที่ผันผวนในฤดูหนาวและฤดูร้อนในเมืองชายทะเลจึงมีความคมชัดน้อยกว่าในเมืองที่ตั้งอยู่ในแผ่นดิน
น้ำร้อนขึ้นและเย็นลงช้ากว่าอากาศ ในฤดูหนาว อุณหภูมิจะเย็นลงและเคลื่อนมวลอากาศอุ่นบนบก ทำให้อากาศบนชายฝั่งอุ่นขึ้น
736 ความจุความร้อนจำเพาะของอะลูมิเนียมคือ 920 J/kg °C สิ่งนี้หมายความว่า?
ซึ่งหมายความว่าต้องใช้ 920 J ในการทำให้อะลูมิเนียม 1 กก. อุ่นขึ้น 1 °C
737 แท่งอะลูมิเนียมและทองแดงที่มีมวลเท่ากัน 1 กก. ถูกทำให้เย็นลง 1 °C พลังงานภายในของแต่ละบล็อคจะเปลี่ยนไปมากน้อยเพียงใด? แถบไหนจะเปลี่ยนมากกว่ากันและมากน้อยแค่ไหน?
738. ต้องใช้ความร้อนเท่าใดในการทำให้เหล็กแท่งหนึ่งกิโลกรัมร้อนขึ้น 45 °C?
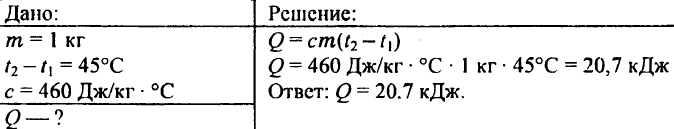
739. ต้องใช้ความร้อนเท่าไรในการให้ความร้อนกับน้ำ 0.25 กก. จาก 30°C ถึง 50°C?

740. พลังงานภายในของน้ำสองลิตรจะเปลี่ยนไปอย่างไรเมื่อถูกความร้อน 5 °C?

741. ต้องใช้ความร้อนเท่าไรในการต้มน้ำ 5 กรัม จาก 20 °C ถึง 30 °C
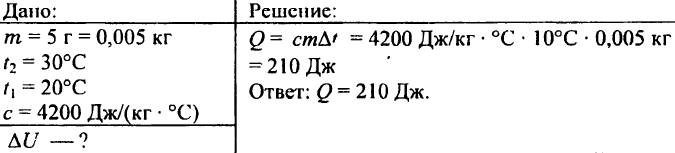
742. ต้องใช้ความร้อนเท่าใดในการให้ความร้อนแก่ลูกบอลอลูมิเนียมที่มีน้ำหนัก 0.03 กก. คูณ 72 °C

743. คำนวณปริมาณความร้อนที่ต้องการให้ความร้อนทองแดง 15 กก. คูณ 80 °C

744. คำนวณปริมาณความร้อนที่ต้องการให้ความร้อนทองแดง 5 กก. จาก 10 °C ถึง 200 °C

745. ต้องใช้ความร้อนเท่าไรในการต้มน้ำ 0.2 กก. จาก 15 °C ถึง 20 °C?

746. น้ำที่มีน้ำหนัก 0.3 กก. เย็นลง 20 °C พลังงานภายในของน้ำลดลงเท่าไหร่?

747. ต้องใช้ความร้อนเท่าไรในการให้ความร้อนกับน้ำ 0.4 กก. ที่อุณหภูมิ 20 °C ถึงอุณหภูมิ 30 °C?

748. ใช้ความร้อนเท่าใดในการทำความร้อนน้ำ 2.5 กก. โดย 20 °C?

749. เมื่อระบายความร้อนด้วยน้ำ 250 กรัม จาก 90 °C ถึง 40 °C จะปล่อยความร้อนออกมาเท่าใด
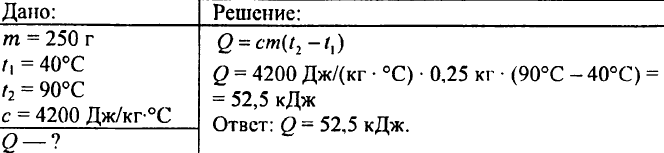
750. ต้องใช้ความร้อนเท่าใดในการให้ความร้อนกับน้ำ 0.015 ลิตร โดย 1 °C
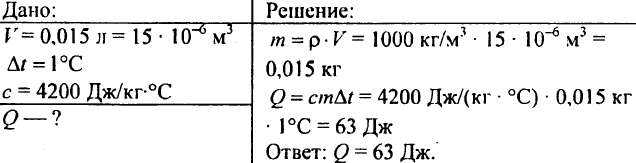
751. คำนวณปริมาณความร้อนที่จำเป็นในการให้ความร้อนแก่บ่อที่มีปริมาตร 300 m3 คูณ 10 °C?
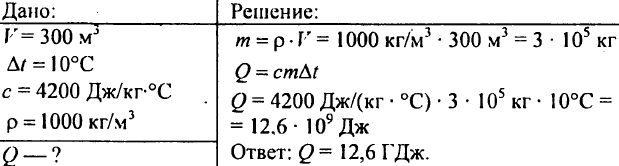
752. ต้องให้ความร้อนกับน้ำ 1 กิโลกรัมมากแค่ไหน เพื่อเพิ่มอุณหภูมิจาก 30°C เป็น 40°C

753 น้ำที่มีปริมาตร 10 ลิตรเย็นลงจากอุณหภูมิ 100 °C เป็นอุณหภูมิ 40 °C ในกรณีนี้ปล่อยความร้อนเท่าไร?

754. คำนวณปริมาณความร้อนที่ต้องการในการให้ความร้อนทราย 1 ลบ.ม. คูณ 60 °C

755. ปริมาณลม 60 ลบ.ม. ความจุความร้อนจำเพาะ 1000 J/kg °C ความหนาแน่นอากาศ 1.29 กก./ลบ.ม. ต้องใช้ความร้อนเท่าไรในการทำให้อุณหภูมิเพิ่มขึ้นถึง 22°C?

756. น้ำร้อน 10 ° C ใช้ความร้อน 4.20 103 J กำหนดปริมาณน้ำ.

757 น้ำที่มีน้ำหนัก 0.5 กก. รายงานความร้อน 20.95 kJ อุณหภูมิของน้ำถ้าอุณหภูมิเริ่มต้นของน้ำคือ 20 องศาเซลเซียส?
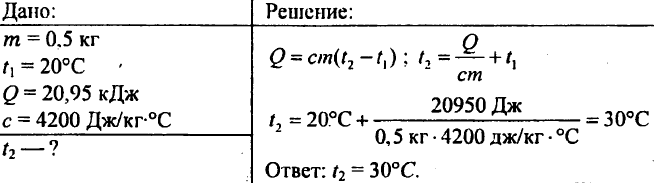
758. น้ำ 8 กก. ที่อุณหภูมิ 10 °C เทลงในกระทะทองแดงน้ำหนัก 2.5 กก. ต้องใช้ความร้อนเท่าไรในการต้มน้ำในกระทะ?

759. เทน้ำหนึ่งลิตรที่อุณหภูมิ 15 °C ลงในทัพพีทองแดงที่มีน้ำหนัก 300 กรัม ต้องใช้ความร้อนเท่าไรในการต้มน้ำในทัพพี 85 °C?

760. วางหินแกรนิตอุ่นชิ้นหนึ่งซึ่งมีน้ำหนัก 3 กก. ลงในน้ำ หินแกรนิตถ่ายเทความร้อน 12.6 kJ สู่น้ำ ทำให้เย็นลง 10 °C ความจุความร้อนจำเพาะของหินคืออะไร?
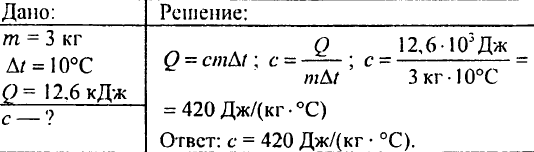
761. เติมน้ำร้อนที่ 50°C ลงในน้ำ 5 กก. ที่ 12°C เพื่อให้ได้ส่วนผสมที่มีอุณหภูมิ 30°C เติมน้ำเท่าไหร่?

762. เติมน้ำที่ 20°C ลงในน้ำ 3 ลิตรที่ 60°C เพื่อให้ได้น้ำที่ 40°C เติมน้ำเท่าไหร่?

763. อุณหภูมิของส่วนผสมจะเป็นอย่างไร ถ้าน้ำ 600 กรัม ที่อุณหภูมิ 80 องศาเซลเซียส ผสมกับน้ำ 200 กรัม ที่อุณหภูมิ 20 องศาเซลเซียส

764. เทน้ำหนึ่งลิตรที่อุณหภูมิ 90°C ลงในน้ำที่อุณหภูมิ 10°C และอุณหภูมิของน้ำกลายเป็น 60°C ที่นั่นมีน้ำเย็นมากแค่ไหน?

765. กำหนดว่าน้ำร้อนที่ร้อนถึง 60°C ควรเทลงในภาชนะเท่าใดหากภาชนะนั้นบรรจุน้ำเย็น 20 ลิตรที่อุณหภูมิ 15°C แล้ว อุณหภูมิของส่วนผสมควรอยู่ที่ 40 °C

766. กำหนดว่าต้องใช้ความร้อนเท่าใดในการให้ความร้อนกับน้ำ 425 g โดย 20 °C

767. น้ำ 5 กก. จะร้อนขึ้นกี่องศาถ้าน้ำได้รับ 167.2 kJ?

768. ต้องใช้ความร้อนเท่าใดในการให้ความร้อนต่อน้ำ m กรัมที่อุณหภูมิ t1 ถึงอุณหภูมิ t2?
769. เทน้ำ 2 กก. ลงในเครื่องวัดความร้อนที่อุณหภูมิ 15 °C อุณหภูมิของน้ำของเครื่องวัดความร้อนจะร้อนขึ้นหากน้ำหนักทองเหลือง 500 กรัมถูกทำให้ร้อนถึง 100 °C ลดลง? ความจุความร้อนจำเพาะของทองเหลืองคือ 0.37 kJ/(kg °C)
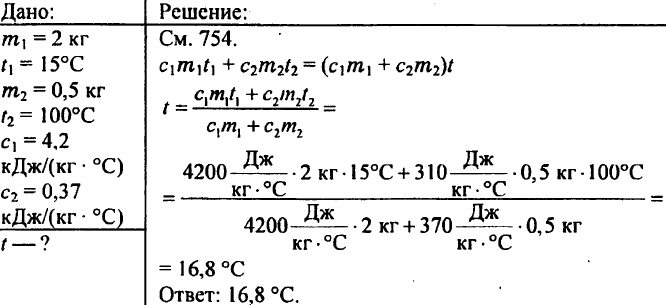
770 มีเศษทองแดง ดีบุก และอะลูมิเนียมที่มีปริมาตรเท่ากัน ชิ้นใดมีความจุความร้อนที่ใหญ่ที่สุดและความจุความร้อนที่เล็กที่สุด?

771 เทน้ำ 450 กรัมซึ่งมีอุณหภูมิ 20 °C ลงในแคลอรีมิเตอร์ เมื่อตะไบเหล็ก 200 กรัมถูกความร้อนถึง 100°C จุ่มลงในน้ำนี้ อุณหภูมิของน้ำก็กลายเป็น 24°C กำหนดความจุความร้อนจำเพาะของขี้เลื่อย

772. เครื่องวัดความร้อนทองแดงที่มีน้ำหนัก 100 กรัมบรรจุน้ำได้ 738 กรัม อุณหภูมิอยู่ที่ 15 °C ทองแดง 200 กรัมถูกลดระดับลงในเครื่องวัดความร้อนที่อุณหภูมิ 100 °C หลังจากนั้นอุณหภูมิของเครื่องวัดความร้อนเพิ่มขึ้นเป็น 17 °C ความจุความร้อนจำเพาะของทองแดงคือเท่าไร?

773. นำลูกเหล็กที่มีน้ำหนัก 10 กรัมออกจากเตาและหย่อนลงไปในน้ำที่อุณหภูมิ 10 °C อุณหภูมิของน้ำเพิ่มขึ้นเป็น 25 องศาเซลเซียส อุณหภูมิของลูกบอลในเตาอบคือเท่าไรถ้ามวลของน้ำเป็น 50 กรัม? ความจุความร้อนจำเพาะของเหล็กคือ 0.5 kJ/(kg °C)
776 นำน้ำที่มีน้ำหนัก 0.95 กรัม ที่อุณหภูมิ 80 องศาเซลเซียส ผสมกับน้ำที่มีน้ำหนัก 0.15 กรัม ที่อุณหภูมิ 15 องศาเซลเซียส กำหนดอุณหภูมิของส่วนผสม 779. สิ่วเหล็กน้ำหนัก 2 กก. ถูกทำให้ร้อนที่อุณหภูมิ 800 °C แล้วหย่อนลงในภาชนะที่มีน้ำ 15 ลิตรที่อุณหภูมิ 10 °C น้ำในภาชนะจะร้อนถึงอุณหภูมิเท่าไร?

(ข้อบ่งชี้ ในการแก้ปัญหานี้ จำเป็นต้องสร้างสมการที่ไม่ทราบอุณหภูมิของน้ำในถังน้ำหลังจากตัดใบมีดลงเป็นค่าที่ไม่ทราบค่า)
780. น้ำจะได้อุณหภูมิเท่าไหร่ถ้าผสมน้ำ 0.02 กก. ที่อุณหภูมิ 15 องศาเซลเซียส น้ำ 0.03 กก. ที่อุณหภูมิ 25 องศาเซลเซียส และ 0.01 กก. ที่อุณหภูมิ 60 องศาเซลเซียส
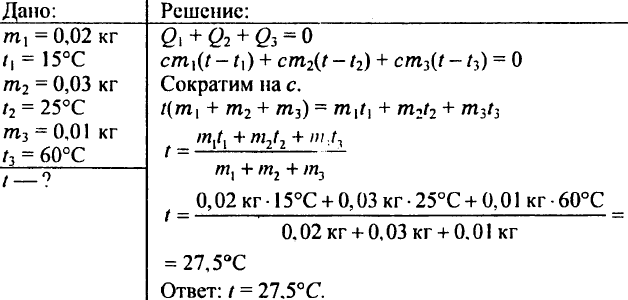
781. การทำความร้อนในชั้นที่มีอากาศถ่ายเทได้ดีต้องใช้ความร้อน 4.19 MJ ต่อชั่วโมง น้ำเข้าสู่เครื่องทำความร้อนที่ 80°C และไหลออกที่ 72°C ควรจ่ายน้ำให้กับหม้อน้ำทุก ๆ ชั่วโมงเท่าไหร่?

782. นำตะกั่วที่ชั่งน้ำหนัก 0.1 กก. ที่อุณหภูมิ 100 °C จุ่มลงในเครื่องวัดปริมาณความร้อนอะลูมิเนียมที่มีน้ำหนัก 0.04 กก. ที่มีน้ำ 0.24 กก. ที่อุณหภูมิ 15 °C หลังจากนั้นอุณหภูมิ 16 °C ถูกสร้างขึ้นในเครื่องวัดความร้อน ความจุความร้อนจำเพาะของตะกั่วคืออะไร?


 ลุงวันยา พล็อตเรื่อง “ลุงอีวาน ทัศนคติต่ออาจารย์ของผู้อื่น
ลุงวันยา พล็อตเรื่อง “ลุงอีวาน ทัศนคติต่ออาจารย์ของผู้อื่น Tsakhes น้อยชื่อเล่น Zinnober
Tsakhes น้อยชื่อเล่น Zinnober Maikov, Apollon Nikolaevich - ชีวประวัติสั้น
Maikov, Apollon Nikolaevich - ชีวประวัติสั้น