У чому полягає біологічний синтез прикладів. Що таке біосинтез у біології? Методи культивування продуцентів антибіотиків
Реакції синтезу органічних речовин у клітині одночасно з процесами розщеплення. Складні специфічні біополімери (білки, жири, вуглеводи, нуклеїнові кислоти) синтезуються із простих речовин, що утворилися в результаті дисиміляції.
Синтезовані органічні речовини використовуються для побудови різних органоїдів клітини, ферментів, секретів та запасних речовин замість витрачених. Всі ці процеси йдуть із поглинанням енергії. Синтез речовин, що йде в клітині, називають біосинтезом або пластичним обміном.
На цьому етапі на ряді проміжних ланок сумарно виділяється 2600 кДж енергії.
На утворення 36 макроергічних зв'язків при перетворенні АДФ в АТФ витрачається 1440 кДж, або 54% енергії, що звільняється, яка переходить у потенційну енергію АТФ. Отже, при кисневому розщепленні утворюється у 13 разів більше енергії, ніж при безкисневому, а клітиною у формі АТФ її зберігається у 18 разів більше.
Сумарне рівняння повного розщеплення глюкози на двох етапах можна записати так:
За способом одержання органічних сполук усі клітини поділяються на автотрофні та гетеротрофні (див. розділ «Ботаніка»).
АТФ, що утворилася при цьому, по каналах ендоплазматичної мережі спрямовується в інші ділянки клітини, де виникає в ній потреба. Таким чином, з енергії, що утворилася при розщепленні глюкози для клітини сумарно зберігається 80 кДж + 1440 кДж = 1520 кДж, або 55% енергії, яка переходить в потенційну енергію і надалі використовується клітиною. Тому реакція розщеплення називається енергетичним обміном.
Фотосинтез(Цв. Табл. I) - це унікальний процес утворення органічних сполук з неорганічних речовин з використанням енергії світла. Вперше процес фотосинтезу і роль ньому хлорофілу рослин описав видатний російський учений Климент Аркадійович Тимірязєв (1843-1920). Фотосинтез – це складний багатоступінчастий процес, що протікає у дві фази – світлову та темнову.
Світлова фазапочинається з освітлення хлоропласту видимим світлом. Під дією квантів світла деякі з рухомих електронів молекул хлорофілу переходять на більш високий енергетичний рівень і набувають потенційної енергії. Частина таких «збуджених» електронів повертається на колишнє місце, а енергія, що при цьому виділяється, розсіюється у вигляді тепла. Інша їх частина за участю переносників виступає в ролі відновників і приєднується до іонів водню, що постійно утворюється в клітинах при дисоціації молекул води (Н 2 O = Н + + ОН -). Іони водню, приєднавши електрон, перетворюються на атоми водню (Н + +е - = Н) і з'єднуються з молекулами речовин-переносників.
Іони ОН - , що залишилися без протиіонів водню, віддають свої електрони іншим іонам і перетворюються на радикали ОН (ОН = е - + ОН). Взаємодіючи між собою, вони утворюють воду та молекулярний кисень (40Н= 2Н 2 O+O 2).
Процес утворення молекулярного кисню під час розкладання води під впливом енергії світла називається фотолізом води. Його вперше вивчив і описав радянський учений Олександр Павлович Виноградов (1895-1975), використовуючи метод мічених атомів. За своїм механізмом фотоліз води подібний до електролізу води.
Крім того, у світлову фазу деякі з «збуджених» електронів хлорофілу та електронів, що відокремилися від іонів ВІН, беруть участь в утворенні макроергічного фосфатного зв'язку при синтезі АТФ з АДФ і неорганічного фосфату (ф) (АДФ + Ф = АТФ).
Таким чином, у світлову фазу фотосинтезу в результаті поглинання хлорофілом світлової енергії за рахунок «збуджених» електронів відбувається фотоліз води з виділенням кисню та синтез АТФ.
Темнова фаза фотосинтезу складається з низки послідовних ферментативних реакцій зв'язування З 2 , у яких утворюється глюкоза, що служить вихідним матеріалом для біосинтезу інших органічних речовин рослини. Цей процес відбувається за рахунок енергії АТФ за участю атомів водню, що утворилися у світлову фазу (6СO 2 +24Н=З 6 Н 12 O 6 +6Н 2 O).
Сумарне рівняння фотосинтезу:
6СO 2 +6Н 2 O = С 6 Н 12 O 6 + 6O 2
Мембранна структура хлоропласту здійснює при цьому розмежування реакційних речовин.
Продуктивність фотосинтезу- 1 г органічної речовини на 1 м 2 листя на 1 год. Щорічно в результаті фотосинтезу утворюється близько 400 млрд. т органічної речовини. Річна потреба однієї людини у кисні забезпечується функціонуванням 10-12 дерев середнього віку протягом вегетації. Встановлено, що продуктивність фотосинтезу зростає з підвищенням, до певного рівня, інтенсивності освітлення, вмісту СО 2 температури і вологості навколишнього повітря. Ці закономірності широко використовують при вирощуванні рослин у захищеному ґрунті.
Хемосинтез було відкрито 1888 р. російським біологом З. М. Виноградським, які довели здатність деяких бактерій асимілювати вуглекислоту з допомогою хімічної енергії. Існує кілька груп хемосинтезуючих бактерій, з яких найбільше значення мають нітрофікуючі, серобактерії та залізобактерії. Наприклад, нітрофікуючі бактерії отримують енергію для синтезу органічних речовин, окислюючи аміак до азотистої, а потім азотної кислоти; серобактерії - окислюючи сірководень до сульфатів, а залізобактерії - перетворюючи закисні солі заліза на окисні. Звільнена енергія акумулюється у клітинах хемосинтезуючих бактерій у формі АТФ. Процес хемосинтезу, при якому з 2 утворюється органічна речовина, протікає аналогічно темновій фазі фотосинтезу.
Завдяки життєдіяльності бактерій – хемосинтетиків у природі накопичуються великі поклади селітри та болотної руди.
Біосинтез білків йде у кожній живій клітині. Найбільш активний він у молодих клітинах, що ростуть, де синтезуються білки, що йдуть на побудову їх органоїдів, а також в секреторних клітинах, де синтезуються білки-ферменти і білки-гормони.
Основна роль визначенні структури білків належить ДНК. Відрізок ДНК, що складається з кількох сотень нуклеотидів, що містить інформацію про структуру одного білка, називають геном. Одна макромолекула ДНК містить кілька сотень генів. У молекулі записаний код про послідовність амінокислот в білку у вигляді нуклеотидів, що точно поєднуються. Сутність коду ДНК полягає в тому, що кожній амінокислоті відповідає ділянка ланцюга ДНК з трьох нуклеотидів, що стоять поруч. триплетів. Наприклад, А - - Ц - А відповідає амінокислоті цистеїну, А - А - Ц - лейцину, Т - Т - Т - лізину і т. д. Різних амінокислот 20, число можливих поєднань з 4 нуклеотидів по 3 дорівнює 64. з надлишком вистачить всім амінокислот.
Біосинтез білка - складний багатоступінчастий процес, що є ланцюгом синтетичних реакцій, що протікають за принципом матричного синтезу.
Суть реакцій матричного синтезуполягає в тому, що нові молекули білка синтезуються точно відповідно до плану, закладеного в структурі існуючих молекул ДНК. У цих реакціях забезпечується точна специфічна послідовність мономерів у полімерах, що синтезуються.
У біосинтезі білка визначають такі етапи, що у різних частинах клітини.
Синтез і-РНК (відбувається у ядрі). Інформація, що міститься в гені ДНК, листується на і-РНК. Цей процес називається транскрипцією (від латів. «Транскриптис» - переписування).

При цьому проти кожного нуклеотиду одним із ланцюгів ДНК постає комплементарний йому нуклеотид і-РНК. Молекули і-РНК є індивідуальними, кожна з них несе інформацію одного гена.
З'єднання амінокислот із молекулами т-РНК(відбувається у цитоплазмі). Молекули т-РНК складаються з 70-80 нуклеотидів. У ланцюжку т-РНК є низка нуклеотидних ланок, комплементарних одне одному. При зближенні вони злипаються, утворюючи структуру, що нагадує лист конюшини (61). До "черешка" листа приєднується певна амінокислота, а на "верхівці" листа розташований кодовий триплетнуклеотидів, що відповідає певній амінокислоті. Для кожної із 20 амінокислот існує своя т-РНК.
«Складання білка»(відбувається у рибосомах). До рибосом направляються з ядра і-РНК. При цьому на одній молекулі і-РНК одночасно розташовуються кілька рибосом, що утворюють комплекс, який називають полірибосомою. Це забезпечує одночасний синтез великої кількості однакових молекул білка.
З цитоплазми т-РНК з «навішеними» на них амінокислотами підходять до рибосом і своїм кодовим кінцем торкаються триплету нуклеотидів і-РНК, що проходить в даний момент через рибосому. У цей час протилежний кінець т-РНК з амінокислотою потрапляє в місце «складання» білка і, якщо кодовий триплет т-РНК виявиться комплементарним триплету і-РНК, який зараз перебуває в рибосомі, амінокислота відокремлюється від т-РНК і потрапляє до складу білка. , А рибосома робить "крок" на один триплет по і-РНК (триплети і-РНК, що відповідають кожній з 20 амінокислот, див. Додаток).

Віддавши амінокислоту, т-РНК залишає рибосому, їй на зміну приходить інша, з іншою амінокислотою, що становить наступну ланку в білковій молекулі, що будується (62). Так ланка за ланкою збирається поліпептидний ланцюг білка, а інформація про структуру білка, записана і-РНК у вигляді послідовності нуклеотидів, відтворюється на поліпептидному ланцюгу білка у вигляді послідовності амінокислот. Цей процес називається трансляцією (від латів. «Трансляція» - перенесення) (див. додаток, завдання 2 та таблицю). Коли синтез молекули білка закінчено, рибосома сходить з іРНК. Білок, що утворився, надходить в ендоплазматичну мережу і по її каналах в інші частини клітини, а рибосома надходить на іншу і-РНК і бере участь у синтезі іншого білка. Усі реакції білкового синтезу каталізуються спеціальними ферментами, а енергію доставляє АТФ.
Біосинтез (біологічний синтез) – це утворення складних речовин із найпростіших у живому організмі.
Останнім біосинтез відрізняється від хімічного синтезу, що йде поза клітинами – у лабораторіях, на хімічних підприємствах, іноді – у водоймах, ґрунті та гірських породах.
Крім того, у біосинтезі завжди задіяні особливі речовини – ферменти. Вони уможливлюють та/або прискорюють хімічні реакції. Ферментів відомо близько 5000, і поза живими організмами вони у природі немає.
Природа мала у своєму розпорядженні мільярди років і зазнала мільярдів способів синтезу. За цей час вона відібрала найкращі речовини, створила мініатюрні структури для їх переробки. Жива клітина перетворилася на хімічний завод, де можуть йти складні перетворення. «Завод» працює автоматично, швидко, з мінімальними втратами та максимальним виходом продукції. Відпрацьовано постачання в клітину «сировини», безперебійне постачання енергії, завжди напоготові записана в генах інформація про те, що і як треба робити.
Візьмемо, наприклад, зелений лист на дереві. На світлі з вуглекислого газу та води він безупинно утворює глюкозу. Рослина нею харчується, отримує енергію. У руках людини потужна наука та могутня техніка. Вуглекислого газу та води – скільки завгодно. З теж, начебто, проблем немає. Але люди, користуючись лише цим, не в змозі синтезувати жодної крупинки глюкози. Ми отримує її зовсім інакше, причому з крохмалю, який синтезували самі рослини.
Чому людина не може скопіювати реакції біосинтезу?
По-перше, тому що у нас немає такого «обладнання», яке має в своєму розпорядженні клітина.
По-друге, більшість ферментів – білки, щоб їх отримати, людина має з'ясувати будову кожного, потім знайти спосіб їх отримати. Все це можливе, але непросто. У результаті препарат хімічного синтезу (наприклад, штучний гормон) виявляється досить дорогим. 
Спростити справу можна, якщо хоча б частину роботи перекласти на живі клітини. Наприклад, аскорбінову кислоту (вітамін С) отримують на заводах у результаті шести хімічних реакцій. Одну з них забезпечують активні бактерії. Подібні схеми широко використовують біотехнологію.
Ми порівнювали клітку із заводом. Але у промисловості перенесення підприємств – звичайна практика. Щось схоже робить генетична інженерія. Так, людський ген білка інсуліну вдалося «влаштувати працювати» у клітину бактерії кишкової палички. У результаті новому місці синтезується інсулін – невідомий і зовсім непотрібний кишкової паличці, але гостро необхідний хворим на діабет.
Як людина використовує продукти біосинтезу?
Він, не замислюючись, використовує їх кожну мить свого життя. Коли ви читаєте ці рядки, у ваших очах йде біосинтез зорових пігментів, у печінці синтезується з глюкози запасна речовина глікоген, кістковий мозок будує молекули гемоглобіну тощо.
Крім того, людина, що споживає готові продукти «чужого» біосинтезу. Що таке наша їжа – хліб, м'ясо, олія, крупи, молоко тощо? Все це суміші білків, жирів, вуглеводів, вітамінів. Тобто продуктів біосинтезу, який пройшов у клітинах рослин та тварин.
Біосинтез забезпечує нас і промисловою сировиною. З цвілевих грибів та бактерій видобуваємо антибіотики та вітаміни. Ми одягнені та взуті в різні види білка – шерсть, хутро та шкіру ссавців, а також у бавовняну клітковину. Натуральний шовк відбираємо у метеликів тутового шовкопряда. Целюлозу, яку дерева синтезували десятиліттями, перетворюємо на папір, глюкозу, віскозу, пластмасу, будматеріали, меблі. 
Можна тільки радіти, що природа створила біосинтез - без нього ми були б всього цього позбавлені. Щоправда, без біосинтезу не було б нас самих.
ДНК – носій усієї генетичної інформації у клітині – безпосередньої участі у синтезі білка (реалізації цієї спадкової інформації) не беруть. У клітинах тварин та рослин молекули ДНК відокремлені ядерною мембраною від цитоплазми, де відбувається синтез білків. До рибосом - місць збирання білків - висилається з ядра посередник, який несе скопійовану інформацію і здатний пройти через пори ядерної мембрани. Таким посередником є інформаційна РНК, яка бере участь у матричних реакціях.
Матричні реакції - це реакції синтезу нових сполук з урахуванням «старих» макромолекул, виконують роль матриці, т. е. форми, зразка копіювання нових молекул. Матричними реакціями реалізації спадкової інформації, в яких беруть участь ДНК та РНК, є:
1. Реплікація ДНК– подвоєння молекул ДНК, завдяки яким передача генетичної інформації здійснюється від покоління до покоління. Матрицею є материнська ДНК.
2. Транскрипція(Лат. transcription– переписування) – це синтез молекул РНК за принципом комплементарності на матриці одного з ланцюгів ДНК. Відбувається в ядрі під впливом ферменту ДНК-залежної РНК-полімерази. Інформаційна РНК – це одноланцюгова молекула, і копіювання гена йде з однієї нитки дволанцюжкової молекули ДНК. Мова триплетів ДНК перекладається мовою кодонів і-РНК. Через війну транскрипції різних генів синтезуються всі види РНК. Потім і-РНК, т-РНК, р-РНК через пори в ядерній оболонці виходять у цитоплазму клітини для виконання своїх функцій.
3. Трансляція (Лат. translatio– передача, переклад) – це синтез поліпетдиних ланцюгів білків на матриці зрілої та-РНК, який здійснюється рибосомами. У цьому вся процесі виділяють кілька етапів:
Етап перший – ініціація(Початок синтезу). У цитоплазмі однією з кінців і-РНК (саме той, з якого починався синтез молекули в ядрі) вступає рибосома і починає синтез поліпептиду. Молекула т-РНК, що транспортує амінокислоту глутамін (т-РНК ГЛН), з'єднується з рибосомою та прикріплюється до початку ланцюга і-РНК (кодом УАГ). Поряд з першою т-РНК (що не має жодного відношення до синтезуючого білка) приєднується друга т-РНК з амінокислотою. Якщо антикодон т-РНК, між амінокислотами виникає пептидна зв'язок, яку утворює певний фермент. Після цього т-РНК залишає рибосому (іде в цитоплазму за новою амінокислотою), а і-РНК переміщається на один кодон.
Другий етап – елонгація(подовження ланцюга). Рибосома переміщається молекулою і-РНК не плавно, а переривчасто, триплет за триплетом. Третя т-РНК з амінокислотою зв'язується своїм антикодоном із кодоном і-РНК. При встановленні компліментарності зв'язку рибосома робить ще крок на один «кодон», а специфічний фермент «зшиває» пептидним зв'язком другу та третю амінокислоту – утворюється пептидний ланцюг. Амінокислоти в зростаючому поліпептидному ланцюгу з'єднуються в тій послідовності, в якій розташовані кодони, що їх шифрують, і-РНК (рис. 14).
Третій етап – термінація(Закінчення синтезу) ланцюга. Відбувається під час трансляції рибосомою одного з трьох «нонсенс-кодонів» (УАА, УАГ, УГА). Рибосоми зіскакують з-РНК, синтез білка завершений.
Таким чином, знаючи порядок розташування амінокислот у молекулі білка, можна визначити порядок нуклеотидів (триплетів) у ланцюзі і-РНК, а по ній – порядок пар нуклеотидів у ділянці ДНК і навпаки, враховуючи принцип компліментарності нуклеотидів.
Але у процесі матричних реакцій можуть відбуватися зміни – мутації. Це генні мутації на молекулярному рівні - результат різних пошкоджень у молекулах ДНК - торкаються одного або кількох нуклеотидів. Усі форми генних мутацій можна розділити на великі групи.
Перша група- Зсув рамки зчитування - являє собою вставки або випадання однієї або кількох дар нуклеотидів. Залежно від місця порушення змінюється та чи інша кількість кодонів. Це найбільш тяжкі ушкодження генів, оскільки в білок будуть включені зовсім інші амінокислоти. На такі делеції та вставки припадає 80% усіх спонтанних генних мутацій.
Найбільшу шкідливу дію мають нонсенс – мутації, які пов'язані з появою кодонів-термінаторів, що викликають зупинку синтезу білка. Це може спричинити передчасне закінчення синтезу білка, який швидко деградує. Результат – загибель клітини чи зміна характеру індивідуального розвитку.
Мутації, пов'язані із заміною, випаданням або вставкою в частині гена, що кодує, фенотипно виявляються у вигляді заміни амінокислот у білку. Залежно від природи амінокислот та функціональної значущості порушеної ділянки спостерігається повна або часткова втрата функціональної активності білка. Це виявляється у зниженні життєздатності, зміні ознак організмів тощо.
Друга група– це генні мутації із заміною пар основ нуклеотидів. Існують два типи заміни основ:
1. Транзиція – заміна одного пуринового на іншу пуринову основу (А на Г або Г на А) або одного піримідинової на іншу піримідинову (Ц на Т або Т на Ц).
2. Трансверсія - заміна однієї пуринової основи на піримідинову або навпаки (А на Ц, або Г на Т, або А на У). Приклад трансверсії є серповидно-клітинна анемія, що виникає через спадкове порушення структури гемоглобіну. У мутантного гена, що кодує один із ланцюгів гемоглобіну, порушено всього один нуклеотид, і в-РНК відбувається заміна аденіну на урацил (ГААна ГУА). В результаті відбувається зміна біохімічного фенотипу, в β-ланцюзі гемоглобіну глутамінова кислота замінена на валін. Ця заміна змінює поверхню гемоглобінової молекули: замість двояковогнутого диска клітини еритроцитів стають схожими на серпи і закупорюють дрібні судини, або швидко видаляються з кровообігу, що швидко призводить до анемії. .
Таким чином, значимість генних мутацій для життєдіяльності організму неоднакова:
· Деякі «мовчазні мутації» не впливають на структуру і функцію білка (наприклад, заміна нуклеотиду, що не призводить до заміни амінокислот);
· Деякі мутації ведуть до повної втрати функції білка та загибелі клітин (наприклад, нонсенс-мутації);
· Інші мутації - при якісній зміні і-РНК та амінокислот ведуть до зміни ознак організму;
· Деякі мутації, що змінюють властивості білкових молекул, надають шкідливу дію на життєдіяльність клітин - такі мутації обумовлюють тяжкий перебіг хвороб (наприклад, трансверсії).
У чому полягає біологічний синтез? Наведіть приклади.
Біологічний синтез – процес утворення біологічних макромолекул, структура яких визначається послідовністю нуклеотидом у молекулі ДНК (синтез білка). Синтез небілкових біополімерів відбувається так: спочатку синтезується білок-фермент, а з його допомогою утворюються молекули вуглеводів, ліпідів, гормонів та вітамінів.
Дайте визначення асиміляції.
Асиміляція (анаболізм чи пластичний обмін) - сукупність реакцій біологічного синтезу, у ході яких із простих речовин, що у клітину ззовні, утворюються речовини, подібні речовинам клітини.
Що таке генетичний код?
Генетичний код - єдина система запису спадкової інформації у молекулах ДНІ та РНК у вигляді послідовності нуклеотидів у них. Несе інформацію про порядок амінокислот у поліпептидному ланцюзі.
Сформулюйте основні властивості генетичного коду.
1. Специфіка. Один і той же триплет завжди відповідає лише одній амінокислоті.
2. Надмірність. Існує 64 можливі комбінації чотирьох азотистих основ (по 3 у триплеті), а кодують вони 20 амінокислот. У результаті деякі амінокислоти кодуються кількома триплетами, що підвищує надійність передачі спадкової інформації.
З. Універсальність. Генетичний код універсальний всім живих організмів. Наприклад, він однаковий у кишкової палички та людини.
4. Неперекриваність. Триплети, що кодують амінокислоти, ніколи не перекриваються, а зчитуються і передаються завжди. Неможливе використання азотистої основи одного триплету у комбінації з азотистими основами іншого триплету.
Де синтезуються рибонуклеїнові кислоти?
Інформація про структуру всіх видів РНК міститься в послідовності нуклеотидів ДНК і реалізується в один етап шляхом комплементарного синтезу молекули РНК на одному з ланцюгів молекул ДНК, тобто в результаті транскрипції.
Де відбувається синтез білка?
Безпосередня збірка білкової молекули відбувається у цитоплазмі, на рибосомах.
Розкажіть, як здійснюється синтез білка.
Процес синтезу білка реалізується у два етапи:
Перший етап - транскрипція - переклад інформації з послідовності триплетів ДНК до послідовності триплетів РНК. Здійснюється шляхом комплементарного синтезу інформаційної РНК однією з ланцюгів молекули ДНК.
Другий етап – трансляція – передача інформації з послідовності триплетів інформаційної РНК у послідовність амінокислот поліпептидного ланцюга. Здійснюється шляхом добірки антикодонів транспортної РНК до кодонів (триплет) інформаційної РНК за принципом комплементарності. Якщо антикодон транспортної РНК комплементарний кодону інформаційної РНК, між ними відбувається з'єднання, і амінокислота включається в полипептидную ланцюг. Цей процес йде в цитоплазмі, на рибосомах, які нанизані на один з кінців інформаційної РНК і пересуваються по ній триплет за триплетом.
Що таке дисиміляція? Охарактеризуйте етапи дисиміляції.
Дисиміляція (катаболізм, енергетичний обмін) – процес, зворотний до реакцій асиміляції. Складні біополімери розпадаються утворюючи прості речовини. У цьому виділяється енергія, необхідна реакцій біосинтезу.
Виділяють три етапи енергетичного обміну.
1. Підготовчий. На цьому етапі молекули полісахаридів, білків, жирів розпадаються більш дрібні молекули глюкозу, амінокислоти, жирні кислоти, гліцерин. Вся енергія, що виділяється, розсіюється у вигляді тепла.
2. Безкисневий (анаеробне дихання, або гліколіз). Цей етап неповного окислення також називають бродінням. При анаеробному окисленні 1 молекули глюкози утворюється 2 молекули АТФ. В АТФ запасається 40% енергії, що виділяється, решта розсіюється у вигляді тепла.
3. Кисневе розщеплення (аеробне дихання). На цьому етапі органічні сполуки окислюються до кінцевих продуктів СО2 та Н20. Кисневе розщеплення супроводжується виділенням великої кількості енергії та запасанням 60% її у 36 молекулах АТФ.
У чому полягає роль АТФ в обміні речовин у клітині?
Енергія, що вивільняється бреши окисленні поживних речовин у клітині, запасається у фосфатних зв'язках молекули АТФ. АТФ забезпечує енергією всі клітинні функції - біосинтез, поділ клітини, м'язове скорочення, перенесення речовин через мембрану, підтримання мембранного потенціалу та проведення нервового імпульсу.
Молекула АТФ складається з азотистого підставі аденіну, цукру рибози та трьох залишків фосфорної кислоти.
Розкажіть про енергетичний о6мен в клітині на прикладі розщеплення глюкози.
1. Підготовчий етап. Розпад глікогену або крохмалю на молекули глюкози:
(C6H10O5)n + nH2O > C6H12O6
2. Анаеробне окислення. З однієї молекули глюкози утворюється 2 молекули піровиноградної кислоти, 2 молекули АТФ та 2 молекули води. Молекули піровиноградної кислоти згодом відновлюються у молочну кислоту:
C 6H 12O 6 + 2H 3PO 4 + 2АДФ > 2C 3H 6O 3 +2АТФ +2H 2O
3. Кисневе окиснення. Молекули молочної кислоти, що утворилися, і присутності кисню окислюються до вуглекислого газу і води з утворенням 36 молекул АТФ:
2СЗНб03 + 60236АДФ + 36НЗРО.1 -
Е 6С02+42Н20+36АТФ.
Які типи живлення організмів вам відомі?
За типом харчування всі організми діляться на автотрофних і гетеротрофних.
Які організми називаються автотрофними?
Автотрофи – організми, що живуть за рахунок неорганічного джерела вуглецю – вуглекислого газу, що використовують для здійснення процесів синтезу енергію сонячного світла – фототрофи або енергію хімічних зв'язків – хемотрофи.
Охарактеризуйте світлову та темнову фази фотосинтезу.
Фотосинтез – процес утворення органічних сполук з неорганічних за рахунок енергії сонячного світла. Виділяють світлову та темнову фази фотосинтезу.
Світлова фаза фотосинтезу. Відбувається поглинання квантів кошторис хлорофілами та фотоліз (розкладання) води. В результаті утворюються молекули АТФ, атомарний водень "Н", які використовуються далі в темновій фазі для синтезу глюкози, і молекулярний кисень (як побічний продукт), що виділяється в навколишнє середовище.
Темнова фаза фотосинтезу. Відбувається утворення глюкози з вуглекислого газу, що поглинається ззовні, водню Н, отриманого в ході світлової фази, з витратою енергії АТФ, синтезованої також світлову фазу.
Чому внаслідок фотосинтезу у зелених рослин в атмосферу виділяється вільний кисень?
В ході реакцій світлової фази фотосинтезу під дією квантів світя і при взаємодії з хлорофілом відбувається розкладання (фотоліз) воли на атомарний водень і вільні радикали.
Оскільки кисень не включається до подальшого каскаду реакцій фотосинтезу, він виділяється у зовнішнє середовище.
Що таке хемосинтез?
Хемосинтез – процес синтезу органічних сполук з використанням вуглецю з вуглекислого газу за рахунок енергії хімічних зв'язків неорганічних речовин.
Які організми називаються гетеротрофними? Наведіть приклади.
Гетеротрофи – організми, які використовують органічне джерело вуглецю. До них належать усі тварини, гриби, більшість рослин.
(Теги: молекули, синтезу, фотосинтезу, відбувається, кислоти, процес, синтез, організми, енергії, кисень, вуглекислого, результаті, послідовності, Кисневе, світлову, амінокислоти, Які, шляхом, здійснюється, триплетів, вуглецю, утворюються, енергія, клітині, амінокислот, комплементарного, нуклеотидів, використовуючи, організмів, сонячного, темний, реалізується, органічних, зв'язків, квантів, розкладання, анаеробне, тепла, Приведіть, цитоплазмі, Розкажіть, обмін, також, транспортної, фотоліз, світловий, вільний, речовини, розсіюється, C6H окислюються, азотистого, послідовність, атомарний, завжди, енергію, триплет, комбінації, розщеплення, утворення, спадкової, поліпептидної, неорганічних, дисиміляція, розпадаються, етапі, етапу, світя, триплета, між, запасається, включається, ззовні, піровиноградної, окисленні полягає, називаються, водень, середовище, харчування, дихання, клітини, окислення, сполук, утворюється, хімічних, хемосинтез, Охарактеризуйте, рослин, записи, Наприклад, людини, що надходять, небілкових, Неперекриваність, генетичного, єдина, вуглеводів, передачі, Несе)
Антибіотики – спеціальні продукти життєдіяльності мікроорганізмів та їх модифікації, які мають високу фізіологічну активність по відношенню до певних груп мікроорганізмів (вірусів, бактерій, грибів, водоростей) або до злоякісних пухлин. Традиційні уявлення про антибіотики пов'язані з їх широким застосуванням у сучасній медицині та ветеринарії. Деякі антибіотичні препарати застосовують як стимулятори росту тварин, у боротьбі з хворобами рослин, при консервуванні харчових продуктів та в наукових дослідженнях (у галузі біохімії, молекулярної біології, генетики, онкології). Відповідно до класифікації, в основі якої лежить хімічна будова, антибіотики можна розділити наступні групи:
1. Ациклічні сполуки (виключаючи жирні кислоти та терпени)
2. Аліциклічні сполуки (зокрема тетрацикліни)
3. Ароматичні сполуки
5. Кисневмісні гетероцикли
7. Пептиди
В даний час розрізняють три способи одержання антибіотиків: біологічний, метод отримання напівсиітетичних препаратів та синтез хімічних сполук – аналогів природних антибіотиків.
Синтетичні антибіотики
Вивчення хімічної структури антибіотиків дало змогу отримувати їх методом хімічного синтезу. Одним із перших антибіотиків, отриманих таким методом, був левоміцетин. Великі успіхи в розвитку, хімії призвели до створення антибіотиків із спрямовано зміненими властивостями, що мають пролонговану дію, активних щодо стійких до пеніциліну стафілококів. До пролонгованих препаратів належать екмоновоцилін, біцилін 1,3,5.
Напівсинтетичні антибіотики
Їх готують комбінованим способом: методом біологічного синтезу одержують основне ядро молекули нативного антибіотика, а методом хімічного синтезу шляхом часткової зміни хімічної структури - напівсинтетичні препарати. Великим досягненням є розробка методу одержання напівсинтетичних пеніцилінів. Методом біологічного синтезу було вилучено ядро молекули пеніциліну - 6-амінопеніциланова кислота (6-АПК), яка мала слабку антимікробну активність. Шляхом приєднання до молекули 6-АПК бензильної групи створено бензилпеніцилін, який тепер одержують і методом біологічного синтезу.
Широко застосовуваний в медицині під назвою пеніцилін, бензилпеіїцилін має сильну хіміотерапевтичну активність, але активний лише щодо грампозитивних мікробів і не діє на стійкі мікроорганізми, особливо стафілококи, що утворюють фермент - β-лактамазу. Бензилпеніцилін швидко втрачає свою активність у кислому та лужному середовищах, тому його не можна застосовувати внутрішньо, оскільки він руйнується в шлунково-кишковому тракті. Напівсинтетичні препарати одержують також на основі 7-аміноцефалоспоринової кислоти (7-АЦК). Похідні 7-АЦК: цефалотин, цефалоридин (цепорії) не дають алергічних реакцій в осіб, чутливих до пеніциліну. Отримані інші напівсинтетичні антибіотики, наприклад рифампіцип - ефективний протитуберкульозний препарат.
Біологічний синтез
Повністю хімічна структура встановлена однієї третини відомих антибіотиків і лише половина може бути отримана хімічним синтезом. Тому мікробіологічний синтез отримання антибіотичних засобів є дуже актуальним. Синтез мікроорганізмами антибіотиків – одна із форм прояву антагонізму; пов'язаний з певним характером обміну речовин, що виник і закріпленим ході його еволюції, тобто це спадкова особливість, що виражається в утворенні одного і більш певних, строго специфічних для кожного виду антибіотичних речовин.
Промислове отримання антибіотиків, як правило, здійснюється шляхом біосинтезу та включає наступні стадії:
· Вибір високопродуктивних штамів продуцента (до 45 тис. ОД / мл)
· Вибір живильного середовища;
· Процес біосинтезу;
· Виділення антибіотика з культуральної рідини;
· Очищення антибіотика.
Вибір високопродуктивних штамів продуцента. Природні штами здебільшого малоактивні і не можуть використовуватися для промислових цілей. Тому після відбору найактивнішого природного штаму підвищення його продуктивності застосовують різні мутагени, викликають стійкі спадкові зміни. Ефективними мутагенами є мутагени фізичної природи - ультрафіолетове та рентгенівське випромінювання, швидкі нейтрони чи хімічні речовини. Використання мутагенів дозволяє як підвищити продуктивність природного штаму, а й отримувати штами з новими невідомими для природного мікроорганізму властивостями.
Велике значення для біосинтезу антибіотика має вибір раціонального складу поживних середовищ. Поняття «середовище для культивування» включає не лише певний якісний та кількісний склад компонентів або окремих елементів, необхідних для конструктивного та енергетичного омену організму (джерела азоту, вуглецю, фосфору, джерела ряду мікроелементів, вітаміни та ростові речовини), але також і фізико-хімічні та фізичні фактори (активна кислотність, окислювально-відновний потенціал, температура, аерація та ін.). Всі ці чинники взаємопов'язані і відіграють істотну роль розвитку мікроорганізмів.
Підбираючи середовища потрібного складу, слід враховувати специфіку організму, що культивується. Це необхідно для створення оптимальних умов, які сприяли б найкращому зростанню мікроба і біосинтезу необхідних продуктів життєдіяльності. Наприклад, якщо організм не може синтезувати деякі істотні для нього життєдіяльності сполуки (наприклад, амінокислоти або вітаміни) з простих речовин субстрату, то для його розвитку слід до складу ввести готові амінокислоти або вітаміни. До таких «вибагливих» організмів належать деякі види бактерій (молочнокислі та ін.). Актиноміцети та переважно плісняві гриби, як правило, будують речовини свого тіла і досить складні за складом кінцеві продукти обміну із сполук, що утворюються із простих компонентів субстрату.
Методи культивування продуцентів антибіотиків
У сучасних умовах найбільш перспективним методом вирощування мікроорганізмів – продуцентів антибіотиків чи інших біологічно активних сполук визнано метод глибинного культивування. Метод полягає в тому, що мікроорганізм розвивається в товщі рідкого живильного середовища, через яке безперервно пропускається стерильний повітря, і середовище перемішується.
Можна вказати чотири основні модифікації глибинного способу вирощування мікроорганізмів.
1. Періодичне культивування. При цьому способі весь процес розвитку мікроорганізмів повністю завершується в одному ферментер, після чого ферментер звільняється від культуральної рідини, ретельно промивається, стерилізується і знову заповнюється свіжим поживним середовищем. Середовище засівається мікроорганізмом, що вивчається, і процес відновлюється. Відокремлений метод. Культивування мікроорганізмів здійснюється у ферментерах із періодичним відбором частини обсягу культуральної рідини (від 30 до 60% загального обсягу). Обсяг культуральної рідини у ферментері при цьому доводиться свіжим живильним середовищем до вихідного рівня.
3. Батарейний метод. Розвиток мікроорганізмів проходить у ряді послідовно з'єднаних ферментерів. Культуральна рідина на певній стадії розвитку мікроорганізму перекачується з першого ферментера до другого, потім з другого - до третього і т. д. Звільнений ферментер негайно заповнюється свіжим живильним середовищем, засіяним мікроорганізмом. При цьому способі вирощування мікроорганізмів відбувається раціональне використання ємностей.
4. Безперервне культивування. Метод принципово відрізняється від зазначених модифікацій глибинного культивування продуцентів антибіотиків. В основі цього методу лежить те, що розвиток мікроорганізму відбувається в умовах безперервної протоки живильного середовища, що дозволяє підтримувати розвиток мікроорганізму на певній стадії його зростання. Стадія розвитку мікроорганізму визначається виходячи з найбільш вигідної для максимального біосинтезу антибіотика або іншої біологічно активної сполуки.
Ще один метод культивування мікроорганізмів – поверхневе культивування. Метод поверхневого культивування на різних агаризованих середовищах широко застосовується в лабораторній практиці та деяких промислових процесах, зокрема для збереження колекційних культур, для вивчення фізіологічних та біохімічних властивостей мікроорганізмів, для аналітичних цілей. У промисловому масштабі цей метод знайшов застосування при отриманні спорового матеріалу для виробництва органічних кислот за допомогою цвілевих грибів роду Aspergillus.
При поверхневому методі культуру мікроорганізму-продуцента вирощують на поверхні тонкого шару рідкого або твердого середовища. Рідкі живильні середовище використовують в основному при виробництві органічних кислот (лимонної, ітаконової), тверді - при виробництві комплексів на основі крохмальної та целюлози сировини, що містить.
Методи виділення антибіотиків із культуральної рідини дуже різноманітні і визначаються хімічною природою антибіотика. В основному використовують такі методи:
1. Висів грунтової суспензії у воді на поверхню агарової пластинки.Певна навішування ґрунту, ретельно розтерта у ступці з невеликим об'ємом води, кількісно переноситься в колбу зі стерильною водою. Вміст колби струшується протягом 5 мні, а потім з водної суспензії робиться ряд послідовних розведень, що висіваються на відповідне авізоване середовище. Для отримання надалі чистих культур окремі колонії після інкубації в термостаті при потрібній температурі пересіваються в пробірки зі скошеним живильним агаром. Кожна чиста культура мікроорганізму пересівається різні за складом середовища проживання і після досить хорошого розвитку перевіряються її антибіотичні властивості.
2. Висів грунту на живильний агар, попередньо засіяний тест-організмом. Поверхня живильного агару засівається тест - культурою необхідного організму, після чого на агарову пластинку розкладають невеликі, не більше просяного зерна, грудочки грунту або грунт наносять у вигляді пилу, розподіляючи її по всій поверхні пластинки. Потім чашки поміщають у термостат і через певний проміжок часу (24-48 год, а іноді і більше) переглядають шматочки ґрунту або окремі його ділянки, навколо яких утворилися зони затримки росту тест-організму. З цих ділянок виділяють чисті культури організмів та піддають їх подальшому вивченню.
3. Метод збагачення ґрунту.Ґрунт, з якого припускають виділити антагоністів, збагачують організмами тих видів, стосовно яких хочуть отримати антагоніст. З цією метою до зразків ґрунту, поміщеним у скляні судини, систематично додають відмиту суспензію необхідних мікроорганізмів. Потім через певні проміжки часу такий ґрунт висівається у вигляді окремих грудочок на агарові пластинки в чашках Петрі, попередньо засіяні тим самим організмом, який використовувався для збагачення ґрунту.
4. Метод центрифугування ґрунтової суспензії.Для виділення актиноміцетів з ґрунтів і особливо з ґрунтів у весняний час, коли в ній розвивається велика кількість грибів і бактерій, застосовується метод центрифугування ґрунтової суспензії. Метод заснований на відмінності швидкості осідання окремих видів мікроорганізмів у відцентровому полі. При 3000 об/хв протягом 20 хв частинки, що відповідають за розмірами спорів плісняв або клітин бактерій, осаджуються на дно пробірки. Частинки ж, відповідні за розмірами спорів актиноміцетів, виявляються при даній швидкості центрифугування поверхневому шарі рідини. Висіваючи надосадову рідину, вдається в більшості випадків (до 92%) одержати на платівках живильного агару лише колонії актиноміцетів.
5. Метод заморожування – відтавання ґрунту.Відомо, що мікроорганізми у ґрунті знаходяться в адсорбованому на ґрунтових частках стані. Для повноти десорбції мікроорганізмів із ґрунтових частинок застосовуються різні методи: хімічні, при яких ґрунтові зразки обробляють різними детергентами, фізичні, в основі яких лежить метод механічного розтирання зразків ґрунту.
Для кращої десорбції мікроорганізмів із ґрунтових частинок рекомендується використовувати метод заморожування – відтавання ґрунту. Суть методу полягає у наступному. Відібраний для виділення актиноміцетів зразок ґрунту міститься у випарнику побутового холодильника при температурі 8°. Через годину зразок виймається з холодильника і витримується при кімнатній температурі до повного розморожування. Процедуру заморожування-відтавання повторюють двічі. Потім навішування ґрунту поміщають у стерильну водопровідну воду, збовтують суспензію протягом 15 хв на круговій гойдалці при 230 об/хв, після чого різні розведення суспензії висівають на живильну агарову пластинку в чашках Петрі.
Метод заморожування - відтавання зразків ґрунту дозволяє виявити в них у 1,2-3,6 рази більше актиноміцетів, ніж у тих самих зразках без заморожування. Це, мабуть, пов'язане з підвищенням десорбції актиноміцетів із поверхні ґрунтових частинок. Очищення антибіотика проводиться хроматографічними методами (хроматографія на оксиді алюмінію, целюлозі, іонітах) або протиточною екстракцією. Очищені антибіотики піддають ліофільному сушінню. Після виділення антибіотика проводять випробування його чистоти. Для цього визначають його елементний склад, фізико-хімічні константи (температуру плавлення, молекулярну масу, адсорбцію у видимій, УФ- та ІЧ-областях спектра, питоме обертання). Досліджують також антибактеріальну активність, стерильність та токсичність антибіотика.
Токсичність антибіотиків визначають на експериментальних тварин, яким протягом певного періоду внутрішньовенно, внутрішньочеревно, внутрішньом'язово або іншим шляхом вводять різні дози антибіотика, що вивчається. За відсутності зовнішніх змін у поведінці тварин протягом 12-15 діб вважають, що випробуваний антибіотик не має помітних токсичних властивостей. При більш глибокому дослідженні з'ясовують, чи має даний антибіотик приховану токсичність і чи впливає на окремі тканини та органи тварин. Одночасно досліджують характер біологічної дії антибіотика – бактеріостатичний чи бактерицидний, що дозволяє прогнозувати механізми його антибактеріальних властивостей.
Наступний етап вивчення антибіотика – оцінка його терапевтичних властивостей. Експериментальні тварини заражають певним видом патогенного мікроба. Мінімальна кількість антибіотика, що оберігає тварину від смертельної дози інфекції, є мінімальною терапевтичною дозою. Чим більше відношення токсичної дози антибіотика до терапевтичної, тим вищий терапевтичний індекс. Якщо терапевтична доза дорівнює токсичній або наближається до неї (низький терапевтичний індекс), то ймовірність застосування антибіотика в лікувальній практиці обмежена або неможлива. У разі, коли антибіотик входить у широку медичну практику, розробляють промислові методи його отримання та детально вивчають його хімічну структуру.
Стандартизація антибіотиків
За одиницю антибіотичної активності приймають мінімальну кількість антибіотика, здатне придушити розвиток або затримати зростання стандартного штаму тест-мікробу у певному обсязі живильного середовища. Величину біологічної активності антибіотиків зазвичай виражають в умовних одиницях дози (ОД), що містяться в 1 мл розчину (ОД/мл) або в 1 мг препарату (ОД/мг). Наприклад, за одиницю антибіотичної активності пеніциліну прийнято вважати мінімальну кількість препарату, здатне затримувати зростання золотистого стафілокока стандартного штаму 209 50 мл поживного бульйону. Для стрептоміцину за одиницю активності прийнято вважати мінімальну кількість антибіотика, що затримує ріст Е. coli в 1 мл поживного бульйону.
Після того, як багато антибіотиків були отримані в чистому вигляді, для деяких з них почали виражати біологічну активність у масових одиницях. Наприклад, встановлено, що 1 мг чистої основи стрептоміцину еквівалентний 1000 ОД. Отже, 1 ОД активності стрептоміцину еквівалентна 1 мкг чистої основи цього антибіотика. Тому в даний час у більшості випадків кількість стрептоміцину виражають у мкг/мг або мкг/мл. Чим ближче число мкг/мг у препаратах стрептоміцину до 1000, тим, отже, чистіший препарат. Зрозуміло, що одиниця біологічної активності антибіотика який завжди збігається з 1 мкг. Наприклад, для бензилпеніциліну 1 ОД еквівалентна приблизно 0,6 мкг, оскільки 1 мг антибіотика містить 1667 ОД.
Методи аналізу антибіотиків
На відміну від інших природних сполук (алкалоїди, глікозиди) для антибіотиків немає загальних групових реакцій. Такі реакції можуть бути використані тільки для антибіотиків одного хімічного класу, наприклад, для тетрациклінів або нітрофенілалкіламінів (левоміцетинів). Для ідентифікації антибіотиків можуть бути використані різні кольорові реакції на функціональні групи; спектральні характеристики у видимій, УФ- та ІЧ-областях спектра; Хроматографічні методи. Для кількісного визначення антибіотиків використовують біологічні, хімічні, фізико-хімічні методи.
Біологічні методи засновані на безпосередньому біологічному дії антибіотика на тест-організм, що застосовується, чутливий до даного антибіотику. Дифузійний метод, що застосовується при цьому, заснований на здатності молекул антибіотиків дифундувати в агарових середовищах. Оцінюється розмір зони, де використовувані тест-організми не розвиваються. Цей розмір залежить від хімічної природи антибіотика, його концентрації, рН та складу середовища, температури експерименту.
В основі іншого різновиду біологічного тестування лежить турбідиметрія - метод кількісного аналізу за інтенсивністю світла, поглиненого зваженими частинками - клітинами мікроорганізмів. При додаванні певних кількостей антибіотиків спостерігається затримка росту клітин мікроорганізмів (бактеріостатичний ефект), а потім їхня загибель (бактерицидний ефект). У цьому змінюється (зменшується) інтенсивність поглиненого світла. В якості альтернативного турбідиметрії методу може бути використаний нефелометричний метод кількісного аналізу інтенсивності світла, розсіяного мікроорганізмами.
Для кількісного визначення антибіотиків застосовують різні спектральні методи - в першу чергу, фотоколориметричні та спектрофотометричні методи. Наприклад, для визначення концентрації розчину еритроміцину можна застосувати фотоколориметричний метод, заснований на зміні абсорбції розчину антибіотика після взаємодії його із сірчаною кислотою. Антибіотики тетрациклінового ряду можуть бути визначені методом спектрофотометрії по смузі поглинання, що зникає після лужного гідролізу діючої речовини. Розроблено спосіб, що поєднує фізико-хімічний та біологічний підходи до оцінки активності ЛЗ. Метод заснований на лазерній дифракції в середовищі, що містить клітини мікроорганізмів при дії на них хімічних речовин, зокрема антибіотиків
Збереження штамів продуцентів антибіотиків в активному стані
Важливе значення для промислового одержання антибіотиків, а також для лабораторних досліджень продуцентів антибіотичних речовин мають методи підтримки життєздатності організмів, що дозволяють зберегти їхню антибіотичну активність на постійному рівні. Відомо, що мікроорганізми і особливо актиноміцети легко змінюються за звичайних методів їх зберігання. До того ж досить часто при цьому спостерігається повна або часткова втрата антибіотичних властивостей. Втрата антибіотичних властивостей залежить, мабуть, від того, що ми не вміємо у звичайних умовах культивування створити такі умови, які сприяли б збереженню організмом його основних фізіологічних особливостей. Нерідко втрата активності спостерігається при культивуванні мікроорганізмів на багатих за складом середовищах та при частих пересіваннях.
Разом про те зміна фізіологічних чи біохімічних властивостей продуцентів антибіотичних речовин може визначатися, їх генетичними закономірностями. Відомо, наприклад, що продуцент граміцидину в процесі розвитку дисоціює на ряд варіантів, деякі з яких не утворюють цей антибіотик. Причому процес дисоціації культури йде у напрямі освіти у великій кількості біологічно неактивних варіантів, що зрештою призводить до повної втрати культурою здатності до утворення граміцидину. В даний час використовується ряд методів збереження культур продуцентів антибіотиків, що забезпечує їхнє тривале перебування в активному стані. В основу цих методів покладено принцип затримки розвитку мікроорганізмів, принцип консервації. Для кожного виду продуцента антибіотичних речовин повинен бути підібраний свій, найбільш вдалий метод консервування, що дозволяє зберегти культури в активному стані протягом тривалого часу.
Найбільш поширеними методами збереження культур мікроорганізмів-продуцентів антибіотиків в активному стані є такі.
1. Ліофілізація культур.
2. Зберігання вегетативних клітин або спор організмів у стерильному ґрунті, стерильному піску або на насінні деяких рослин (наприклад, просі). За даними ряду авторів, культури актиноміцетів, які перебувають у стерильному ґрунті, зберігають життєздатність протягом 30 років та більше.
3. Зберігання спор як водних суспензій в запаяних ампулах.
4. Зберігання суперечок у стерильному кварцовому піску.
5. Зберігання культур на агаровому косячці під мінеральним маслом.
6. Зберігання культур за низьких температур (+4, +5°С).
7. Останнім часом для збереження різних мікроорганізмів в активному стані використовують рідкий азот, який перешкодять відмиту від середовища суспензію клітин. Іноді в газоподібній фазі рідкого азоту зберігають культури актиноміцетів, що знаходяться на агарових блочках, вирізаних з агарової пластинки у чашках Петрі.
Найкращою формою збереження організмів, при якій не спостерігається втрати антибіотичної активності, є їх ліофілізація - метод придатний як для спороутворювальних, так і для безспорових культур мікроорганізмів. Сутність цього методу полягає в тому, що суспензія клітин або спор мікроорганізму, приготовлена на середовищі, багатої білками (часто використовується для цих цілей кров'яна сироватка), швидко заморожується при температурі від - 40 до - 60 ° С і висушується під вакуумом до залишкової вологості ( 05-07%). Після такої обробки ампули зі спорами або клітинами ліофнлізованого мікроба запаюють. Ліофілізовані форми бактерій можуть зберігатися протягом 16-18 років, суперечки грибів не втрачають основних властивостей при зберіганні в ліофілізованому вигляді протягом 10 років.
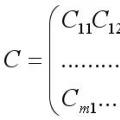 Позначення елементів матриці
Позначення елементів матриці Метод крамаря розв'язання систем лінійних рівнянь
Метод крамаря розв'язання систем лінійних рівнянь Війна в ліжках - Це фейк чи правда
Війна в ліжках - Це фейк чи правда