Использование исследовательских заданий на уроках химии. Развитие исследовательских умений при обучении химии Получение кислорода термическим разложением перкарбонатов
Cлайд 1
Cлайд 2
 Элементы и атомы, В менделеевский взятые круг Сделали химию самой богатой И самой творческой из наук. Г.Санников
Элементы и атомы, В менделеевский взятые круг Сделали химию самой богатой И самой творческой из наук. Г.Санников
Cлайд 3
 Химия - удивительная наука. С одной стороны, она очень конкретна и имеет дело с бесчисленными полезными и вредными веществами вокруг нас и внутри нас. Поэтому химия нужна всем: повару, шоферу, садоводу, строителю.
Химия - удивительная наука. С одной стороны, она очень конкретна и имеет дело с бесчисленными полезными и вредными веществами вокруг нас и внутри нас. Поэтому химия нужна всем: повару, шоферу, садоводу, строителю.
Cлайд 4
 Исследования дома на кухне под руководством учителя Задачи исследования: Образовательные: дать дополнительные сведения о кислотах и основаниях, грамотно их использовать; формирование навыков написания отчетов; научить учащихся самостоятельно мыслить, находить и решать проблемы. Развивающие: развивать умение выделять главное, обобщать, классифицировать; самостоятельно приобретать знания. Воспитательные: научить самостоятельно оценивать, наблюдать явления; развивать познавательный интерес к предмету и творческие способности в процессе самостоятельной работы; формирование интереса к новому предмету.
Исследования дома на кухне под руководством учителя Задачи исследования: Образовательные: дать дополнительные сведения о кислотах и основаниях, грамотно их использовать; формирование навыков написания отчетов; научить учащихся самостоятельно мыслить, находить и решать проблемы. Развивающие: развивать умение выделять главное, обобщать, классифицировать; самостоятельно приобретать знания. Воспитательные: научить самостоятельно оценивать, наблюдать явления; развивать познавательный интерес к предмету и творческие способности в процессе самостоятельной работы; формирование интереса к новому предмету.
Cлайд 5
 Отчет по исследовательской работе выполняется по плану. 1. Название темы работы. Название должно точно отражать содержание работы. Дата, место проведения, фамилию и имя автора. 2. Цель работы и ее задачи. 3. Методика работы. Результаты работы зависят от числа проведенных опытов, наблюдений и их обработки. Какими способами велись наблюдения, сколько их было проведено, с какими веществами. 4. Результаты и их обсуждение. Одно и тоже задание могут получить несколько учеников. Поэтому необходимо обсудить результаты опытов, наблюдений, сравнение отчетов.
Отчет по исследовательской работе выполняется по плану. 1. Название темы работы. Название должно точно отражать содержание работы. Дата, место проведения, фамилию и имя автора. 2. Цель работы и ее задачи. 3. Методика работы. Результаты работы зависят от числа проведенных опытов, наблюдений и их обработки. Какими способами велись наблюдения, сколько их было проведено, с какими веществами. 4. Результаты и их обсуждение. Одно и тоже задание могут получить несколько учеников. Поэтому необходимо обсудить результаты опытов, наблюдений, сравнение отчетов.
Cлайд 6
 Методика проведения исследования. 1. Подготовительный этап: Для опытов потребуется небольшое количество овощей, фруктов, пищевой соды, уксуса, соков, поэтому, необходимо обратиться к родителям с просьбой, не жалеть, если ребенок испортит их в своих опытах, ведь ребенок познает окружающий мир, а это - шаг в большую науку. 2. Знакомство с объектом исследования. Ученик получает карточку – задание. 3. Ознакомление с техникой безопасности.
Методика проведения исследования. 1. Подготовительный этап: Для опытов потребуется небольшое количество овощей, фруктов, пищевой соды, уксуса, соков, поэтому, необходимо обратиться к родителям с просьбой, не жалеть, если ребенок испортит их в своих опытах, ведь ребенок познает окружающий мир, а это - шаг в большую науку. 2. Знакомство с объектом исследования. Ученик получает карточку – задание. 3. Ознакомление с техникой безопасности.
Cлайд 7
 Инструкция по ТБ: Никогда не пейте и не ешьте вещества, которые используете в своих опытах, а также не позволяйте им попадать вам в глаза, рот. Нюхать их следует осторожно, постепенно поднося вещество к носу до момента ощущения его запаха.
Инструкция по ТБ: Никогда не пейте и не ешьте вещества, которые используете в своих опытах, а также не позволяйте им попадать вам в глаза, рот. Нюхать их следует осторожно, постепенно поднося вещество к носу до момента ощущения его запаха.
Cлайд 8
 Проведение исследования. Работа 1. Кислоты и основания на кухне. Вам потребуется: уксус, лимонный, апельсиновый, яблочный соки, лимонная кислота, газированная вода, пищевая сода, моющее средство, стаканы. Насыпьте полную ложку соды в пустой стакан. Налейте в стакан немного уксуса. Что наблюдаете?.Испытайте лимонный, апельсиновый, яблочный соки, газированную воду, моющее средство. Смешайте каплю моющего средства с любой жидкой кислотой (уксусом, фруктовым соком или газировкой). Добавьте небольшое количество полученной смеси в ложку с пищевой содой. Образуется при этом пена? Образование пены указывает на то, что раствор продолжает оставаться кислотой. Добавьте дополнительное количество моющего средства в полученную ранее смесь. Продолжайте тестировать кислотные свойства смеси, наблюдая за выделением пены. Прекращение образования пены будет означать нейтрализацию кислоты.
Проведение исследования. Работа 1. Кислоты и основания на кухне. Вам потребуется: уксус, лимонный, апельсиновый, яблочный соки, лимонная кислота, газированная вода, пищевая сода, моющее средство, стаканы. Насыпьте полную ложку соды в пустой стакан. Налейте в стакан немного уксуса. Что наблюдаете?.Испытайте лимонный, апельсиновый, яблочный соки, газированную воду, моющее средство. Смешайте каплю моющего средства с любой жидкой кислотой (уксусом, фруктовым соком или газировкой). Добавьте небольшое количество полученной смеси в ложку с пищевой содой. Образуется при этом пена? Образование пены указывает на то, что раствор продолжает оставаться кислотой. Добавьте дополнительное количество моющего средства в полученную ранее смесь. Продолжайте тестировать кислотные свойства смеси, наблюдая за выделением пены. Прекращение образования пены будет означать нейтрализацию кислоты.
Cлайд 9
 Работа 2. Выращивание кристаллов. Вам потребуется: соль, сахар, вода прозрачные пластиковые стаканчики, ложка, веревка, карандаш. Положите несколько полных ложек столовой соли в стакан. Заполните стакан на три четверти водой. Перемешайте соль ложкой. Если соль растворилась, добавьте еще одну ложку соли, перемешивайте и добавляйте соль до тех пор, пока раствор не станет насыщенным. Привяжите веревку к середине карандаша, а свободный конец веревки опустите с помощью ложки на дно стакана. На следующий день вы увидите, что на стенках стакана и на веревке выделились кристаллы. Повторите эксперимент, используя сахар или другую соль. Оставьте опытные установки на неделю, тем самым, дав время для прохождения максимальной кристаллизации. Внимательно изучите образовавшиеся кристаллы, и вы заметите, что они разной формы. Замените веревку на нить. Отделите отдельный кристалл и наблюдайте за ним. С каждым днем он будет увеличиваться в размере.
Работа 2. Выращивание кристаллов. Вам потребуется: соль, сахар, вода прозрачные пластиковые стаканчики, ложка, веревка, карандаш. Положите несколько полных ложек столовой соли в стакан. Заполните стакан на три четверти водой. Перемешайте соль ложкой. Если соль растворилась, добавьте еще одну ложку соли, перемешивайте и добавляйте соль до тех пор, пока раствор не станет насыщенным. Привяжите веревку к середине карандаша, а свободный конец веревки опустите с помощью ложки на дно стакана. На следующий день вы увидите, что на стенках стакана и на веревке выделились кристаллы. Повторите эксперимент, используя сахар или другую соль. Оставьте опытные установки на неделю, тем самым, дав время для прохождения максимальной кристаллизации. Внимательно изучите образовавшиеся кристаллы, и вы заметите, что они разной формы. Замените веревку на нить. Отделите отдельный кристалл и наблюдайте за ним. С каждым днем он будет увеличиваться в размере.
Cлайд 10
 Работа 3. Блестящая монета. Вам потребуется: любая медьсодержащая монета, соль, уксус, бумажное полотенце, ложка. Положите монету на бумажное полотенце. Посыпьте на нее немного соли. С помощью ложки полейте сверху уксусом. Потрите монету, и она засияет на ваших глазах! Повторите этот эксперимент с а) одной солью. б) одним уксусом. в) с лимонным соком. г) с солью и лимонным соком. Позволяет ли одна из перечисленных комбинаций очищать монету так же эффективно, как с помощью уксуса и соли?
Работа 3. Блестящая монета. Вам потребуется: любая медьсодержащая монета, соль, уксус, бумажное полотенце, ложка. Положите монету на бумажное полотенце. Посыпьте на нее немного соли. С помощью ложки полейте сверху уксусом. Потрите монету, и она засияет на ваших глазах! Повторите этот эксперимент с а) одной солью. б) одним уксусом. в) с лимонным соком. г) с солью и лимонным соком. Позволяет ли одна из перечисленных комбинаций очищать монету так же эффективно, как с помощью уксуса и соли?
Cлайд 11

Cлайд 12
 Популярными среди учителей химии становятся уроки-исследования. Такие уроки требуют большой подготовки, которая, как показывает практика, себя оправдывает. Такие уроки строятся в соответствии с логикой деятельностного подхода и включают следующие этапы: мотивационно-ориентировочный, операционно-исполнительский (анализ, прогнозирование и эксперимент), оценочно рефлексивный.
Популярными среди учителей химии становятся уроки-исследования. Такие уроки требуют большой подготовки, которая, как показывает практика, себя оправдывает. Такие уроки строятся в соответствии с логикой деятельностного подхода и включают следующие этапы: мотивационно-ориентировочный, операционно-исполнительский (анализ, прогнозирование и эксперимент), оценочно рефлексивный.
Cлайд 13
 Проведение мысленного эксперимента. Способствует развитию умения рассуждать. Это задания, в которых требуется получить конкретное вещество из предложенных; получить вещество несколькими способами; провести все характерные и качественные реакции, свойственные данному классу веществ; выявить генетическую связь между классами неорганических веществ.
Проведение мысленного эксперимента. Способствует развитию умения рассуждать. Это задания, в которых требуется получить конкретное вещество из предложенных; получить вещество несколькими способами; провести все характерные и качественные реакции, свойственные данному классу веществ; выявить генетическую связь между классами неорганических веществ.
Cлайд 14
 Примеры заданий мысленного эксперимента. В реторту насыпали порошок цинка, перекрыли газоотводную трубку зажимом, реторту взвесили и содержимое прокалили. Когда реторта остыла, ее снова взвесили. Изменилась ли масса и почему? Затем открыли зажим. Изменилась ли масса и почему? 2. На чашках весов уравновешены стаканчики с растворами гидроксида натрия и хлорида натрия. Изменит ли положение стрелка весов через некоторое время и почему?
Примеры заданий мысленного эксперимента. В реторту насыпали порошок цинка, перекрыли газоотводную трубку зажимом, реторту взвесили и содержимое прокалили. Когда реторта остыла, ее снова взвесили. Изменилась ли масса и почему? Затем открыли зажим. Изменилась ли масса и почему? 2. На чашках весов уравновешены стаканчики с растворами гидроксида натрия и хлорида натрия. Изменит ли положение стрелка весов через некоторое время и почему?
Cлайд 15
 Творческие задания на прогнозирование свойств веществ. Такие задания способствуют формированию исследовательских умений, стимулируют интерес, позволяют познакомить учащихся с достижениями ученых, увидеть красивые, изящные яркие примеры работы творческой мысли.
Творческие задания на прогнозирование свойств веществ. Такие задания способствуют формированию исследовательских умений, стимулируют интерес, позволяют познакомить учащихся с достижениями ученых, увидеть красивые, изящные яркие примеры работы творческой мысли.
Cлайд 16
 Например, при изучении темы “Углеводы” учащимся предлагаются вопросы: 1.Немецкий химик Христиан Шенбейн нечаянно пролил на пол смесь серной и азотной кислот. Он машинально вытер пол хлопчатобумажным фартуком своей жены. “Кислота может поджечь фартук”, - подумал Шенбейн, прополоскал фартук в воде и повесил сушить над печкой. Фартук подсох, но затем раздался негромкий взрыв и … фартук исчез. Почему произошел взрыв? 2.Что произойдет, если долго жевать хлебный мякиш?
Например, при изучении темы “Углеводы” учащимся предлагаются вопросы: 1.Немецкий химик Христиан Шенбейн нечаянно пролил на пол смесь серной и азотной кислот. Он машинально вытер пол хлопчатобумажным фартуком своей жены. “Кислота может поджечь фартук”, - подумал Шенбейн, прополоскал фартук в воде и повесил сушить над печкой. Фартук подсох, но затем раздался негромкий взрыв и … фартук исчез. Почему произошел взрыв? 2.Что произойдет, если долго жевать хлебный мякиш?
Cлайд 17
 Тема урока: Химические свойства азотной кислоты. Общедидактическая цель урока: создать условия для первичного осознания и осмысления учебной информации с целью развития исследовательских умений учащихся средствами технологии проблемного обучения. Триединая дидактическая цель: Образовательный аспект: способствовать формированию у учащихся понятия "кислота" на примере азотной кислоты; создать условия для выявления общих и специфических свойств азотной кислоты посредством решения экспериментальных и познавательных задач, отработать умения в написании уравнений реакций. Развивающий аспект: содействовать развитию у учащихся исследовательских умений в процессе выполнения и наблюдения эксперимента. Воспитательный аспект: поддерживать интерес к изучению темы через самостоятельную работу; воспитывать сотрудничество; способствовать развитию грамотной химической речи.
Формы реализации методов: проблемный семинар. Приемы реализации методов: создание заданий исследовательского характера; задания на сравнение и анализ ранее полученной информации; задания на самостоятельный перенос знаний в новую учебную ситуацию. Формы организации познавательной деятельности: общеклассная, групповая (на данном уроке предусматривает облегчение выполнения экспериментальной исследовательской работы, способствует созданию адаптивной образовательной среды и экономию реактивов), индивидуальная. Ожидаемый результат: все учащиеся усвоят общие и специфические свойства азотной кислоты, а также почему раствор азотной кислоты взаимодействует с металлами не так как растворы других кислот.
Тема урока: Химические свойства азотной кислоты. Общедидактическая цель урока: создать условия для первичного осознания и осмысления учебной информации с целью развития исследовательских умений учащихся средствами технологии проблемного обучения. Триединая дидактическая цель: Образовательный аспект: способствовать формированию у учащихся понятия "кислота" на примере азотной кислоты; создать условия для выявления общих и специфических свойств азотной кислоты посредством решения экспериментальных и познавательных задач, отработать умения в написании уравнений реакций. Развивающий аспект: содействовать развитию у учащихся исследовательских умений в процессе выполнения и наблюдения эксперимента. Воспитательный аспект: поддерживать интерес к изучению темы через самостоятельную работу; воспитывать сотрудничество; способствовать развитию грамотной химической речи.
Формы реализации методов: проблемный семинар. Приемы реализации методов: создание заданий исследовательского характера; задания на сравнение и анализ ранее полученной информации; задания на самостоятельный перенос знаний в новую учебную ситуацию. Формы организации познавательной деятельности: общеклассная, групповая (на данном уроке предусматривает облегчение выполнения экспериментальной исследовательской работы, способствует созданию адаптивной образовательной среды и экономию реактивов), индивидуальная. Ожидаемый результат: все учащиеся усвоят общие и специфические свойства азотной кислоты, а также почему раствор азотной кислоты взаимодействует с металлами не так как растворы других кислот.
Cлайд 20
 Педагогические выводы 1. В исследовательскую деятельность с удовольствием и интересом включаются учащиеся разного уровня подготовленности и разного возраста, т.е. неверно утверждение о том, что это область интересов и возможностей старшеклассников и что этот вид деятельности под силу только одаренным детям. Педагоги, вовлекающие в исследовательскую деятельность учащихся разного уровня подготовленности, должны учитывать возможности ребенка, прогнозировать уровень результата, темп реализации программы исследования. 2. В ходе исследовательской деятельности развитие способностей ребенка происходит при определенных условиях: - если тема и предмет исследовательской деятельности соответствуют потребностям ребенка; - обучение идет в “зоне ближайшего развития и на достаточно высоком уровне трудностей”; - если содержание деятельности опирается на “субъективный опыт ребенка”; - если идет научение способам деятельности. 3. Обучение навыкам исследовательской работы начинается с урока, который строится по законам проведения научного исследования. Технология исследовательской деятельности ориентирована на развитие умений: - определять цели и задачи исследования, его предмет; - самостоятельного поиска литературы и ее конспектирования; - анализа и систематизации информации; - аннотировать изученные источники; - выдвигать гипотезу, проводить в соответствии с ней практическое исследование с классификаций материала; - описывать результаты исследования, делать выводы и обобщения.
Педагогические выводы 1. В исследовательскую деятельность с удовольствием и интересом включаются учащиеся разного уровня подготовленности и разного возраста, т.е. неверно утверждение о том, что это область интересов и возможностей старшеклассников и что этот вид деятельности под силу только одаренным детям. Педагоги, вовлекающие в исследовательскую деятельность учащихся разного уровня подготовленности, должны учитывать возможности ребенка, прогнозировать уровень результата, темп реализации программы исследования. 2. В ходе исследовательской деятельности развитие способностей ребенка происходит при определенных условиях: - если тема и предмет исследовательской деятельности соответствуют потребностям ребенка; - обучение идет в “зоне ближайшего развития и на достаточно высоком уровне трудностей”; - если содержание деятельности опирается на “субъективный опыт ребенка”; - если идет научение способам деятельности. 3. Обучение навыкам исследовательской работы начинается с урока, который строится по законам проведения научного исследования. Технология исследовательской деятельности ориентирована на развитие умений: - определять цели и задачи исследования, его предмет; - самостоятельного поиска литературы и ее конспектирования; - анализа и систематизации информации; - аннотировать изученные источники; - выдвигать гипотезу, проводить в соответствии с ней практическое исследование с классификаций материала; - описывать результаты исследования, делать выводы и обобщения.
ИСПОЛЬЗОВАНИЕ ИССЛЕДОВАТЕЛЬСКИХ ЗАДАНИЙ НА УРОКАХ ХИМИИ
Один из известных философов как-то заметил, что образование – это то, что остается в сознании ученика, когда все выученное забыто. Что должно остаться в голове ученика, когда забыты законы физики, химии, теоремы геометрии и правила биологии? Совершенно верно – творческие умения, необходимые для самостоятельной познавательной и практической деятельности, и убеждение в том, что любая деятельность должна отвечать моральным нормам.
Учение вообще есть “совместное исследование, проводимое учителем и учеником” (С.Л.Рубинштейн). Именно педагог дает формы и условия исследовательской деятельности, благодаря которым у ученика формируется внутренняя мотивация подходить к любой возникающей перед ним проблеме с исследовательской, творческой позиции. При обучении детей навыкам исследовательской деятельности я сначала использую проблемные вопросы и ситуации. При использовании проблемного обучения нужно понимать, что только тогда можно говорить о развитии мышления, когда проблемные ситуации используются регулярно, сменяя одна другую. Использование проблемных ситуаций на уроках химии способствует формированию диалектического мышления школьников, развитию умений находить и решать противоречия.
Способы создания проблемной ситуации могут быть самыми разнообразными.
К ним можно отнести:
1. Демонстрацию или сообщение некоторых фактов , которые учащимся неизвестны и требуют для объяснения дополнительной информации. Они побуждают к поиску новых знаний. Например, учитель демонстрирует аллотропные видоизменения элементов и предлагает объяснить, почему они возможны, или, например, учащиеся еще не знают, что хлорид аммония может возгоняться, а им предлагают вопрос, как разделить смесь хлорида аммония и хлорида калия.
2. Использование противоречия между имеющимися знаниями и изучаемыми фактами, когда на основании известных знаний учащиеся высказывают неправильные суждения. Например, учитель задает вопрос: «Может ли при пропускании оксида углерода (IV) через известковую воду получиться прозрачный раствор?» Учащиеся на основании предшествующего опыта отвечают отрицательно, а учитель показывает демонстрационный опыт с образованием гидрокарбоната кальция.
3. Объяснение фактов на основании известной теории. Например, почему при электролизе сульфата натрия на катоде выделяется водород, а на аноде – кислород? Учащиеся должны ответить на вопрос, пользуясь справочными таблицами: рядом напряжения металлов, рядом анионов, расположенных в порядке убывания способности к окислению, и сведениями об окислительно-восстановительной сущности электролиза.
4. Построение гипотезы на основе известной теории, а затем ее проверку. Например, будет ли уксусная кислота как кислота органическая проявлять общие свойства кислот? Учащиеся высказывают предположение, учитель ставит эксперимент или проводится лабораторный, а затем дается теоретическое объяснение.
5. Нахождение рационального пути решения, когда заданы условия и дается конечная цель. Например, учитель предлагает экспериментальную задачу: даны три пробирки с веществами; определить эти вещества наиболее коротким способом, с наименьшим числом проб.
6. Нахождение самостоятельного решения при заданных условиях . Это уже творческая задача, для решения которой недостаточно урока, поэтому для решения проблемы необходимо вне урока использовать дополнительную литературу, справочники. Например, подобрать условия для определенной реакции, зная свойства веществ, вступающих в нее, высказать предположения по оптимизации изучаемого производственного процесса.
7. Принцип историзма также создает условия для проблемного обучения. Например , поиск путей систематизации химических элементов, приведший, в конечном счете Д.И. Менделеева, к открытию периодического закона. Многочисленные проблемы, связанные с обеспечением взаимного влияния атомов в молекулах органических веществ на основе электронного строения, также являются отражением вопросов, возникавших в истории развития органической химии.
Наиболее удачно найденной проблемной ситуацией следует считать такую, при которой проблему формулируют сами учащиеся. Исследовательскую деятельность, по моему мнению, также можно отнести к числу технологий личностно ориентированного характера при условии, если педагог проявляет заинтересованность в личностном росте ученика, формировании его ценностных ориентиров, личностных качеств. Это возможно благодаря и содержанию работы, которую выполняет ученик и благодаря общению взрослого и ребенка в ходе исследовательской деятельности.
При выполнении исследовательской деятельности на основе эксперимента предполагаются следующие этапы общенаучной деятельности:
Постановка цели эксперимента, цель определяет, какой результат намерен получить экспериментатор в ходе исследования.
Формулировка и обоснование гипотезы, которую можно положить в основу эксперимента. Гипотеза - это совокупность теоретических положений, истинность которых подлежит проверке.
Планирование эксперимента осуществляется в следующей последовательности: 1) отбор лабораторного оборудования и реактивов; 2) составление плана проведения эксперимента, и, при необходимости изображение конструкции прибора; 3)продумывание работы после окончания эксперимента (утилизация реактивов, особенности мытья посуды и т.д.); 4) выявление источника опасности (описание мер предосторожности при выполнении эксперимента); 5) выбор формы записи результатов эксперимента.
Осуществление эксперимента, фиксация наблюдений и измерений.
Анализ, обработка и объяснение результатов эксперимента предусматривают: 1) математическую обработку результатов эксперимента (при необходимости); 2) сравнение результатов эксперимента с гипотезой; 3) объяснение протекающих процессов в эксперименте; 4) формулировку вывода.
Рефлексия – осознание и оценка эксперимента на основе сопоставления цели и результатов. Необходимо выяснить, все ли операции по выполнению эксперимента были успешными.
Оценка выставляется как за общенаучные умения, такие как умения ставить цель, выдвигать гипотезу, планировать, осуществлять эксперимент, анализировать полученные результаты, делать выводы, но и за специальные умения, предусмотренные данной работой.
При организации таких занятий учащиеся оказываются в условиях, требующих от них умения планировать эксперимент, грамотно проводить наблюдения, фиксировать и описывать его результаты, обобщать и делать выводы, а также осваивать научные методы познания.
Особое значение в формировании исследовательских умений имеют задания, предусматривающие проведение мысленного эксперимента, способствующие развитию умения рассуждать. Это задания, в которых требуется получить конкретное вещество из предложенных; получить вещество несколькими способами; провести все характерные и качественные реакции, свойственные данному классу веществ; выявить генетическую связь между классами неорганических веществ.
Например, при изучении темы “Электролитическая диссоциация” традиционное экспериментальное определение электрической проводимости веществ с помощью прибора начинается с мысленного эксперимента. После этого проводим демонстрационный эксперимент. Учащиеся сравнивают и анализируют результаты, выполняют в тетрадях рисунки и схемы, записывают уравнения реакции электролитической диссоциации.
Приведем примеры заданий мысленного эксперимента.
1. В реторту насыпали порошок цинка, перекрыли газоотводную трубку зажимом, реторту взвесили и содержимое прокалили. Когда реторта остыла, ее снова взвесили. Изменилась ли масса и почему? Затем открыли зажим. Изменилась ли масса и почему?
2. На чашках весов уравновешены стаканчики с растворами гидроксида натрия и хлорида натрия. Изменит ли положение стрелка весов через некоторое время и почему?
По результатам выполнения заданий учитель может судить о готовности ученика к практическому проведению работы.
При изучении качественных реакций на ионы учащиеся приобретают умение составлять план распознавания веществ. Класс разделяется на группы каждой группе дается задание составить план определения в трех пронумерованных пробирках растворов сульфата, карбоната и хлорида натрия. Обязательные условия: наглядность, желаемые условия: быстрота и минимум затраченных реактивов. Каждая группа защищает свой план, используя ранее полученные знания, записывает молекулярные и ионные уравнения реакций. В заключении учащиеся проводят лабораторный опыт, реализуя свой план на практике.
Особую группу составляют задания эвристического и исследовательского характера . Выполняя их, учащиеся используют рассуждения как средство, получить субъективно новое знание о веществах и химических реакциях. При этом школьники осуществляют теоретические исследования, на основе которых формируют определения, находят взаимосвязи между строением и свойствами, генетическую взаимосвязь веществ, систематизируют факты и устанавливают закономерности, проводят эксперимент с целью разрешения проблемы, сформированной учителем или поставленной самостоятельно. Например, при изучении амфотерных гидроксидов можно предложить такое задание:
Будет ли одинаков результат взаимодействия растворов гидроксида натрия и хлорида алюминия при добавлении 1 ко 2 и наоборот?
При изучении темы “Обобщение основных классов неорганических веществ” предлагаем ответить на вопрос: что произойдет, если к раствору сульфата меди (II) добавить раствор гидроксида натрия, а к раствору карбоната натрия гидроксид калия. По теме “Галогены” интерес вызывают вопросы:
1.Какого цвета будет индикаторная бумажка в свежеприготовленном растворе хлора в воде?
2. Какого цвета будет индикаторная бумажка в растворе хлора, который некоторое время находился на свету?
Ответы на данные вопросы подтверждаются опытным путем.
Практика показывает, что использование творческих заданий на прогнозирование свойств веществ способствует формированию исследовательских умений, стимулирует интерес, позволяет познакомить учащихся с достижениями ученых, увидеть красивые, изящные яркие примеры работы творческой мысли.
При изучении темы “Углеводы” учащимся предлагаются вопросы:
1.Немецкий химик Христиан Шенбейн нечаянно пролил на пол смесь серной и азотной кислот. Он машинально вытер пол хлопчатобумажным фартуком своей жены. “Кислота может поджечь фартук”, - подумал Шенбейн, прополоскал фартук в воде и повесил сушить над печкой. Фартук подсох, но затем раздался негромкий взрыв и … фартук исчез. Почему произошел взрыв? (Выяснилось, что азотная кислота в смеси с хлопком - фактически той же целлюлозой - образует взрывчатое вещество, которое Шенбейн назвал пироксилином - "горючим деревом". В те годы пироксилин не смог заменить порох, поскольку был очень взрывоопасен).
Таким образом, учебное исследование является способом творческого обучения, которое спроектированное в соответствии с моделью научного исследования, позволяет построить образовательный процесс на деятельностной основе, и возможно при конструировании уроков химии.
Анализ собственного опыта и знакомство с опытом работы в этом направлении позволяет сделать некоторые педагогические выводы:
1. В исследовательскую деятельность с удовольствием и интересом включаются учащиеся разного уровня подготовленности и разного возраста, т.е. неверно утверждение о том, что это область интересов и возможностей старшеклассников и что этот вид деятельности под силу только одаренным детям. Педагоги, вовлекающие в исследовательскую деятельность учащихся разного уровня подготовленности, должны учитывать возможности ребенка, прогнозировать уровень результата, темп реализации программы исследования.
2. В ходе исследовательской деятельности развитие способностей ребенка происходит при определенных условиях:
Если тема и предмет исследовательской деятельности соответствуют потребностям ребенка;
Обучение идет в “зоне ближайшего развития и на достаточно высоком уровне трудностей”;
Если содержание деятельности опирается на “субъективный опыт ребенка”;
Если идет научение способам деятельности.
3. Обучение навыкам исследовательской работы начинается с урока, который строится по законам проведения научного исследования. Технология исследовательской деятельности ориентирована на развитие умений:
Определять цели и задачи исследования, его предмет;
Самостоятельного поиска литературы и ее конспектирования;
Анализа и систематизации информации;
Аннотировать изученные источники;
Выдвигать гипотезу, проводить в соответствии с ней практическое исследование с классификаций материала;
Описывать результаты исследования, делать выводы и обобщения.
Образованный человек в современном обществе – это не только и не столько человек, вооруженный знаниями, но умеющий добывать, приобретать знания и применять их в любой ситуации. Выпускник школы должен адаптироваться в меняющихся жизненных ситуациях, самостоятельно критически мыслить, быть коммуникабельным, контактным в различных социальных группах.
Речь идет о формировании у обучающихся современных ключевых компетенций: общенаучной, информационной, познавательной, коммуникативной, ценностно-смысловой, социальной.
Химия – одна из самых гуманистически ориентированных естественных наук: ее успехи всегда были направлены на удовлетворение потребностей человечества.
Изучение химии в школе способствует формированию мировоззрения учащихся и целостной научной картины мира, пониманию необходимости химического образования для решения повседневных жизненных проблем, воспитанию нравственного поведения в окружающей среде.
Краткое описание
Самостоятельное открытие малейшей крупицы знания учеником доставляет ему огромное удовольствие, позволяет ощутить свои возможности, возвышает его в собственных глазах. Ученик самоутверждается как личность. Эту положительную гамму эмоций школьник хранит в памяти, стремится пережить еще и еще раз. Так возникает интерес не просто к предмету, а что более ценно - к самому процессу познания - познавательный интерес.
Введение………………………………………………………………………………………………………………………………..3
О развитии исследовательской деятельности учащихся на уроках химии и во внеурочное время………………………………………………………………………………………………………………………………………4
Организация исследовательской деятельности………………………………………………………………….6
Литература…………………………………………………………………………………………………………………………….10
Прикрепленные файлы: 1 файл
Приведу примеры заданий мысленного эксперимента.
1. В реторту насыпали порошок цинка, перекрыли газоотводную трубку зажимом, реторту взвесили и содержимое прокалили. Когда реторта остыла, ее снова взвесили. Изменилась ли масса и почему? Затем открыли зажим. Изменилась ли масса и почему?
2. На чашках весов уравновешены стаканчики с растворами гидроксида натрия и хлорида натрия. Изменит ли положение стрелка весов через некоторое время и почему?
По результатам выполнения заданий учитель может судить о готовности ученика к практическому проведению работы.
При изучении качественных реакций на ионы учащиеся приобретают умение составлять план распознавания веществ.
Особую группу составляют задания эвристического и исследовательского характера. Выполняя их, учащиеся используют рассуждения как средство, получить субъективно новое знание о веществах и химических реакциях. При этом школьники осуществляют теоретические исследования, на основе которых формируют определения, находят взаимосвязи между строением и свойствами, генетическую взаимосвязь веществ, систематизируют факты и устанавливают закономерности, проводят эксперимент с целью разрешения проблемы, сформированной учителем или поставленной самостоятельно.
Например, при изучении амфотерных гидроксидов можно предложить такое задание:
Будет ли одинаков результат взаимодействия растворов гидроксида натрия и хлорида алюминия при добавлении 1 ко 2 и наоборот?
При изучении темы “Обобщение основных классов неорганических веществ” предлагаем ответить на вопрос: что произойдет, если к раствору сульфата меди (II) добавить раствор гидроксида натрия, а к раствору карбоната натрия гидроксид калия.
Практика показывает, что использование творческих заданий на прогнозирование свойств веществ. Такие задания способствуют формированию исследовательских умений, стимулируют интерес, позволяют познакомить учащихся с достижениями ученых, увидеть красивые, изящные яркие примеры работы творческой мысли.
При изучении темы “Углеводы” учащимся предлагают вопросы:
1.Немецкий химик Христиан Шенбейн нечаянно пролил на пол смесь серной и азотной кислот. Он машинально вытер пол хлопчатобумажным фартуком своей жены. “Кислота может поджечь фартук”, - подумал Шенбейн, прополоскал фартук в воде и повесил сушить над печкой. Фартук подсох, но затем раздался негромкий взрыв и … фартук исчез. Почему произошел взрыв?
2.Что произойдет, если долго жевать хлебный мякиш?
Уроки-исследования требуют большой подготовки, которая, как показывает практика, себя оправдывает. Такие уроки строятся в соответствии с логикой деятельностного подхода и включают следующие этапы: мотивационно-ориентировочный, операционно-исполнительский (анализ, прогнозирование и эксперимент) , оценочно-рефлексивный.
Таким образом, учебное исследование является способом творческого обучения, которое спроектированное в соответствии с моделью научного исследования, позволяет построить образовательный процесс на деятельностной основе, и возможно при конструировании уроков химии.
Литература
1.Батаева Е.Н. Формирование исследовательских умений. Ж, Химия: методика обучения. 8.2003-1.2004
2.Емельянова Е.О., Иодко А.Г. Организация познавательной деятельности учащихся на уроках химии в 8-9 классах. М.: Школьная Пресса, 2002.
3.Методические журналы «Химия в школе», «Биология в школе»
4.Степин Б.Д. Занимательные задания и эффективные опыты по химии. М.: Дрофа, 2002.
5.Увлекательный мир химических превращений: Оригинальные задачи с решениями / А.С.Суворов и др. Химия, 1998
§ 14. Закон сохранения массы веществ
Вещества вступают в химические реакции, в результате которых образуются другие вещества. Происходят ли какие-либо изменения с массой вещества в результате реакции? По этому вопросу ученые высказывали различные предположения.
Знаменитый английский химик Р. Бойль, прокаливая в открытой реторте различные металлы и взвешивая их до и после нагревания, обнаружил, что масса металлов становится больше. Основываясь на этих опытах, он не учитывал роль воздуха и сделал неправильный вывод, что масса веществ в результате химических реакций изменяется. Р. Бойль утверждал, что существует какая-то «огненная материя», которая в случае нагревания металла соединяется с металлом, увеличивая массу.
М. В. Ломоносов в отличие от Р. Бойля прокаливал металлы не на открытом воздухе, а в запаянных ретортах и взвешивал их до и после прокаливания. (Реторта с жаровней изображены на рис. 35, см. с. 54.) Он доказал, что масса веществ до и после реакции остается без изменения и что при прокаливании к металлу присоединяется какая-то часть воздуха. (Кислород в то время не был еще открыт.) Результаты этих опытов он сформулировал в виде закона: «Все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимается, столько присовокупится к другому». В настоящее время этот закон формулируется так:
Масса веществ, вступивших в химическую реакцию, равна массе образовавшихся веществ
.
Значительно позже (1789) закон сохранения массы был независимо от М. В. Ломоносова установлен французским химиком А. Лавуазье (с. 55).
Подтвердить правильность закона сохранения массы веществ можно и на простом опыте. В колбу (рис. 16) помещают немного красного фосфора, закрывают пробкой и взвешивают на весах (а). Затем колбу с фосфором (б) осторожно нагревают. О том, что произошла химическая реакция, судят по появлению в колбе белого дыма, состоящего из частиц оксида фосфора (V). При вторичном взвешивании убеждаются, что в результате реакции масса веществ не изменилась (в).
С точки зрения атомно-молекулярного учения закон сохранения массы объясняется так: в результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка.
Так как число атомов до реакции и после остается неизменным, то их общая масса также не изменяется.
Значение закона сохранения массы веществ.
1. Открытие закона сохранения массы веществ способствовало дальнейшему развитию химии как науки.
2. На основании закона сохранения массы веществ производят практически важные расчеты. Например, можно вычислить, сколько потребуется исходных веществ, чтобы получить сульфид железа (II) массой 44 кг, если железо и сера вступают в реакцию в массовых отношениях 7:4. Согласно закону сохранения массы веществ при взаимодействии железа массой 7 кг и серы массой 4 кг образуется сульфид железа (II) массой 11 кг. А так как необходимо получить сульфид железа (II) массой 44 кг, т. е. в 4 раза больше, то и исходных веществ также потребуется в 4 раза больше: 28 кг железа (7-4) и 16 кг серы (4-4).
3. На основе закона сохранения массы веществ составляют уравнения химических реакций.
Ответьте на вопросы 1-3 (с. 42).
§15. Химические уравнения
Химическим уравнением называют условную запись химической реакции посредством химических знаков и формул.
По химическому уравнению реакций можно судить о том, какие вещества вступают в реакцию и какие образуются. При составлении уравнений реакций поступают следующим образом:
1. В левой части уравнения пишут формулы веществ, вступающих в реакцию, а затем ставят стрелку. При этом нужно помнить, что молекулы простых газообразных веществ почти всегда состоят из двух атомов (О 2 , Н 2 , С1 2 и т. д.):
2. В правой части (после стрелки) пишут формулы веществ, образующихся в результате реакции:
3. Уравнение реакции составляют на основе закона сохранения массы веществ, т. е. слева и справа должно быть одинаковое число атомов. Это достигается расстановкой коэффициентов перед формулами веществ. Вначале уравнивают число атомов, которых в реагирующих веществах содержится больше. В наших примерах это атомы кислорода. Находят наименьшее общее кратное чисел атомов кислорода в левой и правой частях записи от стрелки. В реакции магния с кислородом наименьшим общим кратным является число 2, а в примере с фосфором - число 10. При делении наименьшего общего кратного на число соответствующих атомов (в приведенных примерах - на число атомов кислорода) в левой и в правой частях записи от стрелки находят соответствующие коэффициенты, как показано на следующей схеме:
Уравнивают число атомов остальных химических элементов. В наших примерах следует уравнять число атомов магния и фосфора:
В тех случаях, когда при составлении химических уравнений тепловые эффекты реакций не указывают, вместо знака равенства ставят стрелку.
§ 16. Типы химических реакций
Химические реакции
можно подразделить на четыре основных типа: 1)
разложения;
2)
соединения;
3)
замещения;
4)
обмена
(с. 82).
С реакцией разложения вы познакомились на примере разложения воды (с. 13). Реакция соединения вам известна из примера взаимодействия серы с железом (с. 15).
Чтобы познакомиться с реакцией замещения, можно выполнить следующий опыт. В голубой раствор хлорида меди (II) СuС1 2 опускают очищенный железный гвоздь (или железные опилки). Гвоздь (опилки) тотчас покрывается налетом меди, а раствор из голубого становится зеленоватым, так как вместо хлорида меди (II) СuС1 2 образуется хлорид железа (II) FeCl 2 . Происходящую химическую реакцию выражают химическим уравнением
Fe + CuCl 2 ->Cu + FeCl 2
При сравнении рассмотренных выше химических реакций можно дать им определения и выявить их особенности (схема 6).
1 С реакциями обмена вы познакомитесь в дальнейшем курсе химии (с. 82).
2 Для того чтобы началась реакция, во многих случаях требуется нагревание. Тогда в уравнениях реакций над стрелкой ставят знак t.
3 Если в результате реакции выделяется газ, рядом с его формулой ставят стрелку Beepx , а если вещество выпадает в осадок, то рядом с формулой этого вещества ставят стрелку вниз.
Выполните упражнения 5-7 (с. 42-43).
1. Кем, когда и как был открыт закон сохранения массы? Приведите формулировку закона и объясните его с точки зрения атомно-молекулярного учения.
2. В реторту (рис. 35) насыпали порошок цинка, закрыли газоотводную трубку зажимом, реторту взвесили и содержимое прокалили. Когда реторта остыла, ее вновь взвесили. Изменилась ли ее масса и почему? Затем открыли зажим. Остались ли чашки весов в равновесии и почему?
3. Какое теоретическое и практическое значение имеет закон сохранения массы веществ? Приведите примеры.
4. Придерживаясь последовательности, ранее приведенной (см. с. 35), и учитывая валентность элементов, составьте уравнения реакций по следующим схемам:
5. Напишите по два уравнения реакций каждого из известных вам типов и объясните их сущность с точки зрения атомно-молекулярного учения.
6. Даны металлы: кальций Са, алюминий AI , литий Li . Составьте уравнения химических реакций этих металлов с кислородом, хлором и серой, если известно, что сера в соединениях с металлами и водородом двухвалентна.
7. Перепишите приведенные ниже схемы уравнений реакций, вместо знаков вопроса напишите формулы соответствующих веществ, расставьте коэффициенты и поясните, к какому типу относится каждая из указанных реакций:
Новости и события
Москиты теряют чувствительность по отношению к репеллентам и инсектицидам. Ученые выяснили, что насекомые определяют токсичные яды через свои конечности. Специалисты Ливерпульской школы тропичес...
Австралийские фермеры радуются падению цен на моноаммонийфосфат и диаммонийфосфат, проявившееся в последние недели, но считают, что не имеет достоверной информации о них и возможно периодически...
Компания Huhtamaki (Финляндия, www.huhtamaki.com), являющаяся одним из крупнейших европейских поставщиков упаковки для пищевых продуктов и напитков, ввела в строй новую линию в городе Ивантеевка...
Личинки мучного жука, обладающие уникальной способностью поедать разные формы пластика и при этом оставаться безопасным кормом для других животных, могут помочь решить проблему пластикового мусо...
Если Санта станет спускаться по трубе, поможет ли ему огнезащитный костюм? Американское химическое общество проанализировало химический состав антипиренов.
О чём речь?
В переработку пойдут даже бумажные стаканчики, которые раньше в России не перерабатывались
Посетителям сети ресторанов быстрого питания предлагают выбрасывать бумажную упаковку в спец...
Информация
Комара не убить репеллентами: насекомые чувствуют яд через свои конечности
В Австралии дешевеют фосфорные удобрения
Huhtamaki расширяет производство упаковки в России
Каталог организаций и предприятий
с добавленной стоимостью, включая оксид цинка, цинковый порошок и цинк в металле.
Yunnan Luoping Zinc and Electricity Co., Ltd. преимущественно занимается производством цветных металлов, в основном свинца и цинка, а также выработкой гидроэлектроэнергии. Основная продукция компании - цинковые слитки, цинковый порошок , цинковые сплавы...
"АРСЕНАЛ" - динамично развивающаяся компания, которая является крупным оператором на рынке цветных металлов и сплавов Украины. Предприятие специализируется на сплавах на основе цинка, олова, свинца, меди никеля (чушка, прокат, анод, проволока, порошок )...
 Воля: функции, понятие, основные признаки
Воля: функции, понятие, основные признаки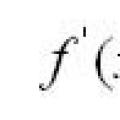 Геометрический и механический смысл производной
Геометрический и механический смысл производной Свойства степеней при сложении
Свойства степеней при сложении