Tính chất hữu ích và ứng dụng của thủy ngân. Sao Thủy: sự thật thú vị
Tất cả các nguyên tố hóa học của bảng tuần hoàn đều được chia theo đường chéo B - At thành kim loại và phi kim. Đồng thời, những cái sau thuộc thiểu số, nằm ở phía trên và bên phải biên giới. Mặt khác, kim loại có lợi thế rõ ràng về số lượng; trong số 118 nguyên tố đã biết, có hơn 80 nguyên tố.
Tất cả chúng đều có tính chất vật lý tương tự nhau, được thống nhất bởi trạng thái tập hợp. Tuy nhiên, có một ngoại lệ - nguyên tố thủy ngân. Hãy nói về nó chi tiết hơn.
Sao Thủy: vị trí trong hệ thống tuần hoàn
Phần tử này chiếm ô của nó trong bảng ở số 80. Đồng thời, nó nằm trong nhóm thứ hai, nhóm phụ thứ cấp, chu kỳ lớn thứ sáu. Nó có khối lượng nguyên tử là 200,59. Nó tồn tại ở dạng bảy đồng vị ổn định: 196, 198, 199, 200, 201, 202, 204.
Đề cập đến các phần tử của họ d, nhưng không chuyển tiếp, vì phần tử sau lấp đầy quỹ đạo s. Thủy ngân là thành viên của phân nhóm kim loại kẽm, cùng với cadmium và copernicium.
Đặc điểm chung của nguyên tố
Các nguyên tố hóa học trong bảng tuần hoàn có sự sắp xếp theo thứ tự chặt chẽ và mỗi nguyên tố có cấu hình điện tử nguyên tử riêng, nói lên tính chất của nó. Sao Thủy cũng không ngoại lệ. Cấu trúc của lớp vỏ electron ngoài cùng và trước lớp ngoài cùng của nó như sau: 5s 2 5p 6 5d 10 6s 2 .
Các trạng thái oxi hóa có thể: +1, +2. Thủy ngân oxit và hydroxit là các hợp chất cơ bản yếu, đôi khi lưỡng tính. #80 - Hg, cách phát âm tiếng Latinh của "hydrargyrum". Tên tiếng Nga bắt nguồn từ ngôn ngữ Proto-Slavic, trong đó nó được dịch là "cuộn". Các quốc gia khác có cách phát âm và tên khác nhau. Thông thường, bản thân nguyên tố này và các chất đơn giản và phức tạp do nó tạo thành được gọi là thủy ngân, thủy ngân. Tên này xuất phát từ thời cổ đại, khi họ so sánh Hg (nguyên tố) với bạc, đã cho nó ý nghĩa thứ hai sau vàng. Mặt trời là biểu tượng của aurum Au, Thủy tinh là biểu tượng của hydrargyrum Hg.
Các dân tộc cổ đại tin rằng có bảy kim loại cơ bản, trong đó có thủy ngân. Một nhóm trong số chúng được phản ánh trong Đó là, vàng được liên kết với Mặt trời, sắt với Sao Hỏa, thủy ngân với Sao Thủy, v.v.
Lịch sử khám phá
Thủy ngân đã được biết đến cách đây khoảng 1500 năm, thậm chí sau đó nó được mô tả là "bạc lỏng", một kim loại di động, khác thường và bí ẩn. Họ cũng đã học cách trích xuất nó từ thời cổ đại.
Tất nhiên, không thể nghiên cứu các tính chất của nó, bởi vì hóa học như vậy vẫn chưa được hình thành. Thủy ngân được bao phủ trong một bức màn bí ẩn và ma thuật, được coi là một chất khác thường, gần giống với bạc và có khả năng biến thành vàng nếu được làm rắn. Tuy nhiên, không có cách nào để thu được thủy ngân nguyên chất ở trạng thái kết tụ rắn, và nghiên cứu giả kim thuật đã không thành công.
Các quốc gia chính nơi thủy ngân đã được sử dụng và khai thác từ thời cổ đại là:
- Trung Quốc;
- Lưỡng Hà;
- Ấn Độ;
- Ai Cập.
Tuy nhiên, chỉ có thể thu được kim loại này ở dạng nguyên chất vào thế kỷ 18, điều này được thực hiện bởi nhà hóa học Thụy Điển Brandt. Đồng thời, cả anh ta và cho đến thời điểm này đều không được cung cấp bằng chứng về tính kim loại của chất này. Vấn đề này đã được làm rõ bởi M. V. Lomonosov và Brown. Chính những nhà khoa học này là những người đầu tiên đóng băng thủy ngân và do đó xác nhận rằng nó được đặc trưng bởi tất cả các tính chất của kim loại - độ sáng, độ dẫn điện, độ dẻo và độ dẻo, ánh kim.
Cho đến nay, nhiều hợp chất thủy ngân đã được thu được, nó được sử dụng trong các lĩnh vực sản xuất kỹ thuật khác nhau.
chất thủy ngân
Là chất đơn giản, là chất lỏng (ở điều kiện thường) màu trắng bạc, di động, dễ bay hơi. Một ví dụ điển hình mà thủy ngân lỏng tinh khiết được sử dụng là để đo nhiệt độ.
Nếu bạn chuyển thủy ngân sang trạng thái rắn, thì nó sẽ là một tinh thể trong mờ không có mùi. Hơi của chất này không màu và có độc tính cao.
Tính chất vật lý
Theo tính chất vật lý của nó, kim loại này là đại diện duy nhất, trong điều kiện bình thường, có thể tồn tại ở dạng chất lỏng. Đối với tất cả các thuộc tính khác, nó hoàn toàn phù hợp với các đặc điểm chung của các đại diện khác của danh mục.
Các thuộc tính chính như sau.
- Trạng thái tổng hợp: điều kiện bình thường - chất lỏng, tinh thể rắn - không cao hơn 352 ° C, hơi - trên 79 K.
- Hòa tan trong benzen, dioxan, tinh thể trong nước. Sở hữu khả năng không làm ướt kính.
- Nó có tính chất nghịch từ.
- dẫn nhiệt.
Sự nóng chảy của thủy ngân xảy ra ở nhiệt độ âm -38,83 o C. Do đó, chất này thuộc nhóm chất nổ khi đun nóng. Trong trường hợp này, dự trữ năng lượng bên trong của hợp chất tăng lên nhiều lần.
Sự sôi của thủy ngân bắt đầu ở nhiệt độ 356,73 o C. Tại thời điểm này, nó bắt đầu chuyển sang trạng thái hơi, đó là các phân tử hoàn toàn không thể nhìn thấy bằng mắt thường, được kết nối với nhau.
Điểm nóng chảy của thủy ngân cho thấy tính chất của kim loại này rõ ràng là khác thường. Chất này bắt đầu bay hơi, biến thành các phân tử vô hình ở trạng thái khí, ở nhiệt độ phòng bình thường, khiến nó đặc biệt nguy hiểm đối với sức khỏe con người và động vật.
Tính chất hóa học
Các nhóm hợp chất dựa trên thủy ngân sau đây ở các trạng thái oxy hóa khác nhau đã được biết đến:
- sunfat, sunfua;
- clorua;
- nitrat;
- hydroxit;
- oxit;
- hợp chất phức tạp;
- chất hữu cơ kim loại;
- liên kim loại;
- hợp kim với các kim loại khác - hỗn hống.
Điểm nóng chảy của thủy ngân cho phép nó tạo thành cả hỗn hống lỏng và rắn. Trong các hợp kim như vậy, kim loại mất hoạt tính, trở nên trơ hơn.
Phản ứng tương tác của thủy ngân với oxy chỉ có thể xảy ra ở nhiệt độ đủ cao, mặc dù khả năng oxy hóa mạnh của phi kim loại. Trong điều kiện trên 380 ° C, là kết quả của quá trình tổng hợp như vậy, một oxit kim loại được hình thành với trạng thái oxy hóa của +2 sau này.
Với axit, kiềm, phi kim ở dạng tự do, kim loại không tham gia tương tác hóa học, tồn tại ở trạng thái lỏng.
Nó phản ứng với các halogen khá chậm và chỉ khi lạnh, điều này được xác nhận bởi điểm nóng chảy của thủy ngân. Kali permanganat là một chất oxy hóa tốt cho nó.
ở trong tự nhiên
Chứa trong vỏ trái đất, đại dương, quặng và khoáng sản. Nếu chúng ta nói về tổng tỷ lệ phần trăm thủy ngân trong lòng trái đất, thì con số này xấp xỉ 0,000001%. Nói chung, chúng ta có thể nói rằng yếu tố này bị phân tán. Các khoáng chất và quặng chính, bao gồm kim loại này, như sau:
- chu sa;
- thạch anh;
- đá vôi;
- mica;
- cacbonat;
- quặng chì kẽm.
Trong tự nhiên, thủy ngân luôn quay vòng và tham gia vào quá trình trao đổi chất của tất cả các vỏ Trái đất.
Bắt thủy ngân
Phương pháp thứ hai dựa trên việc chiết thủy ngân cũng từ sunfua bằng cách sử dụng chất khử mạnh. Chẳng hạn như sắt. Việc thu thập sản phẩm được thực hiện theo cách tương tự như trong trường hợp trước.
Tác động sinh học lên cơ thể sống
Nhiệt độ của thủy ngân cần phải đủ thấp để chuyển sang trạng thái hơi. Quá trình này đã bắt đầu ở 25 ° C, tức là ở nhiệt độ phòng bình thường. Trong trường hợp này, sự hiện diện của các sinh vật sống trong phòng trở nên nguy hiểm cho sức khỏe.
Vì vậy, kim loại có thể xâm nhập vào các sinh vật thông qua:
- da, nguyên vẹn, hoàn toàn nguyên vẹn;
- niêm mạc;
- Hàng không;
- cơ quan tiêu hóa.
Khi vào bên trong, hơi thủy ngân được đưa vào vòng tuần hoàn chung, sau đó đi vào quá trình tổng hợp protein và các phân tử khác, tạo thành các hợp chất với chúng. Đây là cách kim loại có hại tích tụ trong gan và xương. Từ những nơi lưu trữ, kim loại lại có thể được đưa vào các quá trình trao đổi chất, tổng hợp và phân rã, gây ra tình trạng nhiễm độc chậm cho cơ thể, kèm theo những hậu quả nghiêm trọng nhất.
Nó được bài tiết ra khỏi các cơ quan khá chậm và dưới tác dụng của các chất xúc tác, chất hấp phụ. Ví dụ như sữa. Các chất lỏng chính mà kim loại được giải phóng vào môi trường:
- nước bọt;
- mật;
- nước tiểu;
- sản phẩm của đường tiêu hóa.
Có hai dạng ngộ độc chính với chất này: cấp tính và mãn tính. Mỗi loại có những đặc điểm và biểu hiện riêng.
Triệu chứng và điều trị
Dạng cấp tính là điển hình cho các trường hợp tràn thủy ngân xảy ra trong các ngành công nghiệp, nghĩa là khi một lượng lớn chất thải vào khí quyển xảy ra tại một thời điểm. Trong những tình huống như vậy, ở những người không được bảo vệ, tình trạng sức khỏe suy giảm nghiêm trọng bắt đầu, đó là ngộ độc. Các triệu chứng như sau:
- Các cơ quan hô hấp, phổi, niêm mạc miệng và cổ họng bị viêm.
- Nhiệt độ cơ thể tăng lên.
- Các vết loét hình thành trên nướu, chúng chảy máu, sưng tấy và trở nên cực kỳ nhạy cảm. Đôi khi một đường viền thủy ngân được hình thành.
- Có teo gan và thận.
- Ớn lạnh, buồn nôn và nôn, chóng mặt.
- Hệ thống thần kinh bị ảnh hưởng rất nhiều - lời nói và sự phối hợp của các cử động bị rối loạn, các chi bị run.
- Ngộ độc đi kèm với đau đầu và tiêu chảy có lẫn máu.
Nếu tổn thương do hơi thủy ngân xảy ra dần dần thì bệnh sẽ trở thành mãn tính. Trong trường hợp này, các biểu hiện sẽ không quá rõ ràng, nhưng tình trạng sức khỏe xấu đi sẽ tích tụ hàng ngày, ngày càng có đà lan rộng.
- Run tay chân.
- Các bệnh về khoang miệng (viêm nướu, viêm miệng và những bệnh khác).
- Tăng huyết áp và nhịp tim nhanh.
- đổ mồ hôi.
- Thần kinh hưng phấn.
- Đau đầu.
- Trong những trường hợp nghiêm trọng, rối loạn tâm thần nghiêm trọng có thể bị kích động, dẫn đến tâm thần phân liệt.
Tất cả những hậu quả này có thể xảy ra ngay cả khi giải phóng một lượng nhỏ thủy ngân vào khí quyển. Nếu bạn không khử trùng cơ sở kịp thời, thì bạn có thể gây hại rất nhiều cho sức khỏe của mình.
Điều trị trong những trường hợp này thường được thực hiện bằng các loại thuốc sau:
- vitamin;
- thuốc kháng histamin;
- thuốc an thần;
- "Aminazin".
con người sử dụng
Nơi phổ biến nhất để sử dụng và lưu trữ thủy ngân kim loại là nhiệt kế và nhiệt kế. Một thiết bị như vậy có thể chứa tới 3 g kim loại. Ngoài ra, có một số lĩnh vực hoạt động khác của con người trong đó thủy ngân được sử dụng rộng rãi:
- thuốc (calomel, mercusal, promeran, nhiều chất sát trùng);
- hoạt động kỹ thuật - nguồn hiện tại, đèn sợi đốt, máy bơm, phong vũ biểu, kíp nổ, v.v.;
- luyện kim - phun gương, trang trí bằng hỗn hống vàng và bạc, thu được hợp kim kim loại, chất tinh khiết;
- công nghiệp hóa chất;
- Nông nghiệp.
Hiện nay, do việc sản xuất các chất an toàn và tiện lợi hơn, thủy ngân đã được loại bỏ khỏi y học trên thực tế.
Giữa làng Karagash và thành phố Slobodzeya, một kênh truyền hình địa phương đưa tin hôm thứ Sáu, trích dẫn Bộ An ninh Nhà nước (MGB) của nước cộng hòa không được công nhận.
(Hg) - một nguyên tố hóa học thuộc nhóm II của hệ thống định kỳ Mendeleev, số nguyên tử 80, khối lượng nguyên tử 200,59; kim loại nặng màu trắng bạc, lỏng ở nhiệt độ phòng.
Thủy ngân là một trong bảy kim loại được biết đến từ thời cổ đại. Mặc dù thực tế là thủy ngân thuộc về các nguyên tố vi lượng và rất khan hiếm trong tự nhiên (tương đương với bạc), nhưng nó tồn tại ở trạng thái tự do dưới dạng thể vùi trong đá.
Ngoài ra, nó rất dễ bị cô lập trong quá trình nung từ khoáng chất chính - sunfua (cinnabar). Hơi thủy ngân dễ dàng ngưng tụ thành chất lỏng sáng bóng như bạc. Mật độ của nó cao đến mức (13,6 g/cu. cm) đến mức một người bình thường thậm chí không thể nhấc một xô thủy ngân lên khỏi sàn.
Thủy ngân được sử dụng rộng rãi trong sản xuất các dụng cụ khoa học (phong vũ biểu, nhiệt kế, áp kế, bơm chân không, nguyên tố bình thường, máy đo cực, điện kế mao quản, v.v.), trong đèn thủy ngân, công tắc, bộ chỉnh lưu; làm cực âm lỏng trong sản xuất kiềm ăn da và clo bằng điện phân, làm chất xúc tác trong quá trình tổng hợp axit axetic, trong luyện kim để tạo hỗn hợp vàng và bạc, trong sản xuất chất nổ; trong y học (calomel, thăng hoa, organomercury và các hợp chất khác), như một sắc tố (cinnabar), trong nông nghiệp như một loại hạt giống và thuốc diệt cỏ, và cũng như một thành phần sơn của tàu (để chống lại sự bám bẩn của sinh vật).
Ở nhà, thủy ngân có thể có trong chuông cửa, đèn huỳnh quang, nhiệt kế y tế.
Thủy ngân kim loại có độc tính cao đối với mọi dạng sống. Mối nguy hiểm chính là hơi thủy ngân, sự giải phóng hơi thủy ngân từ các bề mặt mở tăng lên khi nhiệt độ không khí tăng. Khi hít vào, thủy ngân đi vào máu. Trong cơ thể, thủy ngân lưu thông trong máu, kết hợp với protein; lắng đọng một phần ở gan, thận, lá lách, mô não, v.v.
Tác dụng độc hại có liên quan đến việc ngăn chặn các nhóm sulfhydryl của protein mô, làm suy yếu hoạt động của não (chủ yếu là vùng dưới đồi). Thủy ngân được đào thải ra khỏi cơ thể qua thận, ruột, tuyến mồ hôi, v.v.
Ngộ độc cấp tính với thủy ngân và hơi của nó rất hiếm. Trong ngộ độc mãn tính, cảm xúc không ổn định, khó chịu, giảm hiệu suất, rối loạn giấc ngủ, run ngón tay, giảm khứu giác và đau đầu. Một dấu hiệu ngộ độc đặc trưng là sự xuất hiện của đường viền màu xanh đen dọc theo mép nướu; bệnh nướu răng (loãng, chảy máu) có thể dẫn đến viêm nướu và viêm miệng.
Trong trường hợp ngộ độc với các hợp chất hữu cơ của thủy ngân (diethylmercury phosphate, diethylmercury, ethylmercuric chloride), dấu hiệu tổn thương đồng thời hệ thần kinh trung ương (viêm não-đa dây thần kinh) và hệ tim mạch, dạ dày, gan và thận chiếm ưu thế.
Biện pháp phòng ngừa chính khi làm việc với thủy ngân và các hợp chất của nó là ngăn không cho thủy ngân xâm nhập vào cơ thể qua đường hô hấp hoặc bề mặt da.
Thủy ngân tràn ra trong nhà phải được thu gom hết sức cẩn thận. Đặc biệt là rất nhiều hơi được hình thành nếu thủy ngân vỡ vụn thành nhiều giọt nhỏ li ti bám vào các vết nứt khác nhau, chẳng hạn như giữa các viên gạch lát sàn. Tất cả những giọt này phải được thu thập.
Điều này được thực hiện tốt nhất với lá thiếc, mà thủy ngân dễ dàng bám vào, hoặc với dây đồng được rửa bằng axit nitric. Và những nơi mà thủy ngân vẫn có thể đọng lại được đổ bằng dung dịch sắt clorua 20%. Một biện pháp phòng ngừa tốt chống ngộ độc hơi thủy ngân là cẩn thận và thường xuyên, trong nhiều tuần hoặc thậm chí nhiều tháng, thông gió cho căn phòng nơi thủy ngân bị đổ.
Hậu quả môi trường của ô nhiễm hơi thủy ngân thể hiện chủ yếu trong môi trường nước - hoạt động sống của tảo và cá đơn bào bị ức chế, quá trình quang hợp bị rối loạn, nitrat, phốt phát, hợp chất amoni, v.v. sự lão hóa của thực vật.
Khoáng chất, thủy ngân kim loại tự nhiên. Một kim loại chuyển tiếp là một chất lỏng nặng, màu trắng bạc ở nhiệt độ phòng, hơi của chúng cực kỳ độc hại. Thủy ngân là một trong hai nguyên tố hóa học (và là kim loại duy nhất) có các chất đơn giản ở điều kiện bình thường ở trạng thái kết tụ lỏng (nguyên tố thứ hai là brom). Đôi khi chứa một hỗn hợp bạc và vàng.
Xem thêm:
KẾT CẤU
Syngony là tam giác, lục giác-thang đo (dưới -39°C).CỦA CẢI
 Màu thiếc trắng. Ánh kim loại mạnh mẽ. Điểm sôi 357 °C. Khoáng chất lỏng duy nhất ở nhiệt độ bình thường. Cứng lại, thu được trạng thái kết tinh ở −38°C. Tỷ trọng 13,55. Khi cháy, nó dễ dàng bay hơi với sự hình thành khói độc. Vào thời cổ đại, hít phải những hơi này là phương pháp điều trị duy nhất đối với bệnh giang mai (theo nguyên tắc: nếu bệnh nhân không chết thì sẽ khỏi bệnh. Đó là một diamagnet.
Màu thiếc trắng. Ánh kim loại mạnh mẽ. Điểm sôi 357 °C. Khoáng chất lỏng duy nhất ở nhiệt độ bình thường. Cứng lại, thu được trạng thái kết tinh ở −38°C. Tỷ trọng 13,55. Khi cháy, nó dễ dàng bay hơi với sự hình thành khói độc. Vào thời cổ đại, hít phải những hơi này là phương pháp điều trị duy nhất đối với bệnh giang mai (theo nguyên tắc: nếu bệnh nhân không chết thì sẽ khỏi bệnh. Đó là một diamagnet.
DỰ TRỮ VÀ SẢN XUẤT
 Thủy ngân là một nguyên tố tương đối hiếm trong vỏ trái đất với nồng độ trung bình là 83 mg/t. Tuy nhiên, do thủy ngân liên kết yếu về mặt hóa học với các nguyên tố phổ biến nhất trong vỏ trái đất nên quặng thủy ngân có thể rất đậm đặc so với đá thông thường. Các quặng giàu thủy ngân nhất chứa tới 2,5% thủy ngân. Dạng chính của thủy ngân được tìm thấy trong tự nhiên là phân tán và chỉ 0,02% trong số đó được tìm thấy trong trầm tích. Hàm lượng thủy ngân trong các loại đá mácma gần nhau (khoảng 100 mg/t). Từ đá trầm tích, nồng độ thủy ngân tối đa được thiết lập trong đá phiến sét (lên tới 200 mg/t). Trong vùng biển của Đại dương Thế giới, hàm lượng thủy ngân là 0,1 µg/l. Đặc điểm địa hóa quan trọng nhất của thủy ngân là, trong số các nguyên tố chalcophile khác, nó có khả năng ion hóa cao nhất. Điều này xác định các tính chất như vậy của thủy ngân như khả năng phục hồi về dạng nguyên tử (thủy ngân tự nhiên), khả năng kháng hóa chất đáng kể đối với oxy và axit.
Thủy ngân là một nguyên tố tương đối hiếm trong vỏ trái đất với nồng độ trung bình là 83 mg/t. Tuy nhiên, do thủy ngân liên kết yếu về mặt hóa học với các nguyên tố phổ biến nhất trong vỏ trái đất nên quặng thủy ngân có thể rất đậm đặc so với đá thông thường. Các quặng giàu thủy ngân nhất chứa tới 2,5% thủy ngân. Dạng chính của thủy ngân được tìm thấy trong tự nhiên là phân tán và chỉ 0,02% trong số đó được tìm thấy trong trầm tích. Hàm lượng thủy ngân trong các loại đá mácma gần nhau (khoảng 100 mg/t). Từ đá trầm tích, nồng độ thủy ngân tối đa được thiết lập trong đá phiến sét (lên tới 200 mg/t). Trong vùng biển của Đại dương Thế giới, hàm lượng thủy ngân là 0,1 µg/l. Đặc điểm địa hóa quan trọng nhất của thủy ngân là, trong số các nguyên tố chalcophile khác, nó có khả năng ion hóa cao nhất. Điều này xác định các tính chất như vậy của thủy ngân như khả năng phục hồi về dạng nguyên tử (thủy ngân tự nhiên), khả năng kháng hóa chất đáng kể đối với oxy và axit.
Một trong những mỏ thủy ngân lớn nhất thế giới nằm ở Tây Ban Nha (Almaden). Tiền gửi thủy ngân được biết đến ở Kavkaz (Dagestan, Armenia), ở Tajikistan, Slovenia, Kyrgyzstan (Khaidarkan - Aidarken) Ukraine (nhà máy thủy ngân Gorlovka, Nikitovsky).
Có 23 mỏ thủy ngân ở Nga, trữ lượng công nghiệp lên tới 15,6 nghìn tấn (tính đến năm 2002), trong đó mỏ lớn nhất được thăm dò ở Chukotka - Zapadno-Palyanskoye và Tamvatneyskoye.
Thủy ngân thu được bằng cách nung chu sa (thủy ngân(II) sulfua) hoặc bằng phương pháp nhiệt luyện kim loại. Hơi thủy ngân được ngưng tụ và thu thập. Phương pháp này được sử dụng bởi các nhà giả kim cổ đại.
NGUỒN GỐC
 Thủy ngân có mặt trong hầu hết các khoáng chất sunfua. Hàm lượng đặc biệt cao của nó (lên đến phần nghìn và phần trăm phần trăm) được tìm thấy trong quặng bạc màu, antimonit, sphalerit và thạch thực. Khoảng cách gần nhau về bán kính ion của thủy ngân hóa trị hai và canxi, thủy ngân hóa trị một và bari quyết định tính đồng hình của chúng trong fluorit và barit. Trong chu sa và metacinnabarit, lưu huỳnh đôi khi được thay thế bằng selen hoặc telua; hàm lượng selen thường là phần trăm và phần mười của phần trăm. Selenua thủy ngân cực hiếm được biết đến - timanite (HgSe) và onophrite (hỗn hợp của timanite và sphalerite).
Thủy ngân có mặt trong hầu hết các khoáng chất sunfua. Hàm lượng đặc biệt cao của nó (lên đến phần nghìn và phần trăm phần trăm) được tìm thấy trong quặng bạc màu, antimonit, sphalerit và thạch thực. Khoảng cách gần nhau về bán kính ion của thủy ngân hóa trị hai và canxi, thủy ngân hóa trị một và bari quyết định tính đồng hình của chúng trong fluorit và barit. Trong chu sa và metacinnabarit, lưu huỳnh đôi khi được thay thế bằng selen hoặc telua; hàm lượng selen thường là phần trăm và phần mười của phần trăm. Selenua thủy ngân cực hiếm được biết đến - timanite (HgSe) và onophrite (hỗn hợp của timanite và sphalerite).
ĐĂNG KÍ
 Thủy ngân được sử dụng làm chất lỏng làm việc trong nhiệt kế thủy ngân (đặc biệt là nhiệt kế có độ chính xác cao), vì nó có phạm vi khá rộng khi nó ở trạng thái lỏng, hệ số giãn nở nhiệt của nó gần như không phụ thuộc vào nhiệt độ và có khả năng tỏa nhiệt tương đối thấp . Một hợp kim thủy ngân với tali được sử dụng cho nhiệt kế nhiệt độ thấp.
Thủy ngân được sử dụng làm chất lỏng làm việc trong nhiệt kế thủy ngân (đặc biệt là nhiệt kế có độ chính xác cao), vì nó có phạm vi khá rộng khi nó ở trạng thái lỏng, hệ số giãn nở nhiệt của nó gần như không phụ thuộc vào nhiệt độ và có khả năng tỏa nhiệt tương đối thấp . Một hợp kim thủy ngân với tali được sử dụng cho nhiệt kế nhiệt độ thấp.
Đèn huỳnh quang chứa đầy hơi thủy ngân, khi hơi phát sáng trong quá trình phóng điện phát sáng. Có rất nhiều tia cực tím trong quang phổ phát xạ của hơi thủy ngân và để chuyển nó thành ánh sáng khả kiến, thủy tinh của đèn huỳnh quang được phủ một lớp phốt pho từ bên trong. Không có phốt pho, đèn thủy ngân là nguồn tia cực tím cứng (254nm), chúng được sử dụng trong công suất nào. Những chiếc đèn như vậy được làm bằng thủy tinh thạch anh truyền ánh sáng cực tím, đó là lý do tại sao chúng được gọi là thạch anh.
Thủy ngân và các hợp kim dựa trên thủy ngân được sử dụng trong các bộ phận ngắt mạch kín.
Thủy ngân được sử dụng trong cảm biến vị trí.
Thủy ngân(I) iodua được sử dụng làm máy dò bức xạ bán dẫn.
Thủy ngân(II) fulminat ("thủy ngân nổ") từ lâu đã được sử dụng làm chất nổ khởi đầu (ngòi nổ).
Thủy ngân(I) bromua được sử dụng trong quá trình phân hủy nhiệt hóa học của nước thành hydro và oxy (năng lượng hydro nguyên tử).
Người ta hứa hẹn sẽ sử dụng thủy ngân trong hợp kim với cesium như một chất lỏng hoạt động hiệu quả cao trong động cơ ion.
Cho đến giữa thế kỷ 20, thủy ngân đã được sử dụng rộng rãi trong phong vũ biểu, áp kế và huyết áp kế (do đó truyền thống đo áp suất bằng milimét thủy ngân).
Các hợp chất thủy ngân đã được sử dụng trong ngành công nghiệp mũ để làm nỉ.
Thủy ngân (anh. Thủy ngân) - Hg
PHÂN LOẠI
| Strunz (tái bản lần thứ 8) | 1/A.02-10 |
| Niken-Strunz (tái bản lần thứ 10) | 1.AD.05 |
| Dana (tái bản lần thứ 7) | 1.1.10.1 |
| Dana (tái bản lần thứ 8) | 1.1.7.1 | Xin giới thiệu CIM | 1.12 |
Thủy ngân là một nguyên tố thuộc phân nhóm phụ của nhóm thứ hai, chu kỳ thứ sáu của hệ thống định kỳ các nguyên tố hóa học của D. I. Mendeleev, với số nguyên tử 80. Nó được ký hiệu bằng ký hiệu Hg (lat. thủy tức).
Thủy ngân là một trong hai nguyên tố hóa học (và là kim loại duy nhất) có các chất đơn giản ở điều kiện thường ở trạng thái kết tụ lỏng (nguyên tố thứ hai là brom). Trong tự nhiên, nó được tìm thấy cả ở dạng tự nhiên và tạo thành một số khoáng chất.
Lịch sử phát hiện ra thủy ngân
Thủy ngân (tiếng Anh Mercury, tiếng Pháp Mercure, tiếng Đức Quecksilber) là một trong bảy kim loại thời cổ đại. Cô ấy đã được biết đến ít nhất trong 1500 năm trước Công nguyên, thậm chí sau đó họ đã biết cách lấy cô ấy từ chu sa. Thủy ngân được sử dụng ở Ai Cập, Ấn Độ, Lưỡng Hà và Trung Quốc; nó được coi là chất khởi đầu quan trọng nhất trong các hoạt động của nghệ thuật bí mật thiêng liêng để sản xuất các loại thuốc kéo dài tuổi thọ và được gọi là viên thuốc trường sinh. Trong thế kỷ IV - III. trước công nguyên. thủy ngân dưới dạng bạc lỏng (từ nước và bạc trong tiếng Hy Lạp) được đề cập bởi Aristotle và Theophrastus. Dioscorides sau đó đã mô tả việc sản xuất thủy ngân từ chu sa bằng cách đốt nóng chu sa bằng than. Sao Thủy được coi là cơ sở của kim loại, gần với vàng, và do đó được gọi là Sao Thủy (Mercurius), theo tên của hành tinh Sao Thủy gần mặt trời nhất (vàng). Mặt khác, tin rằng thủy ngân là một trạng thái nhất định của bạc, người cổ đại gọi nó là bạc lỏng (từ đó có nguồn gốc từ tiếng Latinh Hydrargirum). Tính di động của thủy ngân đã tạo ra một tên gọi khác - bạc sống (lat. Argentum vivum); Từ tiếng Đức Quecksilber xuất phát từ tiếng Low Saxon Quick (sống) và Silber (bạc). Điều thú vị là tên gọi của thủy ngân trong tiếng Bulgari - zhivak - và tiếng Ailen - jiva - có lẽ được mượn từ người Slav.
Ở Ai Cập thời Hy Lạp hóa và người Hy Lạp, cái tên nước Scythia đã được sử dụng, điều này khiến người ta có thể nghĩ đến việc xuất khẩu thủy ngân từ Scythia vào một thời điểm nào đó. Trong thời kỳ Ả Rập phát triển hóa học, lý thuyết thủy ngân-lưu huỳnh về thành phần của kim loại đã nảy sinh, theo đó thủy ngân được tôn sùng là mẹ của kim loại và lưu huỳnh (lưu huỳnh) là cha của chúng. Nhiều tên bí mật của thủy ngân trong tiếng Ả Rập đã được bảo tồn, điều này chứng tỏ tầm quan trọng của nó trong các hoạt động bí mật của giả kim thuật. Những nỗ lực của các nhà giả kim Ả Rập, và sau này là Tây Âu, đã được quy về cái gọi là cố định thủy ngân, tức là chuyển hóa nó thành một chất rắn. Theo các nhà giả kim, bạc nguyên chất (triết học) dễ dàng biến thành vàng. Huyền thoại Vasily Valentin (thế kỷ XVI) đã thành lập lý thuyết về ba nguyên tắc của nhà giả kim (Tria principia) - thủy ngân, lưu huỳnh và muối; lý thuyết này đã được phát triển thêm bởi Paracelsus. Trong phần lớn các chuyên luận về giả kim thuật, phác thảo các phương pháp biến đổi kim loại, thủy ngân ở vị trí đầu tiên hoặc là kim loại ban đầu cho bất kỳ hoạt động nào, hoặc là cơ sở của hòn đá triết gia (thủy ngân triết học).
Sự phổ biến của thủy ngân trong tự nhiênCác nguồn tự nhiên như núi lửa chiếm khoảng một nửa tổng lượng phát thải thủy ngân trong khí quyển. Hoạt động của con người chịu trách nhiệm cho nửa còn lại. Phần chính trong đó là khí thải từ đốt than chủ yếu ở các nhà máy nhiệt điện - 65%, khai thác vàng - 11%, luyện kim loại màu - 6,8%, sản xuất xi măng - 6,4%, xử lý chất thải - 3%, sản xuất soda - 3 %, sắt thép - 1,4%, thủy ngân (chủ yếu dùng cho pin) - 1,1%, còn lại - 2%.
Thủy ngân là một nguyên tố tương đối hiếm trong vỏ Trái đất với nồng độ trung bình là 83 mg/t. Tuy nhiên, do thủy ngân liên kết hóa học yếu với các nguyên tố phổ biến nhất trong vỏ trái đất nên quặng thủy ngân có thể rất đậm đặc so với đá thông thường.
Các quặng giàu thủy ngân nhất chứa tới 2,5% thủy ngân. Dạng chính của thủy ngân được tìm thấy trong tự nhiên là phân tán và chỉ 0,02% trong số đó được tìm thấy trong trầm tích. Hàm lượng thủy ngân trong các loại đá mácma gần nhau (khoảng 100 mg/t). Từ đá trầm tích, nồng độ thủy ngân tối đa được thiết lập trong đá phiến sét (lên tới 200 mg/t). Trong vùng biển của Đại dương Thế giới, hàm lượng thủy ngân là 1 µg/l. Đặc điểm địa hóa quan trọng nhất của thủy ngân là, trong số các nguyên tố chalcophile khác, nó có khả năng ion hóa cao nhất. Điều này xác định các tính chất như vậy của thủy ngân như khả năng phục hồi về dạng nguyên tử (thủy ngân tự nhiên), khả năng kháng hóa chất đáng kể đối với oxy và axit.
Có bằng chứng về sự tồn tại của sự tích tụ thủy ngân tự nhiên dưới dạng một hồ thủy ngân nhỏ.
Thủy ngân có mặt trong hầu hết các khoáng chất sunfua. Hàm lượng đặc biệt cao của nó (lên đến phần nghìn và phần trăm phần trăm) được tìm thấy trong quặng bạc màu, antimonit, sphalerit và thạch thực. Khoảng cách gần nhau về bán kính ion của thủy ngân hóa trị hai và canxi, thủy ngân hóa trị một và bari quyết định tính đồng hình của chúng trong fluorit và barit. Trong chu sa và metacinnabarit, lưu huỳnh đôi khi được thay thế bằng selen hoặc telua; hàm lượng selen thường là phần trăm và phần mười của phần trăm. Selenua thủy ngân cực hiếm được biết đến - timanite (HgSe) và onophrite (hỗn hợp của timanite và sphalerite).
Thủy ngân là một trong những chỉ số nhạy cảm nhất về quá trình khoáng hóa ẩn không chỉ của thủy ngân mà còn của các mỏ sulfua khác nhau; do đó, quầng thủy ngân thường được phát hiện trên tất cả các mỏ sulfua ẩn và dọc theo các đứt gãy tiền quặng. Tính năng này, cũng như hàm lượng thủy ngân thấp trong đá, được giải thích là do hơi thủy ngân có tính đàn hồi cao, tăng khi nhiệt độ tăng và quyết định sự di chuyển cao của nguyên tố này trong pha khí.
Ở điều kiện bề mặt, chu sa và thủy ngân kim loại hòa tan trong nước ngay cả khi không có chất oxy hóa mạnh, nhưng khi có mặt chúng (ozone, hydro peroxide), độ hòa tan của các khoáng chất này lên tới hàng chục mg/l. Thủy ngân hòa tan đặc biệt tốt trong các sunfua kiềm ăn da với sự hình thành, ví dụ, phức hợp HgS nNa 2 S. Thủy ngân dễ dàng bị hấp phụ bởi đất sét, sắt và mangan hydroxit, đá phiến và than.
Khoảng 20 khoáng chất thủy ngân được biết đến trong tự nhiên, nhưng giá trị công nghiệp chính là chu sa HgS (86,2% Hg). Trong một số ít trường hợp, thủy ngân tự nhiên, metacinnabarite HgS và fahlore schvatzit (lên đến 17% Hg) được khai thác. Tại mỏ Guitzuco duy nhất (Mexico), khoáng vật quặng chính là đá sống HgSb 4 S 7 . Khoáng vật thủy ngân thứ cấp được hình thành trong vùng oxy hóa của các mỏ thủy ngân. Chúng bao gồm chủ yếu là thủy ngân tự nhiên, metacinnabarite ít thường xuyên hơn, khác với các khoáng chất chính tương tự ở độ tinh khiết cao hơn của thành phần. Hg 2 Cl 2 calomel tương đối phổ biến. Tại mỏ Terlingua (Texas), các hợp chất halogen hypergene khác cũng rất phổ biến - terlinguaite Hg 2 ClO, aglestonite Hg 4 Cl.
Tính chất vật lý của thủy ngânNó là kim loại duy nhất ở thể lỏng ở nhiệt độ phòng. Nó có các đặc tính của một diamagnet. Hình thức với nhiều kim loại hợp kim lỏng - hỗn hống.
Thủy ngân nặng hơn nước 13,6 lần.
Nó có hệ số giãn nở nhiệt khá lớn - chỉ nhỏ hơn một lần rưỡi so với nước và một bậc độ lớn, hoặc thậm chí gấp hai lần so với các kim loại thông thường.
Tính chất hóa học của thủy ngânThủy ngân là kim loại kém hoạt động (xem dãy điện thế).
Khi đun nóng đến 300 °C, thủy ngân phản ứng với oxy: 2Hg + O 2 → 2HgO Thủy ngân(II) oxit màu đỏ được tạo thành. Phản ứng này có thể đảo ngược: khi đun nóng trên 340 ° C, oxit bị phân hủy thành các chất đơn giản. Phản ứng phân hủy oxit thủy ngân trong lịch sử là một trong những cách đầu tiên để tạo ra oxy.
Khi đun nóng thủy ngân với lưu huỳnh, thủy ngân(II) sunfua được tạo thành.
Thủy ngân không hòa tan trong dung dịch axit không có tính chất oxy hóa, nhưng hòa tan trong nước cường toan và axit nitric, tạo thành muối thủy ngân hóa trị hai. Khi thủy ngân dư được hòa tan trong axit nitric ở nhiệt độ lạnh, Hg 2 (NO 3) 2 nitrat được tạo thành.
Trong số các nguyên tố nhóm IIB, thủy ngân có khả năng phá hủy lớp vỏ electron 6d 10 rất ổn định, dẫn đến khả năng tồn tại các hợp chất thủy ngân (+4). Vì vậy, ngoài Hg 2 F 2 ít tan và HgF 2 bị phân hủy trong nước, còn có HgF 4 thu được do tương tác giữa các nguyên tử thủy ngân và hỗn hợp neon và flo ở nhiệt độ 4K.
Sử dụng thủy ngânThủy ngân được sử dụng trong sản xuất nhiệt kế, hơi thủy ngân chứa đầy thạch anh thủy ngân và đèn huỳnh quang. Trong đó, thủy ngân được sử dụng cả ở dạng nguyên chất và ở dạng hỗn hợp với khí (chủ yếu là argon) để tăng sản lượng ánh sáng. Đèn thủy ngân được sử dụng làm nguồn bức xạ cực tím mạnh. Các tiếp điểm thủy ngân đóng vai trò là cảm biến vị trí. Ngoài ra, thủy ngân kim loại được sử dụng để thu được một số hợp kim quan trọng.
Trước đây, các hỗn hống kim loại khác nhau, đặc biệt là hỗn hống vàng và bạc, được sử dụng rộng rãi trong trang sức, sản xuất gương và trám răng. Trong kỹ thuật, thủy ngân được sử dụng rộng rãi cho phong vũ biểu và áp kế. Các hợp chất thủy ngân được sử dụng làm thuốc sát trùng (thăng hoa), thuốc nhuận tràng (calomel), trong sản xuất mũ, v.v., nhưng do độc tính cao nên đến cuối thế kỷ 20, chúng thực tế đã bị loại bỏ khỏi những lĩnh vực này (thay thế hợp chất thủy ngân). bằng cách phun và mạ điện kim loại, chất trám polyme trong nha khoa).
Ngoài ra, thủy ngân được sử dụng rộng rãi trong sản xuất nhiệt kế. Điểm nóng chảy của thủy ngân là -38 độ, điểm sôi là +356,58. Nhưng có nhiều cách để vượt qua những ranh giới đó và tạo ra nhiệt kế hoạt động ở cả nhiệt độ thấp hơn và cao hơn. Để hạ thấp điểm nóng chảy, tali được thêm vào thủy ngân.
Thủy ngân kim loại đóng vai trò là cực âm để sản xuất điện phân của một số kim loại hoạt động, clo và kiềm, trong một số nguồn dòng điện hóa học (ví dụ: RT loại thủy ngân-kẽm), trong các nguồn điện áp tham chiếu (phần tử Weston). Nguyên tố kẽm-thủy ngân (emf 1,35 Vôn) có năng lượng rất cao xét về thể tích và khối lượng (130 W/h/kg, 550 W/h/dm).
Thủy ngân đôi khi được tạo hợp kim với các kim loại khác. Những bổ sung nhỏ của nguyên tố làm tăng độ cứng của hợp kim kim loại chì-kiềm. Ngay cả khi hàn đôi khi cũng cần đến thủy ngân: chất hàn làm từ 93% chì, 3% thiếc và 4% thủy ngân là vật liệu tốt nhất để hàn ống mạ kẽm.
Thủy ngân được sử dụng để tái chế nhôm thứ cấp và khai thác vàng (xem phần luyện kim hỗn hống).
Một trong những bộ phận chính của ngòi nổ cho đạn phòng không là một vòng xốp làm bằng sắt hoặc niken. Các lỗ chân lông chứa đầy thủy ngân. Bắn - đường đạn đã di chuyển, nó ngày càng tăng tốc độ, quay quanh trục của nó ngày càng nhanh hơn và thủy ngân nặng nhô ra khỏi lỗ chân lông. Nó đóng mạch điện - một vụ nổ.
Thủy ngân được sử dụng làm chấn lưu trong tàu ngầm và để điều chỉnh sự lăn và cắt của một số phương tiện. Người ta hứa hẹn sẽ sử dụng thủy ngân trong hợp kim với cesium như một chất lỏng hoạt động hiệu quả cao trong động cơ ion.
Trước đây, đáy tàu được phủ sơn thủy ngân để chúng không bị vỏ sò phát triển quá mức. Nếu không, con tàu chạy chậm lại, tiêu tốn nhiều nhiên liệu hơn. Nổi tiếng nhất của loại sơn này được tạo ra trên cơ sở muối thủy ngân có tính axit của axit asen HgHAsO 4 . Đúng vậy, thuốc nhuộm tổng hợp gần đây đã được sử dụng cho mục đích này, không chứa thủy ngân.
Thủy ngân-203 (T 1/2 = 53 giây) được sử dụng trong dược lý phóng xạ. Y học cũng sử dụng muối phốt phát của thủy ngân, sunfat, iốt và các loại khác. Ngày nay, hầu hết các hợp chất thủy ngân vô cơ đang dần được thay thế khỏi y học bằng các hợp chất thủy ngân hữu cơ, không có khả năng ion hóa dễ dàng và do đó không quá độc hại và ít gây kích ứng cho các mô.
Muối thủy ngân cũng được sử dụng:
- Thủy ngân iodua được sử dụng như một máy dò bức xạ bán dẫn.
- Thủy ngân fulminat ("Thủy ngân nổ") từ lâu đã được sử dụng làm chất nổ khởi đầu (ngòi nổ).
- Thủy ngân bromua được sử dụng trong quá trình phân hủy nhiệt hóa học của nước thành hydro và oxy (năng lượng hydro nguyên tử).
Một số hợp chất thủy ngân được sử dụng làm thuốc (ví dụ merthiolate để bảo quản vắc-xin), nhưng chủ yếu do độc tính, thủy ngân bị loại bỏ khỏi thuốc (thăng hoa, thủy ngân oxycyanua - thuốc sát trùng, calomel - thuốc nhuận tràng, v.v.) ở giữa cuối thế kỷ 20.
Việc sử dụng các hợp chất thủy ngân
hỗn hống thủy ngân
Một tính chất đáng chú ý khác của thủy ngân là khả năng hòa tan các kim loại khác, tạo thành dung dịch rắn hoặc lỏng - hỗn hống. Một số, chẳng hạn như hỗn hống bạc và cadmium, trơ về mặt hóa học và cứng ở nhiệt độ cơ thể, nhưng dễ dàng mềm ra khi đun nóng. Họ làm trám răng.
Thallium hỗn hống, chỉ cứng lại ở –60°C, được sử dụng trong các thiết kế đặc biệt của nhiệt kế nhiệt độ thấp.
Những chiếc gương cổ xưa không được phủ một lớp bạc mỏng như hiện nay mà bằng một hỗn hống, bao gồm 70% thiếc và 30% thủy ngân. Vào thế kỷ 20, nó không thể chịu được sự cạnh tranh và nhường chỗ cho một quy trình tiên tiến hơn - xyanua hóa.
Một số kim loại, đặc biệt là sắt, coban, niken, thực tế không thể trộn được. Điều này cho phép vận chuyển kim loại lỏng trong các thùng thép trơn. (Đặc biệt là thủy ngân nguyên chất được vận chuyển trong các hộp thủy tinh, gốm hoặc nhựa.) Ngoài sắt và các chất tương tự của nó, tantali, silicon, rheni, vonfram, vanadi, berili, titan, mangan và molypden không được trộn lẫn, nghĩa là hầu hết tất cả các kim loại được sử dụng để hợp kim trở thành. Điều này có nghĩa là thủy ngân không sợ thép hợp kim.
Nhưng natri, ví dụ, hợp nhất rất dễ dàng. Hỗn hống natri dễ bị phân hủy bởi nước. Hai trường hợp này đã và tiếp tục đóng một vai trò rất quan trọng trong ngành công nghiệp clo.
Trong quá trình sản xuất clo và xút ăn da bằng cách điện phân muối ăn, người ta sử dụng cực âm từ thủy ngân kim loại. Để có được một tấn xút ăn da, bạn cần từ 125 đến 400 g nguyên tố số 80. Ngày nay, ngành công nghiệp clo là một trong những ngành tiêu thụ thủy ngân kim loại lớn nhất.
Chu sa - thủy ngân đỏ
chu sa HgS. Nhờ cô ấy, mọi người đã làm quen với thủy ngân từ nhiều thế kỷ trước. Điều này được tạo điều kiện bởi màu đỏ tươi của nó và dễ dàng thu được thủy ngân từ chu sa. Các tinh thể chu sa đôi khi được bao phủ bởi một lớp màng mỏng màu xám chì. Đây là metacinnabarite, về nó bên dưới. Tuy nhiên, chỉ cần chạy một con dao trên phim và một đường màu đỏ tươi sẽ xuất hiện.
Trong tự nhiên, thủy ngân sunfua tồn tại ở ba dạng biến đổi khác nhau về cấu trúc tinh thể. Ngoài cinnabar nổi tiếng với mật độ 8,18, còn có metacinnabar đen với mật độ 7,7 và cái gọi là beta cinnabar (mật độ của nó là 7,2). Những người thợ thủ công Nga ngày xưa khi chuẩn bị sơn đỏ từ quặng chu sa đã đặc biệt chú ý đến việc loại bỏ "tia lửa" và "ngôi sao" khỏi quặng. Họ không biết rằng đây là những biến thể đẳng hướng của cùng một loại thủy ngân sunfua; khi được làm nóng mà không có không khí đến 386 ° C, những sửa đổi này biến thành chu sa "thực sự".
Một số hợp chất thủy ngân đổi màu theo nhiệt độ. Đây là oxit thủy ngân màu đỏ HgO và iodua đồng-thủy ngân HgI 2 · 2CuI.
độc tính thủy ngân
Hơi thủy ngân, cũng như thủy ngân kim loại, rất độc và có thể gây ngộ độc nặng. Thủy ngân và các hợp chất của nó (thăng hoa, calomel, thủy ngân xyanua) ảnh hưởng đến hệ thần kinh, gan, thận, đường tiêu hóa và khi hít phải đường hô hấp (và sự xâm nhập của thủy ngân vào cơ thể xảy ra thường xuyên hơn khi hít phải hơi không mùi của nó) . Theo loại nguy hiểm, thủy ngân thuộc loại đầu tiên (một hóa chất cực kỳ nguy hiểm). Một chất gây ô nhiễm môi trường nguy hiểm, thải ra nước đặc biệt nguy hiểm, vì hoạt động của các vi sinh vật sống ở đáy tạo ra metyl thủy ngân độc hại và hòa tan trong nước.
Ở một số quốc gia, calomel được sử dụng làm thuốc nhuận tràng. Tác dụng độc hại của calomel được thể hiện đặc biệt khi sau khi uống vào bên trong, tác dụng nhuận tràng không xảy ra và cơ thể không đào thải được thuốc này trong thời gian dài.
Thủy ngân(II) clorua, được gọi là thăng hoa, có độc tính cao. Độc tính của thủy ngân(II) nitrat gần giống như độc tính của chất thăng hoa.
Mức ô nhiễm tối đa cho phép đối với thủy ngân kim loại và hơi của nó:
- MPC tại các khu định cư (trung bình hàng ngày) - 0,0003 mg/m³
- MPC trong khu dân cư (trung bình hàng ngày) - 0,0003 mg/m³
- MPC của không khí trong khu vực làm việc (tối đa đơn) - 0,01 mg / m³
- MPC của không khí khu vực làm việc (ca trung bình) - 0,005 mg/m³
- Nước thải MPC (đối với hợp chất vô cơ tính theo thủy ngân hóa trị 2) - 0,005 mg/ml
- MPC của các đối tượng sử dụng nước kinh tế, nước sinh hoạt và văn hóa, trong nước hồ chứa - 0,0005 mg/l
- MPC cho hồ chứa thủy sản - 0,00001 mg/l
- MPC của nước biển - 0,0001 mg/l
- MAC trong đất - 2,1 mg/kg
Sản xuất thủy ngân trên thế giới
Tiền gửi thủy ngân được biết đến ở hơn 40 quốc gia trên thế giới. Tài nguyên thủy ngân thế giới ước tính khoảng 715 nghìn tấn; trữ lượng tính theo định lượng - ở mức 324 nghìn tấn, trong đó 26% tập trung ở Tây Ban Nha, 13% ở Kyrgyzstan và Nga, 8% - ở Ukraine, khoảng 5-6,5% mỗi nước - ở Slovakia, Slovenia, Trung Quốc, An-giê-ri, Ma-rốc, Thổ Nhĩ Kỳ. Việc cung cấp dự trữ thủy ngân đến mức tiêu thụ tối đa, đạt được vào những năm 1990, là khoảng 80 năm đối với thế giới. Từ đầu những năm 1970 do các yếu tố môi trường, thị trường thủy ngân bắt đầu xấu đi rõ rệt. Nếu vào đầu những năm 1970 sản lượng thủy ngân sơ cấp trên thế giới (khai thác và luyện kim) được ước tính là 10.000 tấn mỗi năm, sau đó vào cuối những năm 1980. nó đã tăng hơn gấp đôi. Điều này đi kèm với việc giảm giá thủy ngân: từ 11-12 nghìn đô la Mỹ trên 1 tấn vào năm 1980-1982. lên tới 4-5 nghìn đô la vào năm 1994-1996.
Sản lượng thủy ngân trên thế giới năm 2009 đã là 3049 tấn, và
tài nguyên thủy ngân đã được xác định ước tính khoảng 675 nghìn tấn (chủ yếu ở
Tây Ban Nha, Ý, Nam Tư, Kyrgyzstan, Ukraine và Nga).
Các nhà sản xuất thủy ngân lớn nhất là Tây Ban Nha (1497 tấn), Trung Quốc (550 tấn), Algeria
(290 tấn), Mexico (280 tấn), Kyrgyzstan (270 tấn), v.v.
Lịch sử sản xuất thủy ngân ở Nga
Thông tin đầu tiên về việc tổ chức sản xuất thủy ngân ở Nga có từ năm 1725, theo đó thương gia Pyotr Anisimov bắt đầu xây dựng một nhà máy thủy ngân và ông giữ bí mật về nguồn nguyên liệu thô. Việc khai thác quặng thủy ngân (cinnabar) ở Nga bắt đầu vào năm 1759 tại mỏ Ildikanskoye ở Trans Bạch Mã và tiếp tục với khối lượng nhỏ (theo định kỳ) cho đến năm 1853. Vào cuối thế kỷ 19 - đầu thế kỷ 20. Chu sa được khai thác với số lượng nhỏ từ các sa khoáng phù sa ở Vùng Amur. Gần như cùng lúc đó, các phần riêng lẻ của mỏ thủy ngân của mỏ quặng Birksu (Nam Fergana) và mỏ Khpek (Nam Dagestan) đã được khai thác. Năm 1879, mỏ thủy ngân Nikitovskoe (Donbass) được phát hiện, việc khai thác (đồng thời với quá trình luyện kim) bắt đầu vào năm 1887. Năm 1887-1908. sản lượng thủy ngân hàng năm tại mỏ Nikitovsky dao động trong khoảng 47,3-615,9 tấn). Các tính toán dựa trên dữ liệu cho thấy từ năm 1887 đến 1917, 6762 tấn thủy ngân kim loại đã được thu được ở đây, một phần đáng kể trong số đó đã được xuất khẩu (từ 1889 đến 1907, hơn 5145 tấn thủy ngân đã được xuất khẩu ra nước ngoài). Vào đầu thế kỷ XX. Nga cũng nhập khẩu chu sa và thủy ngân. Ví dụ, năm 1913, 56 tấn chu sa và 168 tấn thủy ngân được nhập khẩu vào nước này, năm 1914 - 41 tấn chu sa và 129 tấn thủy ngân. Năm 1900-1908. mức tiêu thụ thủy ngân ở Nga dao động trong khoảng 49-118 tấn/năm. Vào thời điểm đó, thủy ngân được sử dụng trong y học và dược phẩm, sản xuất gương và sơn, sản xuất nhiệt kế, phong vũ biểu, đồng hồ đo áp suất và các dụng cụ khác, được sử dụng để chà đệm của máy điện, chiết xuất vàng và bạc bằng cách phương pháp hỗn hợp, để mạ đồng và đồng thau, để làm sạch nỉ, trong thêu vàng và thực hành trong phòng thí nghiệm.
Các nguyên tố định kỳ, phân nhóm kẽm, số nguyên tử - 80. Trong điều kiện phòng, chất này xuất hiện dưới dạng chất lỏng nặng màu trắng bạc. hơi thủy ngânđộc. nhiệt độ thủy ngân xác định trạng thái tổng hợp của nó, không phải một kim loại ngoại trừ nó có cấu trúc lỏng ở nhiệt độ phòng.
Sự nóng chảy của thủy ngân bắt đầu ở nhiệt độ 234º K, sôi ở 629º K. Nó hợp kim với nhiều kim loại, tạo thành hợp kim gọi là hỗn hống. thủy ngân trong nước và dung dịch axit không hòa tan, chỉ axit nitric có thể làm điều này hoặc.
Với khó khăn, điều này có thể được thực hiện với axit sulfuric. Khi đạt đến nhiệt độ 300º C, một phản ứng xảy ra với oxy, kết quả là oxit thủy ngân, có màu đỏ (đừng nhầm với “thủy ngân đỏ” hư cấu!).
"Thủy ngân đỏ"- thuật ngữ này đề cập đến một chất được phát minh cho mục đích thương mại. Các đặc tính siêu việt được quy cho đặc tính, trên thực tế, một kim loại như vậy, có nguồn gốc tự nhiên hoặc nhân tạo, vẫn chưa được khoa học biết đến. Hợp chất của lưu huỳnh và thủy ngânở nhiệt độ cao tạo thành thủy ngân sunfua.
Khai thác và nguồn gốc của thủy ngân
Kim loại này được coi là khá hiếm, tập trung chủ yếu trong quặng thủy ngân, cụ thể hàm lượng thủy ngân trong đó khá cao. Nhìn chung, toàn bộ khối lượng thủy ngân tự nhiên được phân tán trong tự nhiên và chỉ một phần nhỏ trong số đó được chứa trong quặng. Tỷ lệ nội dung cao nhất được quan sát thấy trong các loại đá được hình thành sau vụ phun trào và đá phiến trầm tích.

Các khoáng chất sunfua phần lớn cũng chứa thủy ngân. Đây là những loại quặng bị phai màu, sphalerat, realgar và antimonit. Trong tự nhiên, người ta thường tìm thấy các bó phần tử đi kèm với nhau, ví dụ, một vùng lân cận như selen, lưu huỳnh và thủy ngân.
Ít nhất hai mươi loại khoáng chất thủy ngân được biết đến chắc chắn. Khoáng sản được khai thác chính là cinnabar, ít gặp hơn là metacinnabarite hoặc thủy ngân tự nhiên. Livingstonite được khai thác tại một mỏ ở Mexico (Guitzuco).
Các khoản tiền gửi lớn nhất nằm ở Dagestan, Tajikistan, Armenia, Kyrgyzstan, Ukraine, Tây Ban Nha và Slovenia (khoản tiền gửi ở thành phố Idriya được coi là lớn nhất kể từ thời Trung cổ). Ngoài ra còn có ít nhất hai mươi ba khoản tiền gửi ở Nga.
Sử dụng thủy ngân
trước đây được xác định hợp chất thủy ngân, ví dụ, clorua hoặc thủy ngân của nó, có thể dễ dàng tìm thấy ứng dụng trong lĩnh vực y tế. Đây là những loại thuốc nhuận tràng, lợi tiểu và sát trùng khác nhau. Nhưng hiện nay các hợp chất thủy ngân gần như bị loại bỏ hoàn toàn khỏi khu vực này do độc tính của chúng. Một phần, nguyên tố này được sử dụng trong sản xuất nhiệt kế, mặc dù người ta đã tìm thấy một chất thay thế an toàn hơn cho chúng.

Sự hiện diện của nó trong các thiết bị kỹ thuật được coi là dễ chấp nhận hơn. Đây là những nhiệt kế có độ chính xác cao cho mục đích kỹ thuật. Đèn huỳnh quang, nơi hơi của nó được sử dụng. Bộ chỉnh lưu, ổ điện và thậm chí một số mẫu máy hàn. Đây là những cảm biến vị trí và công tắc kín.
Nó cũng được sử dụng trong sản xuất một số loại nguồn hiện tại, với chất làm đầy thủy ngân-kẽm. Một trong những thành phần của vòng bi thủy động cũng là thủy ngân. Cũng trong ngành công nghiệp kỹ thuật, các hợp chất như fulminate, iodua và bromua thủy ngân đã tìm thấy ứng dụng của chúng. Các đặc tính tích cực đã thể hiện nó với Caesium, được sử dụng trong sản xuất động cơ ion.
Trong luyện kim, thủy ngân được sử dụng để nấu chảy nhiều hợp kim khác nhau và trong quá trình xử lý nhôm thứ cấp. Cô tìm thấy thị trường ngách của mình trong sản xuất đồ trang sức, cũng như sản xuất gương. Thủy ngân đã nhận được sự phân phối đáng kể trong quá trình sản xuất vàng; đá chứa vàng được xử lý trước với nó để chiết xuất nó từ chúng. Trong công nghiệp nông thôn, một số hợp chất thủy ngân được sử dụng để xử lý hạt giống và làm thuốc trừ sâu. Mặc dù điều này là rất không mong muốn.
Tác hại của thủy ngân đối với cơ thể con người
Hơi thủy ngân cực kỳ nguy hiểm. Nó có thể xâm nhập vào cơ thể thông qua bay hơi hoặc trực tiếp qua khoang miệng. Loại thứ hai thường xảy ra với trẻ nhỏ, trong trường hợp thủy ngân vỡ từ nhiệt kế. Trong trường hợp này, cần phải gây nôn cho anh ta càng sớm càng tốt và gọi cấp cứu.

Nhưng mọi người đều có thể hít phải hơi của nó, nếu thủy ngân từ nhiệt kế lăn vào tất cả các vết nứt của căn phòng, và bốc hơi từ đó. ngộ độc thủy ngân xảy ra dần dần, trong giai đoạn đầu của các triệu chứng đặc biệt không được quan sát. Trong tương lai, khó chịu quá mức, buồn nôn liên tục và giảm cân xảy ra. Trước hết, cú đánh rơi vào hệ thống thần kinh trung ương và thận.
Những biện pháp phòng ngừa nào được yêu cầu thủy ngân? Phá vỡ một nhiệt kế? phải làm gì và làm thế nào để thu thập thủy ngân từ sàn nhà, hướng dẫn sau đây sẽ chỉ ra. Thông gió khu vực ngay lập tức trong ít nhất vài giờ. Nhưng không cho phép một bản nháp trực tiếp cho đến khi thủy ngân được thu thập hoàn toàn. Hạn chế tiếp cận hiện trường để không làm phát tán thủy ngân ra khắp nhà.

Trước khi bắt đầu thu thập thủy ngân, bạn cần đeo găng tay làm bằng vật liệu không thấm nước vào tay, vào chân - bất kỳ túi nào, trên mặt - băng ngâm trong nước hoặc dung dịch. Cẩn thận thu thập tất cả thủy ngân cuộn và phần còn lại của nhiệt kế bị hỏng trong một thùng chứa nước, điều này sẽ không cho phép thủy ngân bay hơi. Cần phải thu thập thủy ngân càng cẩn thận càng tốt, chẳng hạn như sử dụng ống tiêm.
Nếu thủy ngân rơi xuống dưới ván chân tường hoặc sàn nhà, đừng lười mở nó ra và dọn sạch nó ra khỏi đó, bất kể mất bao lâu. Nếu thủ tục mất đủ thời gian, bạn nên nghỉ giải lao cứ sau mười phút. Bình chứa phải được đậy kín và tránh xa nguồn nhiệt. Vứt bỏ thùng chứa bị nghiêm cấm. Nó sẽ gây ô nhiễm môi trường, trẻ em có thể tìm thấy nó. Do đó, thủy ngân thu được được bàn giao cho các dịch vụ liên quan.
Hiện trường vụ việc được xử lý bằng dung dịch mangan hoặc thuốc tẩy pha loãng. Bạn không thể thu thập thủy ngân bằng chổi hoặc máy hút bụi, điều này sẽ chỉ làm trầm trọng thêm tình hình bằng cách phun thủy ngân lên một khu vực rộng lớn. Ngoài ra, sau đó, máy hút bụi sẽ không sử dụng được do ô nhiễm độc hại.
giá thủy ngân
Tổng khối lượng giao dịch kim loại đất hiếm này và các hợp chất khác nhau của nó là khoảng 150 triệu đô la, với trữ lượng thế giới khoảng 300 nghìn tấn. Do việc thanh lý một số khoản tiền gửi lớn, nguồn cung thủy ngân cho thị trường thế giới đã giảm mạnh, dẫn đến giá của sản phẩm này tăng lên. Để so sánh, năm 2001, một container đo tiêu chuẩn khối lượng 34,5 kg có giá 170 USD, đến năm 2005 giá lên tới 775 USD. Sau đó, nó bắt đầu giảm trở lại, giá cuối cùng là khoảng 550 đô la.

Giải pháp trong trường hợp này là thủy ngân thứ cấp được sản xuất tại các doanh nghiệp trọng điểm. Công nghệ mới nhất đã cung cấp cho thị trường một khối lượng lớn các sản phẩm rẻ hơn, cho phép giảm một số mức giá cắt cổ của thủy ngân tự nhiên. Mặc dù giá vẫn ở mức khá cao.
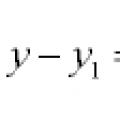 Phương trình đường thẳng và đường cong trong mặt phẳng
Phương trình đường thẳng và đường cong trong mặt phẳng Phương trình thuần nhất tổng quát Phương trình thuần nhất tổng quát cấp 2
Phương trình thuần nhất tổng quát Phương trình thuần nhất tổng quát cấp 2 Nhờ dấu phẩy Do thực tế là trong họ
Nhờ dấu phẩy Do thực tế là trong họ