Газ. Идеальный газ
Сжиженный природный газ или сокращенно СПГ , как принято называть его в энергетической отрасли (англ. соотв. Liquefied Natural Gas , сокр. LNG ) представляет собой обыкновенный природный газ, охлажденный до температуры –162°С (так называемая температура сжижения ) для хранения и транспортировки в жидком виде. Хранится сжиженный газ в при температуре кипения, которая поддерживается вследствие испарения СПГ . Данный способ хранения СПГ связан с тем, что для метана, основной составляющей СПГ , критическая температура –83°С, что гораздо ниже температуры окружающей среды, и не предоставляет возможным хранить сжиженный природный газ в резервуарах высокого давления (для справки: критическая температура для этана составляет +32°С, для пропана +97°С). Для использования СПГ подвергается испарению до исходного состояния без присутствия воздуха. При (возвращении газа в исходное парообразное состояние ) из одного кубометра сжиженного газа образуется около 600 кубометров обычного природного газа.
Температура сжиженного газа
Чрезвычайно низкая температура СПГ делает его криогенной жидкостью . Как правило, вещества, температура которых составляет –100°С (–48°F) или еще ниже, считаются криогенными и требуют специальных технологий для обработки. Для сравнения, самая низкая зарегистрированная температура на Земле составляет –89,2°С (Антарктика), а в населенном пункте –77,8°С (поселок Оймякон, Якутия). Криогенная температура сжиженного природного газа означает, что контакт с СПГ может вызвать изменение свойств контактирующих материалов, которые впоследствии станут ломкими и потеряют свою прочность и функциональность. Поэтому в отрасли СПГ используют специальные и технологии.
Химический состав СПГ
Сырая нефть и природный газ являются ископаемыми видами топлива, известными как «углеводороды» , потому что содержат химические комбинации атомов углерода и водорода. Химический состав природного газа зависит от места добычи газа и его обработки. Сжиженный природный газ представляет собой смесь метана, этана, пропана и бутана с небольшим количеством более тяжелых углеводородов и некоторых примесей, в частности, азотных и комплексных соединений серы, воды, углекислого газа и сероводорода, которые могут существовать в исходном газе, но должны быть удалены перед . Метан является самым главным компонентом, обычно, хотя и не всегда, более чем на 85% по объему.
Плотность сжиженного газа
Поскольку СПГ представляет собой некую смесь, плотность сжиженного природного газа изменяется незначительно с ее фактическим составом. Плотность сжиженного природного газа , как правило, находится в диапазоне 430–470 килограммов на кубический метр, а его объем составляет примерно 1/600 объема газа в атмосферных условиях. Это делает его примерно на треть легче, чем воздух. Другим следствием этих фактов является то, что СПГ имеет меньшую плотность, чем вода, что позволяет ему находиться на поверхности в случае разлива и вернуться к парообразному состоянию достаточно быстро.
Другие свойства СПГ
 Сжиженный природный газ не имеет запаха, бесцветный, не вызывает коррозии, не горюч и не токсичен. СПГ хранится и транспортируется при сверхнизких температурах при атмосферном давлении (отсутствие высоких давлений). При воздействии на окружающую среду СПГ быстро испаряется, не оставляя следов на воде или почве.
Сжиженный природный газ не имеет запаха, бесцветный, не вызывает коррозии, не горюч и не токсичен. СПГ хранится и транспортируется при сверхнизких температурах при атмосферном давлении (отсутствие высоких давлений). При воздействии на окружающую среду СПГ быстро испаряется, не оставляя следов на воде или почве.
В своей жидкой форме сжиженный природный газ не имеет способность взрываться или воспламеняться. При испарении природный газ может воспламениться в случае контакта с источником горения, и если концентрация испарений в воздухе будет составлять от 5 до 15 процентов. Если концентрация паров газа менее 5 процентов, то для начала возгорания испарений недостаточно, а если более 15 процентов, то в окружающей среде будет нехватка кислорода.
Преимущества сжиженного природного газа
- В плотность газа увеличивается в сотни раз, что повышает эффективность и удобство хранения, а также транспортировки и потребления энергоносителя.
- Сжиженный природный газ – нетоксичная криогенная жидкость , хранение которой осуществляется в теплоизолированной емкости при температуре –162°С. Большие объемы СПГ возможно хранить в при атмосферном давлении.
- Возможность межконтинентальных перевозок СПГ специальными , а также перевозка железнодорожным и автомобильным видами транспорта в цистернах.
- Сжиженный природный газ дает возможность газификации объектов, удаленных от магистральных трубопроводов на большие расстояния, путем создания резерва СПГ непосредственно у потребителя, избегая строительства дорогостоящих трубопроводных систем.
С точки зрения потребителя, преимущества сжиженного природного газа, исходя из его , состоят еще и в том, что СПГ является не только источником , транспортируемого по газопроводам, а также источником ШФЛУ (широкая фракция легких углеводородов – этана, пропана, бутанов и пентанов), входящих в состав СПГ и выделяемых из СПГ при регазификации . Эти углеводороды используются в качестве нефтехимического сырья и в качестве источника экологически чистого топлива для различных видов транспорта (а также в быту). В будет происходить выделение фракции С 2 + или С 3 +. Возможность перевозить ШФЛУ в составе сжиженного природного газа выступает не только в пользу потребителя, но также решает и проблемы производителя по транспортировке ШФЛУ с газового месторождения.
Сжиженный природный газ представляет собой безопасный, экологически чистый вид топлива с высокими энергетическими характеристиками и октановым числом. Цена СПГ по стоимости у потребителя ниже цены сжиженного нефтяного газа, мазута и тем более дизельного топлива.
ГАЗ . Газообразным состоянием называется такое состояние вещества, в котором силы, действующие между молекулами, чрезвычайно малы и размеры самих молекул ничтожны сравнительно с промежутками между ними. Между столкновениями молекулы газа двигаются прямолинейно, равномерно и совершенно беспорядочно. При нагревании и разрежении все газы стремятся к предельному состоянию так называемого идеального , или совершенного газа .
В идеальном газе междумолекулярные силы равны нулю, и объем самих молекул бесконечно мал сравнительно с объемом междумолекулярного пространства. Состояние идеального газа является тем предельным разведенным состоянием вещества, к которому стремятся все тела природы при достаточно высоких температурах и достаточно низких давлениях; в этом и заключается особое значение состояния идеального газа, к тому же наиболее просто поддающегося исследованию и потому полнее всего изученного. Вещество, в крайнем разрежении заполняющее межпланетное пространство, может считаться находящимся в состоянии идеального газа.
Газовое давление (р) обусловливается ударами молекул газа о стенки сосуда. Согласно кинетической теории, средняя кинетическая энергия молекул газа пропорциональна абсолютной температуре. В кинетической теории показывается, что идеальный газ строго подчиняется следующему уравнению состояния, связывающему три параметра состояния: v, T и р, из которых два являются независимыми, а третий - их функцией:
Это уравнение (уравнение Клапейрона ) заключает в себе в явной форме три основных закона состояния идеального газа:
1) Закон Бойля-Мариотта . При постоянной температуре (Т) произведение (p∙v) для данного количества идеального газа есть величина постоянная (p∙v = Const), т. е. объем идеального газа (v) обратно пропорционален его давлению (р): изотермы идеального газа в системе координат (v, р) являются равнобокими гиперболами, асимптотами которых служат оси координат.
2) . При постоянном (р) объем данного количества идеального газа линейно возрастает с температурой:
(v 0 - объем при температуре = 0°С, α - коэффициент расширения идеального газа). Изменение (p) с температурой при v = Const подчиняется такому же закону:
(α) в уравнении (3) - коэффициент давления, численно равный коэффициенту расширения (α) в уравнении (2) = 1/273,1 = 0,00367 - величина, независящая от природы газа и одинаковая для всех идеальных газов; р 0 - давление при температуре = 0°С. Вводя вместо температуры абсолютную температуру
находим вместо уравнений (2) и (3):
3) Закон Авогадро . Из уравнения (1) видно, что газовая постоянная R = p 0 ∙v 0 /273,1 пропорциональна нормальному объему v 0 , занимаемому данным количеством газа при нормальных условиях (р 0 = 1 Atm и t 0 = 0°С = 273,1° К), т. е. обратно пропорциональна плотности газа при нормальных условиях D 0 . По закону Авогадро, при одинаковых (р) и (Т) все идеальные газы содержат в равных объемах (например, равных v 0) равное число молекул. Обратно: равное число молекул (например, 1 моль = 1 граммолекуле) всякого газа в идеальном состоянии занимает один и тот же объем v 0 при нормальных условиях, независимо от природы газа (в 1 моле всякого вещества содержится N 0 = 6,06∙10 23 отдельных молекул - число Авогадро ). Найдено с большой точностью, что нормальный молярный объем любого идеального газа (V 0) м равен 22,412 литр/моль. Отсюда можно рассчитать число молекул в 1 см 3 любого идеального газа при нормальных условиях: n0 = 6,06∙10 23 /10 3 ∙22,416 = 2,705∙10 19 см 3 (число Лошмита ). При помощи уравнения (1) закон Авогадро выражается в том, что газовая постоянная R при расчете на 1 моль любого газа будет одна и та же, независимо от природы газа. Т. о. R является универсальной постоянной с размерностью [работа ]/[масса ][температура ] и выражает работу расширения 1 моля идеального газа при нагревании его на 1°С при р = Const:
![]()
в этом и состоит физическое значение R.
находим числовое значение
В других единицах значения R (на 1 моль) таковы:
Кроме разобранных трех законов, из уравнения (1) состояния идеального газа в соединении с двумя началами термодинамики следуют еще такие основные законы:
4) Закон Джоуля . Одно из общих уравнений термодинамики
дает вместе с уравнением (1) следующие условия для внутренней энергии U идеального газа:
т. е. U идеального газа есть функция только Т (закон Джоуля); при изотермическом расширении идеального газа все поглощаемое тепло переходит во внешнюю работу, а при изотермическом сжатии вся расходуемая работа - в выделяющееся тепло.
5) Теплоемкости идеального газа при постоянном объеме c v и при постоянном давлении с р являются функциями одной лишь Т. Термодинамика дает общие уравнения
но для идеального газа (р) и (v) линейно зависят от (Т), по закону Гей-Люссака (4) и (5); следовательно, правые части уравнений (9) обращаются в 0 и
![]()
Теплоемкости с р и c v не независимы друг от друга, но связаны для идеального газа простым условием:
вытекающим из газовых законов (R имеет размерность теплоемкости), т. е., если с р и c v относить к 1 молю идеального газа, то они разнятся между собой на 2 (точнее - на 1,986) – cal/моль∙град.
В кинетической теории принимается, по принципу равномерного распределения энергии, что на каждую степень свободы газовой молекулы приходится энергия k 0 ∙Т/2, а на 1 моль приходится
(k 0 = –R/N 0 есть газовая постоянная, рассчитанная на 1 молекулу - постоянная Больцмана ). Числом степеней свободы (i) называется число независимых друг от друга видов механической энергии, которой обладает молекула газа. Тогда энергия 1 моля

(приближенно, считая R = 2, c v = i, с р = i+2).
В учении о газе важную роль играет отношение c p /c v = γ; из уравнений (11) и (12):
В простейшем случае одноатомного газа (молекула которого состоит из 1 атома, каковы благородные газы и пары многих металлов) i наименьшее и равняется 3: вся энергия молекулы сводится к кинетической энергии ее поступательных движений, которые могут совершаться по трем независимым взаимно перпендикулярным направлениям; тогда
а γ имеет наибольшую возможную величину: γ = 5/3 = 1,667. Для двухатомных газов (Н 2 , O 2 , N 2 , СО и другие) можно считать I = 3+2 (два вращения вокруг двух взаимно перпендикулярных осей, перпендикулярных к линии, соединяющей оба атома); тогда c v = 4,96 ≈ 5, cр = 6,95 ≈ 7 и γ = 7/5 = 1,40. Для трехатомного газа (Н 2 O, СO 2 , H 2 S, N 2 O)i = 3+3 (вращение вокруг трех взаимно перпендикулярных осей) и c v = 5,96 ≈ 6, cр = 7,95 ≈ 7 и γ = 4/3 = 1,33.
При дальнейшем усложнении строения молекулы, т. е. с увеличением i, возрастают c v и с р, а γ = 1 + 2/i и стремится к 1. Табл. 1 показывает, что все сказанное хорошо согласуется с данными опыта, что γ всегда >1 и ≤1,667 и не может быть = 1,50 (для i = 4).

Для одноатомных газов c v и с р, в соответствии с теорией, практически не изменяются с температурой (так, для Ar значения c v и с р лежат в пределах от 2,98 до 3,00 между температурами = 0° и 1000° С). Изменения c v и с р с температурой находят объяснение в теории квант. Впрочем, теплоемкости газов, близких к идеальным, практически почти не изменяются в широких интервалах температуры. Экспериментально определяются обычно с р и у, a c v вычисляется из этих данных.
Реальные газы . Все газы, существующие в действительности, - реальные газы б. или м. уклоняются от законов идеальных газов, но тем меньше, чем выше температура и чем ниже давление. Т. о. законы идеальных газов являются для реальных газов предельными. При обычной температуре уклонения меньше всего у газов, критические температуры которых чрезвычайно низки (т. н. постоянные газы: Не, Н 2 , N 2 , О 2 , воздух); у газов же со сравнительно высокой критической температуры и у паров (паром называется газ при температуре меньше критической температуры) уклонения бывают очень значительны. Причины уклонений реальных газов от газовых законов заключаются в том, что: 1) в них действуют междумолекулярные силы; поэтому поверхностные молекулы втягиваются внутрь газов силами, равнодействующая которых, рассчитанная на единицу поверхности и направленная перпендикулярно к ней, называется молекулярным (внутренним) давлением К ; 2) не весь объем газа (v), а только часть его (v-b) дает свободу для движений молекул; часть объема (b), коволюм , как бы занята самими молекулами. Если бы газ был идеальным, его давление было бы больше наблюдаемого (р) на величину К; поэтому уравнение состояния реального газа напишется в виде.
В этом общем уравнении К и b могут зависеть от Т и v.
Ван-дер-Ваальс показал, что в простейшем случае К = a/v 2 , а b - величина постоянная, равная учетверенному объему самих молекул газа. Таким образом, уравнение Ван-дер-Ваальса имеет вид:
а и b, константы Ван-дер-Ваальса, как показывает опыт, все же зависят от T и v, и потому уравнение (15) является лишь первым приближением; оно хорошо передает качественную форму изотерм реальных газов.

На фиг. 1 изображены для СO 2 теоретической изотермы: S-образные части этих изотерм отвечают термодинамически метастабильным состояниям .

На фиг. 2 изображены для СО 2 экспериментальные изотермы: S-образные части кривых заменены прямолинейными частями; справа от этих частей кривые соответствуют газу (ненасыщенному пару), слева - жидкости, а сами прямолинейные отрезки - равновесию пара и жидкости. Уравнение (15), в полном согласии с опытом, показывает, что с повышением температуры размеры прямолинейных отрезков на изотермах делаются все меньше (фиг. 2) и, наконец, при некоторой температуре равной критической температуре длина этого отрезка обращается в 0. При температуре большей критической температуры газ не может обращаться в жидкость ни при каких давлениях: жидкость перестает существовать. Т. о. уравнение Ван-дер-Ваальса охватывает два состояния - газообразное и жидкое - и служит основанием для учения о непрерывности перехода между этими двумя состояниями. Критические температуры для некоторых газов имеют следующие значения: +360°С для Н 2 О, +31°С для СО 2 , –241°С для Н 2 и –254°С для Не.
Сжижение газа . Всякий газ можно обратить в жидкость надлежащим давлением, предварительно охладив его ниже критической температуры. Необходимые для сжижения СО 2 давления (в Atm) при разных температурах приведены в табл. 2.

Понятно, что эти давления являются давлениями насыщенного пара жидкой углекислоты и тем ниже, чем ниже температура.
Чтобы предварительно сильно охладить газ для сжижения, в технических установках пользуются эффектом Джоуля-Томсона, заключающимся в том, что при адиабатическом расширении (например, при резком падении давления, когда газ вытекает из отверстия) внутренняя энергия газа возрастает на ΔU, а Т изменяется на ΔТ, причем термодинамически
В случае идеальных газов ΔU = 0 и ΔТ = 0 [так как, по уравнению (1), T∙dv/dT – v = 0].
Для реальных газов ΔТ ≠ 0, т. е. происходит охлаждение или нагревание, смотря по тому, будет ли T∙dv/dT – v ≠ 0 (Δp < 0). По уравнению Ван-дер-Ваальса,
![]()
(с достаточным приближением). Т. о. при достаточно высоких температурах все газы при адиабатическом расширении нагреваются (ΔТ > 0, т. к. a/R∙T< b), но с понижением температуры для каждого газа наступает инверсионная точка Т i , определяемая условием
![]()
ниже которой газы начинают охлаждаться при адиабатическом расширении (a/R∙T> b при Т < Т i). Для всех газов, кроме Н 2 и Не, Т i лежит выше обычных температур (так, для воздуха Т i соответствует +360°С), и потому газы могут быть сжижены по принципу Линде , без предварительного охлаждения. Для Н 2 инверсионная точка Т i - 80,5°С, а для Не - даже 15°К; поэтому Н 2 и Не для сжижения д. б. предварительно охлаждены ниже этих температур.
Соответственные состояния . Критические температура Т к, давление р к и объем v к м. б. выражены через константы Ван-дер-Ваальса а, b и R следующим образом:
Если за единицы измерения Т, р и v принять соответственно критические величины, то вместо Т, р и v состояние будет характеризоваться приведенными величинами :
Если ввести θ, π и ϕ в уравнение Ван-дер-Ваальса (15), то константы а, b и R сократятся, и получится приведенное уравнение состояния , с численными коэффициентами
вовсе не содержащее величин, зависящих от природы вещества. Уравнение (19) предполагает, однако, правильность уравнения Ван-дер-Ваальса, и потому уклонения от него часто весьма значительны, особенно в случае ассоциированных веществ. Учение о соответственных состояниях (так называются состояния, отвечающие одинаковым θ, π и ϕ) дает возможность находить большое число универсальных зависимостей, подобных уравнению (19).
Применение газов . Сжатые и сжиженные газы применяются в технике всюду, где нужны значительные количества газа в небольшом объеме; так, СО 2 применяется для газирования вод, Сl 2 и фосген - в военно-химическом деле, O 2 - для медицинских целей, сжатый воздух - для пуска двигателей внутреннего сгорания. Особенное значение сжиженные газы (СО 2 и NH 3) имеют в холодильном деле, в холодильных машинах (например, для получения искусственного льда). Легкие газы (Н 2 , светильный газ, в последнее время Не) применяются для наполнения аэростатов . Инертные газы (N 2 и благородные газы, особенно Аr) применяются для наполнения полуваттных ламп накаливания. Особняком стоит применение газа для освещения или в качестве топлива: светильный, силовой, водяной газы и другие.
Жидкости могут существовать лишь при температурах ниже критической. Поэтому для сжижения газа его нужно прежде всего охладить ниже критической температуры, а затем подвергнуть сжатию. Как видно из таблицы XIII, такие газы, как кислород, азот, водород и особенно гелий, требуют для сжижения очень низких температур.
Таблица XIII (см. скан) Критические температуры и температуры кипения (при атмосферном давлении) для некоторых газов
В одном из первых промышленных методов сжижения газов (метод Линде, 1895) использовался эффект Джоуля - Томсона.
Схема машины Линде представлена на рисунке 6.21. Сжатый компрессором К и вследствие этого несколько нагретый газ проходит через холодильник X, где он отдает тепло проточной воде и охлаждается до первоначальной температуры. Затем газ проходит через змеевик к дроссельному вентилю (крану) и расширяется в приемник В с перепадом давления примерно от сотен атмосфер до одной атмосферы. Сразу после запуска установки понижение температуры недостаточно для сжижения газа. Слегка охлажденный газ направляется опять в компрессор через змеевик Оба змеевика расположены в тесном тепловом контакте (обычно один змеевик вставлен в другой) в противоточном теплообменнике В теплообменнике газ, идущий к компрессору и имеющий более низкую температуру, охлаждает встречный поток газа. Очевидно, во втором цикле газ подойдет к вентилю А с более низкой температурой, чем

это было при первом его прохождении, а после дросселирования температура еще более понизится. С каждым циклом в результате дросселирования и действия теплообменника температура газа будет все более понижаться и в конце концов понизится настолько, что часть газа после расширения превращается в жидкость и накапливается в приемнике В, откуда жидкость может быть слита в сосуд Дьюара через кран
Описанный принцип противоточного теплообмена используется во всех машинах для сжижения газов, хотя конструкция такого рода теплообменников может быть чрезвычайно разнообразной.
Другой промышленный метод сжижения газов (метод Клода, 1902 г.) основан на дополнительном охлаждении газа при совершении им работы. Сжатый газ после вентиля (рис. 6.21) направляется в поршневую машину (детандер), где он, расширяясь, совершает работу по перемещению поршня за счет кинетической энергии молекул (на рисунке детандер не изображен). В результате эффект понижения температуры газа делается более значительным, нежели в машине Линде. Этот метод усовершенствовал советский ученый П. Л. Капица (1934 г.), который вместо поршневого детандера применил небольшую турбину (турбодетандер), приводимую во вращение охлаждаемым газом (ротор детандера небольших размеров, и вес его измеряется всего сотнями граммов).
В настоящее время для сжижения газов в большинстве случаев используют машины с расширением в детандерах. При сжижении гелия для предварительного охлаждения в машинах с турбодетандерами используют не водород, а азот, что значительно повышает производительность и экономическую эффективность устройства. Кроме того, при одинаковой производительности машины с турбодетандерами в несколько раз меньше машин, работающих по схеме Линде.
Инструкция
На вид сжиженный природный газ (СПГ) - это бесцветная жидкость без и запаха, на 75-90% состоящая и обладающая очень важными свойствами: в жидком состоянии он не горюч, не и не агрессивен, что крайне важно при транспортировке. Процесс сжижения СПГ имеет характер, где каждая новая ступень означает сжатие в 5-12 раз, после чего следует охлаждение и переход на следующую ступень. СПГ становится жидким по завершению последней стадии сжатия.
Если же газ необходимо транспортировать на очень большие расстояния, то гораздо выгоднее использовать специальные суда – танкеры-газовозы. От места газа до ближайшего подходящего места на морском побережье протягивают трубопровод, а на берегу строят терминал. Там газ сильно сжимают и охлаждают, переводя в жидкое состояние, и закачивают в изотермические емкости танкеров (при температурах порядка -150оС).
Этот способ транспортировки имеет ряд преимуществ перед трубопроводным. Во-первых, один подобный за один рейс может перевезти громадное количество газа, ведь плотность вещества, находящегося в жидком состоянии, гораздо выше. Во-вторых, основные расходы приходятся не на транспортировку, а на погрузку-разгрузку продукта. В-третьих, хранение и перевозка сжиженного газа гораздо безопаснее, чем сжатого. Можно не сомневаться, что доля природного газа, транспортируемого в сжиженном виде, будет неуклонно возрастать по сравнению с газопроводными поставками.
Сжиженный природный газ востребован в различных областях деятельности человека - в промышленности, в автомобильном транспорте, в медицине, в сельском хозяйстве, в науке и пр. Немалую популярность сжиженные газ ы завоевали за счет удобства их использования и транспортировки, а также экологической чистоты и невысокой стоимости.

Инструкция
Перед сжижением углеводородного газ а его необходимо предварительно очистить и удалить водяной пар. Углекислый газ удаляют, используя систему трехступенчатых молекулярных фильтров. Очищенный таким образом газ в небольших количествах используется в качестве регенерационного. Восстанавливаемый газ либо сжигается, либо применяется для получения в генераторах мощности.
Просушивание происходит с помощью 3-х молекулярных фильтров. Один фильтр поглощает водяной пар. Другой сушит газ , который далее и проходит через третий фильтр. Для понижения температуры газ пропускается через водяной охладитель.
Азотный способ подразумевает производство сжиженного углеводородного газ а из любых газ овых источников. К преимуществам этого метода можно отнести простоту технологии, уровень безопасности, гибкость , легкость и малозатратность эксплуатации. Ограничения этого метода - необходимость источника электроэнергии и высоких капитальных затрат.
При смешанном способе производства сжиженного газ а в качестве хладагента используют смесь азота и . Получают газ также из любых источников. Этот метод отличается гибкостью производственного цикла и небольшими переменными затратами на производство. Если сравнивать с азотным способом сжижения, здесь капитальные затраты более существенны. Также необходим источник электроэнергии.
Источники:
- Что такое сжижение газов?
- Сжиженный газ: получение, хранение и транспортировка
- что такое сжиженный газ
Природный газ добывается из недр Земли. Это полезное ископаемое состоит из смеси газообразных углеводородов, которая образуется в результате разложения органических веществ в осадочных породах земной коры.

Какие вещества входят в состав природного газа
На 80-98% природный газ состоит (CH4). Именно физико-химические свойства метана определяют характеристики природного газа. Наряду с метаном в составе природного газа присутствуют соединения такого же структурного типа – этан (C2H6), пропан (C3H8) и бутан (C4H10). В некоторых случаях в небольших количествах, от 0,5 до 1%, в природном газе обнаруживаются: (С5Н12), (С6Н14), гептан (С7Н16), (С8Н18) и нонан (С9Н20).
Также природный газ включает в себя соединения сероводорода (H2S), углекислого газа (CO2), азот (N2), гелий (He), водяные пары. Состав природного газа зависит от характеристик месторождений, где он добывается. Природный газ, добываемый в чисто газовых месторождениях, состоит в основном из метана.
Характеристики составляющих природного газа
Все химические соединения, входящие в состав природного газа, обладают рядом свойств, полезных в различных сферах промышленности и в быту.
Метан – горючий газ без цвета и запаха, он легче воздуха. Используется в промышленности и быту в качестве горючего. Этан – горючий газ без цвета и запаха, он немного тяжелее воздуха. В основном, из получают этилен. Пропан – ядовитый газ без цвета и запаха. Ему по свойствам близок бутан. Пропан используется, например, при сварочных работах, при переработке металлолома. Сжиженным и бутаном заправляют зажигалки и газовые баллоны. Бутан используют в холодильных установках.
Пентан, гексан, гептан, октан и нонан – . Пентан в небольших количествах входят в состав моторных топлив. Гексан также используется при экстрагировании растительных масел. Гептан, гексан, октан и нонан являются хорошими органическими растворителями.
Сероводород – ядовитый бесцветный тяжелый газ, тухлых яиц. Этот газ даже в маленькой концентрации вызывает паралич обонятельного нерва. Но в силу того, что сероводород обладает хорошими антисептическими свойствами, его в малых дозах применяют в медицине для сероводородных ванн.
Углекислый газ – негорючий бесцветный газ без запаха с кислым вкусом. Углекислый газ используют в пищевой промышленности: в производстве газированных напитков для насыщения их углекислотой, для заморозки продуктов, для охлаждения грузов при транспортировке и т.п.
Азот – безвредный бесцветный газ, без вкуса и запаха. Применяют его в производстве минеральных удобрений, используют в медицине и т.п.
Гелий – один из самых легких газов. Он не имеет цвета и запаха, не горит, не токсичен. Гелий используют в различных областях промышленности – , для охлаждения атомных реакторов, наполнения стратостатов.
Опытный факт охлаждения вещества при испарении был известен издавна и даже практически использовался (например, применение пористых сосудов для сохранения свежести воды). Но первое научное исследование этого вопроса предпринял Джан Франческо Чинья и описал в работе 1760 г. «De frigore ex evaporationе» («О холоде вследствие испарения»).
Чинья доказал, что чем быстрее происходит испарение, тем интенсивнее остывание, а Меран показал, что если дуть на влажный шарик термометра, понижение температуры окажется больше, чем при таком же опыте с сухим шариком термометра. Антуан Боме (1728—1804) обнаружил, что при выпаривании серного эфира охлаждение происходит сильнее, чем при испарении воды. Основываясь на этих фактах, Тиберио Кавалло создал в 1800 г. холодильную машину, а Волластон построил в 1810 г. свой известный криофор, применяемый и в наше время. На основе этого прибора в 1820 г. был создан гигрометр Даниэля. Холодильная машина стала практически применимой лишь после 1859 г., т. е. после того, как Фернан Карре (1824— 1894) опубликовал свой метод получения льда с помощью испарения эфира, впоследствии замененного аммиаком. В 1871 г. Карл Линде (1842—1934) описал созданную им холодильную машину, в которой охлаждение достигается за счет расширения газа. В 1896 г. он скомбинировал эту машину с противоточным теплообменником, описываемым в курсах физики, и это позволило ему получить жидкий водород. Достигнутые к тому времени физиками экспериментальные результаты начали внедряться в промышленность.
Проблема сжижения газов имеет вековую историю, берущую свое начало во второй половине XVIII столетия. Началось все с сжижения аммиака простым охлаждением, которое произвел ван Марум, серного ангидрида — Монж и Клуэ, хлора — Нортмор (1805 г.) и сжижения аммиака компрессионным методом, предложенным Баччелли (1812 г.).
Определяющий вклад в решение этой проблемы одновременно и независимо внесли Шарль Каньяр де Латур (1777—1859) и Майкл Фарадей (1791—1867).
В серии работ, опубликованных в 1822 и 1823 гг., Каньяр де Латур описал опыты, проведенные им для определения существования для жидкости (как это чувствуется интуитивно) некоторого предельного расширения, дальше которого независимо от приложенного давления вся она переходит в парообразное состояние. С этой целью де Латур положил в котел, заполненный на одну треть спиртом, каменный шар и начал постепенно разогревать котел. По шуму, производимому шаром, поворачивавшимся внутри котла, де Латур пришел к выводу, что при определенной температуре весь спирт испарился. Опыты были повторены с небольшими трубками; из трубок удалялся воздух, а затем они заполнялись на 2/5 исследуемой жидкостью (спирт, эфир, бензин) и нагревались в пламени. По мере увеличения температуры жидкость становилась все более подвижной, а граница раздела жидкости и пара все более нечеткой, пока при определенной температуре совсем не исчезала и вся жидкость казалась превратившейся в пар. Соединив эти трубки с манометром со сжатым воздухом, Каньяр де Латур сумел измерить давление, устанавливающееся в трубке в момент, когда исчезает граница раздела между жидкостью и паром, и соответствующую температуру. Вопреки бытующему представлению Каньяр де Латур не только не определил в этих опытах критическую температуру для воды, ему не удалось даже полностью испарить воду, потому что трубки всегда лопались раньше, чем достигался желаемый эффект.
Более конкретный результат содержали опыты Фарадея, проведенные в 1823 г. с загнутыми стеклянными трубками, более длинное плечо, которых было запаяно. В это плечо Фарадей помещал вещество, которое при нагреве должно было давать исследуемый газ, затем закрывал второе, короткое плечо трубки и погружал трубку в охлаждающую смесь. Если, проделав это, нагревать вещество в длинном плече трубки, то образуется газ, давление которого постепенно увеличивается, причем во многих случаях в короткой трубке у Фарадея происходило сжижение газа. Так, нагревая бикарбонат натрия, Фарадей получил жидкую углекислоту; таким же способом он получал жидкий сероводород, хлористый водород, серный ангидрид и др.
Опыты де Латура и Фарадея показали, что можно добиться сжижения газа, подвергая его высокому давлению. В этом направлении начали работать многие физики, в частности Иоганн Наттерер (1821—1901). Однако некоторые газы (водород, кислород, азот) сжижить таким путем не удавалось. В 1850 г. Вертело подверг кислород давлению в 780 атм, но не смог добиться сжижения. Это заставило Вертело присоединиться к мнению Фарадея, который, уверенный, что рано или поздно удастся получить твердый водород, полагал, что одного давления недостаточно для сжижения некоторых газов, прозванных тогда «перманентными» или «неукротимыми».
В том же 1845 г., когда Фарадей высказал это соображение, Реньо, заметив, что при низкой температуре углекислый газ обладает аномальной сжимаемостью, а при приближении к 100° С начинает следовать закону Бой-ля, выдвинул предположение, что для каждого газа существует некая область температур, где он подчиняется закону Бойля. В 1860 г. эту идею Реньо развил и модифицировал Дмитрий Иванович Менделеев (1834—1907), согласно которому для всех жидкостей должна существовать «абсолютная температура кипения», выше которой она может существовать лишь в газообразном состоянии, каково бы ни было давление.
Исследование этого вопроса было возобновлено в 1863 г. в новой форме Томасом Эндрюсом (1813—1885). В 1863 г. Эндрюс ввел в капиллярную трубку углекислый газ, заперев объем газа столбиком ртути. С помощью винта он произвольно устанавливал давление, под которым находился газ, одновременно меняя постепенно температуру. Добившись с помощью одного лишь увеличения давления частичного сжижения газа и затем медленно нагревая трубку, Эндрюс наблюдал те же явления, которые за 30 лет до него исследовал Каньяр де Латур. Когда температура углекислоты достигала 30,92° С, граница раздела между жидкостью и газом исчезала и никаким давлением нельзя было уже получить обратно жидкую углекислоту. В своей обстоятельной работе 1869 г. Эндрюс предложил назвать температуру 30,92° С «критической точкой» для углекислоты. Таким же методом он определил критические точки для хлористого водорода, аммиака, серного эфира, окиси азота. Термин «пар» он предложил сохранить для газообразных веществ, находящихся при температуре ниже критической точки, а термин «газ» применять к веществам, находящимся при температуре выше критической точки. Подтверждением этой точки зрения Эндрюса являлись упомянутые уже опыты Наттерера, проведенные им с 1844 по 1855 г., в которых перманентные газы подвергались давлению до 2790 атм, так и не сжижаясь, и многочисленные аналогичные опыты, начатые в 1870 г. Эмилем Амага (1841—1915), в которых достигалось давление до 3000 атм.
Все эти отрицательные результаты опытов подтверждали гипотезу Эндрюса о том, что перманентные газы — это вещества, для которых критическая температура ниже достигнутых в тот момент значений, так что их сжижение можно было бы осуществить с помощью предварительного глубокого охлаждения, возможно с последующим сжатием. Эта гипотеза была блестяще подтверждена в 1877 г. Луи Кальете (1832—1913) и Раулем Пикте (1846—1929), которым независимо друг от друга удалось после предварительного сильного охлаждения добиться сжижения кислорода, водорода, азота, воздуха. Работы Кальете и Пикте были продолжены другими физиками, но лишь появление холодильной машины Линде, о которой мы уже упоминали, сделало методы сжижения практически доступными, позволив получать сжиженные газы в больших количествах и широко применять их при научных исследованиях и в промышленности.
УДЕЛЬНАЯ ТЕПЛОЕМКОСТЬ ГАЗОВ
Методы определения удельной теплоемкости трудно было применить к газообразным веществам вследствие малого удельного веса газов и паров. Поэтому в начале XIX века Парижская Академия наук объявила конкурс на лучший метод измерения удельной теплоемкости газа. Премия была присуждена Франсуа Деларошу (? — 1813?) и Жаку Берару (1789—1869), предложившим поместить в калориметр змеевик, по которому при известной температуре проходил бы газ при фиксированном давлении. Этот метод фактически не был новым; он был предложен еще за 20 лет до того Лавуазье. Как бы то ни было, результаты, полученные Деларошем и Бераром, приводились в курсах физики в течение полувека. Заслуга этих ученых прежде всего в том, что было привлечено внимание к необходимости различать удельные теплоемкости при постоянном давлении и при постоянном объеме. Последняя величина очень трудно поддается измерению из-за малой величины теплоемкости газа по сравнению с теплоемкостью содержащего его резервуара.
Но за несколько лет до появления работ Делароша и Берара началось исследование любопытного явления, отмеченного Эразмом Дарвином (1731—1802) в 1788 г., а затем в 1802 г. Дальтоном и заключающегося в том, что сжатие воздуха вызывает его разогрев, а расширение приводит к охлаждению. Началом исследования этого явления обычно считают опыт Гей-Люссака (1807 г.), повторенный Джоулем в 1845 г. Гей-Люссак соединил трубкой два баллона, подобно тому как это делал Герике; один из баллонов был наполнен воздухом, а второй пустой; из наполненного баллона воздух мог свободно перетекать в пустой. В результате было установлено понижение температуры первого баллона и повышение температуры второго. Такое тепловое поведение воздуха заставляло считать, что удельная теплоемкость при постоянном давлении должна быть больше, чем при постоянном объеме, какой бы теории природы тепла мы ни придерживались. Действительно, если, расширяясь, газ охлаждается, то, позволяя ему при нагреве расширяться, необходимо сообщить ему дополнительное тепло, чтобы скомпенсировать сопутствующее расширению охлаждение.
Исходя из этих экспериментальных фактов, Лаплас в 1816 г. пришел к гениальной идее о том, что известное несоответствие между значением скорости звука, получающимся из опыта, и его теоретическим значением, получающимся из закона Ньютона, можно объяснить изменением температуры, которое испытывают слои воздуха при чередующихся сжатиях и разрежениях. На основе этих теоретических предпосылок Лаплас исправил формулу Ньютона, введя в нее коэффициент, равный отношению удельных теплоемкостей при постоянном давлении и при постоянном объеме для воздуха. Сопоставление экспериментального значения скорости звука в воздухе и теоретического значения, получающегося по формуле Ньютона, позволило найти отношение удельных теплоемкостей. Таким косвенным путем физикам удалось получить первые данные о значении этого отношения и тем самым, поскольку значение удельной теплоемкости при постоянном давлении было известно, оценить удельную теплоемкость воздуха при постоянном объеме. Несколькими годами позже (1819 г.) Никола Клеману (1779—1841) и Шарлю Дезорму (1777—?) удалось в опытах по расширению газов, многократно повторяющихся другими учеными вплоть до наших дней и вошедших во все учебники по физике, непосредственно определить отношение теплоемкостей, которое в пределах экспериментальных ошибок совпало с найденным Лапласом.
В 1829 г. в результате тонких и кропотливых исследований Дюлонг определил отношение теплоемкостей для различных газов, для чего вызывал звук в трубке с помощью потоков различных газов. Эти эксперименты заставили его прийти к выводу, что в газах и парах при равных условиях (объем, давление, температура) образуется при одинаковом относительном сжатии или расширении одинаковое количество теплоты.
Заметим, что метод Дюлонга был существенно улучшен в 1866 г. Кундтом (1839—1894), который ввел специальную трубку (эта трубка называется теперь трубкой Кундта). Метод Кундта до сих пор считается одним из лучших методов определения отношения удельных теплоемкостей.
Составитель Савельева Ф.Н.
 Воля: функции, понятие, основные признаки
Воля: функции, понятие, основные признаки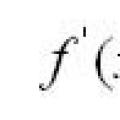 Геометрический и механический смысл производной
Геометрический и механический смысл производной Свойства степеней при сложении
Свойства степеней при сложении